上皮膜蛋白1真核表達載體的構建及其對人舌鱗狀細胞癌細胞遷移和侵襲的影響
代曉華 張軍 鄒慧儒 連小麗 李燕妮 王冠華 顏艷
1.天津市口腔醫院·南開大學口腔醫院中心實驗室;2.頜面外科,天津 300041
·口腔腫瘤學專欄·
上皮膜蛋白1真核表達載體的構建及其對人舌鱗狀細胞癌細胞遷移和侵襲的影響
代曉華1張軍2鄒慧儒1連小麗1李燕妮1王冠華1顏艷1
1.天津市口腔醫院·南開大學口腔醫院中心實驗室;2.頜面外科,天津 300041
目的構建上皮膜蛋白1(EMP1)基因真核表達載體pEGFP-N1-EMP1,探討EMP1基因對人舌鱗狀細胞癌細胞遷移和侵襲的影響。方法采用逆轉錄聚合酶鏈式反應(PCR)擴增EMP1基因,雙酶切法連接至真核表達載體pEGFP-N1雙酶切產物大片段,構建pEGFP-N1-EMP1重組質粒。經測序鑒定后,通過脂質體介導法將pEGFP-N1-EMP1重組質粒和pEGFP-N1空載體轉染至人舌鱗狀細胞癌Tb3.1細胞,熒光顯微鏡下觀察轉染后綠色熒光蛋白的表達情況,實時熒光定量PCR法檢測轉染后24、48、72 h的EMP1過表達水平。利用Transwell遷移及侵襲實驗分析EMP1過表達對Tb3.1細胞遷移及侵襲能力的影響。結果成功克隆EMP1全長基因,經測序分析證實將EMP1基因準確插入真核表達載體pEGFP-N1,轉染后細胞可見綠色熒光表達。實時熒光定量PCR結果顯示,pEGFP-N1-EMP1重組質粒轉染24 h組,Tb3.1細胞中EMP1表達量顯著高于pEGFP-N1空載體組、野生型細胞組以及重組質粒轉染48 h和72 h組。Transwell遷移及侵襲實驗結果顯示,EMP1過表達抑制了Tb3.1細胞的遷移和侵襲能力。結論成功構建了EMP1真核表達載體,并在體外證實了EMP1過表達可抑制舌鱗狀細胞癌細胞的遷移和侵襲能力,為進一步研究EMP1基因在口腔鱗狀細胞癌轉移中的作用及其分子機制奠定了基礎。
上皮膜蛋白1;舌鱗狀細胞癌細胞;載體;轉染;細胞遷移;細胞侵襲
口腔鱗狀細胞癌(oral squamous cell carcinoma,OSCC)是頭頸部最常見的惡性腫瘤,近幾十年,雖然外科手術及放射等治療手段得到不斷發展,但OSCC患者5年生存率卻未能得以顯著提高,腫瘤區域性和遠處轉移是導致治療失敗的主要原因之一[1]。由于舌的淋巴和血運豐富,舌鱗狀細胞癌更易發生轉移,患者術后發生頸淋巴結轉移者大約54%,而隱匿性頸轉移率也可達42%[2]。臨床常用的腫瘤輔助檢查方法,如超聲、CT、MRI和正電子發射計算機斷層掃描(positron emission computed tomography,PET)等對這些隱匿性頸轉移,微小轉移灶等均不敏感;因此,確立有效的舌鱗狀細胞癌轉移分子標志物,對隱匿性及微小轉移灶的早發現、早治療及判斷預后和提高生存率等具有重要意義。上皮膜蛋白1(epithelial membrane protein 1,EMP1),又稱腫瘤相關性膜蛋白(tumor-associated membrane protein,TMP)、進展相關性膜蛋白(progression association protein,PAP)、CL-20和B4B,染色體定位于12p12.3,是由157個氨基酸組成的含4個跨膜結構的糖蛋白,參與細胞的增殖、分化,與腫瘤的發生和發展密切相關[3]。已有研究[4-7]證明,EMP1對多種腫瘤細胞,如喉癌、胃癌及結腸直腸癌等細胞的增殖、遷移和侵襲等具有抑制作用,但對個別腫瘤細胞,如非小細胞肺癌的增殖則起著促進作用。EMP1對舌鱗狀細胞癌細胞遷移、侵襲等生物學行為的影響尚少見報導。本研究旨在構建EMP1基因真核表達載體,轉染舌鱗狀細胞癌Tb3.1細胞系,檢測EMP1對舌鱗狀細胞癌細胞遷移和侵襲能力的影響,為進一步深入研究EMP1在OSCC轉移中的作用機制奠定基礎。
1 材料和方法
1.1主要試劑和儀器
真核表達載體pEGFP-N1質粒(北京鼎國昌盛生物技術有限公司)。RNA提取試劑盒、逆轉錄試劑盒、膠回收試劑盒、DL2000、DL10000、SYBR Premix Ex TaqⅡ[寶生物工程(大連)有限公司],DH5α感受態、無內毒素質粒提取試劑盒(北京博邁德基因技術有限公司),總蛋白提取試劑盒(北京普利萊基因技術有限公司)。T4連接酶(Promega公司,美國),鼠抗人β-actin單克隆抗體、辣根酶標記山羊抗小鼠IgG(北京中杉金橋生物技術有限公司),鼠抗綠色熒光蛋白(green fluorescent protein,GFP)融合蛋白單克隆抗體(南京恩晶生物科技有限公司),Lipofectamine 2000脂質體(Invitrogen公司,美國)。舌鱗狀細胞癌Tb3.1及P160細胞(天津市腫瘤醫院惠贈)。
聚合酶鏈式反應(polymerase chain reaction,PCR)基因擴增儀(Perkin-Elmer公司,美國);DYY-Ⅲ 31B水平電泳儀(北京六一儀器廠);超微量分光光度計(北京凱奧科技發展有限公司);凝膠成像系統(Ultra-Violet Products公司,美國);小型垂直電泳槽和轉膜槽及配套電源(Bio-Rad公司,美國);實時熒光定量PCR儀(Roche Diagnostics GmbH公司,德國);熒光顯微鏡(Zeiss公司,德國)。
1.2方法
1.2.1引物的設計與合成從GenBank中檢索人EMP1核心編碼區cDNA序列,再用DNASIS 2.5計算機軟件輔助設計人EMP1序列上游引物和下游引物,在上下游引物中分別引入限制性內切酶XhoⅠ和Hind Ⅲ位點(下劃線處為酶切位點):上游引物為5'-GCGCCTCGAGATGTTGGTATTGCTGGCTGGTAT-3',下游引物為5'-GCGCAAGCTTTTTCTTTCTCAGGACCAGATAG-3'。用于實時熒光定量PCR的EMP1引物為:上游引物5'-CCCTCCTGGTCTTCGTGT-3';下游引物5'-GGAATAGCCGTGGTGATA-3'。引物均由上海英駿生物技術有限公司合成。
1.2.2EMP1基因克隆擴增P160細胞用含10%胎牛血清的RPMI1640培養基在37 ℃、5%CO2、飽和濕度環境下培養。當P160細胞生長至約90%融合時,進行總RNA提取,具體操作步驟遵照RNA提取試劑盒說明書進行。電泳定量后,取1 μg總RNA,根據逆轉錄試劑盒說明書混合逆轉錄反應體系,進行逆轉錄。以獲取的cDNA為模板擴增EMP1基因,PCR反應體系總體積50 μL,含模板4 μL,上、下游引物各3 μL,dNTP 1 μL,10×PCR buffer 5 μL,Taq酶0.4 μL,ddH2O 33.6 μL。PCR擴增條件:94 ℃預變性5 min,94 ℃變性30 s,58.8 ℃退火30 s,72 ℃延伸40 s,共40個循環;72 ℃ 延伸5 min。PCR擴增產物進行瓊脂糖凝膠電泳,用膠回收試劑盒進行純化回收PCR產物。
1.2.3表達載體的構建克隆擴增的EMP1進行XhoⅠ和Hind Ⅲ雙酶切,經瓊脂糖凝膠電泳分離純化回收目的片段。pEGFP-N1質粒經相同酶切處理,分離純化回收大片段。根據T4連接酶說明書,將純化回收的EMP1 DNA和pEGFP-N1大片段按照質量比1∶10的比例用T4連接酶,室溫下連接3 h。連接產物轉化感受態DH5α后,涂布于卡那霉素抗性的LB軟瓊脂平板,37 ℃過夜培養,挑選瓊脂糖平板上單克隆菌落,進行PCR鑒定和酶切鑒定后測序。
1.2.4細胞轉染測序正確后,采用無內毒素質粒提取試劑盒提取和純化pEGFP-N1-EMP1重組質粒及pEGFP-N1質粒,測定濃度。轉染前24 h將Tb3.1細胞鋪被于6孔板,待細胞貼壁融合達80%~90%時,按Lipofectamine 2000脂質體說明書進行轉染,每孔脂質體5 μL、質粒2.5 μg,熒光顯微鏡下觀察轉染24、48及72 h后,細胞中GFP表達情況。
1.2.5實時熒光定量PCR檢測轉染后細胞EMP1 mRNA的表達分別于轉染后24、48、72 h,采用試劑盒法提取轉染細胞RNA,測定含量和純度,按逆轉錄試劑盒說明書合成cDNA模板,使用實時熒光定量PCR法檢測轉染不同時間點細胞EMP1 mRNA的表達水平。每個樣本設3個重復孔,內參選擇β-actin,基因相對表達量采用2-ΔΔCt法計算。反應體系總體積20 μL,含模板2 μL,上、下游引物各0.8 μL,SYBR Premix Ex Taq Ⅱ10 μL,ddH2O 6.4 μL。反應條件:95 ℃30 s,95 ℃ 5 s,60 ℃ 30 s,共40個循環。
1.2.6Transwell法檢測細胞侵襲和遷移能力侵襲實驗中,首先采用預冷無血清RPMI1640培養基稀釋Matrigel基質膠,鋪被于Transwell上室內,置于37 ℃孵箱中4~5 h。于轉染后24 h收集細胞,用無血清培養基調整細胞密度至1×106個·mL-1,取100 μL接種于含Matrigel基質膠的Transwell小室上室內,下室加入含20%血清的RPMI1640培養基,繼續培養24 h。將上室內細胞輕輕拭去,用PBS洗兩次,再行多聚甲醛固定,結晶紫染色后顯微鏡下觀察,隨機選5個視野,計數穿膜細胞,以每個視野的平均細胞數表示舌鱗狀細胞癌細胞的侵襲能力。遷移實驗時Transwell小室內不鋪被Matrigel基質膠,其余同侵襲實驗。
1.3統計學分析
采用SPSS 18.0軟件進行統計分析,對實時熒光定量PCR和Transwell遷移及侵襲實驗結果行單因素方差分析和多重比較檢驗,檢驗水準為雙側α=0.05。
2 結果
2.1EMP1基因的擴增與重組pEGFP-N1-EMP1表達載體的構建
以P160細胞cDNA為模板,PCR擴增EMP1基因,經瓊脂糖凝膠電泳分離后,在約490 bp處可見特異性擴增條帶,與目的基因相對分子質量相符(圖1)。擴增產物回收純化后連接至T載體,進行轉化篩選,選取鑒定和測序均正確的菌落進行擴增。提取質粒,經XhoⅠ和Hind Ⅲ雙酶切獲取EMP1基因,與同樣經雙酶切的表達載體pEGFP-N1大片段連接,成功構建pEGFP-N1-EMP1表達載體。
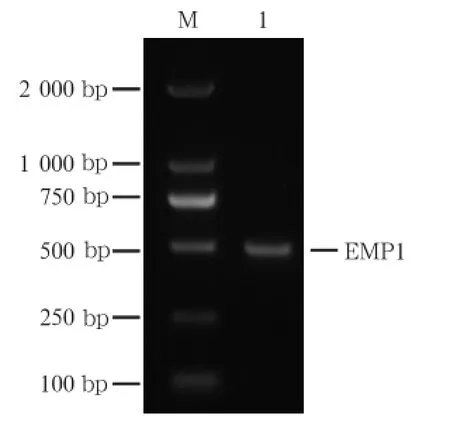
圖1 PCR擴增EMP1基因瓊脂糖凝膠電泳Fig 1 Agarose gel electrophoresis of EMP1 gene by PCR
2.2pEGFP-N1-EMP1表達載體的鑒定
擴增轉化DH5α后在軟瓊脂平板上篩選出單克隆菌落共7個,以其為模板分別進行EMP1 PCR擴增鑒定,其中5個單克隆菌落電泳后可見約490 bp的特異性條帶。對其中一株PCR陽性克隆進行質粒提取,經XhoⅠ和Hind Ⅲ雙酶切后,電泳亦可見一條約490 bp條帶,與目的基因相符(圖2)。經測序鑒定,克隆的人EMP1基因序列與GenBank中已知基因序列完全一致,無突變堿基。
2.3轉染細胞EMP1 mRNA水平的表達
經脂質體介導,將pEGFP-N1質粒和pEGFP-N1-EMP1重組質粒瞬時轉染至Tb3.1細胞,轉染后細胞內可見綠色熒光(圖3),表明pEGFP-N1-EMP1重組質粒和pEGFP-N1質粒在Tb3.1細胞中表達GFP。實時熒光定量PCR檢測結果(圖4)顯示,pEGFP-N1-EMP1重組質粒轉染后,Tb3.1細胞中EMP1表達增強,轉染24 h后,Tb3.1細胞EMP1相對表達量明顯高于其他各組(P<0.05),是pEGFP-N1質粒轉染組(空載體組)的103.7倍,是野生型細胞組的196.1倍;pEGFP-N1質粒轉染組和未轉染的野生型Tb3.1細胞中,EMP1表達量較低,二者間EMP1表達的差異無統計學意義(P>0.05)。

圖2 pEGFP-N1-EMP1表達載體的鑒定Fig 2 Identification of recombinant expression vector pEGFP-N1-EMP1
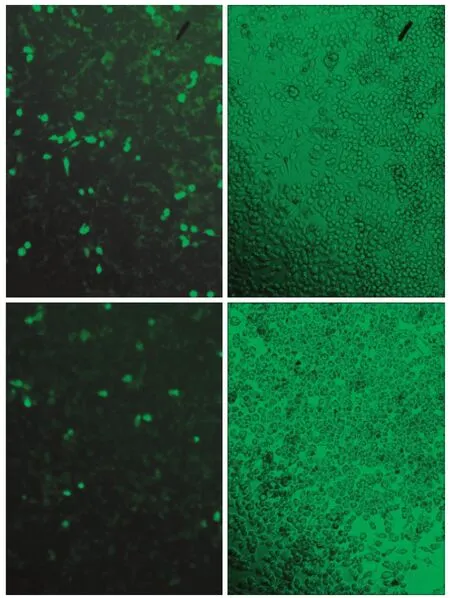
圖3 pEGFP-N1和pEGFP-N1-EMP1質粒轉染Tb3.1細胞48 h后GFP的表達 熒光顯微鏡 × 100Fig 3 GFP expression in the Tb3.1 cells transfected with pEGFPN1 and pEGFP-N1-EMP1 after 48 hours fluorescence microscope × 100
2.4EMP1對舌鱗狀細胞癌細胞體外遷移和侵襲能力的影響
遷移和侵襲實驗檢測結果如圖5、6所示,pEGFPN1-EMP1重組質粒轉染組遷移及侵襲的Tb3.1細胞數均明顯低于pEGFP-N1質粒轉染組和野生型Tb3.1細胞組(P<0.05),pEGFP-N1質粒轉染組和野生型Tb3.1細胞組間遷移及侵襲細胞數差異無統計學意義(P>0.05),表明EMP1可抑制舌鱗狀細胞癌細胞的體外遷移和侵襲能力。
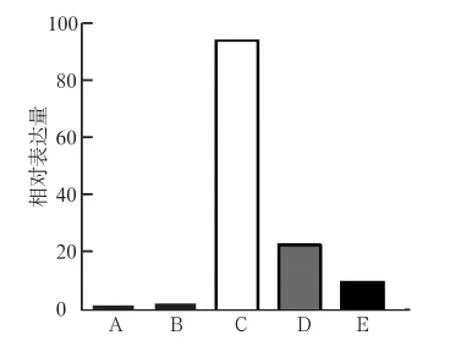
圖4 實時熒光定量PCR檢測Tb3.1細胞EMP1 mRNA表達Fig 4 The expression of EMP1 mRNA in Tb3.1 cells by real-time fluorescence quantitative PCR

圖5 EMP1抑制Tb3.1細胞遷移及侵襲Fig 5 EMP1 inhibited the migration and invasion of Tb3.1 cells
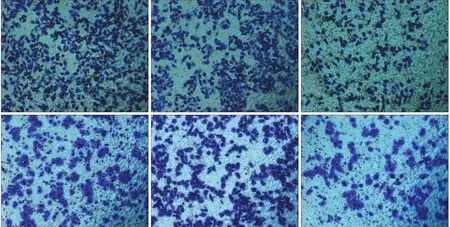
圖6 Tb3.1細胞遷移和侵襲實驗形態學觀察 熒光顯微鏡 × 100Fig 6 Morphological observation of the migration and invasion of Tb3.1 cells fluorescence microscope × 100
3 討論
腫瘤轉移是多基因參與且涉及多環節的復雜過程。癌細胞從原發腫瘤位置侵襲到周圍組織,是導致腫瘤轉移發生的第一步,癌細胞的黏附、運動、遷移和侵襲能力是發生轉移的條件。EMP1基因與外周髓鞘蛋白-22(peripheral myelin protein 22,PMP-22)同屬一個跨膜家族,細胞外結構域序列保守,具有一致的N-糖基化序列。這個糖基化位點攜帶修飾過的含有人自然殺傷細胞抗原-1(human natural killer-1,HNK-1)決定簇的糖鏈,可識別細胞表面糖蛋白,如一些酪脂類、蛋白聚糖等碳水化合物結構,這些蛋白參與細胞黏附,細胞間以及細胞和外界基質間的相互作用,說明EMP1與細胞黏附過程有關,在細胞生長、增殖、分化及凋亡中起著重要作用[3,8-10]。
正常組織中,EMP1在舌和食管等鱗狀上皮中表達豐度較高。體外培養的支氣管上皮細胞鱗狀上皮轉化過程中EMP1表達升高,較之輕中度增生或無化生上皮,嚴重增生或伴有化生的上皮組織中EMP1 mRNA水平較低,提示EMP1高表達與鱗狀上皮分化密切相關[3,8,11]。研究[4-7,12-14]顯示,在胃癌、結直腸癌、乳腺癌、鼻咽癌、前列腺癌等腫瘤組織中EMP1蛋白相對表達量較正常組織顯著下降,且其表達水平與腫瘤侵襲、淋巴結轉移、臨床分期和組織學分級有相關性,EMP1表達越低,患者的5年生存率越差,而EMP1過表達可抑制腫瘤細胞增殖、遷移和侵襲。Sun等[12]研究表明,在EMP1過表達的乳腺癌MCF-7細胞中,Caspase-9增高,血管內皮生長因子C(vascular endothelial growth factor C,VEGFC)蛋白表達降低,提示EMP1可能是通過調節Caspase-9 和VEGFC蛋白表達對乳腺癌進行負性調節。但是,在非小細胞肺癌和神經膠質瘤發生過程中,則伴有EMP1表達顯著上調。另有研究[7,15]顯示,EMP1過表達可促進肺腺癌PC9細胞增殖和無胸腺裸鼠體內PC9成瘤的生長,同時伴有磷脂酰肌醇3激酶/蛋白激酶B(phosphatidylinositol 3 kinase/protein kinase B,PI3K/AKT)信號通路激活,推測EMP1表達可能是通過激活PI3K/AKT通路促進非小細胞肺癌的形成和發展。另外,EMP1還與非小細胞肺癌、胃腸道間質瘤及非白血性白血病等耐藥有關,被認為是吉非替尼耐藥的生物標志物,產生耐藥的機制則可能涉及EMP1與表皮生長因子受體(epidermal growth factor receptor,EGFR)信號通路的相互交聯作用[7,16]。基因表達譜分析表明,OSCC中EMP1表達明顯下調。免疫組織化學分析顯示,EMP1表達與OSCC患者淋巴結轉移和臨床分期存在一定的相關性,但EMP1在OSCC轉移過程中具體作用機制尚不明確[17]。
本研究采用實時熒光定量PCR方法獲得人EMP1基因全長,將其克隆擴增后,連接至真核表達載體pEGFP-N1,成功構建了EMP1真核表達載體。利用脂質體法將pEGFP-N1-EMP1瞬時轉染至舌鱗狀細胞癌Tb3.1細胞。真核表達載體pEGFP-N1具有猿猴病毒40(simian virus 40,SV40)啟動子和巨細胞病毒(cytomegalovirus,CMV)啟動子,可使目的基因在增殖細胞中穩定表達;同時攜帶有新霉素抗藥基因,可用G418篩選穩定轉染的細胞株,利于后續進行EMP1穩定過表達舌鱗狀細胞癌細胞株的篩選。Tb3.1細胞系是人舌鱗狀細胞癌細胞腦轉移株,不僅具有舌鱗狀細胞癌細胞所有的特性,而且更易增殖和轉移[18]。本研究通過熒光顯微鏡觀察和實時熒光定量PCR檢測EMP1瞬時轉染后EMP1表達情況,選擇EMP1表達較高的時間點進行了Transwell遷移和侵襲實驗,結果發現,EMP1過表達有效抑制了轉移性較強的Tb3.1細胞的遷移和侵襲能力。
總之,本研究成功構建了EMP1真核表達載體pEGFP-N1-EMP1,并在體外證明,EMP1基因過表達可有效抑制舌鱗狀細胞癌Tb3.1細胞的遷移和侵襲能力,為進一步探究EMP1在OSCC轉移中的具體作用及其分子機制奠定了基礎。
[1] Neville BW, Day TA. Oral cancer and precancerous lesions [J]. CA Cancer J Clin, 2002, 52(4):195-215.
[2] Ho CM, Lam KH, Wei WI, et al. Occult lymph node metastasis in small oral tongue cancers[J]. Head Neck, 1992, 14 (5):359-363.
[3] Chen Y, Medvedev A, Ruzanov P, et al. cDNA cloning,genomic structure, and chromosome mapping of the human epithelial membrane protein CL-20 gene (EMP1), a member of the PMP22 family[J]. Genomics, 1997, 41(1):40-48.
[4] Durgan J, Tao G, Walters MS, et al. SOS1 and Ras regulate epithelial tight junction formation in the human airway through EMP1[J]. EMBO Rep, 2015, 16(1):87-96.
[5] Sun G, Zhao G, Lu Y, et al. Association of EMP1 with gastric carcinoma invasion, survival and prognosis[J]. Int J Oncol,2014, 45(3):1091-1098.
[6] Sun GG, Wang YD, Cui DW, et al. Epithelial membrane protein 1 negatively regulates cell growth and metastasis in colorectal carcinoma[J]. World J Gastroenterol, 2014,20(14):4001-4010.
[7] Lai S, Wang G, Cao X, et al. EMP-1 promotes tumorigenesis of NSCLC through PI3K/AKT pathway[J]. J Huazhong Univ Sci Technol(Med Sci), 2012, 32(6):834-838.
[8] Marvin KW, Fujimoto W, Jetten AM. Identification and characterization of a novel squamous cell-associated gene related to PMP22[J]. J Biol Chem, 1995, 270(48):28910-28916.
[9] Jetten AM, Suter U. The peripheral myelin protein 22 and epithelial membrane protein family[J]. Prog Nucleic Acid Res Mol Biol, 2000, 64:97-129.
[10] 朱秀麗, 吳軍正, 溫德升, 等. 基因表達譜芯片技術篩選舌癌轉移相關基因[J]. 華西口腔醫學雜志, 2006, 24(2):166-169. Zhu XL, Wu JZ, Wen DS, et al. Screening and identification of metastasis-related gene expression in tongue carcinoma with cDNA microarray assay[J]. West Chin J Stomatol, 2006, 24(2):166-169.
[11] Yu XM, Li CW, Li YY, et al. Down-regulation of EMP1 is associated with epithelial hyperplasia and metaplasia in nasal polyps[J]. Histopathology, 2013, 63(5):686-695.
[12] Sun GG, Wang YD, Lu YF, et al. EMP1, a member of a new family of antiproliferative genes in breast carcinoma[J]. Tumour Biol, 2014, 35(4):3347-3354.
[13] Sun GG, Wang YD, Cui DW, et al. EMP1 regulates caspase-9 and VEGFC expression and suppresses prostate cancer cell proliferation and invasion[J]. Tumour Biol, 2014, 35(4): 3455-3462.
[14] Sun GG, Lu YF, Fu ZZ, et al. EMP1 inhibits nasopharyngeal cancer cell growth and metastasis through induction apoptosis and angiogenesis[J]. Tumour Biol, 2014, 35(4):3185-3193.
[15] Bredel M, Bredel C, Juric D, et al. Functional network analysis reveals extended gliomagenesis pathway maps and three novel MYC-interacting genes in human gliomas[J]. Cancer Res, 2005, 65(19):8679-8689.
[16] 來森艷, 王桂華, 曹小年, 等. 上皮膜蛋白-1作為胃腸道間質瘤耐藥標志物的研究[J]. 中華實驗外科雜志, 2012, 29 (5):885-887. Lai SY, Wang GH, Cao XN, et al. Epithelial membrane protein-1 is a biomarker of imatinib-resistant gastrointestinal stromai tumors[J]. Chin J Exp Surg, 2012, 29(5):885-887.
[17] Zhang J, Cao W, Xu Q, et al. The expression of EMP1 is downregulated in oral squamous cell carcinoma and possibly associated with tumour metastasis[J]. J Clin Pathol, 2011,64(1):25-29.
[18] 李超, 楊丹, 石芳瓊, 等. MHC-Ⅰ類鏈相關基因A真核表達載體的構建及穩定轉染舌鱗癌細胞的實驗研究[J]. 華西口腔醫學雜志, 2011, 29(4):437-441. Li C, Yang D, Shi FQ, et al. Construction of eukaryotic expression vector of major histocompatibility complex class-Ⅰrelated chain A and establishment of its stable transfected Tca8113-Tb cell line[J]. West Chin J Stomatol, 2011, 29(4): 437-441.
(本文編輯吳愛華)
Construction of epithelial membrane protein 1 eukaryotic expression vector and its influence on migration and invasion of human oral tongue squamous carcinoma cells
Dai Xiaohua1, Zhang Jun2, Zou Huiru1, Lian Xiaoli1, Li Yanni1, Wang Guanhua1, Yan Yan1. (1. Research Center, Tianjin Stomatological Hospital, Stomatological Hospital of Nankai University,Tianjin 300041, China; 2. Dept. of Oral and Maxillofacial Surgery, Tianjin Stomatological Hospital, Stomatological Hospital of Nankai University, Tianjin 300041, China)
Supported by: Tianjin Health and Family Planning Commision Foundation (2013KZ053). Correspondence: Zhang Jun, E-mail: zjsurgeon@126.com.
ObjectiveThis study aimed to construct a eukaryotic expression vector pEGFP-N1-EMP1 of epithelial membrane protein 1 (EMP1) and investigate its influence on migration and invasion of human oral tongue squamous carcinoma cells. MethodsThe human EMP1 gene was amplified by reverse transcription polymerase chain reaction and then ligated into the pEGFP-N1 vector by double restriction endonuclease digestion to construct pEGFP-N1-EMP1 recombinant plasmid. After sequencing identification, pEGFP-N1-EMP1 recombinant plasmid and pEGFP-N1 plasmid were transfected into human oral tongue squamous carcinoma Tb3.1 cell line. The expression of green fluorescent protein in cells was observed after transfection using an inverted fluorescence microscope. The overexpression of EMP1 mRNA was identified at 24, 48, and 72 h after transfection by real-time fluorescence quantitative polymerase chain reaction. The effect of EMP1 overexpression on migration and invasion of Tb3.1 cells was detected by Transwell assay. ResultsThe full-length EMP1 gene sequence was successfully obtained. Sequence analysis showed that the EMP1 gene was inserted into the pEGFP-N1 vector correctly. Green fluorescence was observed in the transfected cells under fluorescence microscopy. The results of real-time fluorescence quantitative polymerase chain reaction indicated that the expression of EMP1 at 24 h after pEGFP-N1-EMP1 transfection was significantly higher than the other groups. Transwell assays indicated that overexpression of the EMP1 gene could significantly inhibit the migration and invasion ability of Tb3.1 cells. ConclusionThe eukaryotic expression vector of EMP1 was successfully constructed, and EMP1 overexpression was confirmed to inhibit the migration and invasion of oral tongue squamous carcinoma cells in vitro. This study laid a foundation for further investigation on the influence of the EMP1 gene on the metastasis of oral tongue squamous carcinoma and its molecular mechanism.
epithelial membrane protein 1;oral tongue squamous carcinoma cell;vector;transfection;cell migration;cell invasion
R 73
A
10.7518/hxkq.2016.04.016
2015-11-10;
2016-02-20
天津市衛計委基金(2013KZ053)
代曉華,副研究員,碩士,Email:jstonehome@163.com
張軍,副主任醫師,博士,Email:zjsurgeon@126.com

