青霉胞外合成銀納米粒子及其表征
徐秋紅,黃梅穎,馮家勛,杜良偉
(1.廣西大學化學化工學院, 廣西南寧530004;2.廣西大學亞熱帶農業生物資源保護與利用國家重點實驗室, 廣西南寧530004;3.廣西大學生命科學與技術學院, 廣西南寧530004)
?
青霉胞外合成銀納米粒子及其表征
徐秋紅1, 2,黃梅穎1, 2,馮家勛2, 3,杜良偉1, 2
(1.廣西大學化學化工學院, 廣西南寧530004;2.廣西大學亞熱帶農業生物資源保護與利用國家重點實驗室, 廣西南寧530004;3.廣西大學生命科學與技術學院, 廣西南寧530004)
摘要:為了尋求綠色高效的納米粒子合成方法,在模擬太陽光的照射下,利用青霉濾液快速胞外合成了銀納米粒子。用肉眼觀察、紫外—可見吸收光譜、X射線衍射(XRD)和透射電鏡(TEM)對合成的銀納米粒子進行表征。XRD結果表明合成了優先沿著(111)面生長的晶體結構的銀納米粒子。TEM結果表明,大部分納米粒子以團聚的狀態分散在溶液中,單個納米粒子的形貌呈球形,平均粒徑約為6 nm,團聚物的形狀不規則,其粒徑在20~50 nm。該合成方法具有條件溫和、清潔、無毒、無污染的特點,是一種綠色化學和環境友好的合成方法。
關鍵詞:青霉;生物合成;銀納米粒子;光照
金屬納米粒子因其獨特的物理、化學和生物學特性,被應用于催化、生物傳感器、藥物載體和抗菌藥物等領域中,其廣闊的應用前景已經引起了人們廣泛的關注。發展無毒、生物相容和環境友好的方法來合成金屬納米粒子越來越重要。微生物合成金屬納米材料是一個新興的具有廣闊發展前景的研究領域。
許多微生物能夠合成納米材料,這些微生物被認為是環境友好型的“納米工廠”。1999年,Klaus等[1]首次報道了使用施氏假單胞菌還原制備銀納米粒子,開辟了制備納米材料的微生物合成法,此后,細菌合成納米粒子受到了較多的重視[2]。為了打破這種傳統,印度的國家化學實驗室嘗試用真核生物代替原核生物合成納米粒子,經過兩年的努力,在200多種屬的真菌中發現了輪枝菌和尖孢鐮刀菌可以合成納米粒子[3-4]。與細菌相比,真菌因培養條件溫和、胞外分泌物多和容易進行下游處理等特點而被視為是更高效地合成納米粒子的資源。
早期微生物合成納米粒子的位點主要是在胞內,然而,從分析和應用的角度來說,胞內合成的納米粒子需通過超聲波破碎法[5]、去垢劑破碎法[6]或者加入細胞裂解液[7]等方法使納米粒子從細胞中釋放出來,這個過程復雜繁瑣且耗費時間,因此,在溶液中進行胞外合成比胞內合成更實際可行。在胞外合成中,目前采用較多的是將菌體在無菌水中培養后收集到的濾液與前驅體離子反應生成納米粒子。由于胞外分泌的濾液比較純凈,該合成方法更有利于研究納米粒子的合成。
目前已經有許多微生物被用來合成銀納米粒子,但大多數的合成效率比較低,反應時間長[8-9]。最近,文獻[10-11]報道,光能夠有效地促進銀納米粒子的合成,而且能縮短合成時間。為此,本研究在模擬太陽光照射的條件下,用真菌青霉1-208的濾液胞外合成銀納米粒子,并對合成的納米粒子進行表征,旨在利用可再生的微生物資源快速合成納米粒子。
1實驗部分
1.1實驗試劑
硝酸銀(AgNO3)(上海化學試劑有限公司);胰蛋白胨(北京奧博星生物技術責任有限公司);KH2PO4、(NH4)2SO4、MgSO4·7H2O、HCl、可溶性淀粉(國藥集團化學試劑有限公司);CaCl2(生工生物工程有限公司);FeSO4·7H2O(廣東汕頭新寧化工廠)。所有試劑均為分析純。實驗用水均為去離子水,另有違規除外。
AgNO3儲備液的配制:準確稱取一定量的AgNO3固體,用去離子水溶解并定容,配制成100 mmol/L的AgNO3溶液,用錫紙包裹避光于4 ℃冰箱保存備用。
1.2主要儀器
紫外—可見分光光度計(PerkinElmer Lambda 35,美國);透射電子顯微鏡(Hitachi H-500,日本);X射線衍射儀(Rigaku D/MAX,日本);光化學反應儀(德洋意邦,中國上海);往復式恒溫搖床(Thermo Fisher,美國);GNP-9160型隔水式恒溫培養箱(上海精宏實驗設備有限公司);冷凍離心機(Eppendorf,德國)。
1.3實驗方法
1.3.1青霉的培養
青霉1-208來自于亞熱帶農業生物資源保護與利用國家重點實驗室,將保存在PDA平板上的青霉1-208接種于250 mL的可溶性淀粉培養基[12]中,在28 ℃,180 r/min的往復式恒溫搖床中培養3 d。
1.3.2細胞濾液的獲取
將培養3 d后的菌液用4層無菌紗布進行過濾,并用足夠的無菌去離子水進行沖洗,除掉培養基的成分,以免殘余成分對Ag+離子的還原產生影響。得到2 g新鮮濕重的菌體,向其中加入20 mL無菌去離子水,搖晃均勻,在28 ℃,180 r/min的條件下培養3 d后,6 000 r/min離心5 min,收集上清液。
1.3.3銀納米粒子的合成
在攪拌下將100 mL AgNO3溶液逐滴地加入到10 mL的細胞濾液中,使AgNO3的最終濃度為1 mmol/L。銀納米粒子合成反應是在光輻射的條件下進行,用氙燈(500 W)模擬自然界中的太陽光。把同樣的反應溶液置于黑暗處做對照實驗。
1.4納米粒子的表征方法
1.4.1紫外—可見吸收光譜
在不同的反應時間取反應溶液,將其用去離子水稀釋兩倍后注入石英比色皿中,以去離子水為參比,在200~900 nm的波長范圍內,用紫外—可見分光光度計進行掃描,觀察反應過程中溶液吸收光譜的變化。
1.4.2X射線衍射
將反應30 min后的納米銀溶液滴到潔凈的單晶硅片上,待溶液自然晾干后,以CuKα為輻射源,在40 kV電壓和30 mA電流下,在35~90°范圍內以10°/min的速度掃描,進行XRD分析。
1.4.3透射電鏡
用移液槍吸取少量反應30 min后的溶液滴在稱量紙上,呈液滴狀。用鑷子夾住銅網,使銅網浸入液滴,大約30 s后,用鑷子將銅網取下,讓銅網在空氣中自然晾干,在加速電壓120 kV下對樣品進行TEM觀察。
2結果與討論
2.1肉眼觀察
為了合成銀納米粒子,在攪拌下將AgNO3溶液滴加到細胞濾液中,合成反應是在500 W氙燈的照射下進行。加入AgNO3溶液后,反應溶液立即出現輕微渾濁,我們推斷細胞濾液中可能含有某些陰離子,容易與Ag+離子形成不溶鹽;反應2 min后,溶液呈現微紅色;隨著反應時間的延長,溶液顏色逐漸加深至透明的紅褐色。圖1是濾液反應前后的顏色對比圖,圖1(a)是細胞濾液的顏色,呈淡黃色;反應30 min之后溶液顏色從淺黃色轉變為澄清的紅褐色(圖1(b))。紅褐色是銀納米粒子的特征顏色[13]。由于AgNO3溶液和細胞濾液顏色均很淺,根據顏色的變化初步斷定溶液中形成了銀納米粒子。相比以前報道的胞外生物合成銀納米粒子需幾小時,甚至是幾天[4],本研究反應所需的時間顯著縮短。將同樣的反應溶液置于黑暗中進行對照實驗,結果發現,在相同的時間內,反應溶液的顏色沒有任何變化,即沒有銀納米粒子的生成。由此推斷光在銀納米粒子的合成中起了關鍵作用。

(a) 細胞濾液顏色

(b) 與AgNO3溶液反應后的顏色
圖1青霉1-208的細胞濾液反應前后的顏色
Fig.1The colors of cell filtrate fromPenicilliumsp.1-208 before and after reaction with AgNO3solution
2.2紫外—可見吸收光譜表征
圖2展示了銀納米粒子合成過程中反應溶液隨著時間變化的紫外—可見吸收光譜圖。從曲線1中可以看出,青霉1-208的細胞濾液在300~800 nm范圍內沒有吸收峰。而AgNO3溶液與細胞濾液反應10 min后,在400~430 nm出現了1個明顯的吸收峰(曲線4)。已有文獻證實銀納米粒子的特征峰即表面等離子共振(SPR)峰出現在這個區域[14-15],說明反應溶液中生成了銀納米粒子。接著隨時間的增加,SPR峰逐漸升高,說明反應溶液中銀納米粒子的量也逐漸增加[16]。圖3反映了SPR峰的吸光度隨時間變化的關系圖。吸光度在反應初期顯著增加,隨后緩慢上升,這表明在該反應過程中前期反應速度非常快,后期相對緩慢,當反應到120 min時,吸光度不再增加,表明反應基本完成。

曲線1對應細胞濾液的吸收光譜,曲線2~13分別對應2、5、10、15、20、30、40、60、80、100、120、140 min時反應溶液的吸收光譜
圖2反應溶液在銀納米粒子合成過程中吸收光譜隨時間的變化
Fig.2The absorption spectra of reactionsolution as a function of reaction time

圖3細胞濾液與AgNO3溶液反應過程中吸光度隨時間的變化
Fig.3The absorbance changes against reactiontime during the cell filtrate interactingwith AgNO3solution
2.3XRD表征

圖中標記的峰是元素銀的特征衍射峰圖4 合成的銀納米粒子的XRD圖譜Fig.4 XRD pattern of the synthesized AgNPs
為進一步研究銀納米粒子的結構特性,將反應30 min后得到的銀納米粒子做XRD表征,結果如圖4所示。在銀納米粒子的XRD圖譜中,在38.1°和44.3°處的衍射峰分別對應于面心立方(fcc)銀晶體的Bragg衍射峰(111)和(200),這與大塊的具有面心立方結構銀的特征相一致,證實生成了銀納米晶體[17-18]。該樣品中銀顆粒所產生的衍射峰相對較寬,表明樣品中所形成的銀顆粒粒徑較小。值得注意的是,(111)衍射峰的強度遠高于(200)的衍射峰,這表明銀納米粒子優先沿著(111)面的方向生長[19]。同時,在46.2°、54.8°和57.4°處的衍射峰分別對應于氯化銀的Bragg衍射峰(220)、(311)和(222)[20],說明在反應過程中生成了氯化銀。由此推斷反應初期出現的輕微渾濁可能是因為生成了少量的氯化銀。
2.4TEM表征
TEM表征可以得到納米粒子的形貌、粒徑大小和分散情況的信息[21-22]。將反應30 min后所得的銀納米粒子進行TEM表征。圖5是具有代表性的銀納米粒子的電鏡圖。由圖5(a)中可以觀察到溶液中分布著大量的銀納米粒子,但納米粒子有明顯的團聚,呈不規則的形狀,團聚物的直徑約在20~50 nm,其中還有粒徑極小的納米粒子分散在溶液中。在放大倍數更高的情況下(圖5(b)),可以看到團聚物是由球形或近似球形的單個納米粒子組成的。根據TEM圖對單個納米粒子進行粒徑統計分析,為了確保數據的準確性,所統計的納米粒子的數目在200個以上,結果表明,合成的銀納米粒子的粒徑主要分布在3~12 nm,平均粒徑約為6 nm。

(a) 80 000放大倍數TEM圖

(b) 600 000放大倍數TEM圖
圖5胞外合成的銀納米粒子在不同放大倍數下的透射電鏡圖
Fig.5TEM images of the AgNPs at different magnifications
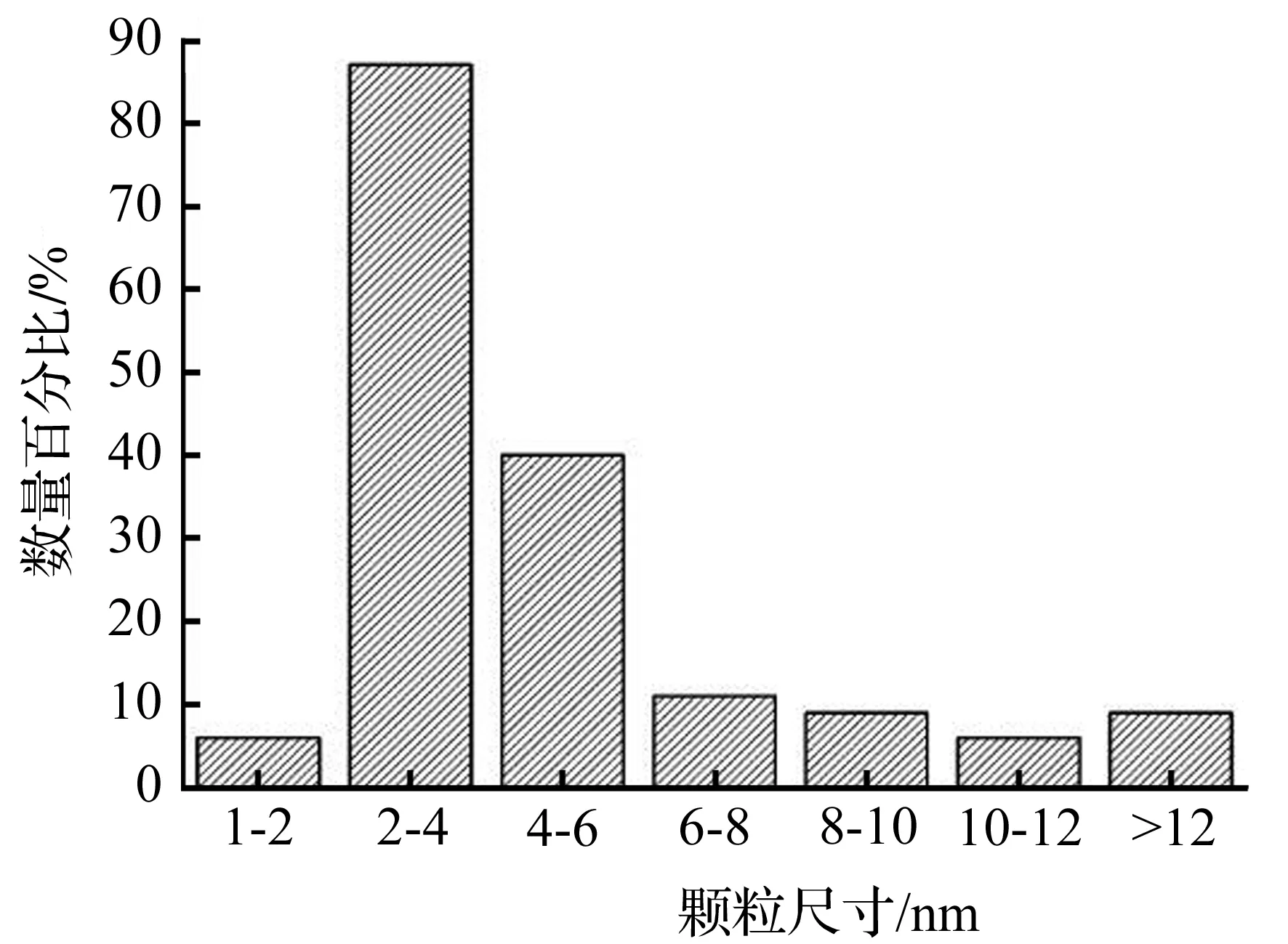
圖6 從TEM圖像中獲得的顆粒尺寸分布圖
3結語
本文在氙燈模擬太陽光的照射下,利用青霉1-208的胞外濾液快速合成銀納米粒子,并對合成的產物進行肉眼觀察、紫外—可見吸收光譜、XRD和TEM表征。結果表明,銀納米粒子是面心立方的晶體結構,并且優先沿著(111)面的方向生長;部分合成的銀納米粒子以團聚物的形式分散在溶液中,團聚物的直徑約在20~50 nm,其中,還有粒徑極小的納米粒子分散在溶液中,單個納米粒子的粒徑主要分布在3~12 nm,平均粒徑約為6 nm。在整個反應體系中,沒有加入額外的化學試劑和保護劑,合成條件溫和、無毒、無污染,反應速度快,說明該合成方法是一種綠色化學和環境友好的合成方法。
參考文獻:
[1]KLAUS T, JOERGER R, OLSSON E, et al.Silver-based crystalline nanoparticles, microbially fabricated[J]. Proceedings of the National Academy of Sciences, 1999, 96(24): 13611-13614.
[2]KLAUS-JOERGER T, JOERGER R, OLSSON E, et al.Bacteria as workers in the living factory: metal-accumulating bacteria and their potential for materials science[J]. Trends in Biotechnology, 2001, 19(1): 15-20.
[3]MUKHERJEE P, AHMAD A, MANDAL D, et al.Fungus-mediated synthesis of silver nanoparticles and their immobilization in the mycelial matrix: a novel biological approach to nanoparticle synthesis[J]. Nano Letters, 2001, 1(10): 515-519.
[4]AHMAD A, MUKHERJEE P, SENAPATI S, et al.Extracellular biosynthesis of silver nanoparticles using the fungusFusariumoxysporum[J]. Colloids and Surfaces B: Biointerfaces, 2003, 28(4): 313-318.
[5]KALIMUTHU K, BABU R S, VENKATARAMAN D, et al.Biosynthesis of silver nanocrystals byBacilluslicheniformis[J]. Colloids and Surfaces B: Biointerfaces, 2008, 65(1): 150-153.
[6]SAMADI N, GOLKARAN D, ESLAMIFAR A, et al.Intra/extracellular biosynthesis of silver nanoparticles by an autochthonous strain ofProteusmirabilisisolated from photographic waste[J]. Journal of Biomedical Nanotechnology, 2009,5(3): 247-253.
[7]HUSSEINY M I, EL-AZIZ M A, BADR Y, et al.Biosynthesis of gold nanoparticles usingPseudomonasaeruginosa[J]. Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy, 2007, 67(3): 1003-1006.
[8]GOPINATH V, VELUSAMY P.Extracellular biosynthesis of silver nanoparticles usingBacillussp.GP-23 and evaluation of their antifungal activity towardsFusariumoxysporum[J]. Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy, 2013, 106: 170-174.
[9]RODRIGUES A G, PING L Y, MARCATO P D, et al.Biogenic antimicrobial silver nanoparticles produced by fungi[J]. Applied Microbiology and Biotechnology, 2013, 97(2): 775-782.
[10]楊素玲,孟佑婷,劉桂君,等.利用產黃青霉培養液的上清液生物合成納米銀影響因素的研究[J]. 安徽農業科學,2013,41(2):503-504,506.
[11]WEI X T, LUO M F, LI W, et al.Synthesis of silver nanoparticles by solar irradiation of cell-freeBacillusamyloliquefaciensextracts and AgNO3[J]. Bioresource Technology, 2012, 103(1): 273-278.
[12]DU L W, XIAN L, FENG J X.Rapid extra-/intracellular biosynthesis of gold nanoparticles by the fungusPenicilliumsp.[J]. Journal of Nanoparticle Research, 2011, 13(3): 921-930.
[13]SANGHI R, VERMA P.Biomimetic synthesis and characterisation of protein capped silver nanoparticles[J]. Bioresource Technology, 2009, 100(1), 501-504.
[14]張杰,張映,郭瑞,等.鉤狀木霉生物合成納米銀及其殺菌性能[J]. 微生物學通報,2016,43(2):386-393.
[15]GANGULA A, PODILA R, M R, et al.Catalytic reduction of 4-nitrophenol using biogenic gold and silver nanoparticles derived fromBreyniarhamnoides[J]. Langmuir, 2011, 27(24): 15268-15274.
[16]白紅娟,賈萬利.固定化球形紅細菌生物合成銀納米材料及其抑菌性能研究[J]. 貴金屬,2013,34(1):8-12.
[17]WEI X T, ZHOU H C, XU L, et al.Sunlight-induced biosynthesis of silver nanoparticles by animal and fungus biomass and their characterization[J]. Journal of Chemical Technology and Biotechnology, 2014, 89(2): 305-311.
[18]GANESH BABU M M, GUNASEKARAN P.Production and structural characterization of crystalline silver nanoparticles fromBacilluscereusisolate[J]. Colloids and Surfaces B: Biointerfaces, 2009, 74(1): 191-195.
[19]ZHU Y P, WANG X K, GUO W L, et al.Sonochemical synthesis of silver nanorods by reduction of silver nitrate in aqueous solution[J]. Ultrasonics Sonochemistry, 2010, 17(4): 675-679.
[20]LIU C, YANG D, WANG Y G, et al.Fabrication of antimicrobial bacterial cellulose-Ag/AgCl nanocomposite using bacteria as versatile biofactory[J]. Journal of Nanoparticle Research, 2012, 14(8): 1-12.
[21]何秋星,李偉洲,陳權.水熱法制備納米Fe3O4的研究[J]. 廣西大學學報(自然科學版),2004,29(2):170-174.
[22]續京,張炎.化學沉淀法制備納米鈦酸鋇粉體[J]. 廣西大學學報(自然科學版),2011,36(3):445-449.
(責任編輯張曉云裴潤梅)
收稿日期:2015-11-30;
修訂日期:2016-04-15
基金項目:廣西自然科學基金資助項目(2012GXNSFGA060005,2013GXNSFBA019098)
通訊作者:杜良偉(198l—),女,河南南陽人,廣西大學副教授;E-mail:dulily@gxu.edu.cn。
doi:10.13624/j.cnki.issn.1001-7445.2016.0857
中圖分類號:TB383
文獻標識碼:A
文章編號:1001-7445(2016)03-0857-06
Biosynthesis and characterization of extracellular silver nanonparticles assisted by Penicillium sp.
XU Qiu-hong1, 2, HUANG Mei-ying1, 2, FENG Jia-xun2, 3, DU Liang-wei1, 2
(1.School of Chemistry and Chemical Engineering, Guangxi University, Nanning 530004, China;2.State Key Laboratory for Conservation and Utilization of Subtropical Agro-bioresources,Guangxi University, Nanning 530004, China;3.College of Life Science and Technology, Guangxi University, Nanning 530004, China)
Abstract:In order to explore green and efficient methods for the synthesis of nanoparticles, extracellular silver nanoparticles (AgNPs) were rapidly synthesized assisted by the cell filtrates of Penicillium sp. 1-208 under simulated sunlight. The synthesized AgNPs were characterized by means of visual observation, UV-Vis absorption spectroscopy, X-ray diffraction (XRD) and transmission electron microscopy (TEM). The XRD results showed that the synthesized AgNPs were crystalline in nature and preferentially oriented in (111) plane. The TEM results showed that most of the nanoparticles dispersed in solution in the form of agglomerated structure, in which the single nanoparticles were spherical in shape with average particle size of 6 nm and the diameter of agglomerated structure with irregular shape ranged from 20 to 50 nm. The approach used in this study is a green and environment-friendly synthesis method with the advantage of mild condition, clean, non-toxicity and non-polluting.
Key words:Penicillium sp.; biosynthesis; silver nanoparticles; light radiation
引文格式: 徐秋紅,黃梅穎,馮家勛,等.青霉胞外合成銀納米粒子及其表征[J].廣西大學學報(自然科學版),2016,41(3):857-862.

