阿瑞匹坦治療化療誘導的爆發性惡心嘔吐的臨床觀察
鄭 琪, 廖子君, 李 旭, 郭亞煥, 徐 瑞, 張彥兵, 周 菁, 翟 陽
(西安交通大學醫學院附屬陜西省腫瘤醫院內一科,西安 710061)
阿瑞匹坦治療化療誘導的爆發性惡心嘔吐的臨床觀察
鄭琪, 廖子君, 李旭, 郭亞煥, 徐瑞, 張彥兵, 周菁, 翟陽
(西安交通大學醫學院附屬陜西省腫瘤醫院內一科,西安710061)
摘要:目的評價阿瑞匹坦治療化療誘導的爆發性嘔吐的有效性和安全性。 方法收集2014-01~2016-01我科出現化療誘導的爆發性惡心嘔吐病例24例,所有患者化療前均使用包含5-羥色胺受體拮抗劑、地塞米松在內的兩聯預防止吐方案,之后的24-72 h所有患者均出現了難以忍受的Ⅱ-Ⅲ度爆發性惡心嘔吐。給予患者肌肉注射甲氧氯普胺10 mg,待惡心嘔吐癥狀有所減輕后,口服阿瑞匹坦(第1日口服125 mg,第2-3日口服80 mg)解救治療,詳細記錄用藥后72 h內反應情況,并對療效和多種臨床因素間的關系進行分析。結果用藥患者的惡心嘔吐總緩解率達到83.3%(20/24),完全緩解率62.5%(15/24),部分緩解率20.8%(5/24),無反應率16.7%(4/24),未見明顯不良反應。統計分析顯示,惡心嘔吐的緩解率與患者性別、年齡、既往化療史、化療方案的致吐風險及患者活動狀態評分等臨床因素無明顯相關性(P>0.05)。結論 阿瑞匹坦對化療誘導的爆發性嘔吐具有良好的療效,安全性好,可作為解救性治療的藥物之一。
關鍵詞:阿瑞匹坦;化療誘導;爆發性惡心嘔吐
化療誘導的惡心嘔吐(chemotherapy-induced nausea and vomiting,CINV)是化療最常見的不良反應之一,惡心、嘔吐對患者的生理、心理和社會功能均可能造成明顯損害,未控制的CINV可導致患者出現代謝紊亂、營養失調及對治療的恐懼心理,嚴重影響患者的生活質量和治療依從性。科學合理地預防和處理CINV,是抗腫瘤治療順利進行的基本保障之一。
腫瘤治療相關嘔吐防治指南(2014版)指出,CINV可分為急性、延遲性、預期性、爆發性及難治性5種類型。急性CINV一般發生在給藥數分鐘至數小時,并在給藥后5-6 h達高峰,多在24 h內緩解;延遲性CINV多在化療24 h之后發生,可持續數天;預期性CINV是指患者在前一次化療時經歷了難以控制的惡心、嘔吐之后,在下一次化療開始之前即發生的惡心嘔吐,是一種條件反射,主要由于精神、心理因素等引起;爆發性CINV是指即使進行了預防處理但仍出現的嘔吐,并需要進行“解救性治療”;難治性CINV是指以往的化療周期中使用預防性和/或解救性止吐治療失敗,而在接下來的化療周期中仍然出現嘔吐[1]。
阿瑞匹坦、5-羥色胺受體拮抗劑加地塞米松的三藥聯合已被NCCN指南推薦用于高致吐性化療方案的預防止吐治療,無論在急性CINV還是在延遲性CINV的防治中均獲得了良好的療效,但有關阿瑞匹坦在爆發性CINV中的作用目前國內外文獻罕有報道。
本文回顧性總結了2014-2015年我科在臨床中使用阿瑞匹坦治療爆發性CINV的病例,通過對療效及其副反應分析,以評價阿瑞匹坦在爆發性CINV治療中的有效性和安全性,現報道如下。
1資料與方法
1.1一般資料
收集2014-01~2016-01我科使用阿瑞匹坦治療CINV的患者,從85例病例中篩選出24例使用阿瑞匹坦解救爆發性CINV的患者,包括肺癌8例,胃癌8例,結直腸癌4例,膽囊癌1例,卵巢癌1例,輸尿管癌1例,肝小細胞癌1例。年齡28-70歲,男12例,女12例。其中19例患者接受了含有順鉑方案的化療,5例接受了含有奧沙利鉑方案的化療。所有患者化療前均常規使用了包含5-HT3受體拮抗劑、地塞米松在內的兩聯止吐方案。
CINV評價標準:化療期間出現Ⅱ度或Ⅱ度以上的CINV定義為爆發性CINV。根據常見不良反應評價標準(common terminology criteria for adverse events,CTC-AE 4.0版)進行分級。①惡心程度分級:0 度,無惡心;Ⅰ度,食欲不振但無飲食習慣的改變;Ⅱ度,進食量減少但無明顯的體重降低,脫水或營養不良輸液補液<24 h ;Ⅲ度,熱量或體液量不足需靜脈補液或全靜脈營養>24 h;Ⅳ度,出現危及生命的后果;Ⅴ度,死亡。②嘔吐程度分級:0度,24 h內無嘔吐;Ⅰ度,24 h內嘔吐<1次;Ⅱ度,24 h內嘔吐2-5次,需靜脈補液但<24 h;Ⅲ度,24 h內嘔吐>6次,需靜脈補液或全胃腸外營養>24 h;Ⅳ度,出現危及生命的后果;Ⅴ度,死亡。
患者活動狀態(performance status,PS)采用美國東部腫瘤協作組(Eastern Cooperative Oncology Group,ECOG)評分系統,將患者的PS分為6個等級:0分,無癥狀,能正常活動;1分,有癥狀,一般行動自由,較重的體力活動受到限制;2分,不能工作,生活尚能自理,白天臥床時間不超過50%;3分,生活僅能部分自理,白天臥床時間超過50%;4分,臥床不起,生活不能自理;5分,死亡。
根據上述標準,評估24例患者在化療后24-72 h內出現的惡心嘔吐。所有患者均排除顱內壓增高、胃腸道梗阻或其他藥物所致的惡心、嘔吐。
1.2治療方法
當患者出現爆發性CINV后,首先使用甲氧氯普胺10 mg肌肉注射,待惡心嘔吐癥狀有所緩解,不影響口服藥物的情況下,給予阿瑞匹坦解救治療方案(第1天阿瑞匹坦125 mg,第2-3天80 mg),同時輸液營養支持治療。觀察所有患者用藥期間(72 h)CINV的緩解情況。
1.3觀察指標
完全緩解(complete response,CR):惡心、嘔吐均為0度;部分緩解(partial response,PR):有Ⅰ度惡心或嘔吐;無效:惡心或嘔吐達Ⅱ度及以上。總有效率(RR)=(CR+PR)/總例數×100%。
1.4統計學方法
采用SPSS19.0統計學軟件進行數據統計分析,采用四格表卡方檢驗,P<0.05表示差異具有統計學意義。
2結果
2.1基本特征
自2014-01~2016-01共收集到24例爆發性CINV患者的臨床資料,患者的年齡、性別、既往化療史、ECOG-PS評分見表1。
2.2療效分析
24例患者的爆發性CINV均發生于化療24 h后,屬于遲發性CINV。解救治療后,20例患者的CINV得到緩解,總有效率83.3%(20/24),其中完全緩解率62.5%(15/24),部分緩解率20.8%(5/24),無反應率16.7%(4/24)。通過統計學分析,CINV的緩解與患者性別、年齡、既往化療史、化療方案的致吐風險等級及ECOG-PS評分等臨床因素無明顯相關性(P>0.05,見表1)。
2.3不良反應
所有患者中,除2例患者出現輕度頭暈外(無法確定是否與使用阿瑞匹坦有關),未發現其他明顯不良反應。
3討論
隨著醫學的進步,無論是急性CINV還是遲發性CINV的防治均取得了較大進展,但對于爆發性CINV的的治療仍然是一個難題[2-4],爆發性CINV的臨床研究也相對較少[5-7]。目前國內外嘔吐治療
表1阿瑞匹坦對爆發性CINV的療效分析(例)
Table 1Effectiveness of aprepitant in treatment of breakthrough CINV(cases)
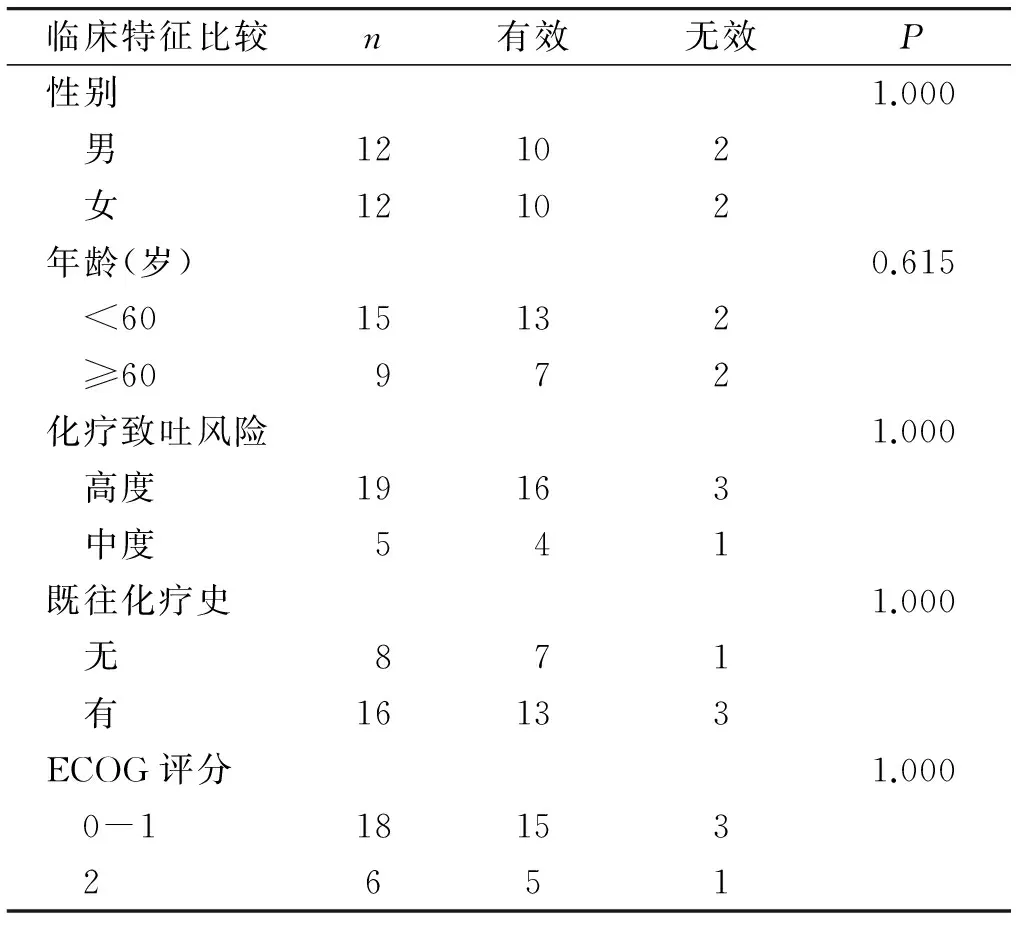
臨床特征比較n有效無效P性別1.000 男12102 女12102年齡(歲)0.615 <6015132 ≥60972化療致吐風險1.000 高度19163 中度541既往化療史1.000 無871 有16133ECOG評分1.000 0-118153 2651
指南均建議,出現爆發性CINV的患者原則上應選用預防性止吐方案中未用過的止吐藥物,如吩噻嗪類、甲氧氯普胺、地塞米松、丁酰苯類、大麻素類、抗膽堿能類藥物和奧氮平[1,7]。一項Ⅱ期臨床研究中指出,丙氯拉嗪(prochlorperazine,奮乃靜)或口服5-HT3受體拮抗劑對CINV具有良好療效,短期有效率達到了75%[8];另一項Ⅱ期臨床研究報道,在CINV患者的掌面皮膚使用含有勞拉西泮(lorazepam)、苯海拉明(diphenhydramine)、氟哌啶醇(haloperidol)的透皮凝膠,對CINV亦有良好療效[9];近期報道的一項Ⅱ期臨床研究發現,口服精神類藥物奧氮平(olanzapine)5 mg、12 h 1次,爆發性嘔吐的完全緩解率、干嘔的控制率和惡心的控制率分別達到了60.9%、71.7%和50.0%,副反應輕微[10]。奧氮平和甲氧氯普胺是國內外指南均推薦用于爆發性CINV的藥物,一項Ⅲ期、雙盲、隨機對照研究對比了兩者在爆發性CINV中的療效。結果顯示,奧氮平對于爆發性CINV的療效要顯著優于后者[11]。但在國內的臨床實踐中,奧氮平尚未被中國國家食品藥品監督管理局(CFDA)批準用于治療爆發性CINV,作為治療精神分裂癥的藥物,其處方受到了嚴格限制,難以推廣使用。
阿瑞匹坦是P物質/神經激肽-1(NK-1)受體的一種選擇性高親和力阻斷劑,其對NK1受體的親和力是其他受體的3 000倍以上,對5-羥色胺、多巴胺和皮質激素受體親和力低或無,且可透過血腦屏障阻斷NK1,通過中樞機制抑制CINV[12-14]。多項臨床研究已經證實,在接受中、高度致吐藥物治療的患者中,阿瑞匹坦、5-羥色胺受體拮抗劑及地塞米松的三藥聯合可顯著提高患者的完全緩解率(無嘔吐且無需解救治療),并且在肺癌、胃癌、大腸癌、乳腺癌、惡性黑色素瘤等多種惡性腫瘤中均有顯著的止吐作用[15-17]。但是,目前國內外指南推薦阿瑞匹坦主要用于高致吐性化療方案所致CINV的預防性治療中,對于爆發性CINV的治療罕見報道[18]。另一方面,阿瑞匹坦雖然于2013年被中國國家食品藥品監督管理局批準在國內上市,用于預防高致吐性化療的初次和重復給藥過程中出現的CINV,但由于其價格較高、未能進入醫保等因素,在西部地區仍然未能普遍用于高致吐性化療方案的止吐治療中。
我科從2014年開始在臨床上使用阿瑞匹坦治療CINV,其療效顯著。由于患者經費和報銷問題(未進入醫保目錄,無法報銷),部分患者化療前不接受在預防止吐方案中加入阿瑞匹坦,但在出現爆發性惡心嘔吐后試用阿瑞匹坦進行解救治療,取得令人滿意的療效。本研究匯總了我科兩年來24例使用阿瑞匹坦治療爆發性CINV的臨床病例,通過觀察和統計分析,爆發性CINV患者使用阿瑞匹坦后,CINV的總緩解率達到了83.3%,化療相關消化道反應明顯減輕,生活質量得到改善,有利于后續治療的順利進行。經過隨訪后,三分之二的患者(16/24)在下一周期的化療中選擇阿瑞匹坦作為預防性止吐用藥。
研究結果還提示,阿瑞匹坦控制爆發性CINV的療效與患者性別、年齡、既往化療史、化療方案的致吐風險等級及ECOG-PS評分等臨床因素無明顯相關性。但由于研究樣本量偏小(24例),尚需要大樣本的臨床研究進一步證實。國外一項隨機對照的Ⅲ期臨床研究顯示,阿瑞匹坦在男性和≥55歲的人群中有效率更高,但可能受到不同化療方案的影響。在各個年齡、性別、地域分組中阿瑞匹坦組止吐療效均優于無阿瑞匹坦組[19]。本研究中,80%(19/24)的患者使用含有順鉑的高致吐性化療方案,其余5例患者均為使用中度致吐性化療方案(FOLFOX,奧沙利鉑+氟尿嘧啶)。患者首次爆發性惡心嘔吐均見于化療24 h后,屬于遲發性CINV。此時常規的兩聯止吐方案(5-HT3受體拮抗劑+地塞米松)仍然在使用過程中。研究發現,急性CINV的發生主要與5-HT3的釋放有關,所以此時使用5-HT3受體拮抗劑效果較好,而遲發性CINV中主要與P物質有關,所以NK-1受體拮抗劑理論上對于遲發性CINV療效更佳[1,20]。
國外研究結果顯示,阿瑞匹坦的安全性良好[21],常見副反應主要有便秘,其他副反應少見且輕微。在本研究中,阿瑞匹坦使用后未觀察到明顯的不良反應,僅2人出現輕度頭暈,不過由于化療期間同時使用了多種藥物,無法判定是否與阿瑞匹坦有關。雖然安全性良好,但阿瑞匹坦的主要代謝途徑是經細胞色素P450同工酶CYP3A4參與完成的,因此需注意阿瑞匹坦與其他同樣經CYP3A4代謝藥物間的相互作用,必要時調整其他藥物用量。
阿瑞匹坦的不足之處在于其劑型為口服制劑,部分發生CINV的患者由于惡心嚴重,飲水后即出現嘔吐,無法順利口服藥物,此時服用阿瑞匹坦可能在藥物未起效時即被嘔出,造成失效和浪費。故建議爆發性CINV的患者首次使用阿瑞匹坦前,給予速效止吐針劑(如甲氧氯普胺,甲氧氯普胺禁忌患者可選用異丙嗪、溴米那普魯卡因胺等藥物)暫時緩解惡心嘔吐,然后口服藥物,同時加強補液支持治療,維持水電解質平衡,保證治療的順利進行。甲氧氯普胺雖然對爆發性CINV有一定療效,但其半衰期短,增加劑量和使用頻率后錐體外系反應的發生率明顯升高,所以用來配合阿瑞匹坦治療更為適合。
另外,對于一些特殊患者,如食管癌、頭頸部腫瘤導致吞咽困難的患者,阿瑞匹坦的應用受到限制。不過,該問題有望被阿瑞匹坦的靜脈劑型(福沙匹坦)解決。福沙匹坦是阿瑞匹坦的前體藥物,注射后在體內迅速轉化成阿瑞匹坦,2010年該藥物已在美國獲批上市,但在我國尚未獲批。臨床研究顯示,福沙匹坦與NK-1受體的結合效率和阿瑞匹坦相當[22]。國產福沙匹坦的Ⅲ期臨床試驗于2015年已經完成,如果順利上市的話,可能解決國內口服給藥困難的患者的問題。
綜上所述,本研究結果表明,阿瑞匹坦對爆發性CINV具有良好的臨床療效,可改善化療患者的生活質量,安全性良好,值得進一步研究。
參考文獻:
[1]中國抗癌協會癌癥康復與姑息治療專業委員會(CRPC),中國臨床腫瘤學會抗腫瘤藥物安全管理專家委員會(ASMC).腫瘤治療相關嘔吐防治指南(2014版)[J].臨床腫瘤學雜志,2014,19(3):263-273.
[2]Tina Shih YC,Xu Y,Elting LS.Costs of uncontrolled chemotherapy-induced nausea and vomiting among working-age cancer patients receiving highly or moderately emetogenic chemotherapy[J].Cancer,2007,110(3):678-685.
[3]Grunberg SM,Deuson RR,Mavros P,etal.Incidence of chemotherapy-induced nausea and emesis after modern antiemetics[J].Cancer,2004,100(10):2261-2268.
[4]Hickok JT,Roscoe JA,Morrow GR,etal.Nausea and emesis remain significant problems of chemotherapy despite prophylaxis with 5-hydroxytryptamine-3 antiemetics: a University of Rochester James P. Wilmot Cancer Center Community Clinical Oncology Program Study of 360 cancer patients treated in the community[J].Cancer,2003,97(11):2880-2886.
[5]Roila F,Herrstedt J,Aapro M,etal.Guideline update for MASCC and ESMO in the prevention of chemotherapy-and radiotherapy-induced nausea and vomiting:results of the Perugia consensus conference[J].Ann Oncol,2010,21 Suppl 5:v232-243.
[6]Basch E,Prestrud AA,Hesketh PJ,etal.Antiemetics:American Society of Clinical Oncology clinical practice guideline update[J].J Clin Oncol,2011,29(31):4189-4198.
[7]National Comprehensive Cancer Network(NCCN).NCCN Clinical Practice Guidelines in Oncology Version 2.2015:Antiemesis,National Comprehensive Cancer Network (NCCN),2015[EB/OL].http://www.nccn.org/professionals/physician gls/PDF/antiemesis.pdf[2016-03-06].
[8]Jones JM,Qin R,Bardia A,etal.Antiemetics for chemotherapy-induced nausea and vomiting occurring despite prophylactic antiemetic therapy[J].J Palliat Med,2011,14(7):810-814.
[9]Bleicher J,Bhaskara A,Huyck T,etal.Lorazepam,diphenhydramine,and haloperidol transdermal gel for rescue from chemotherapy-induced nausea/vomiting:results of two pilot trials[J].J Support Oncol,2008,6(1):27-32.
[10]Chanthawong S,Subongkot S,Sookprasert A.Effectiveness of olanzapine for the treatment of breakthrough chemotherapy induced nausea and vomiting[J].J Med Assoc Thai,2014,97(3):349-355.
[11]Navari RM,Nagy CK,Gray SE.The use of olanzapine versus metoclopramide for the treatment of breakthrough chemotherapy-induced nausea and vomiting in patients receiving highly emetogenic chemotherapy[J].Support Care Cancer,2013,21(6):1655-1663.
[12]Tattersall FD,Rycroft W,Francis B,etal.Tachykinin NK1 receptor antagonists act centrally to inhibit emesis induced by the chemotherapeutic agent cisplatin in ferrets[J].Neuropharmacology,1996,35(8):1121-1129.
[13]Huskey SE,Dean BJ,Bakhtiar R.Brain penetration of aprepitant,a substance P receptor antagonist,in ferrets[J].Drug Metab Dispos,2003,31(6):785-791.
[14]Bergstr?m M,Hargreaves RJ,Burns HD,etal.Human positron emission tomography studies of brain neurokinin 1 receptor occupancy by aprepitant[J].Biol Psychiatry,2004,55(10):1007-1012.
[15]Aapro MS,Schmoll HJ,Jahn F,etal.Review of the efficacy of aprepitant for the prevention of chemotherapy-induced nausea and vomiting in a range of tumor types[J].Cancer Treat Rev,2013,39(1):113-117.
[16]Hesketh PJ,Grunberg SM,Gralla RJ.The oral neurokinin-1 antagonist aprepitant for the prevention of chemotherapy-induced nausea and vomiting:a multinational,randomized,double-blind,placebo-controlled trial in patients receiving high-dose cisplatin-the Aprepitant Protocol 052 Study Group[J].J Clin Oncol,2003,21(22):4112-4119.
[17]毛麗麗,斯璐,王軒.阿瑞匹坦對黑色素瘤患者順鉑治療引起惡心嘔吐的止吐作用[J].腫瘤防治研究,2015,42(7):712-715.[18]Navari RM.Treatment of Breakthrough and Refractory Chemotherapy-Induced Nausea and Vomiting[J].Biomed Res Int,2015,2015:595894.
[19]Uchino J,Hirano R,Tashiro N,etal.Efficacy of aprepitant in patients with advanced or recurrent lung cancer receiving moderately emetogenic chemotherapy[J].Asian Pac J Cancer Prev,2012,13(8):4187-4190.
[20]Curran MP,Robinson DM.Aprepitant:a review of its use in the prevention of nausea and vomiting[J].Drugs,2009,69(13):1853-1078.
[21]Ruhlmann CH,Herrstedt J.Safety evaluation of aprepitant for the prevention of chemotherapy-induced nausea and vomiting[J].Expert Opin Drug Saf,2011,10(3):449-462.
[22]Van Laere K,De Hoon J,Bormans G,etal.Equivalent dynamic human brain NK1-receptor occupancy following single-dose i.v.fosaprepitantvs.oral aprepitant as assessed by PET imaging[J].Clin Pharmacol Ther,2012,92(2):243-250.
Clinical observation on the effects of aprepitant in the treatment of breakthrough chemotherapy-induced nausea and vomiting
ZHENG Qi, LIAO Zijun, LI Xu, GUO Yahuan, XU Rui, ZHANG Yanbing, ZHOU Jing, ZHAI Yang
(FirstDepartmentofMedicalOncology,AffiliatedShaanxiProvincialCancerHospital,CollegeofMedicine,Xi’anJiaotongUniversity,Xi’an710061,China)
Abstract:ObjectiveTo evaluate the efficacy and safety of aprepitant in treating breakthrough chemotherapy-induced nausea and vomiting. MethodsTwenty-four patients who experienced breakthrough chemotherapy-induced nausea and vomiting from January 2014 to January 2016 were collected. All patients were given two-agent prophylaxis schedule including 5-HT3 receptor antagonists and dexamethasone before chemotherapy, and exhibited unbearable Ⅱ-Ⅲ nausea and vomiting in the following 24-72 h. Rescue schedule(oral 125 mg aprepitant at the first day,80 mg at the second and third day)was administered when the symptoms of nausea and vomiting were partly relieved by intramuscular injection of 10 mg metoclopramide. Then reactions of therapy in 72 h were recorded in detail, and the relationship between the efficacy and a series of clinical parameters were analyzed.ResultsThe overall successful rate of aprepitant was 83.3%(20/24), including a complete response rate of 62.5%(15/24), a partial response rate of 20.8%(5/24)and a non-response rate of 16.7%(4/24). No obvious adverse effects were observed. The successful rate was not related with gender, age, chemotherapy history, emetogenicity of chemotherapy regimens, and performance status score(P>0.05).ConclusionAprepitant demonstrate high efficacy and safety in the treatment of breakthrough chemotherapy-induced nausea and vomiting, and can serve as a rescue therapy agent.
Key words:aprepitant;chemotherapy induction;breakthrough nausea and vomiting
作者簡介:鄭琪,男,1979-03生,博士,主治醫師,E-mail:snowpinezq@163.com
收稿日期:2016-03-06
中圖分類號:R730.5
文獻標志碼:A
文章編號:1007-6611(2016)06-0539-05
DOI:10.13753/j.issn.1007-6611.2016.06.012

