奧卡西平納米脂質載體包封率的測定*
金銀秀,王玉新,石 雷,沈佩佩,夏念友,游錦晨,李姿生
(臺州職業技術學院 化學制藥研究所,浙江 臺州 318000)
奧卡西平(Oxcarbazepine,OXC)是一種治療癲癇部分發作和全身強直陣孿性發作的新藥[1]。與卡馬西平相比,具有不良反應少、自身誘導作用小等優點,其體內過程主要通過胃腸道快速吸收并迅速、幾乎完全降解為有藥理活性的代謝產物10,11-二氫-10-羥基卡馬西平(monohydroxycarbazepine,MHD)而發揮作用[2]。但由于OXC幾乎不溶于水,其普通制劑在水中不易潤濕和擴散,用常規的制劑輔料和分散系統制備的口服劑型在胃腸液中易于結晶或沉淀析出,極大地影響了藥物的溶出和吸收。近年來,出現了一些新型的藥物傳遞系統,其中納米脂質載體受到了越來越多的關注[3-5]。納米脂質載體具有脂質藥物載體的固有優勢:難溶性藥物在脂質成分中表現出良好的溶解度,引入液體脂質可以增加藥物的包封率和載藥量;所使用的脂質具有生理相容性,體內毒性低;納米粒子的固體骨架結構使其具有良好的穩定性;具備與固體脂質納米粒相似的緩控釋特性[6-7]。因此進行OXC納米脂質載體的研究是解決上述問題的有益探索。納米脂質載體易于加工成傳統劑型,如片劑、膠囊等[6]。作者研究制備了OXC納米脂質載體,可以進一步制成凍干粉以供臨床使用。為了更好地控制OXC納米脂質載體的質量,建立了其包封率的測定方法。
1 實驗部分
1.1 試劑與儀器
奧卡西平對照品:批號100657-201102,中國食品藥品檢定研究院,供含量測定用;奧卡西平:批號140530,質量分數99.8%,浙江九洲藥業股份有限公司;卵磷脂:批號J1422068,質量分數>70%,阿拉丁試劑(上海)有限公司;大豆油:批號20140429,上海嘉里食品工業有限公司;聚山梨酯80(Tween-80):批號20131220,上海強順化學試劑有限公司;葡聚糖凝膠( Sephadex G50):批號20140703,臺州市路橋四甲生化塑料廠;乙腈、甲醇:色譜純;水為蒸餾水,其它試劑均為分析純,市售。
Agilent 1220型高效液相色譜儀:可變波長檢測器,美國Agilent公司;RE-52AA 型旋轉蒸發器:上海亞榮生化儀器廠;DF-101S型集熱式磁力加熱攪拌儀:金壇市精達儀器制造廠;Scientz-IID型超聲波細胞粉碎機:寧波新芝生物科技有限公司;GL-20M型高速冷凍離心機:上海盧湘儀離心機儀器有限公司。
1.2 OXC納米脂質載體制備[8]
1.2.1 OXC納米脂質載體制備
取10 mg OXC,0.1 g卵磷脂,0.15 g大豆油,0.4 g Tween-80精密稱定,溶解于10 mL乙酸乙酯中,超聲至完全溶解,構成有機相。將有機相倒入30 mL水中,充分攪拌,超聲1 min,得乳濁液;將得到的乳濁液進行旋轉蒸發,除去有機溶劑乙酸乙酯,得到澄清均一的溶液即為奧卡西平納米脂質載體。
1.2.2 空白納米脂質載體的制備
取除主藥OXC外的其它成分按“1.2.1”項下方法制備,即得空白納米脂質載體。
1.3 OXC含量測定方法的建立
1.3.1 色譜條件
色譜柱Agilent ZORBAX C18(4.6 mm×250 mm,5 μm);流動相0.01 mol/L磷酸鹽緩沖液(含質量分數0.2%的三乙胺,用磷酸調節pH= 4.5)-乙腈-甲醇(體積比為15∶45∶40);流速1.2 mL/min;柱溫50 ℃;檢測波長254 nm;進樣量20 μL。
1.3.2 溶液制備
取OXC納米脂質載體及空白納米脂質載體各1 mL,加流動相定容至10 mL,超聲5 min,破壞其脂質結構,作為供試品溶液和空白樣品溶液。取OXC 0.010 0 g精密稱定,流動相溶解定容至25 mL,精密吸取1.0 mL至10 mL量瓶中,用流動相定容,得到質量濃度為40.00 μg/mL的OXC對照品溶液。
1.3.3 方法學考察
1.3.3.1 專屬性
取空白樣品溶液、OXC對照品溶液和供試品溶液,按“1.3.1”項下色譜條件進樣測定,記錄色譜圖。
1.3.3.2 線性關系考察
取OXC 0.010 4 g精密稱定,用流動相定容至250 mL作為母液,分別稀釋為質量濃度0.16、0.31、0.62、1.04、2.16、5.16、20.8、31.2、41.6 μg/mL溶液,按“1.3.1”項下色譜條件進樣測定,記錄峰面積。
1.3.3.3 儀器精密度實驗
精密量取1.04 μg/mL對照品溶液,按“1.3.1”項下色譜條件重復進樣測定 6 次。
1.3.3.4 重復性實驗
取同一批樣品,平行6份,按“1.3.2”項下方法處理,進樣測定。
1.3.3.5 回收率實驗
精密移取9份空白納米脂質載體溶液1 mL,分別加入OXC對照品溶液,流動相定容至10 mL量瓶中,制成質量濃度分別為0.324、3.24、32.4 μg/mL的溶液,按“1.3.1”項下色譜條件進樣測定,記錄峰面積,計算回收率。
1.4 包封率測定方法
1.4.1 葡聚糖凝膠柱層析法
1.4.1.1 洗脫曲線的建立
采用葡聚糖凝膠柱層析法分離載藥納米脂質載體,HPLC法測定游離藥物的含量。稱取葡聚糖凝膠(G50)2.5 g,加純化水水浴加熱煮沸溶脹2 h,靜置溶脹12 h。裝柱平衡,精密吸取OXC納米脂質載體溶液1 mL上樣,用純化水洗脫,流速1.5 mL/min,每管1 mL,收集洗脫液40管后,改用質量分數50%的甲醇洗脫,收集洗脫液40管[9]。洗脫下來的溶液每毫升加無水甲醇2 mL,加流動相2 mL,渦旋15 s,用0.22 μm的有機膜過濾,按“1.3.1”項下色譜條件進樣測定。
1.4.1.2 柱回收率實驗
精密吸取OXC納米脂質載體溶液1 mL,按上述方法過柱分離,取全部80 mL洗脫液,旋轉蒸發濃縮至干,甲醇清洗旋蒸瓶并定容至10 mL,超聲5 min后,按“1.3.1”項下色譜條件進樣測定。另取OXC納米脂質載體溶液1 mL,甲醇定容至10 mL,超聲5 min后,同法測定,計算柱回收率。
1.4.1.3 包封率的測定
取OXC納米脂質載體溶液1 mL,加無水甲醇2 mL,加流動相2 mL,渦旋15 s用0.22 μm的有機膜過濾,按“1.3.1”項下色譜條件進樣測定,計算含量,得到OXC納米脂質載體溶液中藥物總量為ρ總,按上述方法,用純化水洗脫,收集洗脫液前40 mL,旋轉蒸發濃縮至干,甲醇清洗旋蒸瓶并定容至10 mL,超聲5 min后,按“1.3.1”項下色譜條件進樣測定,計算含量,得到OXC納米脂質載體包封藥物的ρ包。OXC納米脂質載體包封率=ρ包/ρ總。
1.4.2 高速冷凍離心法[9]
1.4.2.1 方法學驗證
取處方量的OXC精密稱定,純化水定容至25 mL,取2 mL置離心管中高速冷凍離心(離心條件為22 000 r/min,4 ℃)45 min,傾去上層清液,用甲醇溶解底部沉淀物并定容至10 mL,按“1.3.1”項下色譜條件進樣測定。將空白納米脂質載體溶液按上述方法離心。將處方量的OXC與空白納米脂質載體溶液混合,按上述方法離心并測定。
1.4.2.2 包封率測定
精密吸取OXC納米脂質載體溶液2 mL按“1.4.2.1”項下方法離心并分析測定,計算游離藥物的ρ游。精密吸取OXC納米脂質載體溶液2 mL,用甲醇定容至10 mL,超聲10min破乳,破乳后液體取0.5 mL稀釋至10 mL,按“1.3.1”項下色譜條件進樣測定,計算出總藥物的質量濃度ρ總。OXC納米脂質載體包封率=(1-ρ游/ρ總)×100%。
2 結果與討論
2.1 方法學考察結果
專屬性實驗色譜圖見圖1。
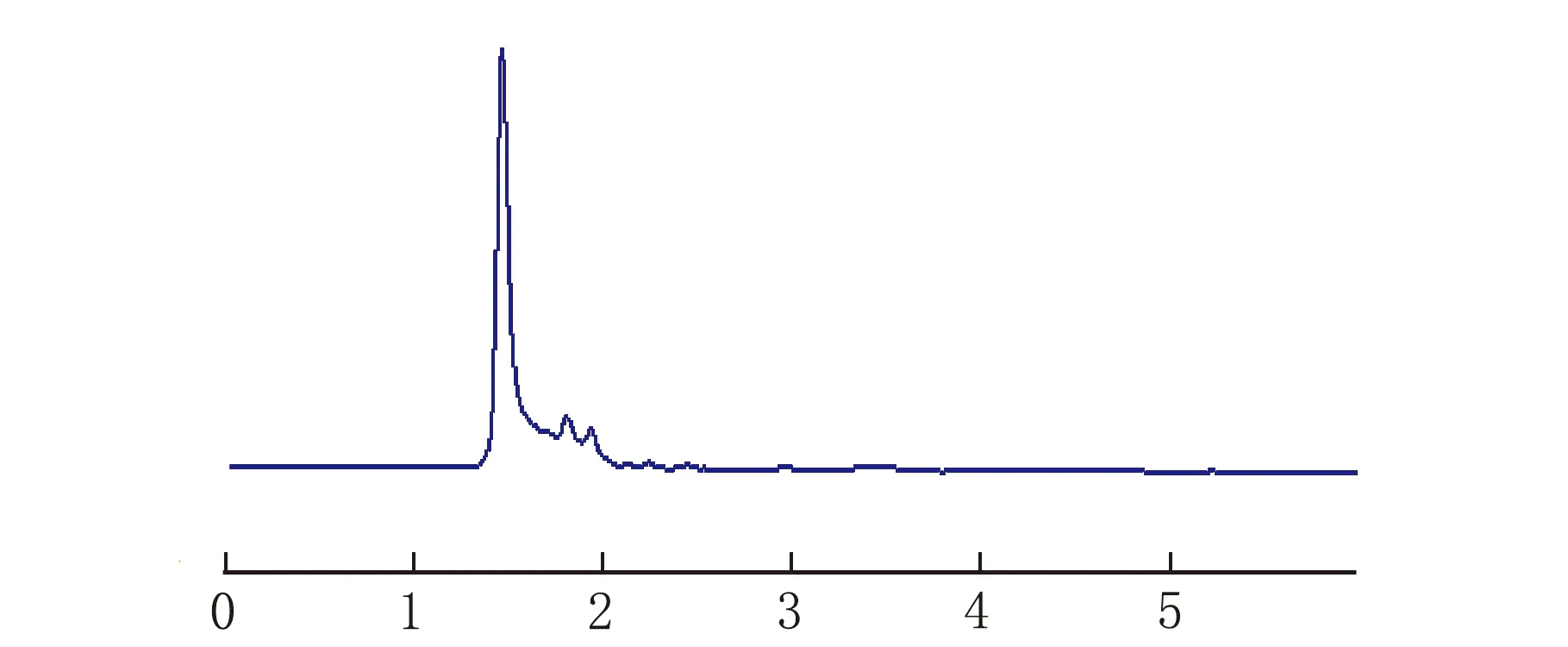
t/min空白樣品溶液
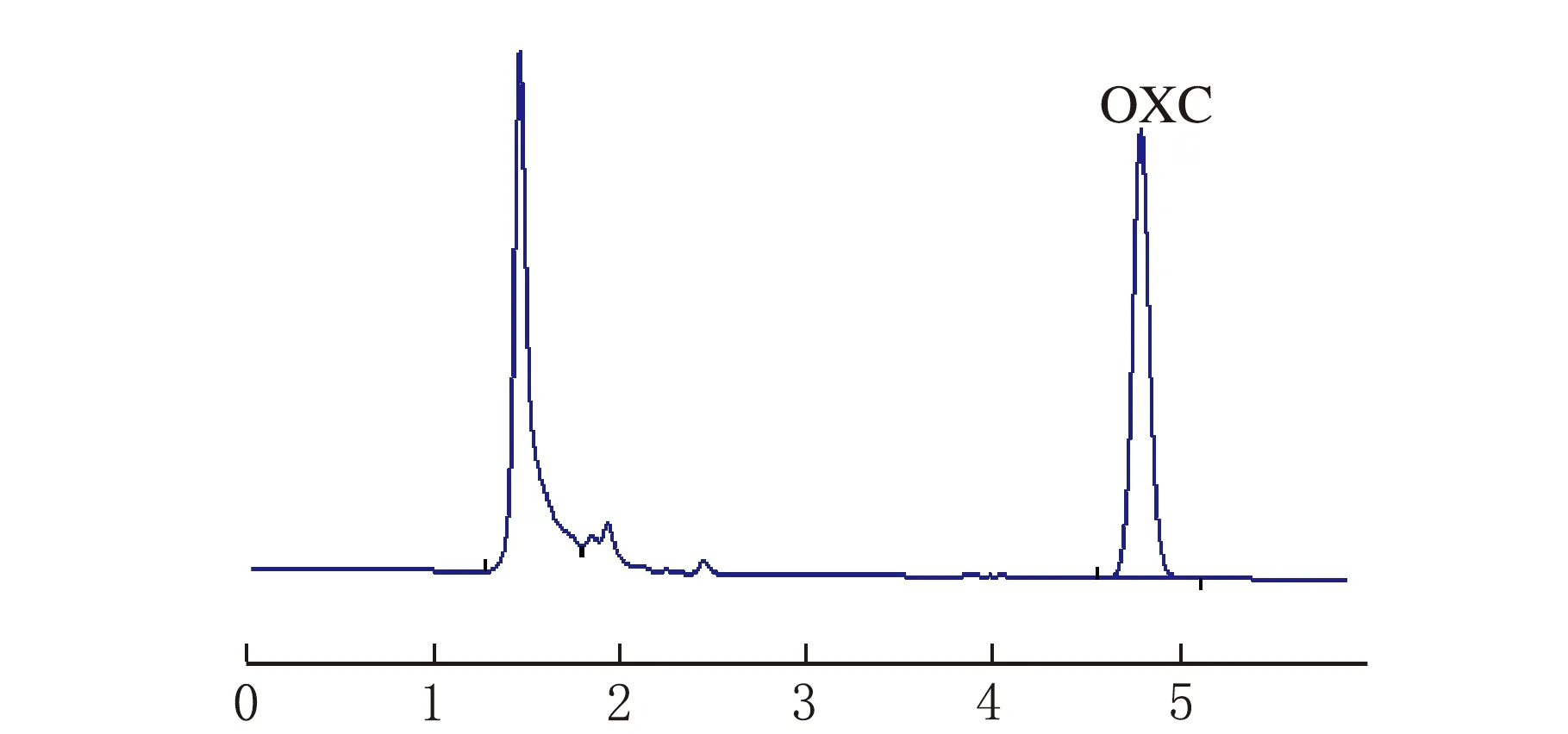
t/min供試品溶液
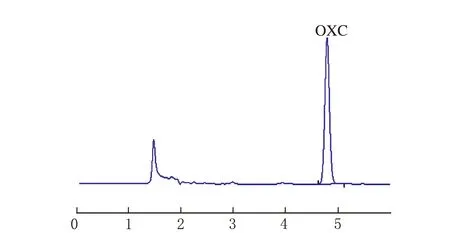
t/minOXC對照品溶液圖1 高效液相色譜法圖
由圖1可見,處方中其它成分不干擾OXC的定量分析。線性關系考察以OXC質量濃度(ρ) 為橫坐標、峰面積(A)為縱坐標進行線性回歸,得回歸方程A=27.86ρ+5.626,r=0.999 8(n=9)。結果表明,ρ(OXC)在0.16~41.6 μg/mL內與峰面積線性關系良好。
精密度實驗中對照品峰面積的RSD=0.45%(n=6),表明儀器精密度良好。
重復性實驗測得平均ρ(OXC)=24.22 μg/mL,RSD=0.81%(n=6),表明方法重復性良好。
回收率實驗結果低、中、高3種濃度的平均回收率為100.8%,RSD=1.24%,表明該方法準確度良好。
2.2 包封率測定結果
2.2.1 葡聚糖凝膠柱層析法
洗脫曲線的測定結果顯示在前40 mL無游離藥物被洗脫出來,在第55~65 mL洗脫液里檢測出游離藥物,表明游離藥物與包封藥物能有效分離。OXC平均柱回收率為99.62%(n=3),結果表明葡聚糖凝膠柱層析法可用于OXC納米脂質載體包封率的測定。測得OXC納米脂質載體的包封率為(98.16±1.59)%。
2.2.2 高速冷凍離心法[9]
方法學驗證結果顯示OXC沉淀藥物量為97.81%,空白納米脂質載體溶液離心后底部未見沉淀,處方量的OXC與空白納米脂質載體溶液混合后離心,測得沉淀藥物量為95.53%。結果表明,高速離心法測定OXC納米脂質載體的包封率可行。測得OXC納米脂質載體的包封率為(95.73±0.77)%。
3 結 論
采用葡聚糖凝膠柱層析法和高速冷凍離心法較好地分離納米脂質載體與游離藥物,并采用高效液相色譜法測定藥物的含量,方法簡單易行,重復性好。經方法學驗證,該法可用于OXC納米脂質載體中藥物包封率的測定。
參 考 文 獻:
[1] 陸志城,余清聲.奧卡西平藥代動力學及其立體選擇性[J].中國臨床藥理學雜志,2003,19(2):134-138.
[2] 穆殿平.奧卡西平與卡馬西平的藥動學研究及代謝差異的初步理論分析[D].天津:天津醫科大學,2006:9-10.
[3] SABA KHAN,SANJULA BABOOTA,JAVED ALI,et al.Nanostructured lipid carriers:an emerging platform for improving oral bioavailability of lipophilic drugs [J].Int J Pharm Investig,2015,5(4):182-191.
[4] MüLLER RH,RADTKE M,WISSING SA.Nanostructured lipid matrices for improved microencapsulation of drugs [J].Int J Pharm,2002,242(1/2):121-128.
[5] MüLLER RH,PETERSEN RD,HOMMOSS A,et al.Nanostructured lipid carriers (NLC) in cosmetic dermal products [J].Adv Drug Deliv Rev,2007,59(6):522-530.
[6] 李艷芝,祁榮,柯學.納米脂質載體應用于口服給藥系統的研究進展[J].藥學與臨床研究,2013,21(4):355-359.
[7] NASERI N,VALIZADEH H,ZAKERI-MILANI P.Solid lipid nanoparticles and nanostructured lipid carriers:structure,preparation and application [J].Adv Pharm Bull,2015,5(3):305-313.
[8] 金鋒,臺州職業技術學院.一種奧卡西平納米結構脂質載體及其制備方法:201410745339.4[P].2015-04-22.
[9] 吳小意,石雷,周婷婷,等.環索奈德固體脂質納米粒包封率的測定方法研究[J].中國藥業,2013,22(12):100-102.
[10] 代文婷,張典瑞,郭晨煜,等.HPLC法測定冬凌草甲素納米脂質載體藥物的含量及包封率[J].藥物分析雜志,2009,29(4):587-590.
[11] 王坤,楊磊,王艷,等.奧扎格雷納米結構脂質載體包封率的測定方法[J].中國新藥雜志,2012,21(22):2693-2696.
[12] 馮飛飛.聯苯雙酯納米脂質載體給藥系統的實驗研究[D].濟南:山東大學,2011:34.
[13] 黃仁杰,鄢雪梨,狄萬鵬,等.蛇葡萄素納米膠束含量與包封率的測定[J].藥物分析雜志,2015,35(2):261-265.

