纈草屬植物的化學成分及生物活性研究概況
王茹靜 黃青 雍妍 李鴻翔 張仕瑾 陳寶華 朱利霞 陳銀

[摘要]結合國內外文獻綜述了纈草屬植物化學成分的研究進展,并對該屬藥用植物的藥理活性進行了總結。纈草屬植物除含有一定的揮發油外,化學成分主要集中于單萜類、倍半萜類、木脂素類、黃酮類、生物堿類等。其中單萜類成分主要以環烯醚萜類化合物為主,根據其結構是否裂環分為環戊烷環環烯醚萜和裂環環烯醚萜。藥理研究表明該屬植物具鎮靜、解痙、抗抑郁、抗腫瘤、抗A1阿糖腺苷受體性和細胞毒性,并對心血管有一定作用。鑒于目前缺少對纈草屬研究的系統回顧和綜述,該文對近年來發表的纈草屬研究文獻進行整理和分析,為其進一步開發利用提供依據。
[關鍵詞]纈草屬;化學成分;藥理活性
[Abstract]The recent progresses on chemical components and pharmacological activities of the genus Valerianawere summarizedBesidesessential oil, the chemical composition of Valerianais mainly focused on monoterpenoids,sesquiterpenoids,lignans, flavonoids, alkaloids, etc Iridoids are the main chemical components ofmonoterpenoids There are two types ofiridoidson the basis of the cyclopentane open or not The Valerianahas been drawmuch attention for their significant sedation,spasmolysis,antidepression,antitumor, against adenosine A1 receptors and cytotoxicityactivity,and had certain function for cardiovascular disease treatment Given to the fact of the lack of systematic review and summary of studies on the Valeriana, we summarized and analyze the study literatures on the pharmacological activity of Valerianain recent years, and providedsome basisfor further study
[Key words]Valeriana; chemical components; pharmacological activities
doi:10.4268/cjcmm20160807
纈草屬Valeriana L隸屬敗醬科Valerianaceae,其植物藥用歷史久遠,全世界約有250余種,大多數分布于溫帶地區,主產于歐洲和亞洲溫帶地區[1];該植物中富含有單萜類、倍半萜類、木脂素類等成分,具有鎮靜、安神等多種功效,臨床上多用于治療精神紊亂性疾病(如癲癇、歇斯底里癥等)、劇烈咳嗽、便秘等多種疾病[2]。在歐洲纈草有悠久的研究歷史,可用作藥用、香料和觀賞。早在1983年,纈草V officinalis已被列入《歐洲藥典》用作鎮靜劑,其制劑被荷蘭、德國、日本、英國等20多個國家藥典收載。目前在國際市場,纈草的提取物及其制劑已成為商品上市。北纈草V fauriei生長在中國東北地區,已有上百年的中藥臨床應用歷史[3]。近年來,國內外學者對纈草屬植物化學成分、藥理活性和作用機制等方面進行了大量研究,并取得了較大的進展。本文對該屬植物的相關研究進行綜述,為開展該植物的研究提供參考。
1國產纈草屬資源概況
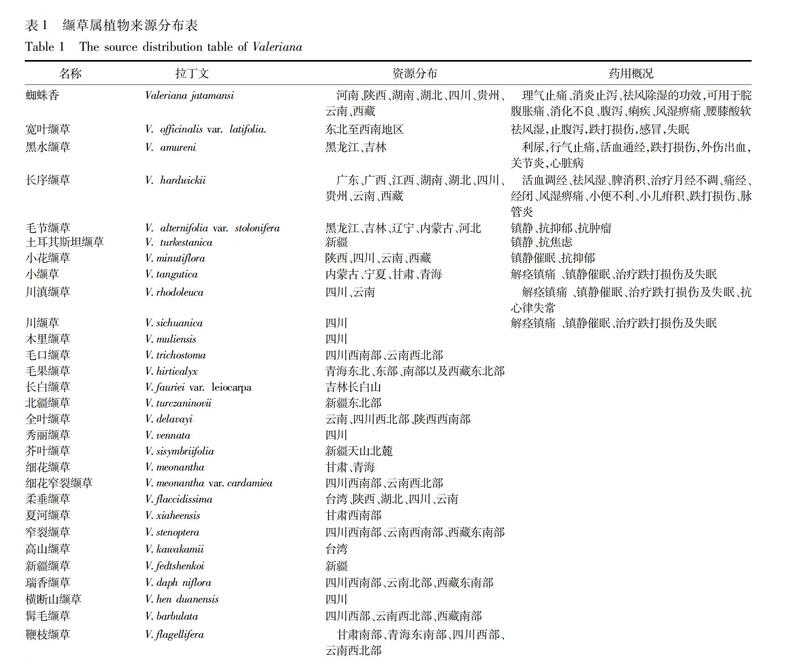
纈草屬作為藥用和芳香植物,目前應用廣泛。有關于纈草種類及分布的記載,不同學者存在不同看法,《中國植物志》認為有17種2變種,《中國種子植物科屬詞典》則收載24種,《中國高等植物圖鑒》則認為我國約有10種。誠靜容等對我國藥用纈草相近種的纈草種類進行分類研究,認為相似種與歐洲均有不同,并根據其分布和形態特征分為6種1變種[4]。纈草屬植物具體來源和分布見表1。
2化學成分
從纈草屬目前分離得到約150種化學成分,其中大多數具有生物活性,經過大量研究發現,纈草提取物中環烯醚萜類化合物、倍半萜類化合物、木脂素、生物堿、纈草素具有較強的鎮靜、細胞毒性、抗腫瘤、抗氧化、血管舒張的活性[5],其中纈草素具有顯著的鎮靜安神的藥理活性。
21環烯醚萜類化合物
環烯醚萜(iridoids)為臭蟻二醛的縮醛衍生物,根據其環戊烷環是否裂環,將其分為環戊烷環環烯醚萜(iridoid)和裂環環烯醚萜(secoiridoid)兩大類。其中半縮醛C1OH性質不穩定,主要與糖形成苷的形式存在于植物體內,其苷鍵極易被酸水解,生成苷元[6]。普通型環烯醚萜類化合物是的由1個環烯醚環和1個環戊烷組成,環戊烷上C6, C7, C8均可被取代基取代,取代基常為酯基或者羥基;環氧醚型類環烯醚萜化合物常見在C78或C6~7間形成環氧醚結構,天然產物中均為β型[7];學者們對纈草屬蜘蛛香的化學成分進行研究中,分離到許多裂環型環烯醚萜類化合物,其常見為C8~9或者C8~10為雙鍵,C7位常連接羥基或者酯基,C10位常酯化形成酯基或者連接羥基[8];近年來有學者通過研究發現氧橋型環烯醚萜類化合物,通常為C3位雙鍵斷裂后與C8位或者C10位的羥基形成氧橋[9];其母核結構見圖1,環烯醚萜類化合物見表2。
22木脂素
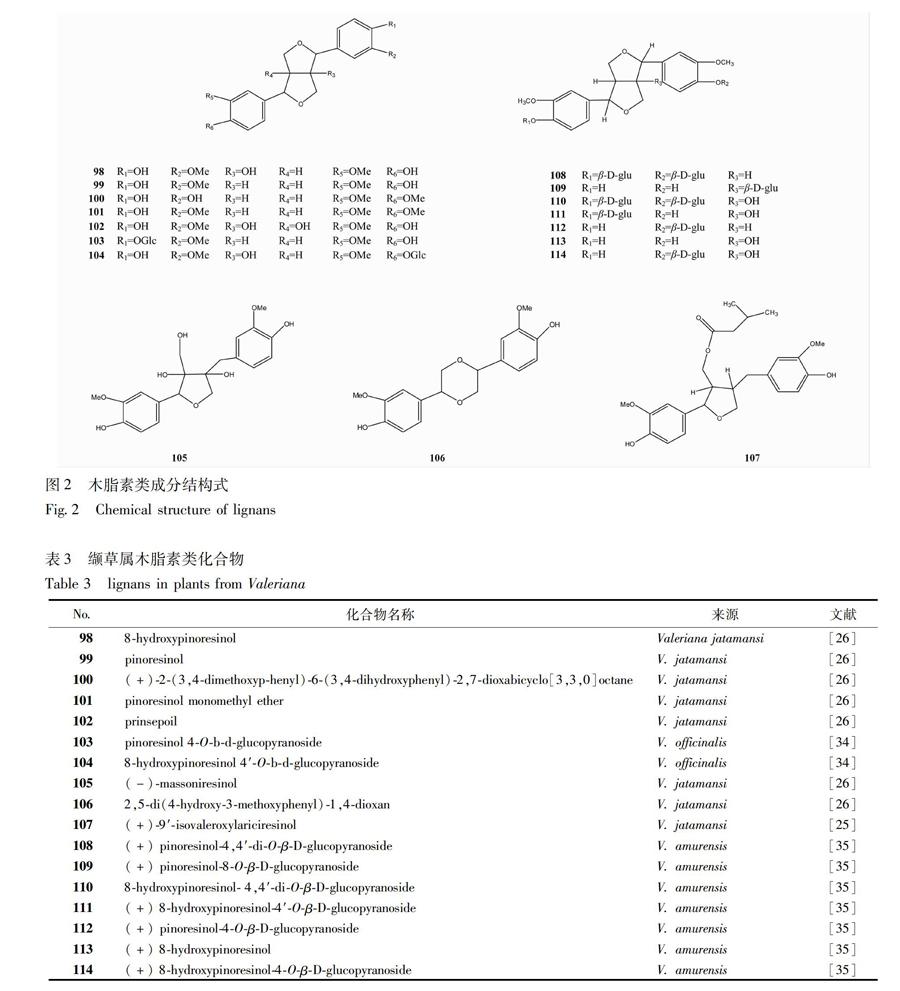
近年來,國內外報道的木脂素類成分大多為雙環氧型或7,9′單環氧型木脂素及其苷類。纈草屬木質素類化合物結構見圖2,表3。
23揮發油
纈草中含揮發油類成分多種多樣,且隨著生態環境的不同而有所不同。目前,在纈草屬揮發油中已經分離到約40種倍半萜類化合物。其中最主要的活性成分有:纈草醛、纈草烯酸和纈草酮等。其主要化合物類型及主要成分與纈草屬其他植物如寬葉纈草、歐纈草等類似。纈草屬揮發油類化合物結構及名稱見圖3,表4。
24其他化學成分
纈草屬的水提物中還含有一些有機酸、生物堿、黃酮等化合物。Tang[37]從蜘蛛香中分離得到2個新的黃酮苷類化合物acacetin 7Oβsophoroside和acacetin 7O(6″Oαlrhamnopyranosyl)βsophoroside;Archana Pande等[38]從蜘蛛香
3藥理作用
31對中樞神經系統的作用
311抗癲癇Wagner等研究發現,纈草素等環烯醚萜三酯顯著延長了驚厥潛伏期,并且降低了驚厥死亡率,同時能夠緩解平滑肌細胞的攣縮,具有較強的中樞神經抑制的作用[39]。纈草提取物可以降低神經網絡的興奮性,當受到β樣淀粉蛋白所致的毒性作用時,其對神經起保護作用,防止神經元容量的減少和相關神經的退化[40]。羅國君等[41]經過研究發現寬葉纈草通過改變GABA轉運體mRNA的表達,從而影響了GABA的濃度,使之起抗癲癇作用,同時探索了寬葉纈草高、中、低劑量對抗對戊四氮(PTZ)的驚厥作用,結果發現3種劑量均有一定的抗驚厥作用,其中高劑量組更明顯,且寬葉纈草對抗PTZ的作用有劑量依賴性。
312鎮靜安神Schulz等應用含纈草素及根提取物的藥物,對睡眠障礙的患者進行臨床實驗,發現患者的慢波睡眠時間顯著增加,K形復合波的密度有所提高,但對β波影響較小,表明了纈草素可以縮短患者的睡眠潛伏期,顯著改善睡眠質量[42]。陳佳帥等[43]通過考察黑水纈草的石油醚部位對小鼠腦內神經遞質5羥色胺(5HT)及γ氨基丁酸(GABA)的含量的影響,結果表明其不同劑量均能使神經遞質的含量顯著升高,明顯延長了小數的睡眠時間。陶濤等[44]通過對纈草醇提物進行研究,發現其與戊巴比妥鈉有較好的協同作用,對小鼠的自發活動有抑制作用,可延長小鼠的睡眠時間。
32對循環系統的作用
纈草能改善心肌缺血,纈草三氯甲烷提取物不僅可以抑制中樞,還有改善心肌循環和預防心肌缺血的作用。薛存寬等通過動物實驗發現,纈草揮發油能增加冠脈流量的微循環關注從而縮小心肌梗死的范圍,由此得到纈草揮發油有抗心肌缺血的作用[45]。 龔占峰[46]首次采用血清藥物化學的方法對纈草抗心律失常的活性部位進行了研究,結果表明纈草代謝產物可能為其抗心律失常的活性物質,對于探討纈草抗心律失常活性物質提供了重要的參考意義。楊乾等[47]在針對寬葉纈草揮發油治療冠心病患者的研究中,采用丹參注射液做對照治療,結果發現,對于康復缺血心肌,改善心肌缺血的作用上,寬葉纈草的療效明顯強于丹參注射液。同時在減少心絞痛發病頻率,改善心絞痛癥狀,縮短心絞痛發作時間方面,寬葉纈草的療效也有明顯優勢,由此說明寬葉纈草在改善心肌缺血和緩解心絞痛癥狀兩方面均有顯著的療效。
33抗腫瘤
纈草中環烯醚萜類成分有較強的抗腫瘤作用,其中以環烯醚萜酯的作用最為明顯[48]。Bounthanh等通過體外實驗,發現纈草波春對肝癌細胞、骨髓造血祖細胞、Kreb2腹水癌細胞和T2淋巴細胞有抑制作用[49]。纈草屬蜘蛛香中的(+)9′isovaleroxy lariciresinol(木脂素類單體成分)可在體外發揮抑制PC3M(前列腺轉移癌細胞)和HCT8(結腸癌細胞)的作用[50]。閆智勇等[51]利用肝癌H22小鼠進行相關研究,最終除提出蜘蛛香中對實驗小鼠發揮抑瘤作用的是其中所含有的總黃酮外,還進一步發表了認為其作用機制是抑制JAK/STAT的信號通路的可能。
34抗菌、抗病毒
楊氏等[24]采用杯盤培養法對纈草體外抑菌活性進行比較,結果發現纈草對枯草芽孢桿菌、大腸桿菌、金黃色釀膿葡萄球菌都有一定的抑制作用,其中纈草中環烯醚萜是抗菌的主要活性成分。纈草總生物堿對革蘭氏陽性菌有較好的抑制作用,可用于治療呼吸道疾病。Murakmi N等研究發現纈草素能抑制細胞調節蛋白Rev從細胞核向細胞質的轉運,從而抑制HIV的復制,具有抗AIDS的活性[52]。
35其他
Parvaneh Mirabi等[53]針對婦女作為研究對象,通過雙盲實驗研究纈草是否具有植物雌激素的作用,結果表明纈草能治療婦女絕經期潮熱。Jéssie Haigert Sudati等[54]采用黑腹果蠅為受試體,研究纈草對于魚藤酮引起的毒性的作用,結果表明有一定的抑制作用,由此認為纈草提取物可能對神經退行性疾病有較好的療效。纈草屬中具體單體化合物的藥理作用見表5。
36藥物安全性
蔣中仁等[55]采用經口灌胃法連續90 d給予SD大鼠后,觀察纈草液對動物生化指標、血液學指標及組織病理學指標等的影響。實驗結束后處死動物,未見受試動物高劑量組引起中毒性損傷改變。
4結語
傳統中醫認為纈草屬植物的主要功效是鎮靜安神,主要治療失眠、抑郁等癥。現有的活性研究發現纈草屬中所含的環烯醚萜類成分有神經保護的作用,木脂素類成分對于退行性疾病老年癡呆有良好的治療作用。通過本文綜述可以看出,纈草屬化學成分的種類較為集中,活性成分專一,藥理作用緩和。但目前大多藥理活性的研究僅局限于粗提物,至于具體何種活性部位或者具體化學成分的作用機制仍需進一步研究。到目前為止,由于其所含的物質基礎研究薄弱,不僅對其抗腫瘤或對心血管產生藥理活性成分亟待明確,而且難以對其進行質量評價,臨床用藥的安全及藥效也難以保證。因此需要在生物活性篩選指導下尋找其活性部位和具體的活性成分,并在活性成分的基礎上進一步闡明其作用的物質基礎和作用機制。其中環烯醚萜類和木脂素類化合物具有很大的生物活性潛力,有望從中開發具有良好藥效的新藥,進一步開拓纈草屬的應用前景。
[參考文獻]
[1]段雪云, 方穎, 周穎,等. 纈草屬植物綜合研究概況[J]. 中國藥師, 2008,11(7):793.
[2]郄建坤, 屈會化, 欒新慧. 纈草屬植物化學成分及藥理研究概況[J]. 中國藥學雜志, 2002, 37(10):729.
[3]Zhang Z X, Dou D Q, Liu K, et al. Studies on the chemical constituents of Valeriana fauriei Briq[J]. J Asian Nat Prod Res, 2006,8(5):397.
[4]黃寶康,鄭漢臣,秦路平, 等. 國產纈草屬藥用植物資源調查[J]. 中藥材,2004,27(9):632.
[5]Wang R, Xiao D, Bian Y H,et al. Minor Iridoids from the Roots of Valeriana wallichii[J]. J Nat Prod, 2008,71(7):1254.
[6]李少華, 閆智勇. 蜘蛛香環烯醚萜類成分的研究進展[J]. 中國新藥雜志, 2012, 21(6):633.
[7]Tiwari N,Yadav AK,Srivastava P,et al. Iridoid glycosides from Gmelina arborea[J]. Phytochemistry, 2008,69(12):2387.
[8]Ji T F, Wang A G, Yang J B, et al. A novel secoiridoid from Olea europaea L. [J]. NatProdReDev,2007,19(3):361.
[9]Teng J, Zhang F G, Zhang Y W, et al. A new iridoid glycoside from Veronica sibirica[J]. Chin Chem Lett, 2008,19(4):450.
[10]Lin S, Shen Y H, Li H L, et al. Acylated iridoids with cytotoxicity from Valeriana jatamansi[J]. J Nat Prod, 2009,72(4):650.
[11]Lin S, Shen Y H, Zhang W D,et al. Revision ofthe structures of 1,5dihydroxy3,8epoxyvalechlorine, volvaltrate B, and valeriotetrate C from Valeriana jatamansi and V. officinalis[J]. J Nat Prod,2010,73(10):1723.
[12]Xu J, Zhao P, Guo Y Q,et al. Iridoids from the roots of Valeriana jatamansi and theirneuroprotective effects[J]. Fitoterpia, 2011, 82(7):1133.
[13]Xu J, Guo Y Q, Jin D Q, et al. Three new iridoids from the roots of Valeriana jatamansi[J]. J Nat Med, 2012, 66(4):653.
[14]Popov S, Handjieva N, Marekov N. A new valepotriate:7epideacetylisovaltrate from Valeriana officinalis[J]. Phytochemistry,1974,13(2):2815.
[15]Tang Y P, Liu X, Yu B. Iridoids from the rhizomes and roots of Valeriana jatamansi[J]. J Nat Prod, 2002,65(12):1949.
[16]Tang Y P, Liu X, Yu B. Iridoids from the Rhizomes and Roots of Valeriana jatamansi[J]. J Nat Prod, 2002, 65(12): 1949.
[17]Salles L A, Silva A L, Rech S B, et al. Constituents of Valeriana glechomifolia Meyer[J]. Biochem Syst Ecol, 2000, 28(9): 907.
[18]Fuzzati N, Wolfender J L, Hostettmann K, et al. Isolation of antifungal valepotriates from Valeriana capense and the search for valepotriates in crude Valeriana ceae extracts [J]. Phytochem Anal, 1996,7(2): 76.
[19]Lin S, Zhang Z X, Chen T,et al. Characterization of chlorinated valepotriates from Valeriana jatamansi[J]. Phytochemistry, 2013, 85:185193.
[20]Xu J, Guo P, Fang L Z, et al. Iridoids from the roots of Valeriana jatamansi[J]. J Asian Nat Prod Res, 2012,14(1):1.
[21]Tomassini L, Gao J J, Serafini M, et al. Iridoid glucosides from Viburnum sargenti[J]. Nat Prod Res, 2005, 19(7):667.
[22]Thies P W, Firmer E, Rosskopf F. Die konfiguration des Valtratum und anderer Valepotriate [J]. Tetrahedron, 1973, 29(20): 3213.
[23]Chen Y G, Yu L L,Huang R,et al. 11Methoxy viburtinal,a new iridoid from Valeriana jatamansi[J]. Arch Pharm Res,2005,28(10):1161.
[24]Yang X P, Li E W, Zhang Q, et al. Five new iridoids from Patrinia rupetris[J]. Chem Biodivers, 2006,3(7):762.
[25]Lin S, Chen T, Liu X H, et al. Iridoids and lignans from Valeriana jatamansi[J]. J Nat Prod, 2010, 73(4): 632.
[26]李元旦,李榮濤,李海舟. 蜘蛛香的化學成分研究[J]. 云南中醫中藥雜志,2011,32(6):80.
[27]Wang P C, Hu J M, Ran X H, et al. Iridoids and sesquiterpenoids from the roots of Valeriana officinalis[J]. JNatProd,2009, 72(9):1682.
[28]Yu L L, Huang R, Han C R, et al. New Iridoid triesters from Valeriana jatamansi[J]. Helvetica Chimica Acta,2005, 88(5): 1059.
[29]Xu J, Zhao P, Guo Y Q, et al. Iridoids from the roots of Valeriana jatamansi and their neuroprotective effects[J]. Fitoterapia, 2011, 82(7):1133.
[30]邸磊. 糙葉敗醬化學成分及其抗腫瘤活性研究[D]. 合肥: 安徽大學,2012.
[31]Wang R, Xiao D, Bian Y H, et al. Minor Iridoids from the Roots of Valeriana wallichii[J]. JNatProd,2008, 71(7): 1254.
[32]李蓉. 蜘蛛香中黃酮類化合物的提取分析及抗炎抑菌活性研究[D]. 蘇州: 蘇州大學, 2009.
[33]Xu J, Li Y S, Guo Y Q, et al. Isolation,structural elucidation,and neuroprotective effects of iridoids from Valeriana jatamansi[J]. BiotechnolBiochem,2012,76(7):1401.
[34]Wang P C, Ran X H, Chen R,et al. Sesquiterpenoids and Lignans from the Roots of Valeriana officinalis L. [J]. Chem Biodivers,2011,8(10):1908.
[35]Wang Q H, Wang C F,Zuo Y M,et al. Compounds from the Roots and Rhizomes of Valeriana amurensis protect against neurotoxicity in PC12 cells[J]. Molecules,2012,17(12):15013.
[36]Xu J, Yang B, Guo Y Q, et al. Neuroprotective bakkenolides from the roots of Valerian jatamansi[J]. Fitoterpia,2011,82(6):849.
[37]Tang Y P, Liu X, Yu B. Two new flavone glycosides from Valeriana jatamansi[J]. J Asian Nat Prod Res, 2003,5(4):257259.
[38]Pande A, Shukla Y N. Naphthoic acid derivative from Valeriana wallichii[J]. Phytochemistry, 1993,32(5):1350.
[39]彭佳. 蜘蛛香環烯醚萜類成分中樞抑制作用研究[D]. 西南交通大學,2009.
[40]Malva J O. Neuroprotective properties of Valeriana officinalis extraets[J]. Neurotoxres,2004,6(2):131.
[41]Luo G J, Wang H, He G H. The effects of Valeriana officinalis var. latifolia on both EEG and behaviors of epileptic rats induceded by pentylenetetrazol[J]. J Clinical Electroneurophysiol,2005,14(2):95.
[42]Schulz H,Jobert M. Effects of Hypericum extract on sleep EEG in older volunteers[J]. J Geriatr Psychiatry Neurol,1994,7(1):39.
[43]陳佳帥,吳軍凱,劉玲,等. 黑水纈草石油醚部位改善小鼠睡眠作用及相關機制研究[J]. 中國實驗方劑學雜志, 2013,19(24):245.
[44]陶濤, 朱全紅. 纈草醇提物的鎮靜催眠作用研究[J]. 中藥材,2004,27(3):209.
[45]Schumacher B, Scholle S, Holzl J,et al. Lignans isolated from Valerian:identification and characterization of a new o1ivil derivative with partial agonistic activity at A1adenosine receptors[J]. J Nat Prod, 2002,65(10): 1479.
[46]龔占峰. 纈草抗心律失常活性成分及血清藥物化學研究[D]. 武漢: 湖北中醫學院, 2009.
[47]楊乾, 鞠愛華, 百萬富, 等. 寬葉纈草的化學成分及藥理活性研究進展[J]. 中國現代應用藥學雜志, 2008, 25(7):613.
[48]薛存寬, 何學斌, 張書勤, 等. 纈草環烯醚萜抗腫瘤作用的實驗研究[J]. 現代中西醫結合雜志, 2005, 14(15):1969.
[49]Bounthanh C, Bergmann C, Pbeek J P,et al. Valepotriates, a new class of cytotoxic and antitumor agents[J]. Planta Medica,1981,41(1):21.
[50]Lin S, Chen T, Liu X H, et al. Iridoids and lignans from Valeriana jatamansi[J]. J Nat Prod, 2010,73(4):632.
[51]閆智勇, 左長英, 陳沖, 等. 蜘蛛香總黃酮抗肝癌作用及對JAK/STAT信號通路的影響[J]. 中國藥理學與毒理學雜志, 2011, 25(5):60.
[52]Murakami N, Ye Y, Kawanishi M,et al. New revtransport inhibitor with antiHIV activity from Valerianae Radix[J]. Bioorg Med Chem Lett,2002,12(20):2807.
[53]Mirabi P, Mojab F. The effects of valerian root on hot flashes in menopausal women[J]. Iran J Pharm Res,2013,12(1):217.
[54]Sudati J H, Vieira F A, Pavin S S,et al. Valeriana officinalis attenuates the rotenoneinduced toxicity in Drosophila melanogaster[J]. Neurotoxicology, 2013, 37:118.
[55]蔣中仁,劉科亮,徐薇,等. 纈草液的大鼠90天喂養試驗[J]. 職業衛生與病傷, 2012, 27(3): 172.
[責任編輯丁廣治]

