氮摻雜碳點的制備及在六價鉻檢測中的應用
曾 強,朱浩波,朱紅艷,朱小利,戴昌雄,鄧 淳,何 瑜,張修華,宋功武
(1.武漢紅金龍印務股份有限公司,湖北 武漢 430056;2.湖北大學化學化工學院,湖北 武漢 430062)
?
氮摻雜碳點的制備及在六價鉻檢測中的應用
曾強1,朱浩波1,朱紅艷1,朱小利1,戴昌雄1,鄧淳2,何瑜2,張修華2,宋功武2
(1.武漢紅金龍印務股份有限公司,湖北 武漢 430056;2.湖北大學化學化工學院,湖北 武漢 430062)
摘要:以破壁靈芝孢子粉為碳源、尿素為含氮摻雜劑,采用一步超聲法制備了氮摻雜熒光碳點(N-CDs),并將其作為熒光探針檢測Cr(6+)。向碳點溶液中加入Cr(6+)后,碳點熒光發生了猝滅,表明碳點與Cr(6+)發生了作用,并在Cr(6+)濃度為0~300 μmol·L(-1)范圍內熒光強度變化值與Cr(6+)濃度表現出良好線性關系,相關系數為0.9818,檢出限為0.3 μmol·L(-1)。在實際樣品檢測中,回收率較好,為94%~102%,說明所制N-CDs可用于Cr(6+)的檢測,具有較高的實用價值。
關鍵詞:Cr(6+);靈芝孢子粉;熒光碳點;氮摻雜;熒光檢測
鉻是一種重要的金屬元素,廣泛應用于電鍍、制革、染料及冶金工業中[1]。在環境中主要以Cr3+和Cr6+兩種形式存在[2]。鉻的毒性與其所處化學價態有關[3],Cr3+為人體所需微量元素[4],主要功能為促進人體糖類[5]、蛋白質[6]和脂類的新陳代謝及人體生長發育[7-8],而Cr6+對人體有毒,易穿透細胞并在細胞內沉積,其強氧化性可引起腎臟、肝臟、神經系統和血液的廣泛病變[9]。因此,對Cr6+的檢測顯得十分必要。
熒光碳點(fluorescentcarbondots,CDs)[10]是繼量子點之后又一種新型的熒光納米材料,具有良好的發光性能與小尺寸特性,而且還具有很低的生物毒性和良好的生物相容性[11],克服了傳統熒光染料的缺點,在細胞成像[12]、標記[13]及檢測[14]等領域具有廣闊的應用前景,有望代替量子點成為最具應用前景的環保型熒光納米材料。
作者以破壁靈芝孢子粉為碳源、尿素為含氮摻雜劑,采用一步超聲法制備氮摻雜熒光碳點(N-CDs),并將其作為熒光探針檢測環境水樣中Cr6+。
1實驗
1.1試劑與儀器
靈芝孢子粉;尿素,分析純,國藥集團化學試劑有限公司;二次去離子水。
LS55型熒光分光光度計、Spectrumone型傅立葉變換紅外分光光度計、Lambda35型紫外分光光度計,美國Perkin-Elmer公司;TecnaiG20型透射電子顯微鏡,美國FEI公司;DTC-8型超聲波清洗機,鼎泰(湖北)生化科技設備制造有限公司。
1.2方法
1.2.1N-CDs的制備及表征
準確稱取1 g破壁靈芝孢子粉溶于100 mL去離子水,向其中加入1 g尿素,攪拌均勻,超聲反應4 h。反應結束后冷卻至室溫,離心抽濾,得到淡黃色上清液即為N-CDs溶液,將其稀釋100倍,4 ℃儲存,備用。
通過熒光光譜、TEM、FTIR、UV-Vis對制備的N-CDs進行表征。
1.2.2N-CDs的穩定性
N-CDs在應用中會受到環境酸堿度及離子強度的影響,測定N-CDs溶液在pH值2~12、KCl溶液濃度在0~100 mmol·L-1范圍內的440 nm處的熒光強度,考察酸堿度和離子強度對N-CDs熒光性質的影響。
1.2.3N-CDs對Cr6+的檢測
配制一系列不同濃度(0~300 μmol·L-1)的鉻酸鉀溶液,與N-CDs溶液混合。在900 V電壓、激發與發射狹縫分別為15 nm和20 nm的條件下,固定激發波長325 nm,測定體系熒光強度,得到熒光猝滅譜圖。
2結果與討論
2.1N-CDs的表征(圖1)
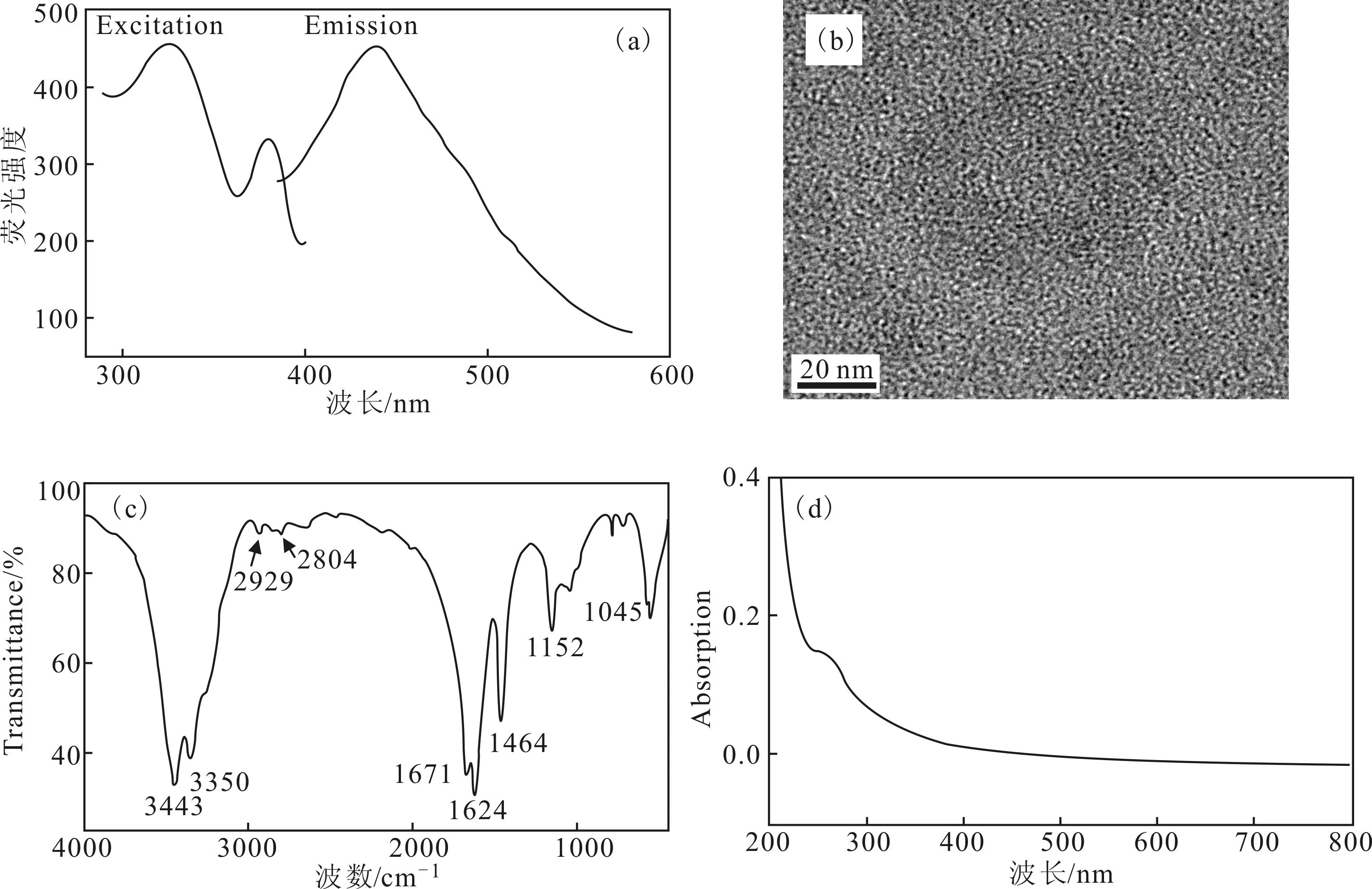
圖1 N-CDs的熒光激發光譜和發射光譜(a)、透射電鏡照片(b)、紅外光譜(c)、紫外光譜(d)
由圖1a可知,制備的N-CDs具有良好的熒光特性,激發峰和發射峰分別在325 nm和440 nm處,表明N-CDs可以用于熒光方面的應用。由圖1b可知,制備的N-CDs粒度均一,分散性好,粒徑為2 nm左右,符合碳點基本特性。由圖1c可知,3 443 cm-1、3 350 cm-1為氨基伸縮振動峰,1 671 cm-1為氨基彎曲振動峰,表明成功摻雜了氮。由圖1d可知,N-CDs在250 nm處具有紫外吸收。
2.2N-CDs的穩定性(圖2)
由圖2a可知,在pH值為2~12時,N-CDs的熒光強度變化不大,表明N-CDs具有良好的pH值穩定性。由圖2b可知,在不同濃度KCl溶液中,N-CDs在440 nm處的熒光強度與未加KCl的熒光強度幾乎一致,表明制備的N-CDs在較高離子強度溶液中具有良好的穩定性。
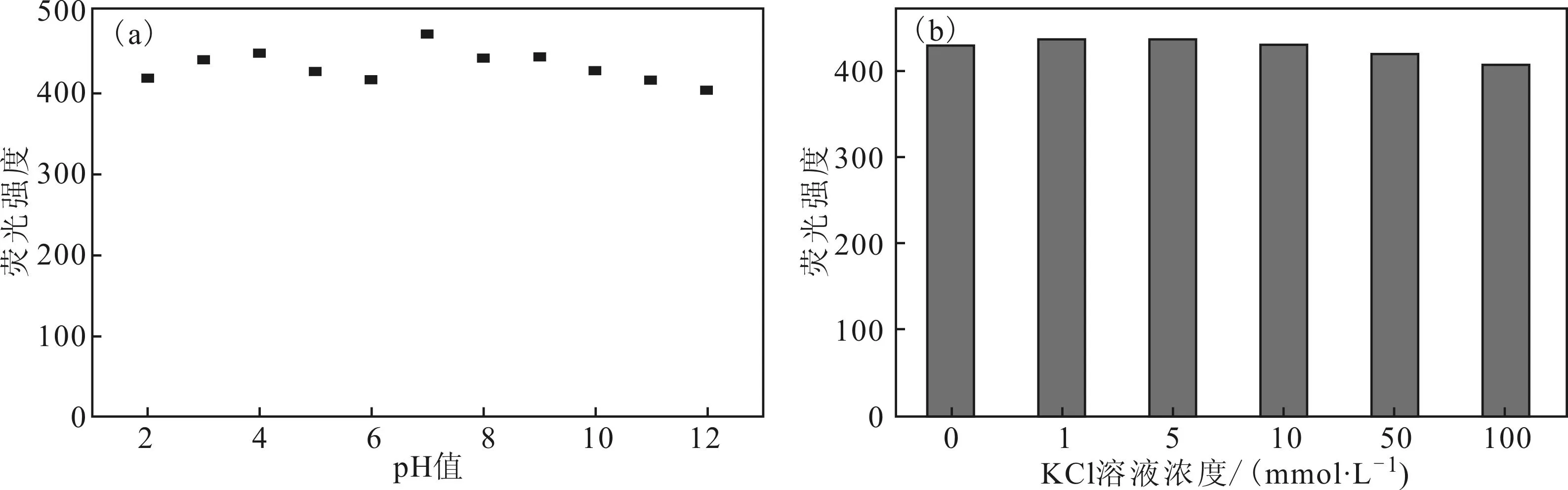
圖2N-CDs在不同pH值(a)和離子強度(b)下的熒光強度
Fig.2The fluorescence intensity of N-CDs at different pH values(a) and ionic strengths(b)
2.3N-CDs檢測Cr6+的可行性
為探究所制備的N-CDs檢測溶液中Cr6+的可行性,測定了加Cr6+前后N-CDs的熒光發射光譜,見圖3。
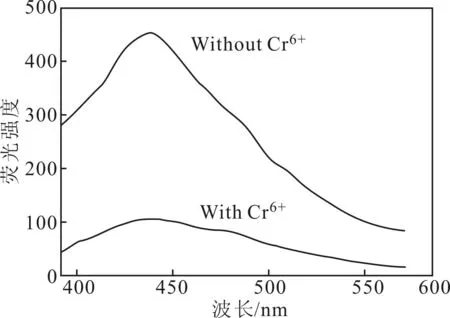
圖3 加Cr6+前后N-CDs的熒光發射光譜
由圖3可知,加Cr6+后N-CDs溶液在440 nm處熒光強度極大降低,發生了猝滅,表明制備的N-CDs具有檢測Cr6+的可行性。
環境酸堿度不僅可能影響N-CDs熒光強度,也可能會影響N-CDs在檢測中對目標物的熒光響應性,測試150 μmol·L-1Cr6+在不同pH值環境中對N-CDs熒光強度猝滅百分比,結果見圖4。
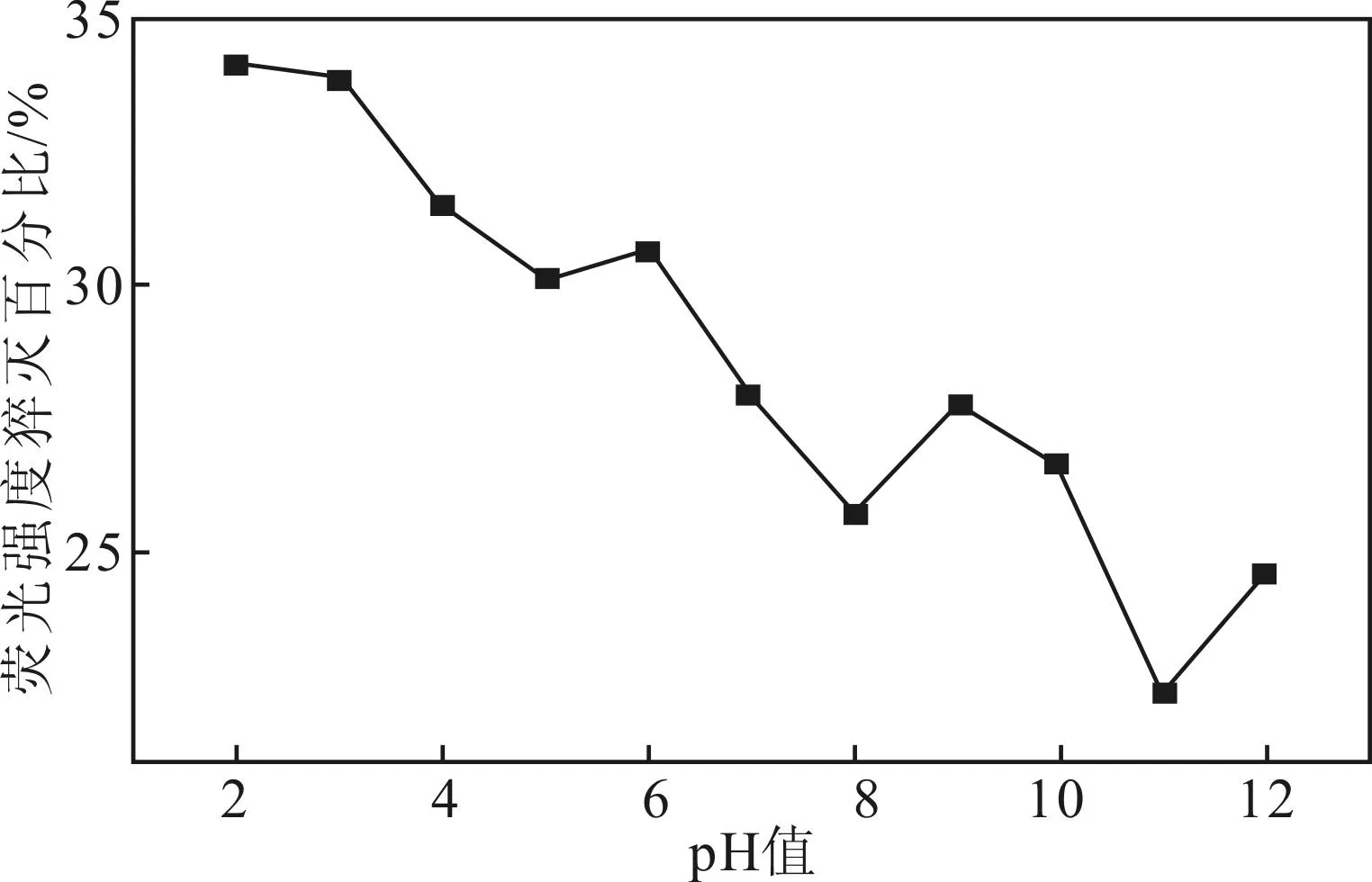
圖4 不同pH值下Cr6+對N-CDs熒光強度猝滅百分比
由圖4可知,在pH值為2和3的條件下,Cr6+對N-CDs熒光強度猝滅百分比最大,響應最靈敏,故選取溶液pH值為3作為最佳檢測條件。
在pH值為3的條件下,考察不同濃度Cr6+對N-CDs熒光強度的影響,結果見圖5。

圖5 不同濃度Cr6+對N-CDs熒光強度的影響
由圖5可知,N-CDs熒光強度隨著Cr6+濃度的增大而逐漸減弱,說明Cr6+與N-CDs發生了相互作用,并且猝滅十分明顯,表明N-CDs可以應用于Cr6+檢測。
為驗證N-CDs對Cr6+檢測的靈敏度,測定440 nm處N-CDs溶液加Cr6+前后的熒光強度(F0、F),由F0/F對Cr6+濃度作圖(圖6),得到檢測Cr6+的工作曲線,線性擬合方程為F0/F=0.732+0.011cCr6+,相關系數R2=0.9818。Cr6+濃度線性范圍為0~300 μmol·L-1,檢出限為0.3 μmol·L-1,表明該檢測方法可行,并且檢測靈敏。
2.4離子選擇識別性
N-CDs在檢測Cr6+過程中,可能會受到環境中各種金屬離子的干擾,對N-CDs檢測Cr6+的靈敏度進行了選擇識別性測試實驗。在pH值為3、Cr6+濃度為200 μmol·L-1的條件下,測試了環境中的其它12種濃度為1 mmol·L-1的金屬離子(Ni2+、Mn2+、Co2+、Fe2+、Fe3+、Ag+、Mg2+、Zn2+、Cd2+、Cu2+、Hg2+、Cr3+)對N-CDs熒光強度猝滅百分比,結果見圖7。
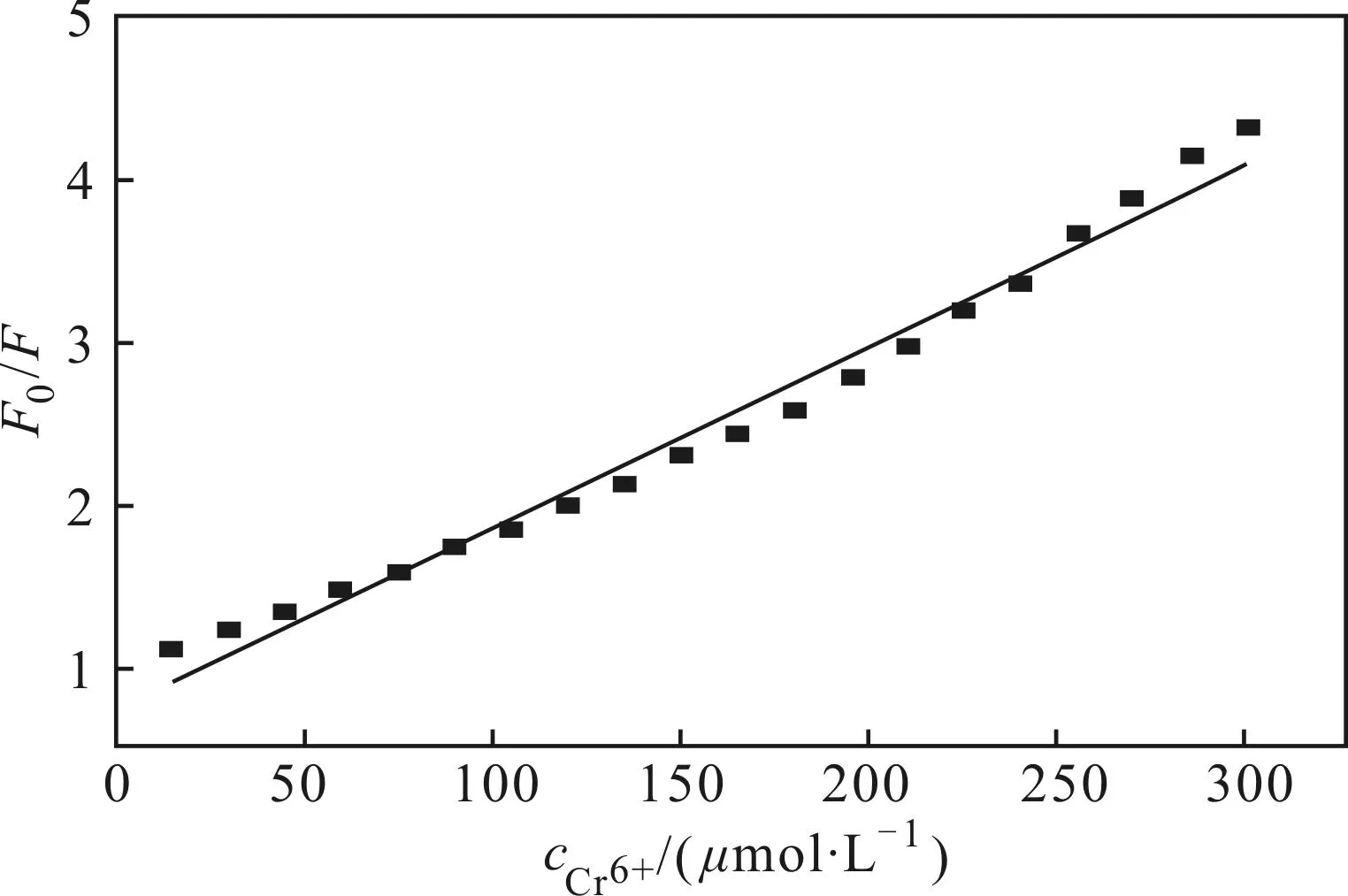
圖6 440 nm處熒光強度與Cr6+濃度關系
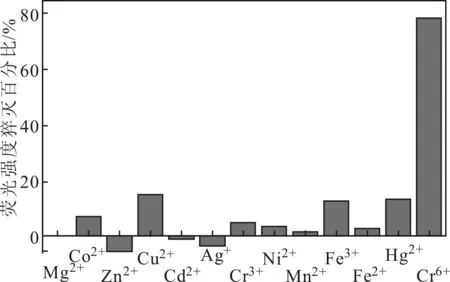
圖7 N-CDs對Cr6+選擇識別性
由圖7可知,12種金屬離子對N-CDs熒光響應較小,表明N-CDs對Cr6+的選擇識別性較好。
2.5實際樣品檢測
分別對長江水、東湖水、沙湖水進行簡單過濾后,進行加標回收測試,N-CDs對3種未稀釋實際水樣中的Cr6+加標回收檢測結果見表1。
表1
實際樣品檢測結果(n=3)
Tab.1The detection results of real samples(n=3)
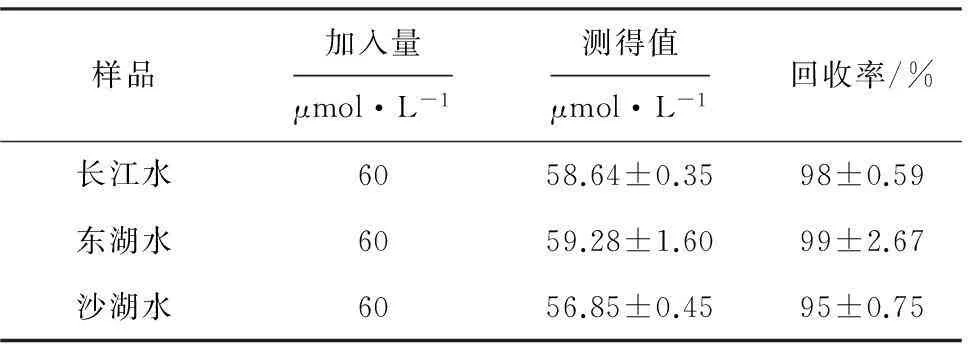
樣品加入量μmol·L-1測得值μmol·L-1回收率/%長江水6058.64±0.3598±0.59東湖水6059.28±1.6099±2.67沙湖水6056.85±0.4595±0.75
由表1可知,N-CDs在實際樣品檢測中的結果達到期望值,回收率均在94%~102%之間,適合微量分析,說明制備的N-CDs在Cr6+檢測中具有較高的實用價值。
2.6N-CDs熒光檢測Cr6+的機理
熒光猝滅機理通常分為2種:動態猝滅和靜態猝滅。動態猝滅機理一般用Stern-Volmer方程(式1)描述;靜態猝滅機理則用Lineweaver-Burk方程(式2)解釋。
F0/F=1+KSVcq
(1)
1/(F0-F)=1/F0+KLB/(F0cq)
(2)
式中:F、F0分別是猝滅劑存在與不存在下體系的熒光強度;KSV為動態猝滅常數(即Stern-Volmer猝滅常數),KLB為靜態猝滅常數(即Lineweaver-Burk猝滅常數);cq為猝滅劑濃度。
以不同濃度猝滅劑存在下的熒光強度F0/F對猝滅劑濃度作圖,得到線性方程F0/F=0.732+0.011cCr6+,線性相關系數為0.9818,表明Cr6+猝滅N-CDs遵循Stern-Volmer方程,屬于動態猝滅,說明熒光猝滅可能是Cr6+與激發態的N-CDs發生相互碰撞而導致的。
為了進一步討論Cr6+的檢測機理,考察了加Cr6+前后N-CDs的紫外光譜,見圖8。
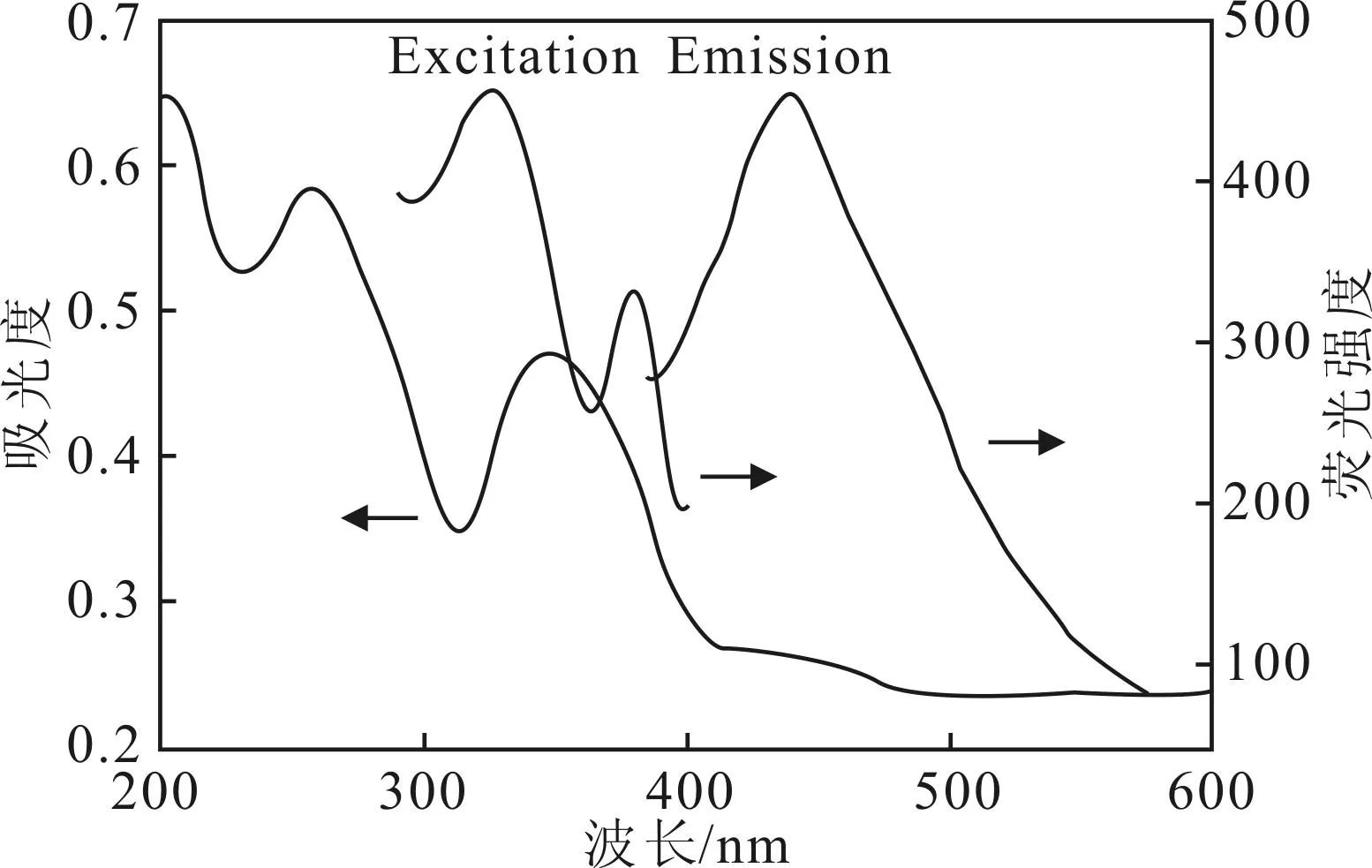
圖8 N-CDs的熒光猝滅機理
由圖8可知,Cr6+在350 nm處的紫外吸收峰與N-CDs在325 nm處的熒光激發峰部分重合,在440 nm處的紫外吸收峰與N-CDs在440 nm處的熒光發射峰重合,說明在檢測過程中,Cr6+不僅能吸收N-CDs的激發能量也能吸收N-CDs的發射能量,即檢測過程中存在能量傳遞行為[15]。
3結論
以破壁靈芝孢子粉為碳源、尿素為含氮摻雜劑,采用一步超聲法制備了N-CDs。所制備的N-CDs粒徑為2 nm左右,粒度均一,熒光性質穩定,對Cr6+選擇識別性好,可以作為Cr6+熒光探針。在Cr6+濃度為0~300 μmol·L-1范圍內N-CDs熒光強度變化值與Cr6+濃度表現出良好線性關系,相關系數為0.9818,檢出限為0.3 μmol·L-1。N-CDs對Cr6+的檢測靈敏度較高,并且在實際樣品檢測中得到預期結果,表明制備的N-CDs可以較好地應用于實際樣品檢測,具有較高的實用價值。該方法簡單快速,測定條件溫和,極具推廣價值。
參考文獻:
[1]AJMAL M,RAO R A K,AHMAD R,et al.Removal and recovery of heavy metals from electroplating wastewater by using kyanite as an adsorbent[J].Journal of Hazardous Materials,2001,87(1-3):127-137.
[2]DORSA M,PEREIRA M C,BARTOLOEE V,et al.Toxic effects and specific chromium acquired resistance in selected strains ofDyctiosphaeriumchlorelloides[J].Chemosphere,2010,81(2):282-287.
[3]KOCBERBER N,DONMEZ G.Chromium(Ⅵ) bioaccumulation capacities of adapted mixed cultures isolated from industrial saline wastewater[J].Bioresour Technol,2007,98(11):2178-2183.
[4]SANG D K,KYEONG S P,MAN B G.Toxicity of hexavalent chromiumDaphniamagnainfluence of reduction reaction by ferrous iron[J].Journal of Hazardous Materials,2002,93(2):155-164.
[5]鄧莉.葡萄糖耐量因子在治療糖尿病中的應用[J].中國農村醫學,1997,(9):29-32.
[6]王永芳.鉻與健康研究進展[J].中國食品衛生雜志,2001,13(1):46-48.
[7]WANG Y S,PAN Z Y,LANG J M,et al.Bioleaching of chromium from tannery sludge by indigenousAcidithiobacillusthiooxidans[J].Journal of Hazardous Materials,2007,147(S1-2):319-324.
[8]RAI V,VAJPAYEE P,SINGH S N,et al.Effect of chromium accumulation on photosynthetic pigments,oxidative stress defense system,nitrate reduction,proline level and eugenol content ofOcimumtenuiflorumL.[J].Plant Science,2004,167(5):1159-1169.
[9]ARUN K S,CARLOS C,HERMINIA L T,et al.Chromium toxicity in plants[J].Environment International,2005,31:739-753.
[10]黃淮青,曾萍,韓寶福,等.熒光碳點的合成及對釀酒酵母的毒性研究[J].無機化學學報,2012,28(1):13-19.
[11]RAY S C,ARINDAM S,NIKHIL R,et al.Fluorescent carbon nanoparticles:Synthesis,characterization,and bioimaging application[J].J Phys Chem C,2009,113(43):18546-18551.
[12]NIU X,LIU G,LI L,et al.Green and economical synthesis of nitrogen-doped carbon dots from vegetables for sensing and imaging applications[J].RSC Advance,2015,5(115):95223-95229.
[13]LI Z,NI Y,KOKOT S.A new fluorescent nitrogen-doped carbon dot system modified by the fluorophore-labeled ssDNA for the analysis of 6-mercaptopurine and Hg(Ⅱ)[J].Biosensors & Bioelectronics,2015,74:91-97.
[14]LIU L,FENG F,PAAU M C,et al.Carbon dots isolated from chromatographic fractions for sensing applications[J].RSC Advances,2015,5(129):106838-106847.
[15]BARATI A,SHAMSIPUR M,ABDOLLAHI H.Hemoglobin detection using carbon dots as a fluorescence probe[J].Biosensors & Bioelectronics,2015,71:470-475.
Preparation of Nitrogen Doped Carbon Dots and Their Application as Fluorescence Probe for Cr6+Detection
ZENG Qiang1,ZHU Hao-bo1,ZHU Hong-yan1,ZHU Xiao-li1,DAI Chang-xiong1,DENG Chun2,HE Yu2,ZHANG Xiu-hua2,SONG Gong-wu2
(1.WuhanHongjinlongPrintingCo.,Ltd.,Wuhan430056,China;2.CollegeofChemistry&ChemicalEngineering,HubeiUniversity,Wuhan430062,China)
Abstract:In this paper,using the Ganoderma lucidum spores as a carbon source,urea as a nitrogen dopant,nitrogen doped fluorescent carbon dots(N-CDs) were prepared with one-step ultrasound method.The prepared N-CDs were used as a fluorescence probe for Cr(6+) detection.The fluorescence intensity of N-CDs quenched after adding Cr(6+).The fluorescence intensity showed a good linear relationship with the concentration of Cr(6+) range from 0 to 300 μmol·L(-1),the correlation coefficient was 0.9818 and the detection limit was 0.3 μmol·L(-1).The recoveries of real samples were 94%~102%,which indicated a good practical application of N-CDs.
Keywords:chromium(Ⅵ);Ganoderma lucidum spores;fluorescent carbon dots;nitrogen doped;fluorescence detection
中圖分類號:O 613.71
文獻標識碼:A
文章編號:1672-5425(2016)03-0048-05
doi:10.3969/j.issn.1672-5425.2016.03.013
作者簡介:曾強(1980-),男,湖北武漢人,工程師,研究方向:環境分析,E-mail:zengqiang@hjlprint.com。
收稿日期:2015-12-28

