硫化鋅精礦氧壓酸浸渣中硫和鐵的物相存在形式及其含量的測定
秦樹辰 蔣開喜 張邦勝 王海北
(北京礦冶研究總院,北京 100160)
硫化鋅精礦氧壓酸浸渣中硫和鐵的物相存在形式及其含量的測定
秦樹辰 蔣開喜*張邦勝 王海北
(北京礦冶研究總院,北京 100160)
利用X射線衍射(XRD)方法分析研究了硫化鋅精礦加壓酸浸渣的物相存在形式,總結了硫和鐵元素的存在形態,根據其相存在形式特點,提出并研究了在硫元素化學物相分析流程中同時測定鐵物相的方法。實驗表明,硫的相對誤差小于5%,各物相有較好的重現性;鐵物相分析誤差不及硫,但多數小于5%,基本上符合分析測試要求,具有一定參考價值。建立了一種快速、有效表征硫和鐵物相的方法,揭示了浸出渣中硫和鐵元素賦存狀態以及分布狀態,為工藝研究、渣相處理以及理論分析提供了一種有效的表征方法。
化學物相分析;浸出渣;硫;鐵;賦存狀態
0 前言
硫化鋅精礦通常含有閃鋅礦、黃鐵礦、方鉛礦和黃銅礦等多種礦物,加壓酸浸過程中多種復雜礦物發生反應較為復雜[1]。硫化礦被高溫氧化成單質硫或硫酸鹽,浸出的金屬離子發生氧化、水解等反應,形成含有鉛鐵礬類硫酸鹽等復雜化合物的浸出渣[2];而且此類復雜化合物會因浸出條件不同而發生轉變,如黃鉀鐵礬會因溫度不同而發生轉變[3]。硫化鋅精礦加壓酸浸渣成分復雜,準確定量分析其組成,尤為困難。
硫和鐵的物相分析有利于研究浸出渣中各種物相分布情況,能夠用于元素賦存狀態和渣相形成機理研究[4]。
目前硫元素化學物相分析一般呈固定模式[5]:首先利用化學反應或有機試劑分析單質硫含量,然后將其殘渣溶解于鹽溶液中分析硫酸鹽含量,再用強氧化性試劑溶解二次殘渣分析硫化物含量,或者直接用差減法計算硫化物含量。一般鐵化學物相分析因礦石中含有磁鐵礦、赤鐵礦、黃鐵礦等多種含鐵礦物,其分析流程較為繁瑣[6]。
針對本實驗浸出渣,采用傳統分析方法會非常繁瑣。因此,將硫和鐵化學物相分析方法相結合,在分析硫化物的同時測定其鐵含量,分析鐵礬類硫酸鹽的同時測其鐵含量,可以同時查明浸出渣中硫和鐵元素的狀態及含量。
1 實驗部分
1.1 儀器與試劑
Rigaku D/max-Ultima IV型X-射線衍射分析儀(日本理學公司),720/725 系列離子色譜分析儀(美國安捷倫科技公司)。
四氯化碳、氯化鈉、溴素均為分析純,實驗所用水均為二次去離子水。
1.2 浸出渣性質
浸出渣是硫化鋅精礦在溫度為150 ℃下氧壓酸浸1.5 h形成的,為了明確渣相組成,對其進行XRD法分析,其衍射圖見圖1。
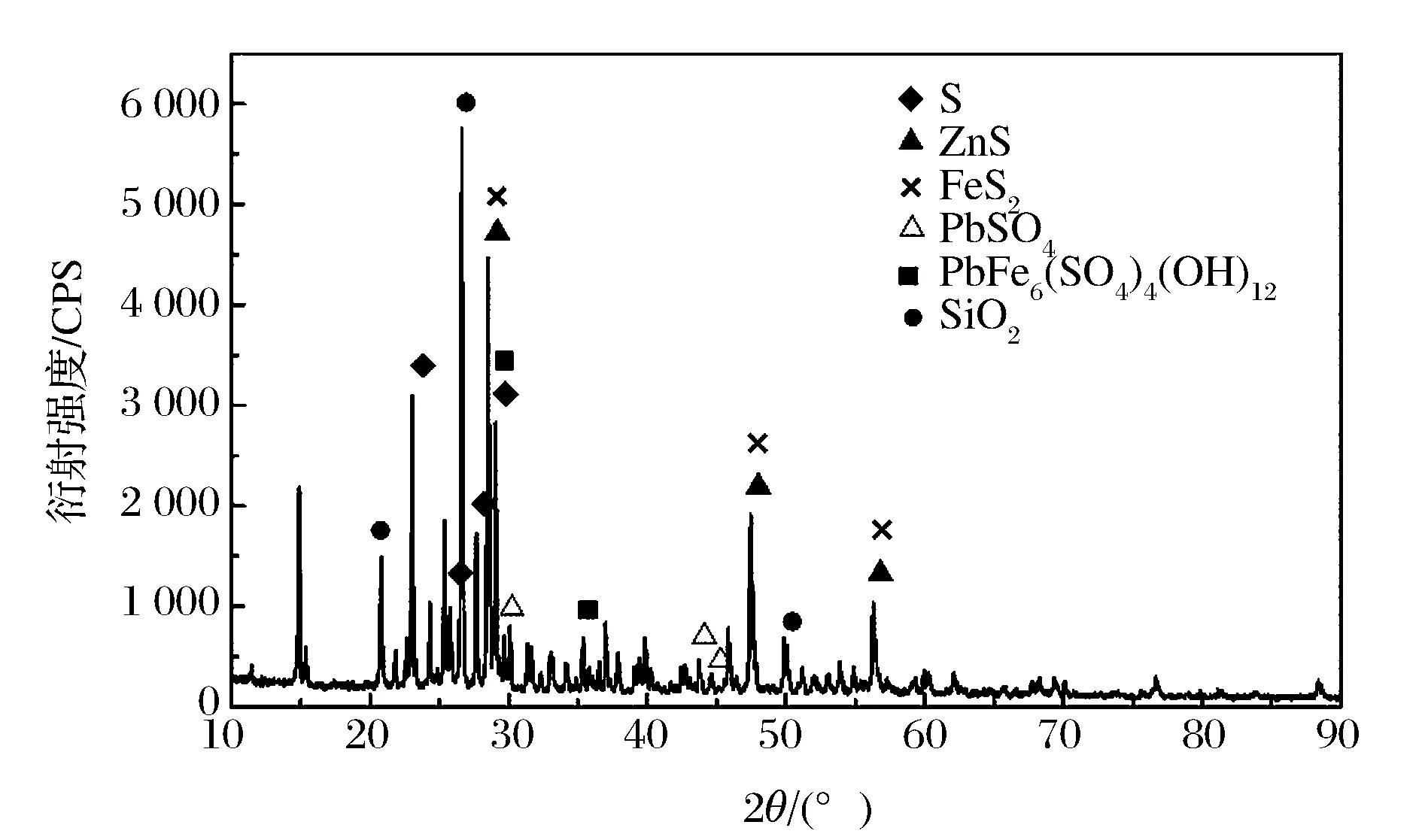
圖1 浸出渣XRD圖Figure 1 XRD pattern of leaching residue.
從圖1中可以看出,浸出渣成分復雜,含有殘余閃鋅礦、黃銅礦、黃鐵礦和二氧化硅以及生成的單質硫、硫酸鉛、硫酸鈣和鉛鐵礬類硫酸鹽。硫在浸出渣中存在狀態主要是單質硫、硫化物、可溶性硫酸鹽和鐵礬類硫酸鹽四類。硫化物包括閃鋅礦、黃鐵礦和黃銅礦,可溶性硫酸鹽包括硫酸鈣和硫酸鉛。鐵存在狀態主要是硫化物含鐵和鐵礬類硫酸鹽含鐵。硫化物含鐵是黃鐵礦、黃銅礦以及閃鋅礦中類質同象的鐵。
1.3 元素硫的測定
目前單質硫含量分析方法主要有化學反應法和有機試劑萃取法。化學法分相過程存在很多影響因素,故而準確度不高;有機試劑萃取法影響因素較少,準確度較高,缺點是使用的溶劑是易揮發有毒的四氯化碳或者二氯化烯。蘇秀珠等[7]研究了化學反應法和萃取法誤差分析,研究指出萃取法測定值的絕對誤差和相對誤差都比化學法測定的數據小近10倍,萃取法測定準確度更高、偏差極小,具有更高的精密度和準確度。故實驗選用有機試劑萃取法。
1.3.1 測定原理
根據相似相容原理:由于極性分子間的電性作用,使得極性分子組成的溶質易溶于極性分子組成的溶劑,難溶于非極性分子組成的溶劑;非極性分子組成的溶質易溶于非極性分子組成的溶劑,難溶于極性分子組成的溶劑。
硫單質是非極性分子,能夠溶于非極性溶劑四氯化碳中,其它形態的硫在四氯化碳中溶解度極小,從而與其它狀態的硫分離,而且四氯化碳不會對硫酸鹽、硫化物造成溶解、分解、氧化等影響。四氯化碳沸點較高(76.8 ℃),在加熱條件下進行單質硫溶解較為快速而且完全。溶解有硫的四氯化碳溶液揮發或者蒸餾結晶,使得硫單質析出,通過稱量析出硫單質重量即可知元素硫含量。
1.3.2 測定方法
準確稱取2.0~2.5 g(精確至0.001 g)渣樣于干燥的縮口燒杯中,加入100 mL 50~60 ℃四氯化碳溶液,置于溫度為50~60 ℃恒溫水浴振蕩器中加熱浸出振蕩1 h,靜止后快速將上層清液過濾于恒重干燥燒杯中,殘渣再加入50 mL熱四氯化碳溶液,繼續浸取0.5 h,在原濾紙上過濾,用熱四氯化碳洗滌3~5次,濾液在低溫電熱板上加熱,蒸餾四氯化碳至3~5 mL后,將燒杯移入75~80 ℃的烘箱中蒸干,保持45 min。取出后冷卻至室溫,稱量。
1.4 硫酸鹽的測定
目前硫酸鹽的分析方法主要是利用水、弱酸性的氯鹽溶液或堿性的碳酸鈉作為溶劑溶出硫酸鹽,形成游離態硫酸根離子,通過測定硫酸根離子從而確定硫酸鹽含量。溶液中硫酸根離子測定方法主要有經典的硫酸鋇重量法、離子色譜法、滴定法等,經典的硫酸鋇重量法雖然適用范圍廣、準確度高,但耗時長、操作繁瑣,影響晶粒生長大小因素較多(溶液酸度、氯化鋇加入速度及攪拌速度都會對結果造成影響),對實驗操作人員技術要求高。離子色譜法具有操作簡便、線性范圍寬、靈敏、準確等優點,能夠滿足本實驗要求。因此,實驗采用離子色譜法測定硫酸根離子含量[8]。
考慮到本渣樣中所含硫酸鹽為方鉛礦產生的硫酸鉛,在水中不溶解,同時含有少量的殘余硫化物,因此選擇中性氯化鈉溶液作為溶劑。
1.4.1 測定原理
渣樣中難溶于水的硫酸鈣和硫酸鉛都能夠溶解于氯化鈉溶液。高濃度氯離子絡合性較強,與硫酸鉛發生絡合反應會生成更穩定的四氯合鉛酸根離子,提高了硫酸鉛溶解性,同時釋放了硫酸根離子。硫酸鉛與氯鹽反應形成PbCl42-和SO42-。其反應式為:
只有硫酸鋇不溶于氯鹽溶液中,而渣樣中并不含有硫酸鋇,故不影響硫酸鹽的測定。
1.4.2 測定方法
稱取上述浸取單質硫后的殘渣1.0~2.0 g(精確至0.001 g)于縮口燒杯中,加入100 mL中性氯鹽溶液,浸取1 h。用致密濾紙過濾于250 mL容量瓶中,用去離子水洗滌5~7次,定容后利用離子色譜法測定SO42-含量。
1.5 硫化物的測定
目前硫化物分析方法主要是利用飽和溴水、乙酸-乙酸銨或稀硝酸溶解硫化物或者差減法。本試樣中含有多種硫化物和不溶的鐵礬類物質,實驗采用飽和溴水溶出硫化物的方法。
1.5.1 測定原理
渣樣中硫化物如閃鋅礦、黃鐵礦和方鉛礦能夠和飽和溴水發生反應,使得硫化物中的硫被氧化為可溶性SO42-。其反應式為:
1.5.2 測定方法
準確稱取上述浸取可溶性硫酸鹽后的殘渣,加入飽和溴水溶液,浸取1 h,用快速濾紙過濾浸出液,多次洗滌后定容至250 mL容量瓶中,利用離子色譜法測定SO42-和Fe含量。
1.6 鐵礬類硫酸鹽的測定
渣樣中含有的鐵礬類硫酸鹽為鉛鐵礬,在飽和鹵族溶液中既不溶解也不反應,殘留于渣中。通過分析殘渣中S和Fe含量即為鐵礬類硫酸鹽中S和Fe含量。
1.7 總硫的測定
1.7.1 測定原理
樣品在1 250~1 300 ℃空氣中燃燒,硫化物中的硫、單質硫及硫酸鹽中的硫都轉變為SO2后,用過氧化氫溶液吸收并氧化成H2SO4,以甲基紅、次甲基藍為混合指示劑,用氫氧化鈉標準溶液滴定。其反應式如下:
1.7.2 測定方法
準確稱取0.1~0.5 g(精確至0.001 g)渣樣,蓋上0.5 g紫銅粉,放入1 300 ℃的燃燒爐中預熱1 min,然后開始抽氣、吸收,控制抽氣速度;10 min后,用NaOH標準溶液滴定,直到溶液由紫色轉為亮綠色,即為滴定終點。
2 結果與討論
按實驗方法對多個浸出渣進行了分析,同時分析硫和鐵元素含量。
2.1 硫的物相分析
2.1.1 影響硫物相分析的因素
硫化學物相分析過程中,主要的影響因素有粒度和溫度兩方面。減小粒度能夠提高礦物有效表面積,溶解速度加快;升高溫度能夠提高其溶解速度和溶解度。四氯化碳萃取單質硫過程中,粒度太大和溫度太低會造成單質硫溶解不完全,樣品粒度需要磨至小于或等于0.074 mm。溫度需要保持在60 ℃左右。否則對后續硫的其它物相分析造成較大影響。
在分析硫化物過程中,硫化物可能會浸出不完全或者氧化不完全產生單質硫,造成硫化物含量偏低,也會使得不可溶性硫酸鹽含量偏高。可以通過加入強氧化劑促進其氧化反應,也可以加入絡合金屬陽離子試劑,降低生成物濃度,促進硫化物氧化浸出。但是添加過多的液溴會包裹試樣,同樣會影響測量值[9]。
2.1.2 硫物相分析的準確度實驗
物相分析存在浸出完全和相互間的干擾等影響,按照實驗方法考察方法的準確度和精確度,通過各分相之和與實際總硫對比考察其準確性(各分相之和與總硫的差值用相對誤差表示,見表1),并且通過配制標準物質驗證硫物相分析的準確性(見表2),通過平行重復測定考察其精密度(表3)。

表1 加壓浸出渣中硫物相分析結果Table 1 Phase analysis results for sulfur in pressure leaching residue /%
從表1可以看出,樣品硫各物相分析結果之和與總硫含量一致性較好,其相對誤差小于5%,基本上符合分析測試要求。
由于浸出渣成分的特殊性和復雜性,沒有與其一致的標準物質,因此利用升華硫、硫酸鉛、硫酸鈣和硫化鋅試劑配制標準物質作對比,驗證其硫物相分析的準確性。分析結果如表2所示,由表2可以看出,單質硫的分析準確性最高,相對偏差能夠達到0.5%。其它硫物相分析也較好,相對偏差均低于5%。
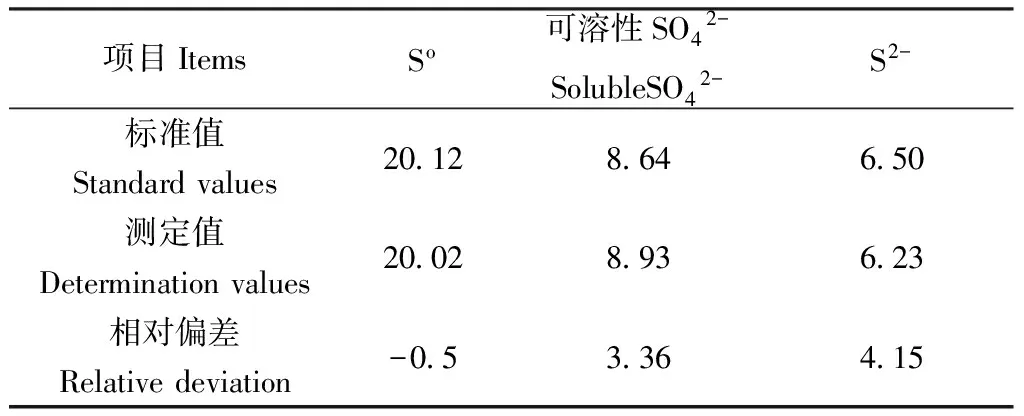
表2 配制標準物質對比結果Table 2 Comparison of standard material preparation /%
2.1.3 硫物相分析的精密度實驗
為了考察硫物相分析的穩定性,通過平行重復測定5次以考察其測定的精密度,結果見表3。
從表3可以看出,樣品中硫在不同相態的含量均能有較好的重現性,單質硫的相對標準偏差RSD最小,其它各種硫物相的RSD也能滿足測試要求。

表3 硫物相分析測定精密度Table 3 Precision tests for sulfur phase analysis (n=5) /%
2.2 鐵的物相分析
2.2.1 影響鐵物相分析的因素
鐵的物相是在硫化學物相分析流程中同時測定的,鐵物相分析結果影響主要有兩方面:一方面是硫化學物相分析流程是否將各個物相分相準確,且沒有串相;其影響因素和硫物相分析一致,主要是粒度和溫度的影響。另一方面是測定元素鐵的準確性,采用離子色譜儀能夠滿足分析要求。
2.2.2 鐵物相分析的準確度實驗
將鐵的物相分為硫化鐵和鐵礬兩類物相,通過兩類物相之和與總鐵含量對比考察其準確度(見表4)。
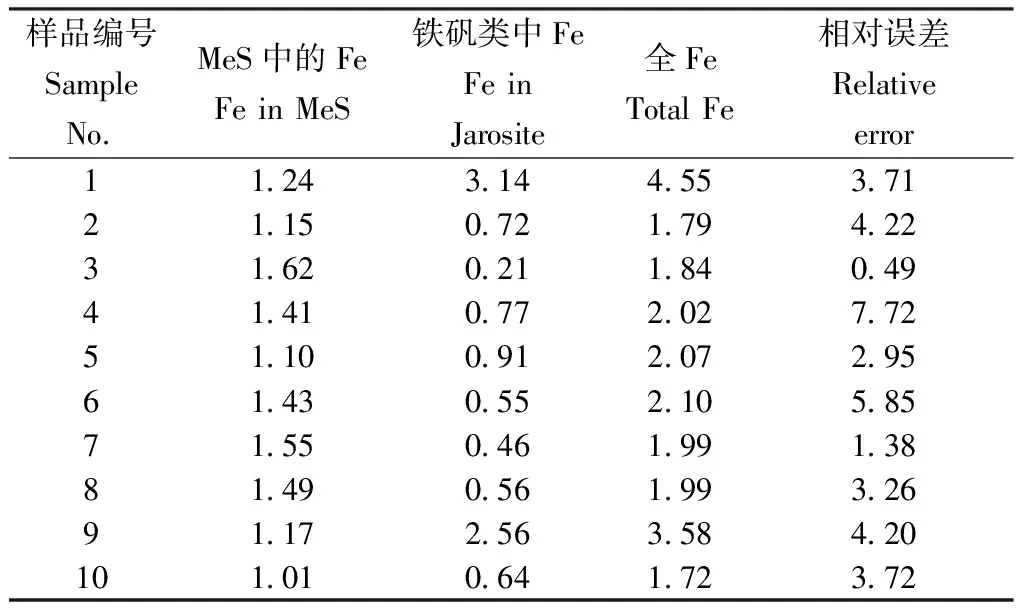
表4 加壓浸出渣鐵物相分析結果Table 4 Phase analysis results for iron in pressure leaching residue /%
從表4可以看出,兩類鐵相態分析結果相對誤差最大為0.49%~7.72%,最小為0.49%,其數據多數都小于5%,鐵的測定符合測試準確度要求。
2.2.3 鐵物相分析的精密度實驗
為了考察鐵物相分析的穩定性,通過平行重復5次測定,考察其精密度,結果見表5。
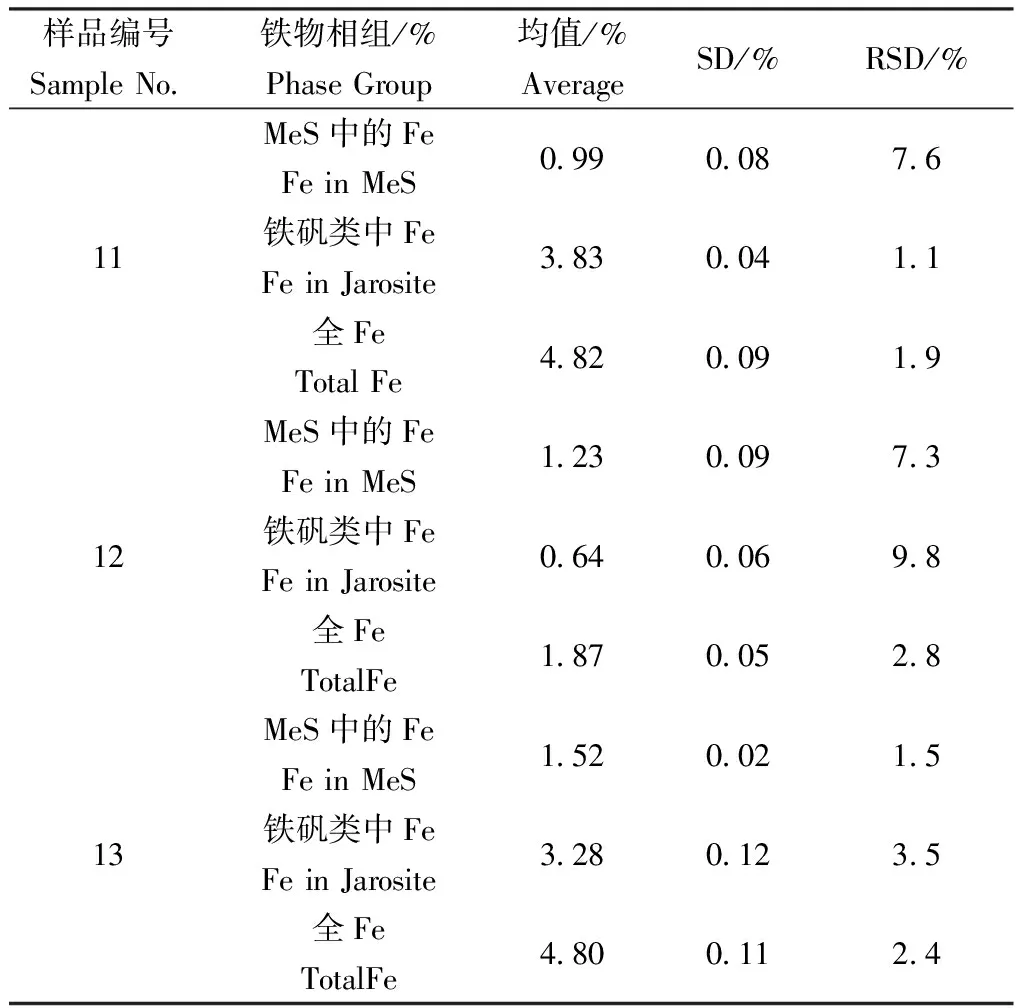
表5 鐵物相分析測定精密度Table 5 Precision tests for iron phase analysis(n=5)
從表5可以看出,鐵的各相分析結果有少許波動,鐵的物相分析精密度較硫物相分析的精密度差,但是也能夠滿足測定要求,能對實驗有一定的參考性。
3 結語
根據具體試樣類型擬定相應的分析測定方法,其數據的重現性、準確性以及快速分析對于生產、科研的需求是至關重要的。硫和鐵的物相分析可以定量表征渣相組成,能夠反映浸出過程中發生的反應,可用于計算各種物相的轉化率。有利于冶煉工藝制定和有效控制有價金屬浸出,避免無用礦物溶出,實現高效提取有用礦物,同時也有利于渣相形成的理論研究。
本文建立了硫化鋅精礦氧壓酸浸渣中各硫物相的逐級順序測定,同時測定鐵物相的分析方法。其硫和鐵各物相加和與總硫和總鐵吻合較好。硫和鐵的化學物相分析能夠滿足分析要求。可用于具有類似組成的渣樣物相分析。
[1] 張新莊,張向陽,張利濤.高鐵低品位硫化鉛鋅混合精礦氧壓酸浸試驗研究[J].濕法冶金(HydrometallurgyofChina),2015,34(1):6-9,20.
[2] 唐際流,周曉源.鐵在硫化鋅精礦加壓浸出過程中的行為[J].有色金屬(冶煉部分)[NonferrousMetals(ExtractiveMetallurgy)],1987(3):32-35.
[3] Dutrizac J E. Converting jarosite residues into compact hematite products[J].JOM,1990,42(1):36-39.
[4] 有色金屬工藝分析叢書編輯委員會.礦石和工業產品化學物相分析[M].北京:冶金工業出版社,1992.
[5] 黃寶貴,張志勇,楊林,等.中國化學物相分析研究的新成就(下)[J].中國無機分析化學(ChineseJournalofInorganicAnalyticalChemistry),2011,1(3):8-15.
[6] 張琦.硫物相分析測定方法的應用[J].黃金.,2006,27(11):52-54.
[7] 蘇秀珠,許濤,廖占丕,等.礦石中硫賦存狀態分析方法[J].武漢工程大學學報(JournalofWuhanInstituteofTechnology),2012,34(12):16-20.
[8] 劉春峰.離子色譜法測定鎳鈷錳氫氧化物中硫酸根離子含量[J].中國無機分析化學(ChineseJournalofInorganicAnalyticalChemistry),2013,3(增):29-30.
[9] 黃正海.飽和溴水浸取硫化鐵的一些問題及鐵礦石中硫化鐵的測定[J].分析化學(ChineseJournalofAnalyticalChemistry),1985,13(5):377-379.
Study on Phase Form and Content of Sulfur and Iron in OxygenPressure Acidic Leaching Residue of Sphalerites
QIN Shuchen, JIANG Kaixi*, ZHANG Bangsheng, WANG Haibei
(BeijingGeneralResearchInstituteofMining&Metallurgy,Beijing100160,China)
In this paper, the phase form of sulfur and iron in oxygen pressure acidic leaching residue of sphalerites was analyzed by XRD.According to the characteristics of the phase forms, a new method was developed and used to investigate the phase form of iron in the process of analyzing chemical phase of sulfur element. The results showed that the standard deviation for sulfur was less than 5%. Each phase form had good reproducibility. The standard deviation for iron was not good as for sulfur, but still less than 5%. The method can basically meet the requirement for analysis and is valuable. In this article, a rapid and effective method for quantitative characterization of the phase form of sulfur and iron was established. It can be used to reveal the occurrence state and distribution of sulfur and iron element in oxygen pressure acidic leaching residue of sphalerites. And it also provides an effective characterization method for process study, slag phase processing and theoretical analysis.
chemical phase analysis; leaching residue ;sulfur; iron; occurrence
2016-01-27
2016-2-18
國家自然科學基金——硫化礦加壓濕法冶金的機理研究項目(5143000389)資助
秦樹辰,男,在讀研究生,主要從事有色金屬冶煉工藝應用與理論研究。E-mail:qshuchen@163.com
*通信作者:蔣開喜,男,教授。E-mail:jiangkx@bgrimm.com
10.3969/j.issn.2095-1035.2016.03.014
O658.6;TH744.15
A
2095-1035(2016)03-0057-05

