運用手持技術探究銀氨溶液的成分
任峰 張典俊 郭孝兵
摘要:從理論推導和實驗探究兩個方面,對硝酸銀溶液與氨水反應制得的銀氨溶液的堿性和主要成分進行了探討,證明用該方法配制出來的銀氨溶液呈弱堿性,其溶質主要成分不是Ag(NH3)2OH,而應是Ag(NH3)2NO3。
關鍵詞:銀氨溶液;成分分析;手持技術;實驗探究
文章編號:1005–6629(2016)3–0073–03 中圖分類號:G633.8 文獻標識碼:B
銀氨溶液又稱托倫試劑(Tollens reagent),用于檢驗和定量測定有機物中含有的醛基。銀氨溶液檢驗醛基時發生的反應被稱為銀鏡反應,該反應是大學及中學有機化學中鑒定醛基化合物的一個典型實驗。人們常常認為銀氨溶液中的溶質是Ag(NH3)2OH。例如,人教版高中教材《有機化學基礎》中有關銀氨溶液的制備實驗的相關描述如下[1]:在潔凈的試管中加入1mL 2%的AgNO3溶液,然后邊振蕩試管邊逐滴加入2%的稀氨水,至最初產生的沉淀恰好完全溶解為止,制得銀氨溶液。并給出了銀鏡反應的化學方程式:
CH3CHO+2Ag(NH3)2OH△CH3COONH4+ 2Ag↓+3NH3+H2O。
由此可以看出,教材認為硝酸銀與氨水生成的銀氨溶液的主要成分是Ag(NH3)2OH。并且由于Ag(NH3)2OH是強堿,許多人就想當然地認為銀氨溶液的堿性應該比配制銀氨溶液所用的氨水堿性強。事實果真如此嗎?此處所得銀氨溶液中的溶質主要成分究竟是不是Ag(NH3)2OH?本文從反應原理分析和實驗驗證兩個方面進行探討。
銀氨溶液的制備實驗中發生的先后反應可以用化學方程式表示如下[1]:
①AgNO3+NH3·H2O=AgOH↓+NH4NO3
②AgOH+2NH3·H2O=Ag(NH3)2OH+2H2O
由反應②可見,實驗中所得溶液的溶質主要成分似乎是Ag(NH3)2OH。但事實并非如此,因為Ag(NH3)2OH是強堿,其電離出的OH-必然會跟第①步中的產物NH4NO3電離出的NH4+結合生成NH3·H2O:
③Ag(NH3)2OH+NH4NO3=Ag(NH3)2NO3+ NH3·H2O
而③式生成的NH3·H2O又會作為反應物參與②式的化學反應。
因此,由①+②+③得:
④AgNO3+2NH3·H2O=Ag(NH3)2NO3+2H2O

所以Ag(NH3)2NO3只能呈微弱堿性,而Ag(NH3)2OH呈強堿性。因此,我們只要通過實驗測定按教材中所用的方法制得的銀氨溶液的pH,就可以證明銀氨溶液的成分。
2.1 實驗過程
為了驗證上述推理,我們利用以下藥品和器材完成了兩個實驗。
實驗藥品:2%的AgNO3溶液、約2%的氨水
實驗器材:燒杯、pH傳感器(已校準)、滴數傳感器(已校準)、磁力攪拌器等
實驗1 用pH傳感器測定約2%氨水的pH,其pH為11.69。
實驗2 按圖1所示裝置,邊用磁力攪拌器攪拌邊向25.00mL 2% AgNO3溶液中逐滴加入上述氨水,用pH傳感器和滴數傳感器同時測量燒杯內溶液的pH和所用氨水的體積,直到生成的沉淀完全溶解,繼續滴加1~2mL氨水。實驗測得溶液的pH隨氨水加入體積的增加的變化曲線如圖2所示。重復多次實驗,所得曲線均與圖2相似。
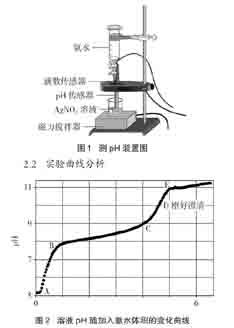
由圖2可以看出,曲線起點A點AgNO3溶液的pH為5.16,呈酸性。這是因為AgNO3溶液水解的原因造成的。隨著氨水的加入,AB之間pH快速升高,此時能看到有白色沉淀生成。B點pH為7.9左右。BC之間開始生成大量沉淀,后來沉淀又逐漸減少。C點后,沉淀量明顯減少,溶液逐漸變得澄清,到達D點時溶液迅速變得澄清透明。此時D點pH為10.29,用去的氨水體積為4.71mL,約為AgNO3溶液體積的1/5。
圖2中的pH曲線出現了兩個突躍:AB段與CE段。在AB段,溶液由AgNO3溶液的弱酸性變為堿性,只需少量氨水即可,因而會出現pH的突躍;在C點,AgOH的溶解已經接近尾聲,此時加入的氨水不會繼續被反應物大量消耗,使得溶液中的OH-離子濃度快速升高,因而再次出現pH的突躍。CE段的pH突躍標志著配制銀氨溶液的化學反應已經完成。
圖2中的pH曲線出現了兩個相對平緩的上升階段:BC段與E點之后。在BC段,雖然加入了大量的氨水,但是pH并沒有顯著升高,這是因為加入的氨水主要用于AgOH的生成和AgOH的溶解,氨水被消耗殆盡,因而溶液中的OH-的濃度沒有明顯的變化。在E點之后,溶液的pH僅有緩慢升高,其原因顯然是因為此時溶液的pH較大,氨水濃度的增大對pH影響就非常有限了。
2.3 實驗數據分析
(1)查相關資料[2]可知:實驗中使用的2%硝酸銀溶液密度為1.015 g·mL-1,則其物質的量濃度為:
c(AgNO3)=1.015 g·mL-1×1000 mL·L-1×2%÷(170 g·mol-1)=0.120 mol·L-1。
(2)用濃氨水配制2%稀氨水時,由于濃氨水的質量分數不準確,導致稀釋后的2%氨水濃度也不準確。因此用鹽酸作為標準液標定本實驗中使用的約2%氨水濃度為1.275 mol/L。則其OH-物質的量濃度為:
c(OH-)=[c(NH3·H2O)×Kb]1/2=[1.275×1.8×10-5]1/2 mol/L=4.79×10-3 mol/L
pH=11.68。
此計算值與實驗1中測得的氨水的pH為11.69非常接近。由于2%氨水的物質的量濃度大約是2%硝酸銀溶液的10倍,根據反應④,AgNO3~2NH3·H2O,所以實驗2中所用氨水的體積約為AgNO3溶液體積的1/5。此比例關系恰恰也證明了所得銀氨溶液的主要成分是Ag(NH3)2NO3。

近似:x很小,故b-2×(a-x)≈b-2a
a、b均為混合后體積增大后的濃度,其中a=0.120 mol/L×25.00mL÷(25.00+4.71)mL= 0.100 mol/L,b=1.275 mol/L×4.71mL÷(25.00+ 4.71)mL≈0.202 mol/L。
求得c(Ag+)=x≈a÷[(b-2a)2×Kf]=a÷[(b-2a)2×1.12×107]
=0.100÷[(0.202-2×0.100)2×1.12×107]
=2.2×10-3 mol/L。
由于Ag+濃度很低,水解程度又很小,因此其水解作用忽略不計。此時,c[Ag(NH3)2+]=a-x=(0.100-2.2×10-3) mol/L≈0.098 mol/L。c(NH3·H2O)=b-2a≈0.002 mol/L
因為c/Kb=0.002÷(1.8×10-5)<400,則c(OH-)=[-Kb+(Kb2+4cKb)1/2]÷2
=[-1.8×10-5+(1.82×10-10+4×0.002×1.8×10-5)1/2]÷2=1.81×10-4 mol/L pH=10.26。
此計算結果與實驗2測定的溶液剛好澄清時的pH 10.29非常接近,比2%氨水的pH小得多。既然銀氨溶液的堿性沒有配制銀氨溶液所用的氨水堿性強,那么就表明其主要成分的確為Ag(NH3)2NO3。
(4)與上述銀氨溶液物質的量濃度相當的Ag(NH3)2OH溶液,即濃度為0.098 mol/L的Ag(NH3)2OH溶液,由于其完全電離出OH-,所以其pH=14+lg0.098=12.99。與實驗2測定的溶液剛好澄清時的pH為10.29相比,Ag(NH3)2OH溶液的堿性要強得多。因此,實驗所得銀氨溶液中的溶質主要成分不可能是Ag(NH3)2OH。
3.1 方法分析
由于銀氨溶液在反應中生成Ag(NH3)2NO3和 Ag(NH3)2OH時,溶液的pH差異較大,Ag(NH3)2NO3是配位化合物,在水溶液中完全電離生成Ag(NH3)2和NO3-,而Ag(NH3)2+只能微弱電離出Ag+和NH3,所以Ag(NH3)2NO3溶液的OH-主要來自于NH3·H2O的電離,故溶液中OH-濃度較小,溶液的堿性較弱;而Ag(NH3)2OH為強堿,在水溶液中則是完全電離的,與Ag(NH3)2NO3等物質的量濃度時,OH-濃度要大得多,溶液堿性自然要強一點。而且,實驗過程中并無其他影響溶液pH的因素,所以,本實驗著眼于該原理,通過測定溶液的pH及其變化,準確度是高的,方法也是合理的。
3.2 結果分析
從實驗結果來看,實驗數據的準確性和理論計算結果是非常吻合的。微弱的差別可能源于儀器的靈敏度、溶液濃度的準確性、環境溫度等因素。所以,在實驗過程中,我們盡可能地排除干擾因素,如對pH傳感器做了多次校準,對溶液濃度進行了精確配制,對于氨水的物質的量濃度還進行了滴定處理等,以保障測量數據的準確性和實驗結果的可靠性。
無論是反應原理分析還是實驗探究結果均可以明確得出結論:硝酸銀溶液與氨水反應制得的銀氨溶液中溶質的主要成分不是Ag(NH3)2OH,而是Ag(NH3)2NO3;溶液的OH-主要來自于NH3·H2O的電離,故溶液僅呈弱堿性。基于上述推導和實驗探究,建議在高中教材中對乙醛的銀鏡反應的化學方程式做適當的修改。修改以后的化學方程式為:
CH3CHO+2Ag(NH3)2NO3+H2O
CH3COONH4+2Ag↓+2NH4NO3+NH3。
參考文獻:
[1]課程教材研究所,化學課程教材研究開發中心.有機化學基礎(第二版)[M].北京:人民教育出版社,2007:53~54.
[2]北京師范大學.實用化學手冊[M].北京:北京出版社,1980:6,208.
[3]李成剛,何小穩.用于銀鏡反應的銀氨溶液成分及堿性的探究[J].化學教學,2013,(9):39~41.

