糯米糠抗氧化肽的制備工藝及自由基清除能力研究
李俐樺,殷鐘意,鄭旭煦,,*
(1.重慶工商大學環境與生物工程學院,重慶400067;2.重慶工商大學催化與功能有機分子重慶市重點實驗室,重慶400067)
糯米糠抗氧化肽的制備工藝及自由基清除能力研究
李俐樺1,殷鐘意2,鄭旭煦1,2,*
(1.重慶工商大學環境與生物工程學院,重慶400067;2.重慶工商大學催化與功能有機分子重慶市重點實驗室,重慶400067)
為開發利用糯米糠資源,研究了糯米糠抗氧化肽的制備工藝及自由基清除能力。選取中性蛋白酶為水解酶,以抗氧化肽還原力為指標,采用單因素實驗和正交實驗方法優化糯米糠抗氧化肽的制備工藝。結果表明,制備糯米糠抗氧化肽的最佳工藝條件為糯米蛋白底物濃度4%、[E]/[S]2%、pH7、酶解溫度40℃、酶解時間6h,在該條件下制備的糯米糠抗氧化肽對羥基自由基和超氧陰離子自由基的清除能力明顯優于米糠抗氧化肽,且存在一定的量效關系,提示糯米糠抗氧化肽可用作功能性食品或天然抗氧化劑被深入研究和開發利用。
糯米糠,抗氧化肽,酶解,自由基清除能力
米糠是大米加工的下腳料,含有米皮層或米胚碎米等,油脂含量14%~24%,蛋白質含量12%~18%;我國是世界上米糠資源最為豐富的國家,但米糠有效利用率較低,大多用作飼料,資源浪費較為嚴重,因此聯合國工業發展組織將其稱為一種未充分利用的原料[1]。近年來,隨著科技的不斷進步,米糠資源正逐步被國內外學者關注,深加工產品主要有稻米油、蛋白、植酸、膳食纖維、高蛋白飼料粉與抗氧化肽等,它們在食品、飼料、醫藥行業等均有廣泛應用前景[2]。但是,國內外關于糯米糠的研究極少,除早期可見糯米糠成分[3]和近期可見糯米抗氧化肽[4]的研究報道外,有關糯米糠深加工產品的開發利用鮮見報道。
眾所周知,清除自由基并防止其氧化作用對人體細胞及組織造成破壞的研究非常重要。多項研究表明[1,5-7],水解米糠蛋白而獲得的抗氧化肽不僅對自由基具有較強的清除作用,而且本身無任何毒副作用,其開發利用前景看好。近期本課題組研究發現,糯米糠的組成以及蛋白質含量和氨基酸組成不同于米糠,而糯米糠的抗氧化肽是否也有異于米糠抗氧化肽。為此,本文以糯米糠為原料,以米糠為對照,通過研究糯米糠抗氧化肽的制備工藝及自由基清除能力,旨在為糯米糠深加工產品的開發利用提供理論依據。
1 材料與方法
1.1材料與儀器
糯米糠、米糠重慶市長壽區鳳城鎮;脫脂糯米糠、米糠采用超臨界CO2萃取油脂后的糯米糠和米糠;中性蛋白酶9068-59-1(酶活力≥100U/mg) 上海金穗生物科技公司(BR);氫氧化鈉、鹽酸、三氯乙酸、鐵氰化鉀、Tris等均為國產分析純。
二元智能水浴HH-S2鄭州長城科工貿有限公司;高速冷凍離心機Biofuge Stratos D-37520 Osterode;PB-10酸度計賽多利斯科學儀器(北京)有限公司;V-1200可見光分光光度計MAPADA;微量移液器上海昂精密科學儀器有限公司制造;CL-4A型平板加熱磁力攪拌器鄭州長城科工貿有限公司;DZF-1B型真空恒溫干燥箱上海躍進醫療器械廠。
1.2實驗方法
1.2.1糯米糠抗氧化肽的制備工藝
1.2.1.1糯米糠蛋白的制備工藝首先將脫脂糯米糠粉碎,在烘箱中干燥15min,使其水分含量不高于8%;然后用pH10.0的NaOH溶液(1∶100)浸提3h,離心分離10min;最后用HCl溶液調節上清液的pH至4.5,待沉淀完全后,在6000r/min離心10min,將沉淀干燥,得到糯米糠蛋白[8]。
1.2.1.2糯米糠抗氧化肽的制備工藝首先在100℃水浴鍋中放入已配好一定底物濃度的糯米糠蛋白,加熱20min,進行蛋白質變性處理;然后冷卻至室溫后,加入中性蛋白酶,調節pH,在不同條件下進行酶水解;最后將水解液于90℃水浴鍋中加熱20min,再6000r/min離心10min,將清液真空干燥至水分含量不高于8%,得到糯米糠抗氧化肽,測定其性能指標[6]。
綜上所述,制備工藝流程為:脫脂糯米糠→粉碎烘干→浸提→離心分離→酸水解→離心分離→沉淀干燥→糯米糠蛋白→糯米糠蛋白溶液→熱變性處理→酶水解→滅酶→離心分離→濃縮干燥→糯米糠活性肽→性能測定。
1.2.1.3糯米糠抗氧化肽制備的單因素實驗
a.不同糯米蛋白底物濃度對還原力的影響以米糠抗氧化肽的還原力為指標,在[E]/[S]為2%、pH為7、酶解溫度為40℃、酶解時間為5h的條件下,分別選取糯米蛋白底物濃度為2%、3%、4%、5%、6%,按照1.2.1.2方法進行實驗。
b.不同加酶量[E]/[S]對還原力的影響以米糠抗氧化肽的還原力為指標,在底物濃度為3%、pH為7、酶解溫度為40℃、酶解時間為5h的條件下,分別選取加酶量[E]/[S]為1%、2%、3%、4%、5%,按照1.2.1.2方法進行實驗。
c.不同pH對還原力的影響以米糠抗氧化肽的還原力為指標,在底物濃度為3%、[E]/[S]為2%、酶解溫度為40℃、酶解時間為5h的條件下,分別選取溶液pH為6.0、6.5、7.0、7.5、8.0按照1.2.1.2方法進行實驗。
d.不同酶解溫度對還原力的影響以米糠抗氧化肽的還原力為指標,在底物濃度為3%、[E]/[S]為2%、pH為7、酶解時間為5h的條件下,分別選取酶解溫度為35、40、45、50、55℃按照1.2.1.2方法進行實驗。
e.不同酶解時間對還原力的影響以米糠抗氧化肽的還原力為指標,在底物濃度為3%、[E]/[S]為2%、pH為7、酶解溫度為40℃的條件下,分別選取時間為2、3、4、5、6h,按照1.2.1.2方法進行實驗。
1.2.1.4糯米糠抗氧化肽制備的正交實驗在單因素實驗的基礎上,采用L16(45)正交表(見表1)進行正交實驗,確定米糠抗氧化肽制備的最佳酶解工藝。
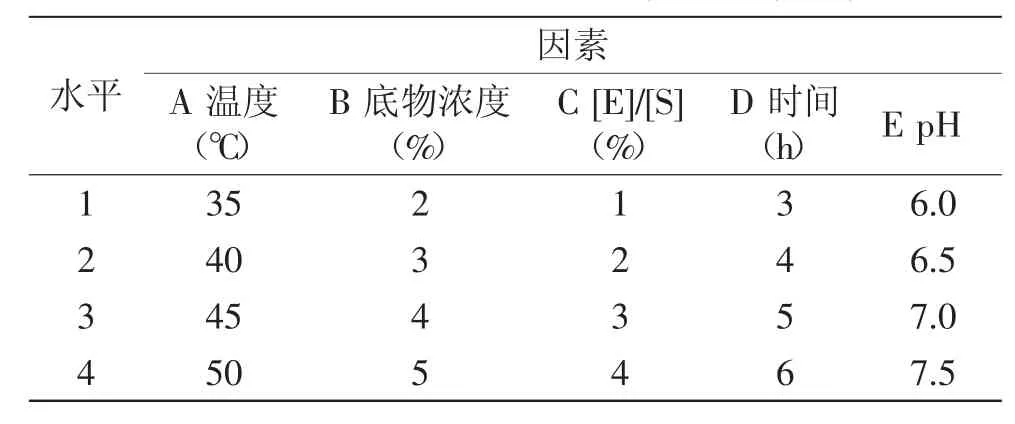
表1 酶解反應因素水平表Table.1 Factors and levels of enzymatic hydrolysis
1.2.2性能指標測定
1.2.2.1還原力的測定其反應原理[9]為K3Fe(CN)6與抗氧化劑混合后被還原成K4Fe(CN)6,K4Fe(CN)6進一步與Fe3+發生反應生成綠色Fe4[Fe(CN)6]3,其在700nm波長處有較大的吸收,吸光值越大,則抗氧化劑的還原能力越強。其測定方法[1]為:在15mL試管中分別加入糯米糠抗氧化肽樣品1mL、磷酸鹽緩沖液(0.2mol/L pH6.6)2.5mL和1%鐵氰化鉀5mL。在50℃水浴中反應20min,然后加入10%的三氯乙酸5mL,搖勻,吸取上清液2.5mL,加入2.5mL蒸餾水和0.5mL的 0.1%的三氯化鐵溶液,最后在700nm處測定吸光值。以樣品的吸光度值代表其抗氧化肽的還原力。
1.2.2.2羥基自由基的清除率測定配制濃度為9× 10-3mol/L的水楊酸-乙醇溶液、9×10-3mol/L雙氧水和9×10-3mol/L的硫酸亞鐵溶液。以75%乙醇為空白對照,分別加入1mL水楊酸-乙醇溶液,依次加入不同體積的糯米糠或米糠抗氧化肽樣品溶液、1mL硫酸亞鐵溶液和1mL雙氧水,加蓋搖勻,靜置1h,然后稀釋至10mL以終止反應,最后在510nm下測定吸光度值。
清除率(%)=(A0-A)/A0×100(A和A0分別表示加入樣品溶液和空白液后的吸光度值)。
1.2.2.3超氧陰離子的清除率測定配制0.1mol/L pH為8.0的Tris-HCl緩沖液,按表2加樣后迅速混勻,在320nm下每隔30s讀取吸光度,反應4.5min結束[6]。
清除率(%)=(A0-A)/A0×100
式中,A和A0分別表示加入抑制物和雙蒸水后的鄰苯三酚的自氧化速率,即每分鐘光吸收的平均變化率。

表2 活性肽清除O2-·加樣表Table.2 Sample table of antioxidant peptides for scavenging O2-·
2 結果與討論
2.1糯米糠抗氧化肽制備的單因素實驗
2.1.1不同糯米蛋白底物濃度對還原力的影響按1.2.1.2方法進行實驗的結果見圖1。
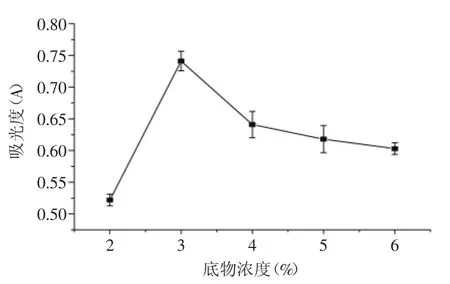
圖1 底物濃度對糯米糠抗氧化肽還原力的影響Fig.1 Effect of different concentration of substrate on reducing power
由圖1可知,隨著底物濃度增加,所得抗氧化肽的還原力呈現先增加后降低以至平緩的變化趨勢;當底物濃度達到3%時,還原能力達到最大。這是因為底物濃度過低,酶與底物結合幾率低,制備的抗氧化肽較少,還原力偏低;當底物濃度增加,酶與底物結合幾率增加,制備的抗氧化肽增多,還原力增強;
但底物濃度過大,底物分散困難,較多的底物相互包埋,反應難度增加,導致抗氧化肽減少,還原力下降。所以,酶解適宜的底物濃度為3%。
2.1.2不同加酶量[E]/[S]對還原力的影響按1.2.1.2方法進行實驗的結果見圖2。
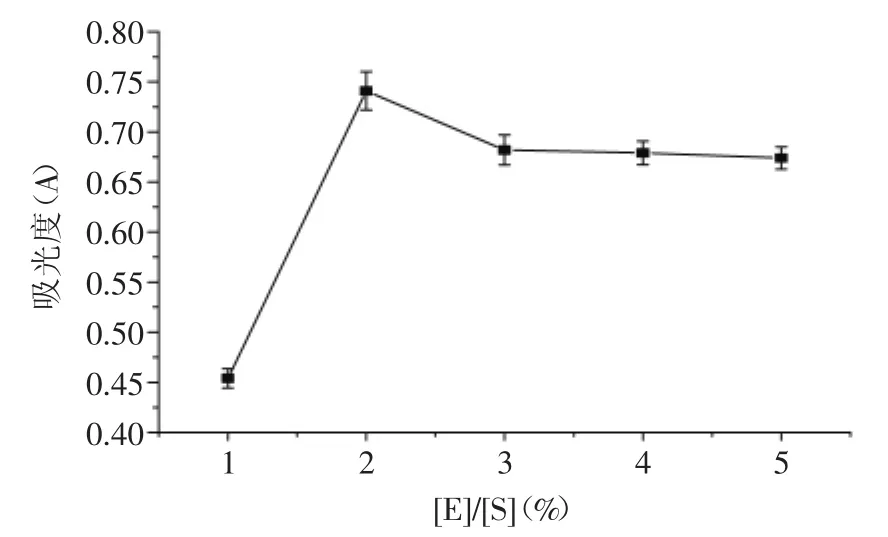
圖2 [E]/[S]對糯米糠抗氧化肽還原力的影響Fig.2 Effect of different dosage of[E]/[S]on reducing power
由圖2可知,隨著[E]/[S]的增加,所得抗氧化肽的還原力呈現先增加后降低以至趨于穩定的變化趨勢;當[E]/[S]為2%時,還原力達到最大。這是因為在一定的反應時間內,隨著[E]/[S]的增加,酶的活性基團增加,加速了酶促反應,制備的抗氧化肽增多,還原力增加;但是若[E]/[S]增加過多,酶促反應過快,水解度過大,具有抗氧化活性的肽段被水解,破壞了維持其抗氧化活性的結構上的完整特征[5],導致抗氧化肽還原力降低。所以,酶解工藝適宜的[E]/[S]在2.0%左右。
2.1.3不同pH對還原力的影響按1.2.1.2方法進行實驗的結果見圖3。
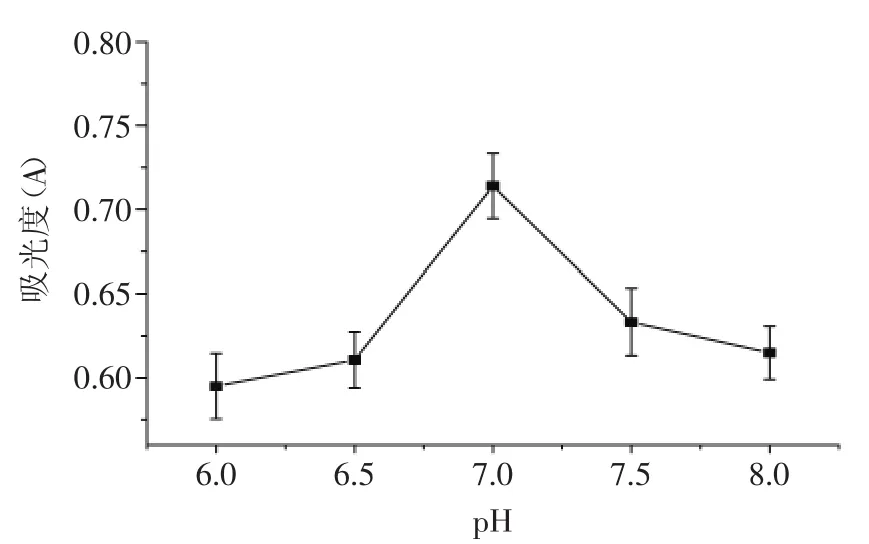
圖3 pH對糯米糠抗氧化肽還原力的影響Fig.3 Effect of different pH on reducing power
由圖3可知,糯米糠抗氧化肽的還原力隨著pH的增加呈現先增加后減小的變化趨勢,在pH=7.0時,還原力最強。這是因為中性蛋白酶的水解反應適宜在中性條件下進行。因此,酶解工藝適宜的pH在7.0左右。
2.1.4不同酶解溫度對還原力的影響按1.2.1.2方法進行實驗的結果見圖4。
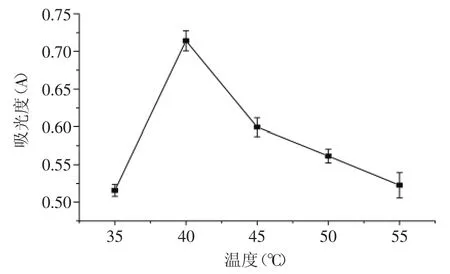
圖4 酶解溫度對糯米糠抗氧化肽還原力的影響Fig.4 Effect of different reaction temperature on reducing power
由圖4可知,隨著酶解溫度的升高,糯米糠抗氧化肽的還原力呈現先增加后降低的變化趨勢,當酶解溫度為40℃時,還原力達到最大值。這是因為酶解溫度較低時,酶活力增強,體系粘度降低,擴散系數增大,有利于酶促反應進行,所得抗氧化肽的還原力增加;但是,當酶解溫度過高時,將引起酶受熱變性,反應能力下降,導致制備的抗氧化肽還原力降低。所以,適宜的酶解溫度在40℃左右。
2.1.5不同酶解時間對還原力的影響按1.2.1.2方法進行實驗的結果見圖5。
由圖5中可知,隨著酶解時間的增加,糯米糠抗氧化肽的還原力隨之增強,當酶解時間超過5h后,其還原力有所下降。這可能是因為酶解時間影響了水解度,酶解時間過長,水解度過大,具有抗氧化活性的肽段被水解,導致抗氧化肽還原力下降。所以,適宜的酶解時間在5h左右。
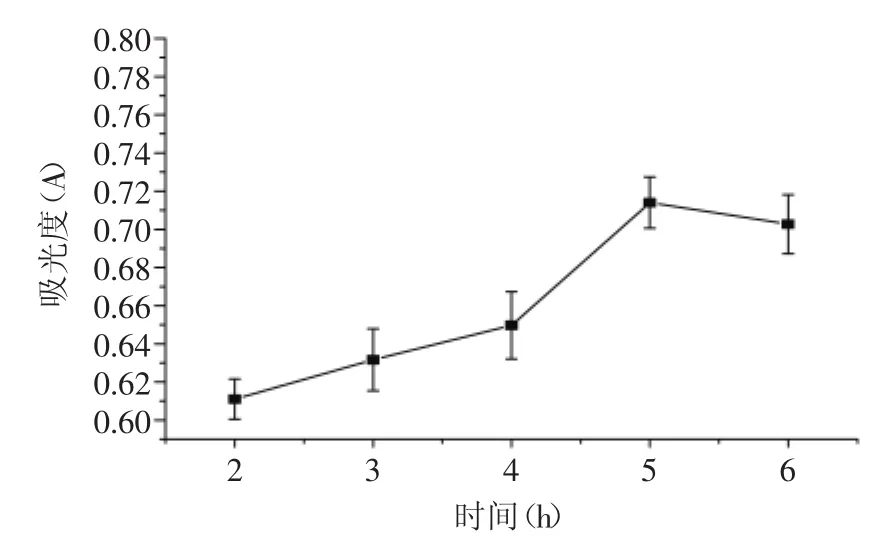
圖5 酶解時間對糯米糠抗氧化肽還原力的影響Fig.5 Effect of different reaction time on reducing power
2.2糯米糠抗氧化肽制備的正交實驗
根據表1進行正交實驗,實驗結果見表3。
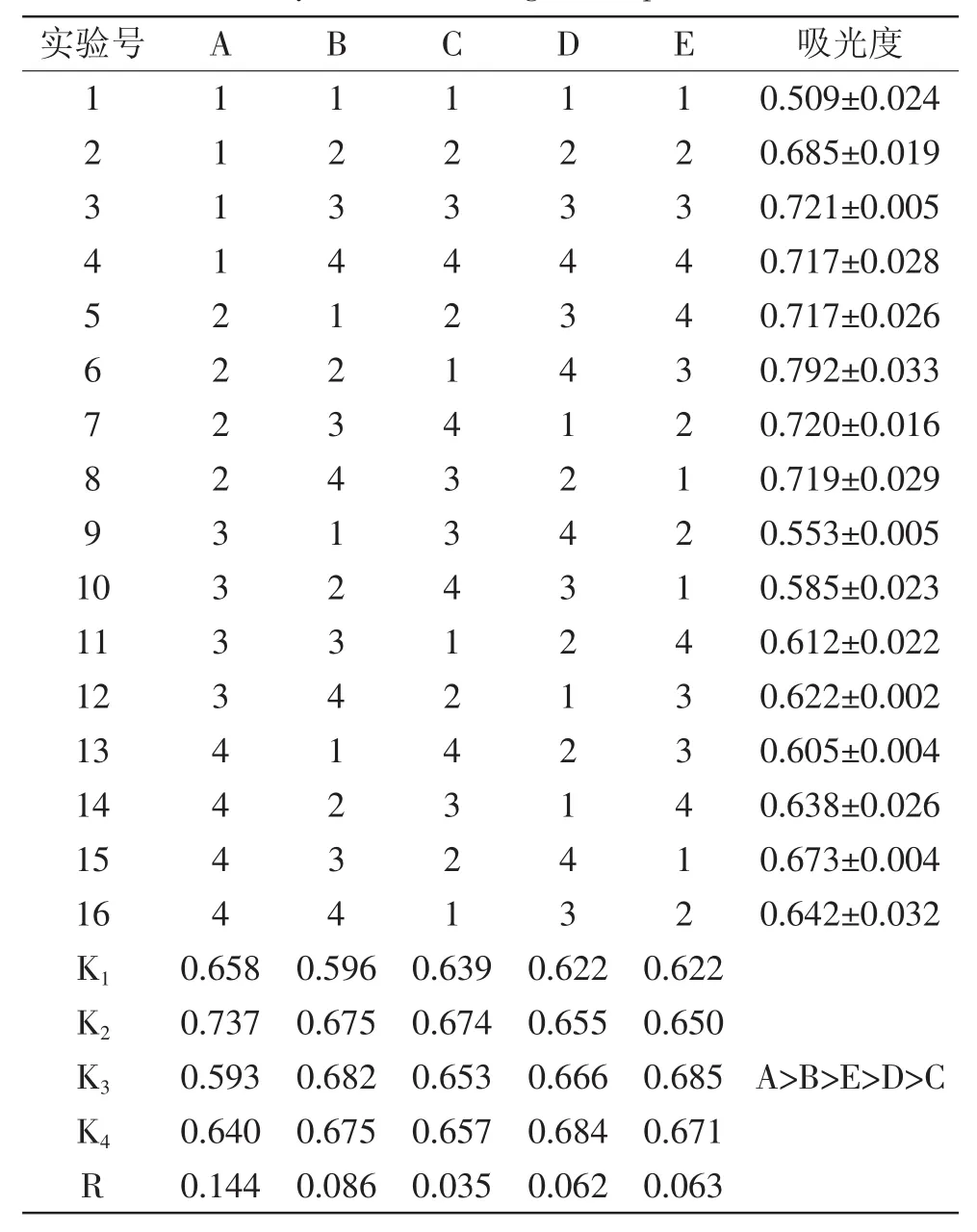
表3 正交實驗結果分析表Table.3 Analysis of the orthogonal experimental results
根據表3的極差分析可知,因素主次順序為:A>B>E>D>C,即影響糯米糠抗氧化肽還原力的因素主次順序為:酶解溫度>底物濃度>pH>酶解時間>加酶量,最佳酶解條件是A2B3C2D4E3,即酶解溫度為40℃、底物濃度為4%、[E]/[S]為2%、酶解時間為6h、pH為7.0;在此條件下,還原力測定的吸光度0.819,高于表3的各個實驗組。
2.3糯米糠抗氧化肽對羥基自由基和超氧陰離子自由基的清除能力
以米糠為對照,在上述最佳工藝條件下分別制備糯米糠和米糠抗氧化肽,進行羥基自由基和超氧陰離子自由基清除能力實驗,結果見圖6。
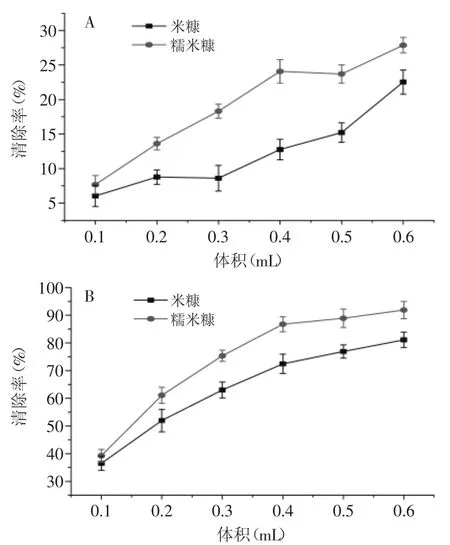
圖6 抗氧化肽對羥基和超氧陰離子自由基的清除能力Fig.6 Scavenging activities on·OH and O2-·free radicals ofantioxidant peptide
由圖6可知,米糠和糯米糠抗氧化肽對羥基自由基和超氧陰離子自由基的清除率均隨用量的增加而增大,存在一定的量效關系,且糯米糠抗氧化肽對羥基和超氧陰離子自由基的清除能力均明顯優于米糠抗氧化肽,可能的原因是糯米糠和米糠蛋白在中性蛋白酶水解下產生了不同結構或肽鏈的活性多肽,導致二者的自由基清除能力出現明顯差異。有關糯米糠抗氧化肽的純化和肽鏈結構鑒定研究,有待另文進一步報道。
3 結論
綜上所述,本文以中性蛋白酶為水解用酶,以抗氧化肽還原力為指標,考察糯米蛋白底物濃度、加酶量、pH、酶解溫度、酶解時間等因素對糯米糠抗氧化肽制備效果的影響,采用單因素實驗和正交實驗優化其制備工藝。結果表明,糯米糠抗氧化肽的最佳制備工藝條件為糯米蛋白底物濃度4%、[E]/[S]2%、pH7、酶解溫度40℃、酶解時間6h;在該條件下制備的糯米糠抗氧化肽對羥基自由基和超氧陰離子自由基的清除能力明顯優于米糠抗氧化肽,且存在一定的量效關系,提示糯米糠抗氧化肽可用作功能性食品或天然抗氧化劑被深入研究和開發利用。
[1]張強,周正義,王松華.從米糠中制備抗氧化肽的研究[J].食品工業科技,2007,28(7):145-147.
[2]姚惠源.高科技開發米糠資源的戰略意義[J].糧食與食品工業,2012,19(6):1-2.
[3]徐杰.貴州黑糯米的稻米表皮中有機成分的分離純化和結構鑒定[J].華南師范大學學報:自然科學版,1996(4):20-27.
[4]李宏睿,麥錦莘,徐明生,等.糯米酶解工藝以及抗氧化活性研究[J].食品研究與開發,2011,32(7):15-18.
[5]樊金娟,羅霞,董智.米糠抗氧化肽的提取和純化工藝研究[J].食品科技,2008,33(12):169-173.
[6]王若蘭,楊壯,周菲.中性酶從米糠中制取抗氧化性活性肽的研究[J].河南工業大學學報:自然科學版,2008,29(6):1-4.
[7]徐亞元,周裔彬,萬苗,等.脫脂米糠抗氧化肽的制備工藝研究[J].中國油脂,2014,39(2):28-32.
[8]張強,周正義,孫玉軍,等.米糠抗氧化肽的分離純化研究[J].安徽科技學院學報,2008,22(1):29-33.
[9]秦垂新,姚松君,唐青濤,等.抗氧化肽及其化學活性測定方法的研究概述[J].食品工業科技,2014,35(1):394-400.
Study on preparation technology and free radical scavenging capability of antioxidant peptide from glutinous rice bran
LI Li-hua1,YIN Zhong-yi2,ZHENG Xu-xu1,2,*
(1.Environmental and Biological Engineering Institute,Chongqing Technology and Business University,Chongqing 400067,China;2.Chongqing Key Lab of Catalysis&Functional Organic Molecules,Chongqing Technology and Business University,Chongqing 400067,China)
The optimum preparation process of antioxidant peptide from glutinous rice bran and its free radical scavenging capability were studied to exploit and utilize the resources of glutinous rice bran.Neutral protease was selected as hydrolytic enzyme,the single-factor experiment and the orthogonal tests were carried to optimize the preparation process of antioxidant peptide with reducing power of antioxidant peptide to an index. The results showed that the most optimum preparation condition of antioxidant peptides from glutinous rice bran protein with neutral protease were substance concentration 4%,[E]/[S]2%,pH 7,hydrolytic temperature 40℃ and time 6h.The scavenging activities to·OH and O2-·of antioxidant peptide from glutinous rice bran were stronger than which from rice bran,and their concentration and scavenging rate were definite dose-effect relationship,indicating the antioxidant peptide from glutinous rice bran could be used as functional food or natural antioxidants and be in-depth researched and developed and utilized.
glutinous rice bran;antioxidant peptide;enzymolysis;free radical scavenging capability
TS255.1
B
1002-0306(2015)04-0251-05
10.13386/j.issn1002-0306.2015.04.046
2014-06-19
李俐樺(1987-),女,碩士研究生,主要從事廢棄生物質資源化利用方面的研究。
鄭旭煦(1964-),女,博士,教授,主要從事生物資源與天然藥物方面的研究。
重慶市百名學術學科領軍人才培養計劃(渝教人[2011]60號)。

