Cu2O微納晶可控合成及其光催化性能研究*
——推薦一個綜合化學實驗
張萬群 楊凱萍 柯玉萍
(中國科學技術大學化學實驗教學中心 安徽合肥 230026)
Cu2O微納晶可控合成及其光催化性能研究*
——推薦一個綜合化學實驗
張萬群 楊凱萍 柯玉萍
(中國科學技術大學化學實驗教學中心 安徽合肥 230026)
介紹一個綜合化學實驗——Cu2O微納晶可控合成及其光催化性能研究。采用簡單配合物作為前驅(qū)物,在水熱條件下通過調(diào)節(jié)反應條件,合成多種形貌的Cu2O微納晶體,并對所得的不同產(chǎn)品結(jié)構(gòu)、形貌和光學性質(zhì)進行表征,對其光催化能力作對比性研究。
水熱法 Cu2O 綜合性實驗
實驗教學是本科教學的重要組成部分, 是培養(yǎng)學生實際工作能力和創(chuàng)新思維的重要手段,在本科教學中占有重要地位。然而,以往的化學實驗采用的是自成體系、相互脫節(jié)的模式,難以起到培養(yǎng)和提高學生分析、解決實際問題能力的作用。為了培養(yǎng)學生的創(chuàng)新能力,綜合性實驗作為實驗教學改革的一項新措施,已越來越受到各高校實驗教學工作者的重視[1-2]。
Cu2O是一種重要的P型半導體材料。Cu2O禁帶寬度僅為2.17eV,可被600nm波長的可見光激發(fā)。 1998年,Hara 發(fā)現(xiàn)在可見光下Cu2O能光催化分解水生成氫氣和氧氣[3],作為一種重要的可見光半導體催化劑,在降解有機污染物方面有很好的應用前景,因此備受國內(nèi)外科學工作者的關注,有望成為繼TiO2之后新一代可見光催化劑的研究熱點。筆者結(jié)合以往的科研工作,選用簡單的配合物為前驅(qū)物,采用簡易的合成路徑,通過調(diào)節(jié)反應條件,合成帶有多種形貌的功能性材料微納晶體,并對所得不同產(chǎn)品的結(jié)構(gòu)、形貌和性質(zhì)進行了表征,證實不同結(jié)構(gòu)形貌微晶會對性質(zhì)產(chǎn)生不同的影響[4-6]。在此科研成果基礎上,我們經(jīng)過反復篩選、實踐,將近年的科研成果“Cu2O微納晶體的可控合成及光催化性能研究”轉(zhuǎn)化為綜合化學實驗。該綜合性實驗的設計體現(xiàn)了材料研究“合成制備—分析表征—實際應用”的特點,不僅可以使學生掌握無機微納材料常見的合成方法和表征手段,還能通過該實驗學習光催化性能測試的技術,提高綜合運用材料化學基本原理和實驗技能解決實際問題的能力。
1 實驗目的
① 通過查閱文獻,了解Cu2O光催化的基本原理,研究熱點和現(xiàn)狀。
② 掌握結(jié)晶化學基本概念以及水熱法制備微納晶體的原理和方法。
③ 在特定的合成體系中,了解外界環(huán)境因素對晶體生長產(chǎn)生的影響。
④ 學習利用X射線粉末衍射儀、掃描電子顯微鏡、紫外-可見分光光度計對材料的表征,以及掌握對材料光催化性能進行評估的方法。
2 實驗原理
Cu2O是少數(shù)能被可見光激發(fā)的光催化材料,在太陽光照射下能有效降解廢水中的有機污染物。其光催化原理是當半導體材料Cu2O受波長小于或等于其禁帶激發(fā)波長的光照射時,半導體價帶上的電子被激發(fā)后躍遷至導帶形成電子空穴對,如果介質(zhì)中存在合適的俘獲劑或者表面缺陷,電子與空穴的復合受到抑制,就會在表面發(fā)生氧化還原反應。在水和空氣體系中,空穴與表面吸附的H2O和OH-反應形成具有強氧化性的表面羥基·OH。電子與表面吸附的分子氧發(fā)生作用生成超氧基,超氧基和電子與H2O反應得到H2O2和·OH。這些產(chǎn)物能氧化大部分有機染料,達到降解有機染料的目的[3,7]。
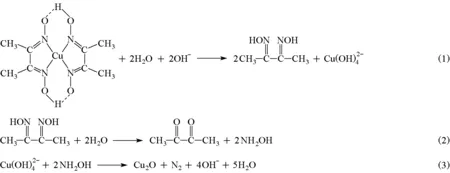
Cu2O微納晶的制備方法主要包括固相法、液相法和電化學沉積法等。水熱法是液相法中的一種重要制備方法。水熱法又稱熱液法。這種方法是在特制的密閉反應器(高壓釜)中,以水溶液作為反應介質(zhì),通過加熱,得到一個高溫、高壓的反應環(huán)境;水在反應體系中擔當溶劑、礦化劑和壓力的傳媒劑。在此環(huán)境中,絕大多數(shù)物質(zhì)能溶解于水,使反應在接近均相中進行,可加快反應的進度。通過水熱過程制備的微納材料通常具有物相均勻、純度高、尺寸及形狀可控等特點,從而成為微納材料制備的一種有效方法。一般來說,在水熱體系中,晶體生長分為兩個階段,開始的成核階段和隨后的晶體生長階段。在開始的成核階段,種子的結(jié)晶相內(nèi)在的對稱性和結(jié)構(gòu)決定了晶體固有的形貌;隨后的生長階段是一個動力學和熱力學控制的過程,在此過程中可以通過改變反應參數(shù)(如溫度、濃度、反應時間、環(huán)境相成分、雜質(zhì)和酸堿度等)得到更多復雜的形貌[8-9]。現(xiàn)在很多實驗證實了無機離子和有機添加劑可以調(diào)節(jié)晶體的形貌。這是因為晶體表面對離子具有選擇性吸附,而某些晶面的吸附會強于其他物質(zhì),即優(yōu)先吸附。在晶體生長過程中,添加特定離子或有機物會產(chǎn)生優(yōu)先吸附,優(yōu)先吸附晶面的表面能降低。由于低表面能的晶面生長速度慢,可顯露出來;而高表面能的晶面的生長速度快,會隨著晶體的進一步生長而消失,從而導致生成各種形貌[10-11]。本實驗體系是以丁二酮肟(dmg,dimethylglyoxime)與Cu2+形成Cu(Hdmg)2配合物作為前驅(qū)物,在水熱條件下通過改變反應溫度和NaOH濃度可控合成不同形貌的Cu2O微納晶,進而影響材料的光催化性能。

3 試劑和材料
氫氧化鈉(NaOH),丁二酮肟(C4H8N2O2),一水醋酸銅(Cu(Ac)2·H2O)和羅丹明B,所有試劑都是分析純級,購于上海國藥集團。試劑在使用前都未進一步純化。實驗中的反應容器為聚四氟乙烯襯里的不銹鋼釜,容積為80mL。
4 儀器設備
粉末X射線衍射儀(XRD),場發(fā)射掃描電子顯微鏡(SEM),紫外-可見分光光度計,電子天平,光催化裝置,比表面積及孔隙度分析儀。
5 實驗步驟
1) 在燒杯中,將0.5~2g氫氧化鈉加入55mL去離子水中,攪拌溶解,氫氧化鈉濃度為0.23~0.91mol/L;然后加入0.32g丁二酮肟,攪拌后溶解變成澄清溶液。
2) 在澄清溶液中加入0.28g Cu(Ac)2·H2O,溶液顏色變成黑棕色,劇烈攪拌4h,直至配合反應進行完全。
3) 將黑棕色懸濁液轉(zhuǎn)移到洗滌干凈的聚四氟乙烯內(nèi)襯的不銹鋼反應釜中。溫度由室溫上升到150~200℃,維持20h。冷卻后,紅棕色粉末被收集,再用蒸餾水和乙醇洗滌多次,在真空干燥箱里烘干。
4) 將干燥的產(chǎn)物進行X射線衍射、場發(fā)射掃描電子顯微鏡、紫外-可見分光光度計和比表面積及孔隙度分析儀表征。
5) 可見光催化反應在自制的間歇式反應裝置中進行。反應光源為500W鹵鎢燈, 使用一組濾光片, 以保證入射光為可見光(400nm<λ<800nm )。分別準確稱取0.04g不同形貌的Cu2O微晶光催化劑, 放入100mL光催化反應瓶中, 然后移取80mL 1×10-5mol/L的羅丹明B 水溶液加入到該光催化瓶中, 置于磁力攪拌器上,在暗處攪拌1h, 達到吸附平衡, 然后讓光垂直照射到溶液上。每隔30分鐘取少量溶液, 離心分離后, 取清液用紫外-可見分光光度計測定其吸收光譜, 掃描范圍400~700nm,在λmax=554nm測定羅丹明B 溶液的吸光度。以羅丹明B的吸光度為縱坐標,時間為橫坐標,繪制不同Cu2O微晶光催化降解羅丹明B的動力學曲線。
6 結(jié)果與討論
6.1 物相分析
圖1顯示了在此反應體系中含有不同濃度氫氧化鈉所制備樣品的粉末X射線衍射圖,所有樣品的衍射峰可以指標為立方相的Cu2O,晶胞參數(shù)分別為:a1=0.429nm,a2=0.428nm和a3=0.429nm,與標準卡片數(shù)據(jù)相符(JCPDS 05-0667,a=0.4269nm)。值得注意的是,圖1a所有衍射峰的強度和標準卡片值基本一致,但圖1b和圖1c(111)衍射峰要比標準卡片值強很多。這是由于樣品特有的形貌引起的擇優(yōu)取向。圖1a顯示衍射峰有寬化現(xiàn)象,用謝樂公式計算出(111)衍射峰所對應的晶粒尺寸為31.2nm。
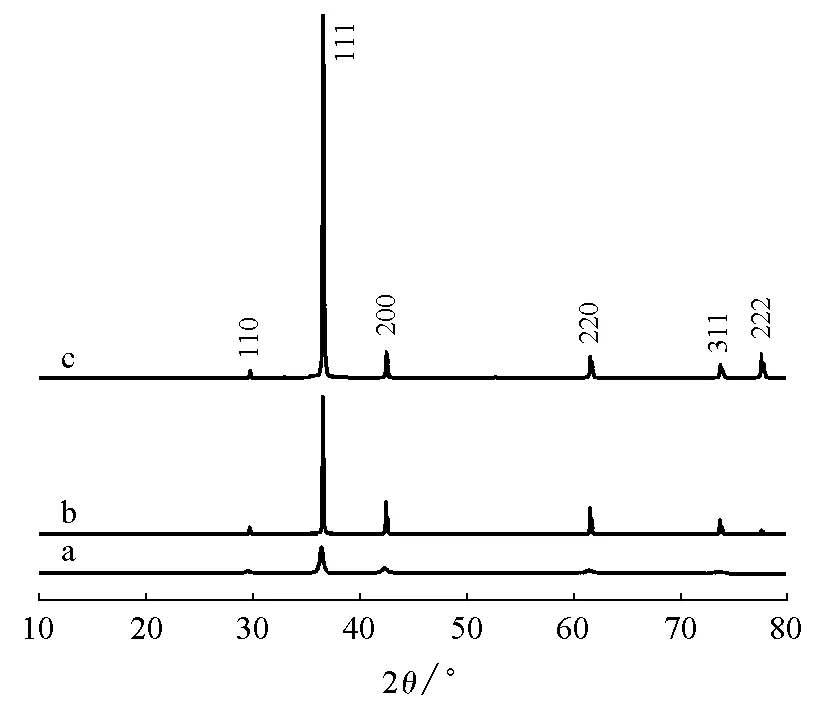
圖1 在不同氫氧化鈉濃度下所制備樣品的XRD (a) 0.23mol/L;(b) 0.45mol/L;(c) 0.91mol/L
6.2 形貌分析
當氫氧化鈉濃度為0.23mol/L時,圖2a顯示產(chǎn)物幾乎全由多孔空心Cu2O微球組成。多孔空心微球直徑約為5~9μm。通過高倍的SEM觀察發(fā)現(xiàn),許多孔分布在微球的表面(圖2b)。如果氫氧化鈉的濃度增加到0.45mol/L,所得到的產(chǎn)物是新穎的Cu2O帶孔的多面體籠狀結(jié)構(gòu)(圖2c和圖2d)。放大的場發(fā)射掃描電鏡照片表明這個多面體是由八面體切除頂角和棱所形成的多面體籠狀結(jié)構(gòu)。從一個不完整的Cu2O多面體籠狀結(jié)構(gòu)的場發(fā)射掃描電鏡照片中,可以清楚地看到Cu2O帶孔的多面體籠狀結(jié)構(gòu)是中空的。通過場發(fā)射掃描電鏡,從<100>、<111> 和 <110> 3個方向仔細直觀地觀察籠狀結(jié)構(gòu),就會發(fā)現(xiàn)此籠狀結(jié)構(gòu)是由8個中間帶孔的{111}面、6個{100}面和8個像柳葉狀的曲面組成的(圖3)。當氫氧化鈉濃度繼續(xù)增加到0.91mol/L,得到完美的由{111}面構(gòu)成的Cu2O八面體結(jié)構(gòu)(圖2e)。
反應溫度也對產(chǎn)物Cu2O形貌產(chǎn)生很大影響。圖4顯示當氫氧化鈉濃度為0.45mol/L,溫度提高到180℃和200℃時Cu2O微晶的形貌。在180℃時,獲得切除頂角和邊的八面體微晶。微晶軸長6~7μm,包含6個八邊形{100}面,8個切除頂角三角形{111}面和12個四邊形{110}面(圖4a)。隨著反應溫度提高到200℃時,長方形{110}面變得粗糙,寬度變大,{100}面變得更接近于圓形(圖4b)。

圖2 在不同氫氧化鈉濃度下所制備Cu2O的場發(fā)射掃描照片 (a),(b) 0.23mol/L;(c),(d) 0.45mol/L;(e) 0.91mol/L

圖3 分別從<100>,<111>和<110> 3個方向觀察Cu2O多面體籠狀結(jié)構(gòu)的場發(fā)射掃描電鏡照片

圖4 不同溫度下合成的Cu2O微晶場發(fā)射掃描電鏡照片 (a) 180℃;(b) 200℃
6.3 UV-Vis光譜分析
圖5顯示所得不同形貌Cu2O的紫外-可見吸收譜。通過吸收邊可以估算出半導體的帶隙。八面體,多面體籠和切除頂角和棱的八面體吸收峰的位置分別在576nm,541nm和558nm。用截線法求得它們的吸收邊約為652nm,645nm和646nm。計算得出帶隙分別為1.90eV,1.92eV和1.92eV。從紫外-可見吸收譜可看出所合成的樣品在可見光區(qū)有很強的吸收。

圖5 不同形貌Cu2O微納晶的紫外-可見吸收光譜 (a) 多面體籠;(b) 切除頂角和棱的八面體;(c) 八面體
6.4 產(chǎn)物的比表面積測定
為了準確測定Cu2O微晶的比表面,采用的測定方法是氮吸附靜態(tài)容量法(BET)。樣品測試前須在200℃條件下干燥10h,再在77k下進行氮氣等溫吸附-解吸分析。樣品的比表面積由相對壓力在0.05~0.2所取的8個數(shù)據(jù)點計算得出(相對壓力指的是吸附平衡時氮氣的壓力與吸附平衡溫度下氮氣的飽和蒸氣壓比)。八面體、多面體微籠和切除頂角和棱的多面體的比表面積分別為:0.25m2/g、1.71m2/g和0.41m2/g。
6.5 產(chǎn)物的光催化性能研究
為了檢驗結(jié)構(gòu)與功能的相關性,以3種具有代表性形貌的Cu2O微晶(八面體,多面體微籠和切除頂角和棱的多面體)作為平行比較的光催化劑。Cu2O微晶催化降解羅丹明B的實驗結(jié)果顯示:雖然由{111}面圍成的八面體Cu2O微晶的比表面積要比切除頂角和棱的多面體小,但卻具有更高的催化能力。對于這種現(xiàn)象,有報道認為Cu2O{111}面Cu原子的懸鍵比較多,在表面帶正電荷,這使它們與帶負電荷的染料分子有很強的相互作用,因此促進了Cu2O微晶的光降解效率;而其他晶面,如{100}面的外層原子為價鍵飽和的氧,顯電中性,因此與染料分子之間的相互作用弱,吸附能力差,催化活性就比較低[12-13]。多面體籠有最好的光催化能力,這可能得力于以下幾方面綜合因素的影響:比較大的比表面(1.71m2/g),表面擁有部分的{111}面以及空腔結(jié)構(gòu)。空腔結(jié)構(gòu)有利于光在空腔內(nèi)多次反射,增強光的利用率,也有利于提高光催化能力。
7 注意事項
(1) Cu(Ac)2·H2O和丁二酮肟的堿溶液混合后,要保持攪拌4小時以上,以使絡合反應進行完全。
(2) 反應釜內(nèi)的液體填充量不得超過四分之三。
(3) 在反應釜升溫之前,一定要擰緊;在反應結(jié)束之后,要等溫度降到室溫才能打開反應釜。
8 思考題
(1) 產(chǎn)物的形貌不同會對X射線衍射譜產(chǎn)生怎樣的影響?
(2) 為什么氫氧化鈉的濃度影響Cu2O微晶的形貌?
(3) Cu2O對有機染料催化降解的機理?
9 結(jié)束語
本實驗選用丁二酮肟銅為前驅(qū)物,在水熱條件下,通過調(diào)節(jié)反應條件,合成了多種形貌的Cu2O微納晶體;對所得不同產(chǎn)品的結(jié)構(gòu)、形貌和光學性質(zhì)進行了表征,對各種形貌Cu2O微晶光催化能力作對比性研究。本實驗來源于科研成果,是集制備、表征和性能為一體的綜合性較強的實驗,所用藥品便宜易得,實驗重復性好,實驗內(nèi)容新穎,能夠激發(fā)學生的科研興趣,對學生的知識學習以及能力與素質(zhì)的培養(yǎng)都有積極意義。
[1] 廖德仲,何節(jié)玉,毛立新,等.大學化學,2006,21(5):47
[2] 朱亞先,夏海平,袁右珠,等.大學化學,2010,25(5):17
[3] Hara M,Kondo T,Komoda M,etal.ChemCommun,1998(3):357
[4] Zhang W Q,Tang K B,Liu Y K,etal.Carbon,2007,45:1571
[5] Zhang W Q,Shi L,Tang K B,etal.EurJInorgChem,2010(7):1103
[6] Zhang W Q,Xu L Q,Tang K B,etal.EurJInorgChem,2005(4):653
[7] Schwitzgebel J,Ekerdt J G,Gerischer H,etal.JPhysChem,1995,99:5633
[8] Puntes V F,Zanchet D,Erdonmez C K,etal.JAmChemSoc,2002,124:12874
[9] Puntes V F,Krishnan K M,Alivisatos A.Science,2001,291:2115
[10] Murphy C J.Science,2002,298:2139
[11] Wang Z L.JPhysChemB,2000,104:1153
[12] Kuo C H,Huang M H.JPhysChemC,2008,112:18355
[13] Ho J Y,Huang M H.JPhysChemC,2009,113:14159
Controllable Synthesis of Cu2O Micro/Nano-crystallites and Their Photocatalytic Properties*
Zhang Wanqun Yang Kaiping Ke Yuping
(ChemistryExperimentTeachingCenter,UniversityofScienceandTechnologyofChina,Hefei230026,Anhui,China)
A facile hydrothermal method using simple complex as the precursor has been used for the controllable synthesis of Cu2O microcrystals in the comprehensive chemistry experiment. In this experimental class, reaction conditions are altered to prepare Cu2O microcrystals with various morphologies. The structure, morphology and optical properties of Cu2O microcrystals are characterized, and the photocatalytic properties are compared.
Hydrothermal method; Cu2O; Comprehensive experiment
O6-3;G64
國家自然科學基金資助項目(No.GG2060190106);中國科學技術大學校級教學研究項目(No.WW5160000102)

