原子的相對原子質量一定比其質量數數值小嗎
周國亮
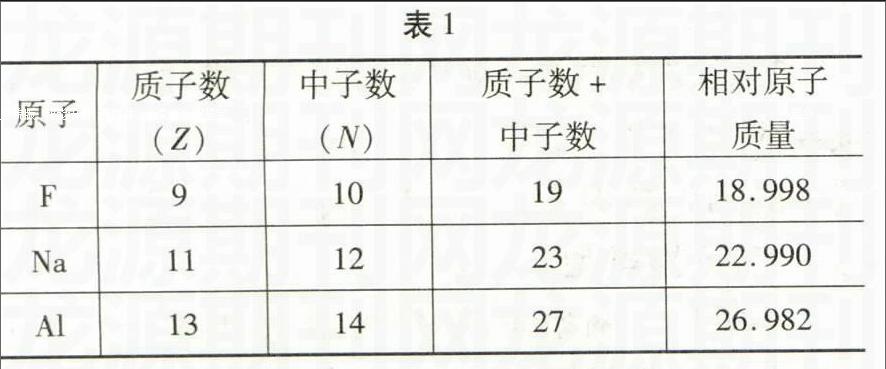
化學必修1(蘇教版)第31頁表1-8列舉了幾種原子的質子數、中子數和相對原子質量的關系見表1。從表1可以看出,幾種原子的相對原子質量都比其質量數(質子數+中子數)數值小。我們知道,原子是由原子核和核外電子構成,原子核又是由質子和中子構成的。如果按教材本頁表1-7提供的質子、中子相對質量1.007、1.008,忽略電子的質量(電子的相對質量為0.00055),氟原子的相對原子質量應約為9×1.007+10×1.008=19.143才對,這樣比較的話相對原子質量應該比質量數在數值大才合理,為什么其實際的相對原子質量比我們計算出來的相對原子質量和質量數數值要小呢?
其實,由于質子和中子結合成原子核時要放出巨大的能量,根據愛因斯坦質能方程E=mc2(E表示能量,m表示質量,c表示光速2.998×108m·s-1),物質的能量與它的質量呈正比,如果物質的能量增加了
ΔE,物質的質量也相應的增加Δm,反之亦然,即ΔE=Δmc2。由此可知,質子和中子若結合成原子核就有質量虧損。如1 mol D(氘)的質量比1 mol質子和1 mol中子的質量和小約0.004312 g,這一差值就是質量虧損。同樣的道理,原子核和電子結合成原子也有質量虧損。因此,一個原子核的質量不等于構成它的單個核子(質子、中子)質量的簡單加和,一個原子的質量也不等于構成它的質子、中子和電子質量的簡單加和,表1-8中列舉的幾種原子的數據就證明了這一點,而教材表1-7中的質子、中子的質量是指質子、中子的靜止質量。那是否所有原子的相對原子質量都比其質量數小呢?
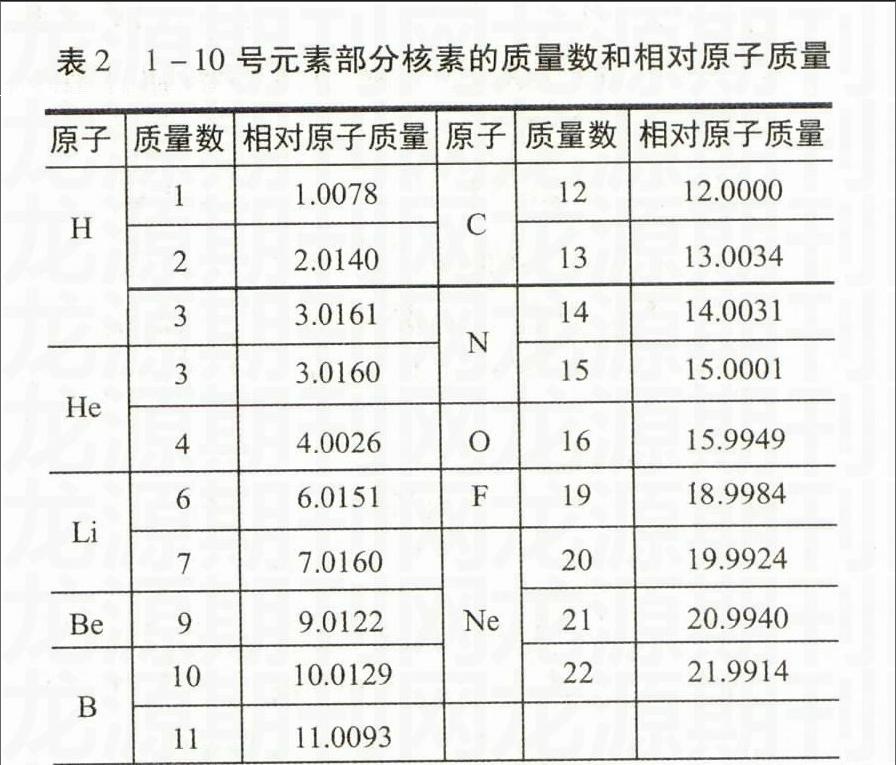
為此,筆者查閱了相關書籍,得到的相關數據見表2。
從表2可以看出,只有質子數大于8(包括8)的元素的同位素的相對原子質量才小于它的質量數,而質子數小于8的元素的同位素,其相對原子質量還是大于質量數。這是因為質子數小于8的元素核子數較少,聚變為核時“虧損”質量也較少;而質子數大于8的元素核子數較多,聚變為核時“虧損”質量也較多的緣故。
(收稿日期:2014-09-25)

