健康兒童腸道大腸埃希菌產ESBLs菌株耐藥性研究*
李金梅,李雨珊,劉 華,黃義山
(1.四川省南充市中心醫院檢驗科 637000;2.川北醫學院附屬醫院檢驗科,四川南充 637000)
?
·論 著·
健康兒童腸道大腸埃希菌產ESBLs菌株耐藥性研究*
李金梅1,李雨珊1,劉 華1,黃義山2△
(1.四川省南充市中心醫院檢驗科 637000;2.川北醫學院附屬醫院檢驗科,四川南充 637000)
目的 了解無氟喹諾酮類抗菌藥物用藥史的健康兒童腸道大腸埃希菌產超廣譜β-內酰胺酶(ESBLs)菌株的檢出率及對常用藥物的耐藥狀況,為臨床兒科大腸埃希菌產ESBLs菌株異位感染的經驗用藥提供依據。方法 從440例健康兒童大便中分離、鑒定大腸埃希菌,采用法國梅里埃VITEK-2 compact的AST-13全自動微生物鑒定藥敏檢測系統儀與K-B紙片擴散法進行藥敏試驗及ESBLs表型確認試驗。用WHONET5.3軟件分析藥敏試驗數據,采用SPSS19.0進行耐藥率數據分析。結果 440株大腸埃希菌產ESBLs率為47.3%,產酶株與非產酶株的耐藥率分別是:頭孢他啶80.8%、43.1%;頭孢噻肟80.8%、43.9%;頭孢曲松88.5%、51.7%;頭孢吡肟73.1%、34.5%;環丙沙星57.7%、39.7%;左氧氟沙星51.9%、37.9%;阿米卡星11.5%、3.4%。結論 南充地區部分無氟喹諾酮類抗菌藥物用藥史的健康兒童腸道內大腸埃希菌具有產ESBLs的較高概率,且對3、4代頭孢類、氟喹諾酮類、氨基糖苷類抗菌藥物具有不同程度的多重耐藥性。
大腸埃希菌; 健康兒童; 耐藥性; 產超廣譜β-內酰胺酶
大腸埃希菌是人體腸道菌群中的主要正常菌,同樣也是重要的條件致病菌。了解它們對當前常用抗菌藥物的耐藥狀況,對指導臨床兒科大腸埃希菌產超廣譜β-內酰胺酶(ESBLs)菌株異位感染的經驗用藥具有重要意義。有報道指出,部分感染患者大腸埃希菌產ESBLs菌株檢出率大于50%[1-2]。對于兒童,由于機體防御功能較成年人存在一定差異,感染率可能更高。而對于健康個體尤其是健康兒童(無氟喹諾酮類抗菌藥物用藥史)的腸道大腸埃希菌這部分的調查研究數據較少。因此,為了解南充地區健康兒童腸道大腸埃希菌產ESBLs的發生率及耐藥狀況,本文以10歲以下無氟喹諾酮類抗菌藥物用藥史的健康兒童作為研究對象,將他們大便中分離出的440株大腸埃希菌進行分析,現報道如下。
1 資料與方法
1.1 研究對象
1.1.1 選取南充地區5個縣市440例10歲以下無氟喹諾酮類抗菌藥物用藥史的健康兒童,其中男234例,女206例;年齡1~10歲,平均6歲。
1.1.2 菌株來源 (1)標本:外觀正常、成形的大便標本。(2)大腸埃希菌質控菌株(ATCC 25922):英國Oxoid公司。
1.2 菌株分離鑒定及藥敏試驗 按《全國臨床檢驗操作規程》(第3版)進行細菌分離、鑒定。采用VITEK-2 compact的AST-13全自動微生物鑒定藥敏檢測系統儀與K-B紙片擴散法進行藥敏試驗并進行ESBLs表型確認試驗。抗菌藥物藥敏紙片:頭孢他啶、頭孢噻肟、頭孢曲松、頭孢吡肟、環丙沙星、左氧氟沙星、阿米卡星,均購自英國Oxoid公司。用大腸埃希菌(ATCC 25922)做室內質量控制。
1.3 藥敏試驗結果及ESBLs確認判定標準 美國臨床和實驗室標準化協會(CLSI)2010年版。頭孢噻肟及頭孢噻肟/克拉維酸和頭孢他啶及頭孢他啶/克拉維酸,任一組抑菌環直徑大于或等于5 mm者,確認為產ESBLs菌株。
1.4 統計學處理 采用WHONET5.3軟件進行藥敏試驗數據分析,采用SPSS19.0進行耐藥率的數據分析。以P<0.05為差異有統計學意義。
2 結 果
2.1 大腸埃希菌ESBLs分離率 440株大腸埃希菌中,ESBLs確認試驗陽性208株,陽性率為47.3%。
2.2 440株大腸埃希菌對4種β-內酰胺類抗菌藥物藥敏試驗結果 見表1。440株大腸埃希菌對第3代頭孢類抗菌藥物耐藥率超過60.0%;產ESBLs株的耐藥率明顯高于不產酶株,差異有統計學意義(P<0.05)。產酶株不敏感率(耐藥率+中介率)>50.0%;其中頭孢曲松(92.3%)>頭孢他啶(82.7%)和頭孢噻肟(82.7%)>頭孢吡肟(75.0%)。

表1 4種頭孢類抗菌藥物耐藥性(%)
2.3 440株大腸埃希菌對氟喹諾酮類、氨基糖苷類抗菌藥物的藥敏試驗結果 見表2。440株大腸埃希菌對氟喹諾酮類耐藥率超過45.0%,對氨基糖苷類超過11.0%。
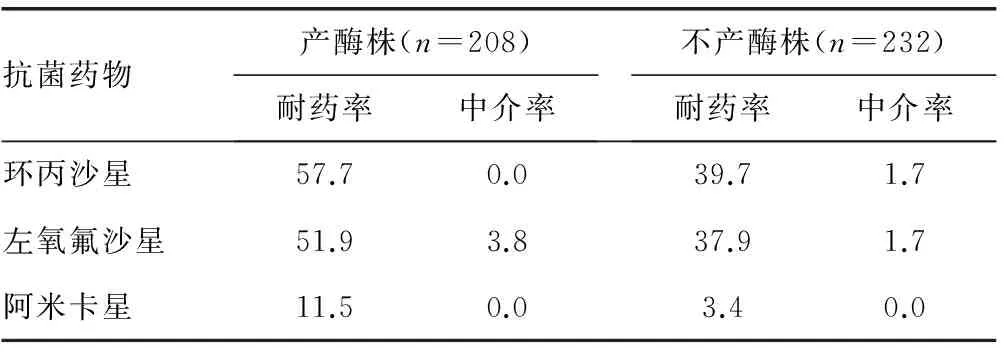
表2 3種氟喹諾酮類、氨基糖苷類抗菌藥物耐藥性(%)
3 討 論
大腸埃希菌是人體腸道的正常寄生菌,也是最常見的異位感染菌。部分兒童機體抵抗力較低,容易發生大腸埃希菌感染性疾病。本文調查了南充地區440例10歲以下無氟喹諾酮類抗菌藥物用藥史的健康兒童腸道大腸埃希菌產ESBLs的發生率及耐藥狀況,結果顯示,440株大腸埃希菌產ESBLs菌株檢出率為47.3%,與王麗和張永弘[3]報道相近;產酶株對第3代頭孢類抗菌藥物不敏感率超過了80.0%,第4代頭孢類抗菌藥物(頭孢吡肟)不敏感率達70.0%以上,同余珍珠和劉曉紅[4]的報道基本一致。造成如此高的耐藥率的可能原因為:(1)我國臨床抗菌藥物的應用存在嚴重不科學現象,從而導致醫院內或社區耐藥細菌傳播;(2)β-內酰胺類抗菌藥物,如頭孢2、3代是兒科常用藥物,有的醫療機構占臨床抗菌藥物用藥的前3位[5],曾經患過細菌性感染疾病的兒童體內正常菌群可能受這些藥物的壓力而出現耐藥株;(3)近年來兒童住院率增加、住院時間延長也增加了ESBLs菌株的感染機會[6]。
氟喹諾酮類藥物為腸桿菌科細菌尿路感染最常用且有效的藥物,但它可能影響骨骼發育而被兒童禁用。基于此,本文也探討了此類藥物在并無用藥史的兒童中的耐藥情況,結果顯示,440例健康兒童腸道大腸埃希菌對氟喹諾酮類藥物的耐藥率超過了45.0%。熊自忠等[7]報道成人產ESBLs大腸埃希菌對氟喹諾酮類藥物耐藥率在80.0%~90.0%。細菌質粒介導的氟喹諾酮基因與超廣譜酶基因可以隨細菌感染播散,成人體內的致病基因可播散至并無用藥誘導耐藥史的健康兒童,這可能是造成如此現象的原因之一[3]。
本文結果表明,就南充地區而言,隨著第3代頭孢類抗菌藥物的廣泛應用和濫用,大腸埃希菌作為人體腸道正常寄生菌,迫于生存壓力對以上常用抗菌藥物已產生多重耐藥的趨勢。產ESBLs菌株的概率較高,且在無氟喹諾酮類抗菌藥物用藥史的健康兒童中耐藥率也如此之高,這給兒童腸桿菌科細菌異位感染疾病的治療與感染控制帶來了極大的困難。
因此,在診治兒童細菌性感染疾病時,臨床醫生應充分考慮到南充所屬地區兒童腸道大腸埃希菌的耐藥趨勢,科學合理使用抗菌藥物。
[1]高偉,劉志敏.ICU內超廣譜β-內酰胺酶肺炎克雷伯菌和大腸埃希菌的檢測及耐藥性分析[J].中國綜合臨床,2011,27(6):572-574.
[2]黃斌,張盛斌.產超廣譜β-內酰胺酶革蘭陰性桿菌的檢測和耐藥性研究[J].中國基層醫藥,2011,18(12):1585-1586.
[3]王麗,楊永弘.兒科產超廣譜β-內酰胺酶大腸埃希菌耐藥的流行特征分析[J].中華醫學雜志,2008,88(20):1372-1375.
[4]余珍珠,劉曉紅.新生兒重癥監護病房細菌感染及耐藥性檢測[J].中國小兒急救醫學,2013,20(4):413-416.
[5]Tonkic M,Goic-Barisic I,Punda-Polic V.Prevalence and antimicrobial resisyance of extended-spectrum beta-lactamas Esproducing Escherichia coli and Klebasiella pneumoniae strai-Ns isolated in a university hospital in Split,Croatia[J].Int Microbiol,2005,8(2):119-124.
[6]蔡桂豐.十二歲以內患兒大腸埃希氏菌和肺炎克雷伯氏菌的耐藥性監測[J].實用醫學雜志,2005,21(7):747-748.
[7]熊自忠,李濤,李慧,等.產超廣譜β-內酰胺酶大腸埃希菌對喹諾酮類抗菌藥物的耐藥性檢測[J].中國微生態學雜志,2005,17(6):452-453.
Resistance research of E.coli producing ESBLs strains in the gut for healthy children*
LIJin-mei,LIYu-shan,LIUHua,HUANGYi-shan△
(1.DepartmentofClinicalLaboratory,NanchongCentralHospitalofSichuanProvince,Nanchong,Sichuan637000,China;2.DepartmentofClinicalLaboratory,theAffiliatedHospitalofNorthSichuanMedicalUniversity,Sichuan637000,China)
Objective To understand the fluorine free history of quinolones drugs in the intestines of healthy children E.coli to produce ultra broad spectrum beta lactamase (ESBLs)strains of detection rate and drug resistance to commonly used medicines,for clinical pediatric E.coli producing ESBLs strains of ectopic infection provides the basis for empirical use.Methods E.coli in the stool were separated and identificated from 440 healthy children,VITEK-2 compact AST-13 and K-B disc diffusion method were used for drug susceptibility and ESBLS phenotype confirmation test.WHONET5.3 software was used to analyze susceptibility data,and SPSS19.0 was used to analyze the percentages of data .Results The producing ESBLs rate was 47.3% for 440 strains of E.coli,The drug resistance rate of enzyme production strains and non-enzyme production strains respectively:Ceftazidime were 80.8%,43.1%;Cefotaxime were 80.8%,43.9%;Ceftriaxone were 88.5%,51.7%;Cefepime were 73.1%,34.5%;Ciprofloxacin were 57.7%,39.7%;Levofloxacin were 51.9%,37.9%;Aminoglycoside amikacin were 11.5%,3.4%.Conclusion The region part of fluorine-free quinolones drugs with a history of healthy children in the gut of E.coli has a higher probability of producing ESBLs,and for 3,4 generation cephalosporins,fluoroquinolone,aminoglycoside antibiotic drugs with different degree of multiple drug resistance.
E.coli; healthy children; drug resistance; ESBLs
四川省衛生廳科研項目(090146)。
李金梅,女,本科,初級檢驗技師,主要從事臨床微生物學研究。
△通訊作者,E-mail:13890731234@163.com。
10.3969/j.issn.1672-9455.2015.03.009
A
1672-9455(2015)03-0310-02
2014-08-26
2014-10-20)

