注射用頭孢呋辛鈉與氟康唑氯化鈉注射液配伍穩(wěn)定性考察
劉晶晶
(中國人民解放軍307醫(yī)院靜脈藥物配置中心二區(qū),北京 100071)
注射用頭孢呋辛鈉與氟康唑氯化鈉注射液配伍穩(wěn)定性考察
劉晶晶
(中國人民解放軍307醫(yī)院靜脈藥物配置中心二區(qū),北京 100071)
目的研究不同溫度、光照、放置時(shí)間下注射用頭孢呋辛鈉與氟康唑氯化鈉的配伍穩(wěn)定性。方法采用高效液相色譜(HPLC)法考察,模擬臨床用藥的實(shí)際情況,分析不同溫度、光照等變量因素對(duì)兩者配伍穩(wěn)定性的影響。溫度為4℃和25℃,光照強(qiáng)度為2 500 Lx和無光,觀察時(shí)間在配伍后的0,0.5,1,2,4,6,8 h。考察內(nèi)容包括外觀、不溶性微粒、pH和含量測(cè)定等。結(jié)果溫度、光照、時(shí)間等均會(huì)影響配伍液的穩(wěn)定性。光照對(duì)外觀、pH、不溶性微粒的影響不大;從外觀上看,25℃時(shí)藥物在4 h時(shí)便出現(xiàn)逐漸變黃的趨勢(shì),4℃則6 h出現(xiàn)變化;從pH上看,25℃時(shí)在6 h時(shí)變化較大,4℃時(shí)在觀察時(shí)間內(nèi)變化不大;從不溶性微粒上看,觀察時(shí)間內(nèi)均呈透明;從含量測(cè)定上看,隨著時(shí)間的推移,25℃、光照條件下的配伍液主藥含量較25℃、無光條件下配伍液主藥含量下降快;在同樣避光的條件下,4℃配伍液主藥含量隨時(shí)間變化較小。結(jié)論注射用頭孢呋辛鈉與氟康唑氯化鈉注射液配伍,可能會(huì)受到光照、溫度等影響,影響藥物的外觀、不溶性微粒、pH和主藥含量,故應(yīng)盡量保證在低溫、無光照的條件下保存。
頭孢呋辛鈉;氟康唑輸液;配伍穩(wěn)定性;高效液相色譜法
頭孢呋辛鈉為第2代頭孢菌素類抗生素,殺滅革蘭陽性菌的效果略差于第1代頭孢菌素類,但耐β-內(nèi)酰胺酶的效果則有一定優(yōu)勢(shì)[1]。雖具有溶解速度慢、穩(wěn)定性相對(duì)較差、有疼痛感等缺點(diǎn),但注射用頭孢呋辛鈉在臨床應(yīng)用廣、療效佳,在治療呼吸道、耳鼻喉、皮膚、產(chǎn)科等方面有顯著優(yōu)勢(shì),且外科多用其來預(yù)防外科手術(shù)感染[2]。氟康唑氯化鈉注射液是一種新型的抗真菌藥物,抗菌譜有很大擴(kuò)展,但當(dāng)嚴(yán)重疾病有變異菌出現(xiàn)的可能時(shí),多聯(lián)合應(yīng)用2種藥物,不僅可增強(qiáng)療效,可降低不良反應(yīng)的發(fā)生率,縮短用藥時(shí)間,促進(jìn)穩(wěn)定性[3]。筆者考察了注射用頭孢呋辛鈉與氟康唑氯化鈉注射液配伍的穩(wěn)定性,現(xiàn)報(bào)道如下。
1 儀器與試藥
Agilent 1100型 高效液相色譜儀(安捷倫科技有限公司);pHS-25型雷磁數(shù)顯pH計(jì)(上海精密科學(xué)儀器有限公司);光阻法粒子計(jì)數(shù)器(美國HIAC Royco8000A);Auto ScienceAP-01P型純凈水發(fā)生器(天津奧特賽恩斯儀器有限公司)。頭孢呋辛標(biāo)準(zhǔn)品(中國食品藥品檢定研究院,批號(hào)為 130493-201105,純度為92.1%);注射用頭孢呋辛鈉(蘇州中化藥品工業(yè)有限公司,批號(hào)為09512007,規(guī)格為每瓶0.75 g);氟康唑氧化鈉注射液(山東魯抗辰欣藥業(yè)有限公司,批號(hào)為1005215202,規(guī)格每100 mL含有氟康唑 0.2g和氯化鈉0.9g);乙腈為色譜純(Fisher Scientific公司),其他試劑為分析純。
2 方法與結(jié)果
2.1 含量測(cè)定
2.1.1 色譜條件
色譜柱:Diamonsil C18柱(250 mm×4.6 mm,5 μm);流動(dòng)相:甲醇(A)-0.2%甲酸水溶液(B),梯度洗脫,0~5 min時(shí)20% ~40%A,5~15 min時(shí)40% ~75%A,15~20 min時(shí)75% ~95%A,20~25 min時(shí)保持95%A不變;柱溫:25℃;體積流量:0.8 mL/min;檢測(cè)波長:270 nm;進(jìn)樣量:10 μL。
2.1.2 溶液制備[4]
精密稱取25 mg頭孢呋辛標(biāo)準(zhǔn)品,置25 mL容量瓶,放入由純凈水發(fā)生器產(chǎn)生的蒸餾水,作為標(biāo)準(zhǔn)溶液,配制質(zhì)量濃度為1.00 g/L,在4℃無光照條件下保存。根據(jù)臨床應(yīng)用頭孢呋辛鈉時(shí)的濃度配制,將0.75 g注射用頭孢呋辛鈉置250 mL容量瓶內(nèi),以氟康唑氧化鈉注射液作為溶劑配制配伍液。
2.1.3 方法學(xué)考察
線性關(guān)系考察:精確吸取頭孢呋辛鈉和氟康唑貯備液0.50,1.00,2.00,3.00,4.00,5.00 mL各置于6個(gè)10 mL容量瓶中,加對(duì)應(yīng)流動(dòng)相定容,混合均勻。分別進(jìn)樣20 μL,以峰面積(A)對(duì)質(zhì)量濃度(C)作回歸計(jì)算。得回歸方程,頭孢呋辛鈉 A=2.43× 104C+1.38×105(r=0.999 87,n=6),線性范圍為 55.40~561.80 μg/mL;氟康唑 A=7.05×105C+3.75×104(r=0.999 37,n=6),線性范圍為0.34~2.44 μg/mL。
精密度試驗(yàn):精確吸取頭孢呋辛鈉和氟康唑貯備液,反復(fù)6次進(jìn)樣并測(cè)定峰面積。結(jié)果頭孢呋辛鈉的 RSD為0.53%(n=6),氟康唑的 RSD為0.49%(n=6),表明該方法精密度良好。
重復(fù)性考察:取同一批樣品,依法制備配伍液并進(jìn)樣測(cè)定,結(jié)果頭孢呋辛鈉和氟康唑峰面積的 RSD分別為0.86%和0.75% (n=6),表明該方法重復(fù)性良好。
穩(wěn)定性試驗(yàn):取同一頭孢呋辛鈉和氟康唑氧化鈉注射液,加磷酸鹽緩沖液配置成質(zhì)量濃度分別為0.1 g/L和0.5 g/L溶液,于0,1,2,3,4 h時(shí)測(cè)定峰面積。結(jié)果頭孢呋辛鈉在4 h內(nèi)穩(wěn)定,氟康唑在3 h內(nèi)穩(wěn)定,RSD分別為0.87%(n=6)和0.73%(n=5)。
加樣回收試驗(yàn):取頭孢呋辛鈉配伍溶液1.0 mL,分成10份,分別加入已知含量的頭孢呋辛鈉標(biāo)準(zhǔn)溶液,搖勻進(jìn)樣,計(jì)算平均回收率為99.50%,RSD為0.65%(n=10)。另取氟康唑氧化鈉注射液1.0 mL,分成10份,分別加入已知含量的氟康唑氧化鈉注射液,搖勻進(jìn)樣,計(jì)算平均回收率為98.20%,RSD為0.49% (n=10)。
2.2 配伍穩(wěn)定性試驗(yàn)
設(shè)置的試驗(yàn)變量有溫度、光照,檢查包括4℃光照、4℃無光,25℃光照、25℃無光,光照強(qiáng)度為2 500 Lx。分別在 0,0.5,1.0,2.0,4.0,6.0,8.0 h時(shí)觀察配伍液外觀、不溶性微粒、pH和含量等。pH的檢查由pHS-25雷磁數(shù)顯pH計(jì)完成,含量由光阻法粒子計(jì)數(shù)器檢查所得,外觀、不溶性微粒由人眼觀察所得。結(jié)果見表 1及表2。可見,光照對(duì)外觀、pH、不溶性微粒的影響不大,不做對(duì)比;溫度對(duì)3者的影響主要體現(xiàn)在促進(jìn)作用,溫度越高則出現(xiàn)變化的時(shí)間越短,呈現(xiàn)出外觀發(fā)黃、有沉淀、pH升高。將溫度變量控制在25℃時(shí),觀察光照對(duì)含量的影響,無光條件下藥物含量變化明顯慢于有光照;觀察范圍內(nèi),無光時(shí)藥物含量仍在98.80%以上,而有光照時(shí)則下降到 97.30%左右。控制光照條件,溫度在4℃時(shí),藥物含量隨著時(shí)間的推移變化較小,含量僅下降至99.20%左右。經(jīng)測(cè)定,6 h時(shí)頭孢呋辛鈉和氟康唑的峰面積RSD分別為0.91%和0.89%,表明配伍液在6 h內(nèi)穩(wěn)定性良好。

表1 配伍液外觀、pH、不溶性微粒受溫度的影響比較
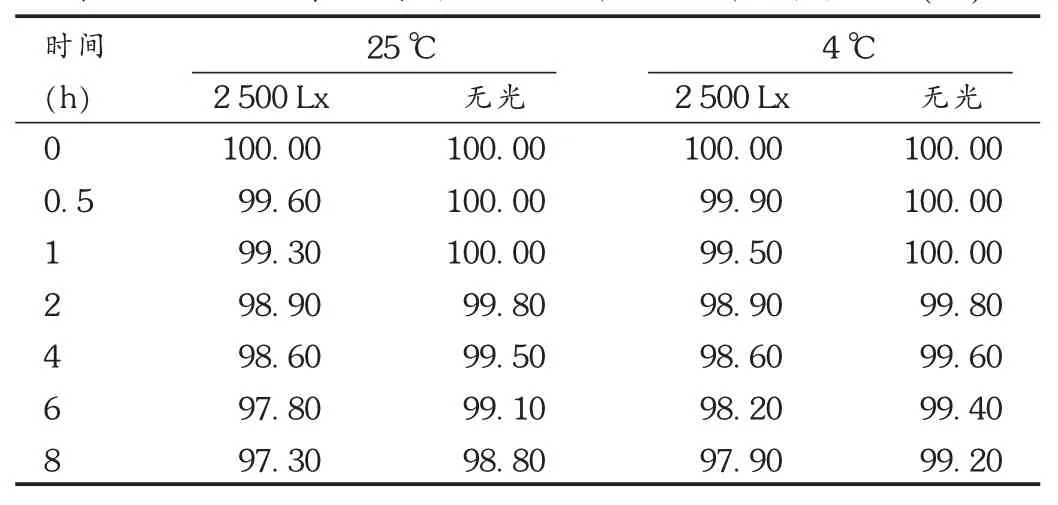
表2 不同溫度、光照條件下配伍液中頭孢呋辛鈉含量變化(%)
3 討論
外觀:是鑒別2種藥物配伍是否合適最直觀的方法,外觀雖然不能明確判定為 2種藥物不合適,但可鑒別 2者不合適[5-6]。當(dāng)配伍液在25℃時(shí),4 h時(shí)出現(xiàn)淡黃色改變,6 h便出現(xiàn)黃色,并有加重現(xiàn)象,在4℃時(shí)則6 h時(shí)出現(xiàn),且無加重情況。
pH:頭孢呋辛鈉在堿性液體中可出現(xiàn)沉淀,影響其藥物效果,降低療效、引起過敏等不良反應(yīng),當(dāng)配伍液中堿性越來越大時(shí)可作為配伍禁忌判斷依據(jù)。注射用頭孢呋辛鈉與氟康唑氯化鈉的配伍液25℃時(shí)在6 h堿性迅速增大,影響藥物效果,而4℃時(shí)在8 h內(nèi)未發(fā)生劇烈的液體pH改變。
不溶性微粒:在8 h的觀察范圍內(nèi)、溫度升高未引起配伍液明顯改變。
以上3個(gè)觀察指標(biāo)受光照影響較小。可見,兩者配伍液外觀受溫度影響,應(yīng)注意低溫保存,這對(duì)于保存配伍液的效果、減少不良反應(yīng)發(fā)生率具有顯著效果。
關(guān)于藥物含量,是注射用頭孢呋辛鈉與氟康唑氯化鈉的配伍穩(wěn)定性研究最重要的觀察指標(biāo)。控制不同變量,考察影響頭孢呋辛鈉含量的因素,溫度控制在25℃時(shí),8 h后在光照下的藥物含量快速下降了3%左右,而無光照時(shí)僅下降2%,當(dāng)溫度控制在4℃時(shí),無光照的時(shí)候藥物濃度幾乎沒有下降。表明為減少藥物含量下降、控制外觀、pH等,應(yīng)在低溫、無光下保存藥物,在注射時(shí)也應(yīng)盡量在6 h內(nèi)靜脈滴注結(jié)束。尤其在夏季時(shí),應(yīng)特別注意以上因素,才會(huì)在含量未下降時(shí)全部注入體內(nèi)并起效。
綜上所述,頭孢菌素類抗生素在臨床中應(yīng)用最廣,且多與其他藥物配伍使用,但配伍禁忌較多。氟康唑氯化鈉與注射用頭孢呋辛鈉的配伍穩(wěn)定性較好,但易受溫度、光照等影響,在使用過程中應(yīng)注意。
[1]汪笑秋.頭孢類抗菌藥物配伍穩(wěn)定性研究進(jìn)展[J].中國藥業(yè),2013, 22(9):124-126.
[2]唐 蕾,解 楚,趙龍山,等.頭孢呋辛鈉、頭孢呋辛賴氨酸與5種輸液的配伍穩(wěn)定性研究[J].中國抗生素雜志,2014,39(4):272-281.
[3]黃滔敏,馬 勤,陳念祖.頭孢呋辛鈉在果糖氯化鈉注射液中的配伍穩(wěn)定性考察[J].藥學(xué)服務(wù)與研究,2014,14(1):39-41.
[4]楊 靜,劉自玲,楊 建,等.注射用頭孢西丁鈉與鈉鉀鎂鈣葡萄糖注射液的配伍穩(wěn)定性考察[J].中國藥房,2014,25(34):3 217-3 218.
[5]張曉鈺,劉 冬,張 晉,等.注射用頭孢唑肟鈉與奧硝唑注射液的配伍穩(wěn)定性研究[J].中國醫(yī)院用藥評(píng)價(jià)與分析,2015,15(2):167-170.
[6]諶 勇.熱毒寧注射液與頭孢菌素類藥物配伍的穩(wěn)定性研究[J].深圳中西醫(yī)結(jié)合雜志,2014,24(3):67-68.
Stability Evaluation of the Compatibility of Cefuroxime Sodium with Fluconazole Sodium Chloride Injection
Liu Jingjing
(Center for Intravenous Medicine Pharmacy,PLA 307 Hospital,Beijing,China 100071)
Objective To investigate the stability of the compatibility of cefuroxime sodium with Fluconazole Sodium Chloride Injection.M ethods The stability of the compatibility of cefuroxime sodium and fluconazole and sodium chloride injection was analyzed by high performance liquid chromatography(HPLC)method,the main operation was to medicate and analyze simulation of the actual situation of clinical in different temperature,illumination and other factors in the impact of changes in the stability of the compatibility between the two drugs.The temperature was set at 4℃ and 25℃,and there were 2 cases of illumination:2 500 Lx and none.The observation time was after compatibility at 0,0.5,1,2,4,6,8 h.The contents of the observation time included appearance,insoluble particles,pH examination and content determination,etc.Results The results showed that temperature,light,and time would affect the stability of the compatibility of cefuroxime sodium and fluconazole and sodium chloride injection.The illumination had little effect on the appearance,pH and insoluble particles.Judging from the appearance,at 25℃,the drug gradually turned yellow at 4 h;and at 4℃ the change began at 6 h.Judging from pH,at 25℃ the drug had large changes at 6 h;at 4℃ there was little change over time.Judging from the insoluble particles,the drug showed transparent during the observation time.Judging from the content determination,the main drug content at 25 ℃ and in light conditions decreased faster than those at 25℃ and without light conditions;in the same lightless conditions,the main drug content changed little over time at 4℃.Conclusion The compatibility of cefuroxime sodium with Fluconazole Sodium Chloride Injection may be subjected to the influence of light,temperature and effects of the drug on the appearance,insoluble particles,pH and drug concentration.Therefore,we should try to ensure that stored at low temperature,illumination conditions,will ensure drug kept for a longer period of time.
cefuroxime sodium;fluconazole infusion;compatibility stability;HPLC
R969.2;R978.1+1;R978.5
A
1006-4931(2015)21-0052-03
劉晶晶(1979-),女,大學(xué)本科,護(hù)師,主要研究方向?yàn)樽o(hù)理和藥學(xué),(電子信箱)18613889051@163.com。
2015-05-07;
2015-06-04)

