高效液相色譜法測定糖維膠囊中鹽酸小檗堿含量
趙嚴麗,魏燕珍
(1.廣東省河源市食品藥品檢驗所,廣東 河源 517000; 2.廣東醫學院,廣東 東莞 523808)
高效液相色譜法測定糖維膠囊中鹽酸小檗堿含量
趙嚴麗1,魏燕珍2
(1.廣東省河源市食品藥品檢驗所,廣東 河源 517000; 2.廣東醫學院,廣東 東莞 523808)
目的 建立測定糖維膠囊中鹽酸小檗堿含量的高效液相色譜法。方法 色譜柱為Inertsil C18柱(250 mm×4.6 mm,5 m),流動相為0.05%磷酸二氫鉀溶液(每100 mL加十二烷基硫酸鈉0.4 g,以磷酸調節pH至4.0)-乙腈(52∶48),檢測波長為265 nm。結果 鹽酸小檗堿進樣量在0.069 73~0.129 5 g范圍內與峰面積線性關系良好(r=0.999 9),平均加樣回收率為101.14%,RSD=0.59%(n=6)。結論 該方法簡便、準確、專屬性強,可作為糖維膠囊控制原藥材和成品質量的方法。
糖維膠囊;高效液相色譜法;鹽酸小檗堿
糖維膠囊[1]由黃連、天花粉、黃精、黃芪、丹參、葛根、西洋參、格列本脲組方,具有益氣養陰、化瘀清熱的功效,用于氣陰兩虛夾瘀所致消渴。處方中黃連具有清熱燥濕、瀉火解毒作用,其有效成分為鹽酸小檗堿,對痢疾桿菌、大腸桿菌、肺炎雙球菌、金黃色葡萄球菌、鏈球菌、傷寒桿菌及阿米巴原蟲有抑制作用,臨床主要用于腸道感染及菌痢等的治療。本研究中建立了測定鹽酸小檗堿含量的高效液相色譜(HPLC)法,現報道如下。
1 儀器與試藥
LC-2010 A型高效液相色譜儀,UV-1601型紫外分光光度計(日本島津);Mettler AG-135型電子分析天平(準確度為0.01 mg);KQ250DA型超聲清洗器。鹽酸小檗堿對照品(中國食品藥品檢定研究院,批號為 110713-201212,供含量測定用,含量為86.7%);糖維膠囊(河北世濟唐威藥業有限公司,批號分別為C01118,C011256,C012112,規格為每粒 0.5 g);乙腈為色譜純,甲醇、磷酸均為分析純,水為超純水,十二烷基硫酸鈉(廣州化學試劑廠)為化學試劑。
2 方法與結果
2.1 色譜條件與系統適用性試驗
色譜柱:Inertsil C18柱(250 mm×4.6 mm,5 μm);流動相:0.05%磷酸二氫鉀溶液(每100 mL加十二烷基硫酸鈉0.4 g,再以磷酸調節pH至4.0)-乙腈(52∶48);測定波長:265 nm;柱溫:30℃;流速:1.0 mL/min;進樣量:10 μL。理論板數按鹽酸小檗堿峰計算應不低于4 000。在此條件下,色譜圖見圖1。
2.2 溶液制備
稱取鹽酸小檗堿對照品適量,精密稱定,加甲醇制成質量濃度為0.099 62 g/L的對照品貯備液;再精密量取對照品貯備液適量,加甲醇制成質量濃度為9.962 μg/mL的對照品溶液。取裝量差異項下的樣品內容物約0.5 g,精密稱定,置50 mL容量瓶中,加入鹽酸-甲醇(1∶100)適量,超聲處理(功率250 W,頻率40 kHz)30 min,放冷,再用鹽酸-甲醇(1∶100)加至刻度,搖勻,再用移液管精密移取3 mL,置100 mL容量瓶,用鹽酸 -甲醇(1∶100)加至刻度,即得供試品溶液。取處方中除黃連外的其余藥材,按處方量依法制成細粉,再按供試品溶液制備方法制成陰性對照品溶液。
2.3 方法學考察
專屬性試驗:分別精密吸取2.2項下3種溶液各10 μL,注入高效液相色譜儀,記錄色譜圖,見圖1。可見,供試品溶液色譜中,在與鹽酸小檗堿對照品溶液色譜相應位置上有相同保留時間的色譜峰,陰性對照品溶液無干擾。
線性關系考察:分別精密吸取質量濃度為9.962 μg/mL的對照品溶液7,8,9,10,11,12,13 μL,注入高效液相色譜儀,測量峰面積。以峰面積(Y)為縱坐標、質量濃度(X)為橫坐標進行線性回歸,得回歸方程 Y=4.9E+6 X+4 635.5,r=0.999 9(n=7)。結果表明,鹽酸小檗堿進樣量在0.069 73~0.129 5 μg范圍內與峰面積線性關系良好。
精密度試驗:精密吸取同一對照品溶液(9.962 μg/mL)10 μL,重復進樣6次。結果的 RSD為0.22%(n=6),表明儀器精密度良好。
穩定性試驗:取同一供試品溶液,室溫下放置,于0,4,8,12,18,24 h時分別進樣測定。結果的 RSD為0.39%(n=6),表明供試品溶液在24 h內穩定。
重復性試驗:取樣品(批號為C01118)6份,每份約0.5 g,依法制備供試品溶液并進樣測定。結果鹽酸小檗堿含量為26.15 mg/g,RSD為0.56%(n=6),表明方法重復性較好。
加樣回收試驗:精密稱取已知含量的樣品(批號為 C01118,鹽酸小檗堿含量為26.15 mg/g,平均粒重為每粒0.524 0 g)0.26 g,共6份,分別置50 mL容量瓶中,加入鹽酸-甲醇(1∶100)適量,超聲處理(功率250 W,頻率40 kHz)30 min,放冷,再用鹽酸-甲醇(1∶100)加至刻度,搖勻,再用移液管精密移取3 mL,置100 mL容量瓶,再另取對照品貯備液(0.099 62 g/L),精密量取4,5,6 mL各2份,分別加入上述100 mL樣品瓶中,用鹽酸-甲醇(1∶100)加至刻度,搖勻,即得供試品溶液,依法進樣測定,并計算回收率。結果見表1。
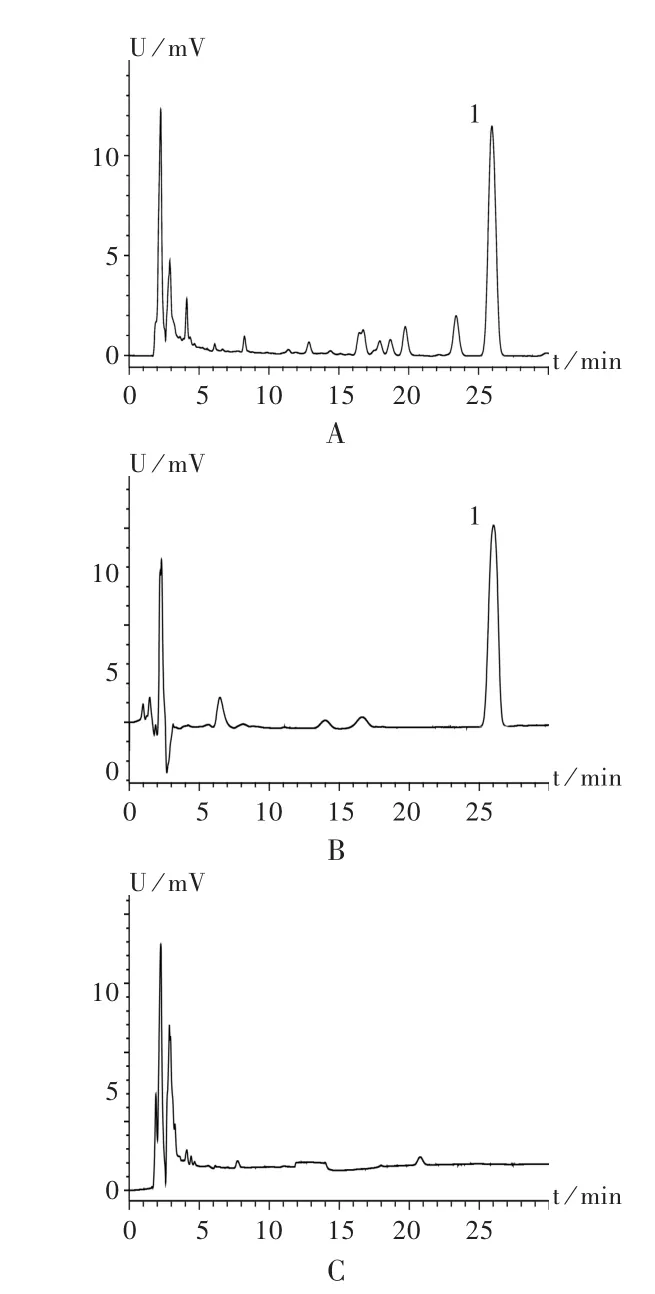
圖1 高效液相色譜圖
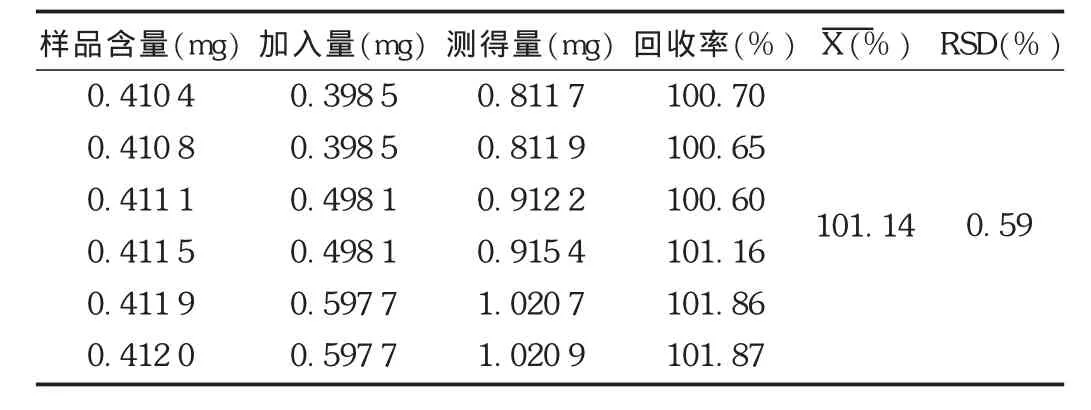
表1 鹽酸小檗堿加樣回收試驗結果(n=6)
2.4 樣品含量測定
分別精密吸取供試品溶液與對照品溶液各10 μL,注入高效液相色譜儀,測定3批樣品的鹽酸小檗堿峰面積,按外標法計算含量。結果批號為C01118,C011256,C012112的 3批樣品,平均粒重分別為 0.522 9,0.529 4,0.525 0 g,平均含量分別為每粒13.673 8,13.622 7,13.757 5 mg。
3 討論
制備供試品溶液時,曾選用超聲、振搖、水浴等方法[2-3],比較了水浴和超聲時間,結果以鹽酸-甲醇(1∶100)混合溶液超聲處理30 min的方法,提取完全,含量較穩定。用紫外分光光度計對對照品溶液在200~400 nm波長范圍進行掃描,結果在265 nm波長處具有最大吸收,故選擇265 nm作為測定波長。試驗中比較了2種不同比例的流動相[2-3],即乙腈 -0.2%磷酸溶液(30∶70)和乙腈-0.2%磷酸溶液(48∶52),結果用乙腈-0.2%磷酸溶液(48∶52)作為流動相時,色譜圖基線較穩,樣品中鹽酸小檗堿與其他雜質峰能夠完全分離,鹽酸小檗堿的理論板數大于4 000。因此,該方法準確、簡便,穩定性、重復性及回收率均較好,可作為該制劑的質量控制方法。
[1]WS-624(Z-107)-2005(Z)-2007,國家藥品標準[S].
[2]國家藥典委員會.中華人民共和國藥典[M].北京:中國醫藥科技出版社,2010:1 042.
[3]葉建晨.高效液相色譜法同時測定芩連膠囊中黃芩苷及鹽酸小檗堿的含量[J].中國藥業,2013,22(6):61-63.
Content Determination of Berberine Hydrochloride in Tangwei Capsules by HPLC
Zhao Yanli1,Wei Yanzhen2
(1.Heyuan Municipal Institute for Food and Drug Control,Heyuan,Guangdong,China 517000; 2.Guangdong Medical College,Donguan,Guangdong,China 523808)
Objective To establish a high performance liquid chromatography(HPLC)method for the content determination of berberine hydrochloride in Tangwei Capsules.M ethods The Inertsil C18column(250 mm×4.6 mm,5 μm)was used.The mobile phase was 0.05% potassium dihydrogen phosphate(adding sodium dodecyl sulfate 0.4 g per 100 mL and then adjusting pH to 4.0 by phosphoric acid)-acetonitrile(52∶48).The detection wavelength was 265 nm.Results Berberine hydrochloride showed good linearity within the range of 0.069 73-0.129 5 μg(r=0.999 9).The average recovery rate was 101.14%,RSD=0.59%(n=6).Conclusion The established method is simple and accurate with good specificity,which can be used as the quality control method of the raw materials and finished products of Tangwei Capsules.
Tangwei Capsules;HPLC;berberine hydrochloride
趙嚴麗(1978-),女,主管藥師,主要從事中藥分析檢驗工作,(電話)0762-3220319(電子信箱)zhao-yanli@163.com。
2014-06-24)
R284.1;R286.0
A
1006-4931(2015)04-0045-02

