乳腺浸潤性微乳頭狀癌臨床病理學觀察及免疫組化分析
趙偉志 葉曉霞
乳腺浸潤性微乳頭狀癌(IMPC)是一種具有特殊的病理形態學表現、高度的淋巴結轉移率和淋巴管侵襲性的罕見乳腺癌類型。在WHO 2003版及2012版乳腺腫瘤分類[1-2]中將其列為一種獨立的組織學類型。本研究回顧性分析2009年1月-2013年10月在本院行手術治療和會診的11例IMPC患者的臨床病理資料,并結合文獻對其臨床表現、病理形態特點、免疫表型、鑒別診斷進行探討,以加強對該罕見乳腺癌的認識,防止誤診誤治。
1 資料與方法
1.1 一般資料 收集本院2009年1月-2013年10月接受手術治療的213例乳腺浸潤癌患者,從中選取癌巢中伴有IMPC成分的6例患者,另收集本院病理科會診中確診IMPC的5例患者。其中IMPC成分在整個腫瘤中所占的比例>50%者2例,25%~49%者5例,<25%者4例。所有病例資料完整,10例行乳腺癌改良根治手術,1例行乳腺區段切除及腋下淋巴結清掃術,其中6例術中行腫塊快速冰凍切片和細胞印片檢查。
1.2 方法 6例于手術中取新鮮腫瘤組織行快速冰凍切片,同時于腫塊最大切面行印片細胞學檢查,HE染色,光鏡觀察。手術后標本經4%中性緩沖甲醛固定,梯度酒精脫水,二甲苯透明,石蠟包埋,常規切片,HE染色,采用光鏡觀察。選用ER、PR、Her-2、EMA、E-cadherin、CD31、p53、Ki-67抗體進行免疫組化染色,采用S-P法,DAB顯色,免疫組化步驟均按照S-P即用型試劑盒說明書進行操作,用已知陽性切片做陽性對照,用PBS緩沖液代替一抗做陰性對照。抗體及試劑盒均購自福建邁新生物技術有限公司。
1.3 免疫組化陽性結果判斷標準 以癌細胞出現棕褐色著色為陽性,其中ER、PR、p53、Ki-67陽性定位于細胞核;EMA、E-cadherin陽性定位于細胞膜;CD31陽性定位于細胞膜和/或胞質陽性。Her-2按照ASCO/CAP標準[3]進行評估,判定IHC3+的標準為>30%浸潤性癌細胞膜呈全周的強著色。
2 結果
2.1 臨床特征 11例IMPC患者均為女性,本院6例手術標本占同期乳腺癌的2.82%。年齡34~ 67歲,平均54.5歲。腫塊直徑1.3~4.5 cm,平均2.3 cm。左側6例,右側5例。其中7例可見血管淋巴管癌栓。發現發生腋下淋巴結轉移者7例(63.64%),多淋巴結(>3個)轉移者6例(54.55%)。
2.2 組織病理形態特征 IMCP在石蠟常規切片中大多數情況是與浸潤性導管癌混合存在,其IMCP成分具有獨特的病理形態學表現:腫瘤細胞呈微乳頭狀或小腺管狀排列,微乳頭簇中的細胞呈里面朝外(insideout)極性倒轉的排列方式,中央缺乏纖維血管軸心,其外緣毛糙呈鋸齒狀和或毛刺樣改變[4]。腫瘤細胞團周圍環繞間質空隙,類似于淋巴管侵犯,但腔隙內無內皮細胞被覆,腔隙之間有多少不等的纖維組織分隔[5],見圖1。IMCP癌細胞核常為低到中級別,常伴有導管原位癌成分(微乳頭型和篩狀亞型)。淋巴結內轉移灶形態與原發灶類似,見圖2。在快速冰凍切片中病理形態表現為浸潤性癌圖像,未見到IMPC的特征性形態學表現。2.3 細胞病理形態特征 IMPC印片細胞形態學常表現為細胞數量豐富,可見較多核大、核深染、核漿比增大的核異型癌細胞團,細胞質較少嗜中性,背景中可見較多的散在癌細胞,無雙極裸核細胞。在腫瘤成分中IMPC成分占多數的病例中可見其細胞團多明顯黏合成緊密的三維,桑葚體樣細胞團,細胞團無纖維血管軸心,其內細胞相互聚集,彼此相嵌,其表面細胞質呈鋸齒樣毛刺樣改變,見圖3。

圖1 HE切片圖

圖2 IMPC淋巴結內轉移圖

圖3 IMPC細胞印片圖
2.4 免疫組化 EMA與E-Cadherin 11例均陽性(100%),EMA表達于腫瘤微乳頭的邊緣和腺管樣結構的外側緣,瘤細胞胞質內不表達或呈微弱陽性表達,見圖4。E-Cadherin腫瘤細胞間連接面的細胞膜強表達,而微乳頭朝向間質面的細胞膜則表達減弱或消失[6],見圖5。CD31標記顯示腫瘤微乳頭中央缺乏血管軸心。ER陽性 9例(81.81%),見圖 6。PR陽性8例(72.73%)。Her-2陽性(+++)2例(18.18%)。Ki-67陽性表達定位于細胞核,標記指數為10%~70%,平均30.3%。p53陽性7例(63.64%)。
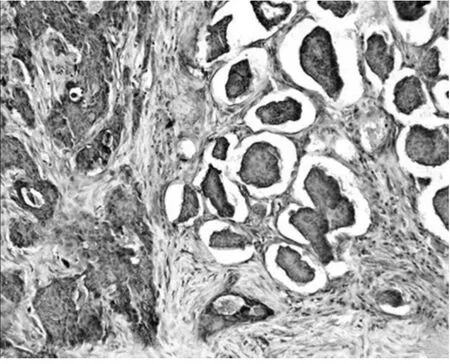
圖4 EMA免疫組化圖
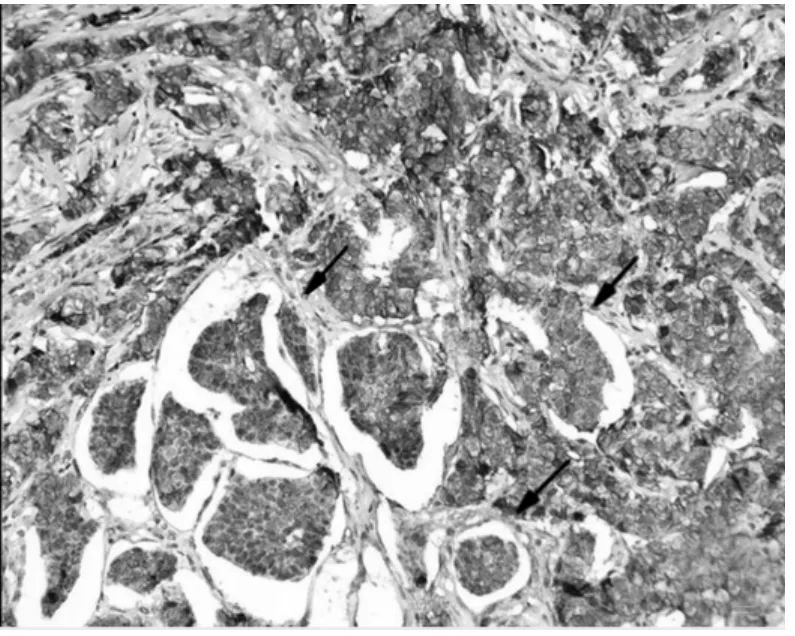
圖5 E-Cadherin免疫組化圖

圖6 ER免疫組化圖
3 討論
乳腺癌是現在女性最常見的癌癥,IMPC作為浸潤性乳腺癌中的一種獨立亞型,因其高度的淋巴管侵襲性和淋巴結轉移率近年來受到廣泛關注。1993年Siriaunkgul等[7]首次正式提出了IMPC的概念,并總結了其形態特征。IMPC在臨床表現、大體檢查、影像學檢查方面與普通型浸潤性導管癌無明顯不同,只是初診時發現腋窩淋巴結腫大的比例較高。IMPC診斷只有依靠病理醫師的鏡檢觀察。其獨特的病理形態學特點可總結為以下3點:(1)微(假)乳頭狀或小腺管狀排列的腫瘤細胞團,其中的細胞呈里面朝外(inside-out)極性倒轉的排列方式;(2)纖細的纖維組織分隔,分隔帶無內襯細胞;(3)腫瘤細胞團和分隔帶之間有明顯的腔隙形成主間質分離,付麗等[5]認為這種現象是兩者的結合弱點,組織在固定、脫水等制片過程中出現的人工假象,本組研究在快速冰凍切片中未見到IMPC的特征性主間質分離表現,支持此觀點。
IMPC顯微鏡下雖具有特征性的病理形態學表現,但由于單純性IMPC很少見,IMCP在大多數情況是與浸潤性導管癌混合存在,IMPC成分究竟占多大比例才診斷為IMPC一直存在爭議,最新版2012版WHO乳腺腫瘤分類[2]仍然沒有明確規定。Middleton等[8]認為IMPC成分應占75%以上才可診斷。Tsumagari等[9]報道,即使IMPC的成分不足腫瘤成分的10%,其淋巴結轉移率和淋巴管侵犯也都明顯高于不伴有IMPC成分的病例。國內付麗等[5]發現IMPC的成分即使小于25%或腫瘤直徑<2 cm,其淋巴管侵犯、淋巴結轉移率及轉移個數也明顯地高于對照組普通型浸潤性導管癌。本組研究中IMPC的成分<25%者4例,其淋巴管侵犯、淋巴結轉移率也較高,支持本觀點。因此筆者提倡只要腫瘤有IMPC的成分,就應在診斷中報告,同時注明IMPC所占比例,以引起臨床醫師的充分注意。IMPC的發生率報告不一,為2.0%~7.5%不等[1-2,5],這可能與診斷標準不統一與取材規范性不同有關系。付麗等[5]報告一組采用術前沒有活檢的全乳腺切片檢查的病例,IMPC發生率是6.2%,高于本組的2.82%,提示規范化的取材有助于發現IMPC成分。
IMPC的微陣列基因表達譜分析顯示這些腫瘤應歸入腺腔A型或B型,極少表達“基底樣”標記物[2]。以往文獻顯示ER、PR和Her-2陽性表達率不一,特別是Her-2,可能與陽性判斷標準、試劑差異和樣本數有關,本組研究呈現高ER表達,符合腺腔A型或B型的免疫組化表達。本組Ki-67陽性表達率平均30.3%,表明癌細胞具有較高的增殖指數,有較高生長能力,與以往研究相似。癌細胞p53陽性表達率高,提示它在IMPC的發生、發展過程中起重要作用。
IMPC與乳腺微乳頭狀導管原位癌、浸潤性乳頭狀癌、大汗腺癌、高分化管狀腺癌、黏液癌這些預后較好的乳腺癌鑒別意義非常重要。微乳頭狀導管原位癌的乳頭狀結構位于導管基底膜內。浸潤性乳頭狀癌為真性乳頭,乳頭中央可見纖維脈管軸心。大汗腺癌由胞漿豐富紅染的大汗腺樣細胞組成,可見頂漿分泌現象,表達GCDFP-15。高分化管狀腺癌的腺管為真性腺管,EMA表達于腺管內腔面。黏液癌表面雖也可見有微絨毛,但癌細胞與間質之間常可見有分泌的黏液,而IMPC的間質腔隙透明沒有黏液,黏液染色可助鑒別。最近有文獻[10]報道了具有微乳頭狀結構的乳腺黏液癌,目前對于該乳腺黏液癌亞型的研究有限、分類不明,可能是單純型黏液癌出現晚期復發和轉移的重要原因。此外,IMPC還需與其他類型的浸潤性癌由于固定不良造成的人工間隙和脈管內癌栓鑒別,其癌細胞異型性常比IMPC更加明顯,缺少外緣毛糙呈鋸齒狀和或毛刺樣改變的特點。總之,掌握好IMPC特征性病理形態特點結合EMA與E-Cadherin等標記物可以很好地與上述腫瘤鑒別。
總之,IMPC是一種具有特殊形態學表現的高增殖、高轉移潛能的罕見乳腺癌,在日常外檢中規范化的取材有助于發現浸潤性導管癌中的IMPC成分,對該病的準確的病理診斷對正確治療和提高預后具有非常重要的意義。
[1]Tavassoli F A,Devilee P.World Health Organization classification of tumors.Pathology and genetics of tumors of the breast and female genital organs[M].Lyon:LARC Press,2003:35-36.
[2]Lakhani S R,Ellis I O,Schnitt S J,et al.WHO classification of tumors of the breast.World health organization classification of tumors[M].4th ed.Lyon:IARC Press,2012:54-55.
[3]Wolff A C,Hammond M E,Schwartz J N,et al.American Society of Clinical Oncology/College of American pathologists guideline recommendations for human epidermal growth factor receptor 2 testing in breast cancer[J].J Clin Oncol,2007,25(18S):118-145.
[4]史尼特,科林斯.乳腺病理活檢解讀[M].北京:北京科學技術出版社,2010:263-265.
[5]付麗,付笑影,劉彤華.乳腺浸潤性微乳頭狀癌的形態改變與生物學行為的關系[J].中華病理學雜志,2004,33(1):21-25.
[6]范宇,郎榮剛,王穎,等.乳腺浸潤性微乳頭狀癌上皮性鈣黏附素的表達及意義[J].中華病理學雜志,2004,33(4):308-311.
[7]Siriaunkgul S,Tavassoli F A.Invasive micropapillary carcinoma of the breast[J].Modern Pathology,1993,6(6):660-662.
[8]Middleton L P,Tressera F,Sobel M E,et al.Infiltrating micropapillary carcinoma of the breast[J].Modern Pathology,1999,12(5):499-504.
[9]Tsumagari K,Sakamoto G,Akiyama F,et al.The pathological diagnosis and clinical significance of invasive micropapillary carcinoma of the breast[J].Jpn J Breast Cancer,2001,16(3):441-447.
[10]劉芳芳,付麗.具有微乳頭狀結構的乳腺黏液癌的臨床病理學特征及研究現狀[J].臨床與實驗病理學雜志,2013,29(8):896-898.

