復方鹽酸左氧氟沙星滴眼液的穩定性試驗研究
劉世萍,柳玉杰,郭美華,白建海,張新建,王琪(.哈爾濱醫科大學附屬第一醫院藥學部,哈爾濱5000;.哈爾濱市食品藥品監督管理局,哈爾濱 5008;.哈爾濱醫科大學附屬第一醫院眼科,哈爾濱5000)
穩定性試驗研究是評價藥品質量的主要內容之一,在藥品的研究、開發和注冊管理中占有重要地位。通過穩定性試驗,考察藥物在不同環境條件(如溫度、濕度、光線等)下藥品特性隨時間變化的規律,以認識和預測藥品的穩定趨勢,為藥品生產、包裝、貯存、運輸條件、有效期的確定提供科學依據[1]。復方鹽酸左氧氟沙星滴眼液系由鹽酸左氧氟沙星、地塞米松磷酸鈉、鹽酸萘甲唑啉3種成分以適當比例組方,并輔以氯化鈉及注射用水而制成的眼用制劑,可用于結膜炎、角膜炎、淚囊炎、白內障術后感染等外眼感染。筆者采用高效液相色譜(HPLC)法測定該制劑中的3種主藥含量,并對其在強光照射及高溫、加速等條件下的穩定性進行了研究,方法靈敏、準確、重復性好。
1 材料
1.1 儀器
Waters 600 HPLC系統,包括2996 PDA檢測器、717自動進樣器(美國Waters公司);SB3200型超聲波儀(上海必能信超聲有限公司);AE200型電子天平[梅特勒-托利多儀器(上海)限公司]。
1.2 藥品與試劑
鹽酸左氧氟沙星對照品(批號:130455-201005,純度:100%)、鹽酸萘甲唑啉對照品(批號:100111-201104,純度:99.2%)、地塞米松磷酸鈉對照品(批號:100016-201015,純度:100%)均來自中國食品藥品檢定研究院;鹽酸左氧氟沙星原料藥(江西大地制藥有限責任公司,批號:120716-2,純度:97.8%);鹽酸萘甲唑啉原料藥(天津天成制藥股份有限公司,批號:120308,純度:99.7%);地塞米松磷酸鈉原料藥(揚州制藥有限公司,批號:DL20120039,純度:99.2%);復方鹽酸左氧氟沙星滴眼液(哈爾濱醫科大學附屬第一醫院自制,批號:20120529、20120530、20120531,規格:5 ml/瓶);甲醇、乙腈為色譜純,其他試劑均為分析純,水為超純水。
2 方法與結果
2.1 處方
鹽酸左氧氟沙星原料藥3 g,地塞米松磷酸鈉原料藥1 g,鹽酸萘甲唑啉原料藥0.25 g,氯化鈉8.5 g,注射用水適量,制成1000 ml。
2.2 制備
稱取處方量鹽酸左氧氟沙星原料藥,加適量注射用水使其溶解,然后分別取處方量地塞米松磷酸鈉、鹽酸萘甲唑啉原料藥和氯化鈉,加適量注射用水使其溶解后加入到上述溶液中,再加注射用水至全量,用G3過濾器過濾,無菌條件下灌封,即可。
2.3 性狀
本品為淡黃色的澄明液體。
2.4 鑒別
在“2.6.1”項色譜條件下,供試品中3種主藥的保留時間與對照品溶液中3種對照品主峰的保留時間分別一致。
2.5 檢查
參照2010年版《中國藥典》(二部)附錄ⅠG眼用制劑[2]項下要求制訂本品的檢查項目,包括pH、滲透壓摩爾濃度、可見異物及無菌等項,均按相關步驟及原則執行。
2.6 含量測定
2.6.1 色譜條件。色譜柱:Kromasil 100-5 C18(250 mm×4.6 mm,5 μm);流動相:三乙胺溶液(取三乙胺7.5 ml,加水稀釋至14000 ml,用磷酸調節pH至3.5±0.05)-甲醇-乙腈(50∶45∶5,V/V/V),流速:1.0 ml/min;檢測波長:222 nm;柱溫:25 ℃;進樣量:10 μl。
2.6.2 溶液的配制。對照品溶液:取鹽酸左氧氟沙星、鹽酸萘甲唑啉及地塞米松磷酸鈉對照品適量,精密稱定,加流動相制成0.1243、0.0113、0.0405 mg/ml的混合對照品溶液,即得。供試品溶液:精密量取本品1 ml,置于25 ml量瓶中,用流動相稀釋至刻度,搖勻,即得。陰性供試品溶液:分別依次取處方量的除鹽酸左氧氟沙星、鹽酸萘甲唑啉、地塞米松磷酸鈉外的其他成分,按照供試品溶液的制備方法分別制成陰性供試品溶液Ⅰ、Ⅱ、Ⅲ。
2.6.3 方法專屬性。分別精密吸取對照品溶液、供試品溶液和陰性供試品溶液Ⅰ、Ⅱ、Ⅲ各10 μl,進樣。結果基線平穩,3種主藥及雜質峰之間分離度良好(分離度分別為4.0、7.2),各組分之間測定無干擾,柱效高(以鹽酸左氧氟沙星計理論板數為2500),峰形理想。
2.6.4 線性關系考察。取對照品溶液適量,過濾后進樣,分別以自動進樣器依次進樣1、2、4、8、16、20 μl,記錄峰面積。以峰面積響應值(y)為縱坐標、對照品進樣量(x,μg)為橫坐標,繪制標準曲線,得回歸方程:鹽酸左氧氟沙星y=5.27×106x-2.66×105(r=0.99998),線性范圍為0.1243~2.4860 μg;鹽酸萘甲唑啉y=2.47×107x-3.37×104(r=0.99996),線性范圍為0.0113~0.2260 μg;地塞米松磷酸鈉y=2.18×106x-2.52×104(r=0.99995),線性范圍為0.0113~0.2260 μg。
2.6.5 回收率試驗。分別精密量取陰性供試品溶液Ⅰ、Ⅱ、Ⅲ適量,分成3組,每組3份,每份1 ml,置于25 ml量瓶中,分別精密加入高、中、低3個水平量的鹽酸左氧氟沙星對照品(2.3908、2.9885、3.5862 mg)、鹽酸萘甲唑啉對照品(0.2048、0.2560、0.3072 mg)及地塞米松磷酸鈉對照品(0.8004、1.0005、1.2006 mg),按“2.6.2”項下方法制備供試品溶液,進樣分析,計算回收率。結果3種主藥平均回收率分別為99.22%(RSD=0.72%,n=9)、99.87%(RSD=0.86%,n=9)、100.02%(RSD=0.91%,n=9)。
2.6.6 精密度試驗。取同一份對照品溶液和同一份供試品溶液適量,分別在“2.6.1”項色譜條件下連續進樣6次,計算峰面積的RSD。結果3種主藥RSD分別為0.14%和0.32%、0.21%和0.48%、0.45%和0.64%(n=6),說明精密度良好。
2.6.7 穩定性試驗。取同一份供試品溶液適量,分別于0、1、2、4、6、8、10 h進樣測定,測定峰面積。結果RSD 分別為0.41%、0.52%和0.85%(n=7),可見溶液10 h內穩定性良好。
2.6.8 重復性試驗。取同一批樣品,共6份,在“2.6.1”項色譜條件下測定供試品溶液和對照品溶液的峰面積,計算含量。結果3種主藥的平均含量分別為:3.01 mg/ml(RSD=0.38%,n=6)、0.255 mg/ml(RSD=0.47%,n=6)和1.02 mg/ml(RSD=0.53%,n=6)。
2.7 穩定性試驗研究
2.7.1 影響因素試驗。(1)強光照射試驗:取樣品3批,置于密封潔凈容器中,于(4500±500)lx的光照箱內考察10 d,分別于第5天及第10天取樣,考察性狀、3種主藥含量等指標的變化,詳見表1(表中,*:表示淡黃色的澄明液體,**:表示黃色的澄明液體,+:表示符合規定,以下表格同)。
由表1可知,在此條件下樣品的性狀發生了變化,顏色有所加深,3種主藥的含量均呈下降趨勢,但仍在合格范圍內(應為標示量的90.0%~110.0%),有待進一步考察研究。同時提示,本品應選擇深色包材,以求遮光。
(2)高溫試驗:取樣品3批,置于密封潔凈容器中,置于恒溫培養箱中(40、60℃),考察10 d,分別于第5天及第10天取樣,考察性狀、3種主藥含量等指標的變化,詳見表2、表3。
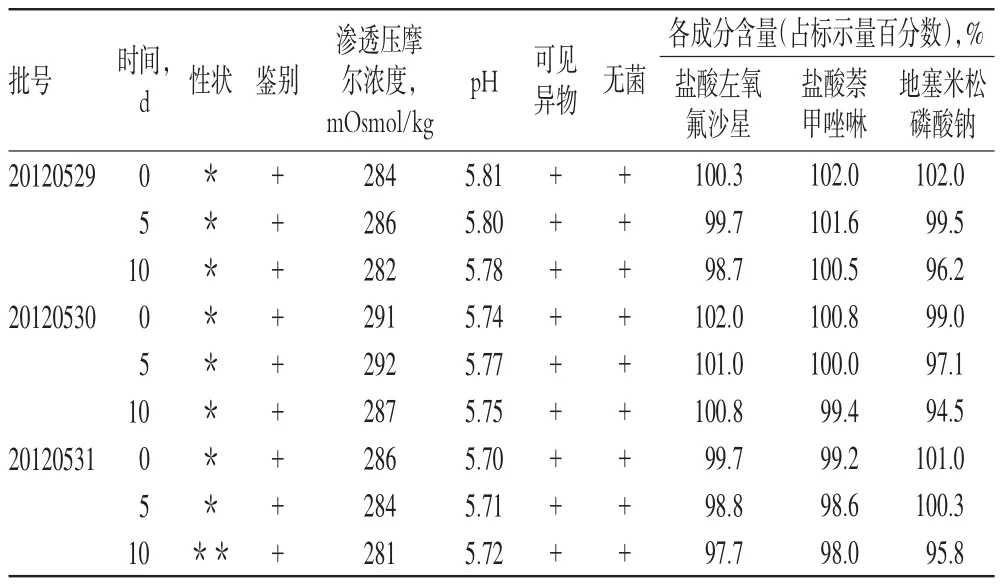
表1 強光照射試驗結果(n=3)Tab 1Results of highlight exposure test(n=3)
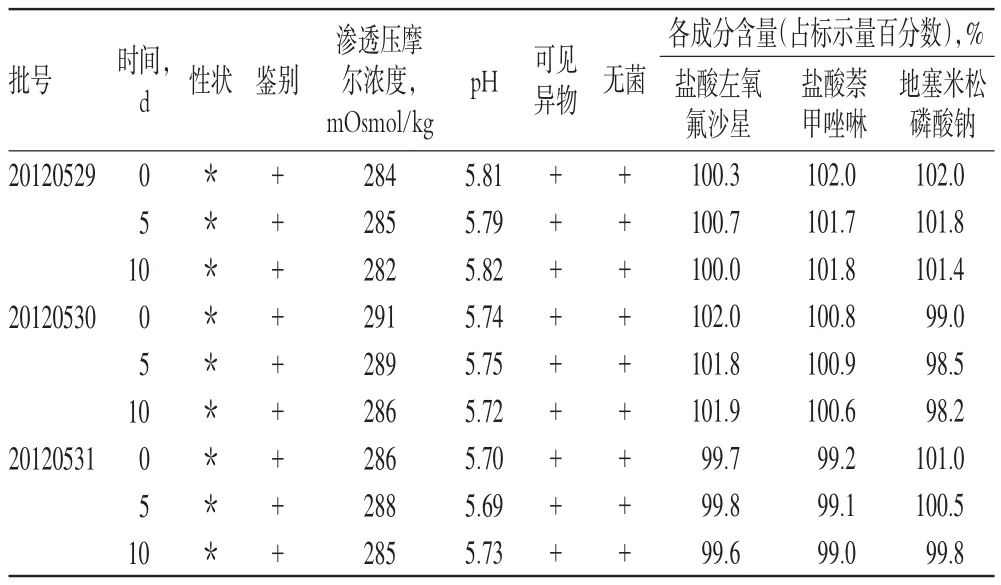
表2 高溫試驗結果(40℃,n=3)Tab 2Results of high temperature test(40℃,n=3)
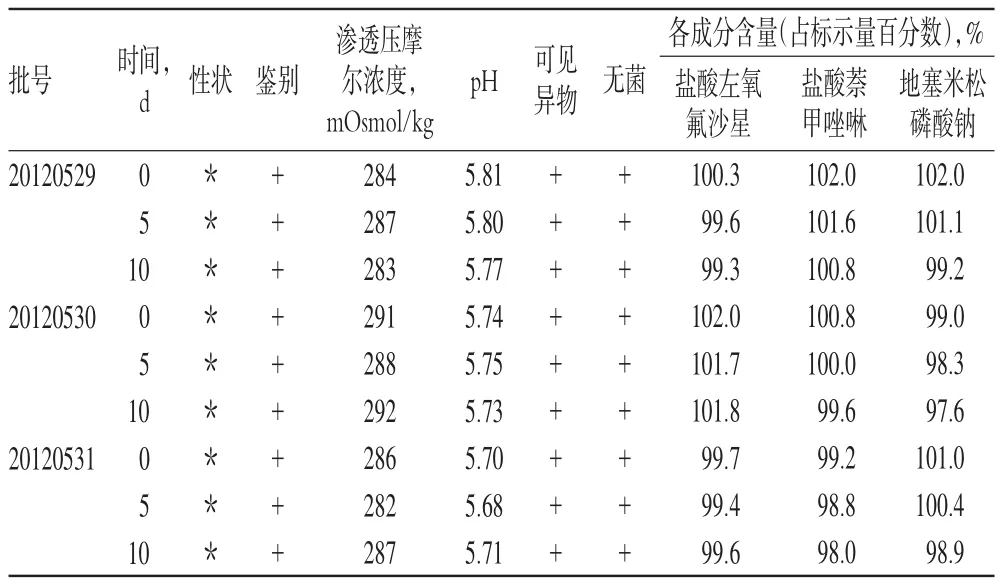
表3 高溫試驗結果(60℃,n=3)Tab 3Results of high temperature test(60℃,n=3)
由表2、表3可知,在40、60℃的條件下各項指標無明顯變化。
2.7.2 加速試驗。取樣品3批,不除去外包裝,保持內包裝的完整性及密封性,于溫度(40±2)℃、相對濕度(75±5)%的條件下分別放置1、2、3、6個月,按時取樣,考察性狀、3種主藥含量等指標的變化。結果各項指標基本穩定,詳見表4。
2.7.3 長期試驗。取樣品3批,不除去外包裝,保持內包裝的完整性及密封性,于溫度(25±2)℃、相對濕度(60±10)%的條件下放置12個月。分別于放置0、3、6、9、12個月時,按時取樣,考察性狀、3種主藥含量等指標的變化。結果各項指標未見明顯改變,詳見表5。
3 討論
根據研究目的和條件的不同,穩定性試驗研究內容可分為影響因素試驗、加速試驗和長期試驗等。影響因素試驗是在劇烈條件下探討藥物的穩定性、了解影響其穩定性的因素及所含成分的變化情況,其為制劑處方設計、工藝篩選、包裝材料和容器的選擇、貯存條件的確定、有關物質的控制提供依據[1],并為加速試驗和長期試驗應采用的溫度和濕度等條件提供參考。其中,高濕度試驗目的是考察供試品的吸濕潮解性能,以吸濕增重的百分比進行考察,因本品為液體制劑,所以未進行高濕度試驗。在強光照射試驗中,樣品的性狀發生了變化,顏色有所加深,3種主藥的含量均呈下降趨勢,但在合格范圍內,有待進一步考察研究提示本品應選擇深色包材,遮光保存。在高溫試驗中,40、60℃放置,本品各指標無明顯變化,提示本品應在低于40℃溫度下保存。
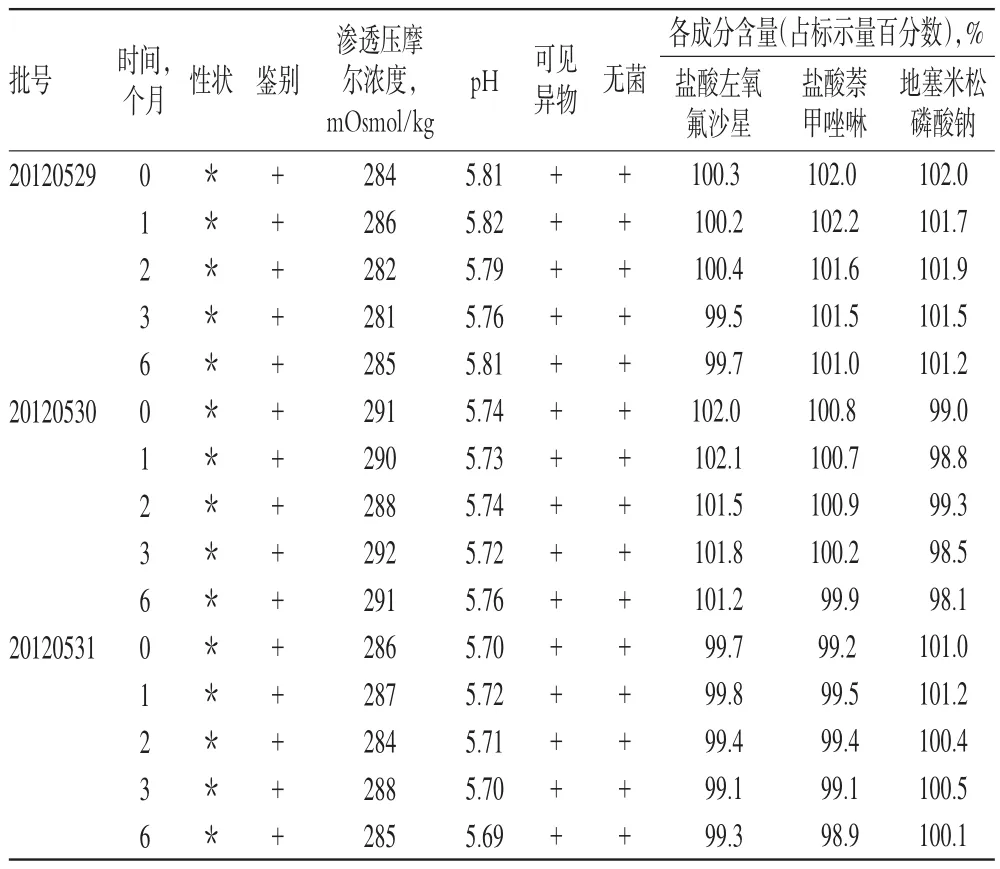
表4 加速試驗結果(40℃,n=3)Tab 4Results of accelerated test(40℃,n=3)

表5 長期試驗結果(n=3)Tab 5Results of long-term test(n=3)
加速試驗目的是在較短的時間內,了解制劑的化學、物理和生物學方面的變化。本品的各項考察指標均無明顯變化,說明本制劑的工藝及包裝等設計合理,符合制劑穩定性的要求。
長期試驗是在接近藥品的實際貯存條件下進行的穩定性試驗,為制訂藥物的有效期提供依據。在設計的包裝條件下室溫留樣12個月,結果顯示各項指標基本穩定,與加速試驗結果一致。所以本包裝能夠保證本產品質量,結合考察結果,可將本品有效期暫定為1年。
本試驗的標準曲線是用體積定量法(自動進樣器)進行繪制的。與傳統方法相比較,采用不同體積產生不同響應值的辦法獲得標準曲線,簡化步驟,方便快捷;其所獲得曲線的相關系數(r)更好,可達到0.9999以上,曲線標準差(s)更小,精密度更高,更準確。用新方法定量未知樣品時,采用體積進樣,可以根據需要靈活調整,不受限制。
綜上,筆者參照文獻[2-5]建立的主藥含量測定方法,簡便易行,方法靈敏、準確、重復性好。
[1]郭美華,張新建,馬妍妍,等.安神益心液的穩定性考察[J].中國藥師,2011,14(8):1149.
[2]國家藥典委員會.中華人民共和國藥典:二部[S].2010年版.北京:中國醫藥科技出版社,2010:附錄9、10、44、75、76、103.
[3]閆瑾,劉美欣,張蕊,等.復方鹽酸左氧氟沙星丁卡因滴眼液的制備及其質量控制[J].中國藥房,2012,23(29):2729.
[4]胡正波,李航.HPLC法測定鹽酸左氧氟沙星氯化鈉注射液的含量[J].中國藥師,2008,11(1):108.
[5]蔡佳玉,孫樹茂,孟永春,等.HPLC測定微球中鹽酸左氧氟沙星的含量[J].中國現代應用藥學,2012,29(5):437.

