轉(zhuǎn)錄因子IRF8抑制Th17細(xì)胞分化并減輕T細(xì)胞免疫介導(dǎo)的小鼠結(jié)腸炎*
李慶山, 杜慶華, 謝健晉, 鄧家德, 余碧珍, 江雪杰, 孟凡義△
炎癥性腸病(inflammatory bowel disease,IBD)包括克羅恩病(Crohn disease,CD)和潰瘍性結(jié)腸炎(ulcerative colitis,UC)是除了腸道惡性腫瘤以外比較嚴(yán)重的慢性腸道疾病,近年來的研究發(fā)現(xiàn)該疾病與腸道黏膜免疫反應(yīng)失衡有關(guān)。雖然目前該病的病因和發(fā)病機(jī)制尚不完全明確,但是許多研究認(rèn)為它是與Th1細(xì)胞有關(guān)的自身免疫性疾病。目前的研究表明,實(shí)驗(yàn)變態(tài)反應(yīng)性腦脊髓炎(experimental allergic encephalomyelitis,EAE)、膠原誘導(dǎo)的關(guān)節(jié)炎(collagen-induced arthritis,CIA)以及一些腸炎,是由白細(xì)胞介素23(interleukin 23,IL-23)依賴的Th17細(xì)胞或其它分泌IL-17的淋巴細(xì)胞引起的。新型的藥物ustekinumab可以通過阻斷IL-12和IL-23/Th17軸,從而減輕炎癥性腸病[1],提示Th17細(xì)胞及其相關(guān)細(xì)胞因子在炎癥性腸病的發(fā)病機(jī)制中起到至關(guān)重要的作用,因而中和IL-17A和IL-17F可以作為炎癥性腸病的靶向治療[2-3]。此外臨床常見的自身免疫性疾病特發(fā)性血小板減少性紫癜與大鼠的自身免疫性心肌炎的發(fā)病均與Th17細(xì)胞及其相關(guān)的細(xì)胞因子有關(guān)[4-5]。
干擾素調(diào)節(jié)因子(interferon regulatory factor,IRF)家族成員與Th17細(xì)胞發(fā)育密切相關(guān)。它存在于多種類型細(xì)胞中,被干擾素 γ(interferon γ,IFN-γ)所誘導(dǎo)。通常IRF8被樹突狀細(xì)胞和巨噬細(xì)胞中IFN-γ所誘導(dǎo),但其作為轉(zhuǎn)錄的激活或者抑制劑,依靠于IRF8異源二聚體DNA結(jié)合點(diǎn)與其它上皮細(xì)胞特異性轉(zhuǎn)錄(epithelium-specific transcription,EST)因子家族和IRF家族轉(zhuǎn)錄因子結(jié)合形成不同的復(fù)合物有關(guān)[6]。IRF家族重要成員之一的IRF4不僅對(duì)Th2的發(fā)育至關(guān)重要,而且在小鼠EAE模型中,不能發(fā)生EAE與來源于IRF4基因敲除小鼠的Th細(xì)胞不能向Th17分化有關(guān),提示有利于向調(diào)節(jié)性T細(xì)胞分化[7]。已經(jīng)有研究明確IRF8在髓系細(xì)胞分化、促進(jìn)單核細(xì)胞向粒細(xì)胞分化中起到關(guān)鍵性的作用[8],在DC細(xì)胞發(fā)育、分化和功能各個(gè)方面也是至關(guān)重要的調(diào)節(jié)因子[9],因此對(duì)先天性免疫反應(yīng)的建立是必不可少的。盡管IRF8對(duì)免疫細(xì)胞的生長、分化和生存的調(diào)節(jié)至關(guān)重要[10],但是IRF8對(duì)T細(xì)胞激活、分化的直接效應(yīng)仍未被完全揭示。重組激活基因(recombination activating gene,RAG)編碼 Ig分子和 TCR基因重排的重組酶,小鼠RAG1或者RAG2基因被敲除后,Ig和TCR既不能重排也不能表達(dá),表現(xiàn)為T、B淋巴細(xì)胞重癥聯(lián)合缺陷。本研究通過轉(zhuǎn)染IRF8全基因敲除和野生型小鼠初始T細(xì)胞(CD4+CD45RBhiT細(xì)胞)給RAG1-/-小鼠的實(shí)驗(yàn)性腸炎模型研究,探討轉(zhuǎn)錄因子IRF8是否通過對(duì)Th17細(xì)胞分化的影響而調(diào)控小鼠結(jié)腸炎的發(fā)生、發(fā)展。
材料和方法
1 動(dòng)物
野生型(WT)C57BL/6(B6)小鼠和IRF8全基因敲除(IRF8-/-)C57BL/6(B6)小鼠購自 Jackson′s Lab,均為雄性,均為 9~10周齡,在特殊無菌(specific pathogen free,SPF)級(jí)飼養(yǎng)籠飼養(yǎng),溫度18~22℃,濕度50% ~60%。動(dòng)物實(shí)驗(yàn)方案得到倫理委員會(huì)的同意。
2 脾臟和淋巴結(jié)淋巴細(xì)胞的分離、純化與處理
2.1 小鼠淋巴細(xì)胞的收集 頸椎脫臼法處死各組供體(WT或者IRF8-/-)小鼠,無菌取脾、淋巴結(jié),用200目篩網(wǎng)碾磨脾臟或者淋巴結(jié),過濾后收集細(xì)胞懸液,紅細(xì)胞裂解液裂解紅細(xì)胞,300×g離心5 min,并用PBS清洗3次,進(jìn)行細(xì)胞計(jì)數(shù)。
2.2 Naive CD4+T細(xì)胞的的分選 Naive CD4+T細(xì)胞(CD4+CD62L+CD44low)的分選采用熒光激活細(xì)胞流式細(xì)胞術(shù)分選,CD4+T細(xì)胞采用抗CD4磁珠(Miltenyi Biotec)和MACS分離柱進(jìn)行純化(純度可大于95%),為了獲得naive CD4+T細(xì)胞,上述獲得的單個(gè)細(xì)胞懸液加入抗 B220-PE、抗 CD8α-PE、抗CD11b-PE、抗 CD11c-PE和抗 CD49b-PE,所有的單抗均為1∶100稀釋,抗Ter119-PE采用1∶66稀釋,冰上放置20 min,然后與抗PE磁珠(1∶20稀釋)在冰上孵育 20 min,除去的部分加抗 CD4-PECy7、抗CD62L-FITC和抗CD44-APC,細(xì)胞分選在流式細(xì)胞儀(FACSVantage)上進(jìn)行,獲得的 CD4+CD62L+CD44lowT細(xì)胞,純度>99%。
2.3 磁珠法分選WT和IRF8-/-小鼠CD4+CD25+Treg細(xì)胞 免疫磁珠分選儀(autoMACS Pro Separator)購自Miltenyi Biotec;具體按CD4+CD25+Treg細(xì)胞的分選試劑盒說明書進(jìn)行操作。0.4%臺(tái)盼藍(lán)染色后檢測細(xì)胞活性,流式細(xì)胞術(shù)檢測細(xì)胞純度>99%。
2.4 Naive CD4+T細(xì)胞的體外分化 將上述獲得的naive CD4+T細(xì)胞進(jìn)行體外分化培養(yǎng),細(xì)胞加入96孔培養(yǎng)板中,加入抗CD3抗體(1 mg/L;BD Biosciences)和可溶性抗CD28(2 mg/L;BD Biosciences)激活48 h后,加入佛波酯(phorbol 12-myristate 13-acetate,PMA)和離子霉素重新刺激5 h,采用流式細(xì)胞術(shù)檢測細(xì)胞內(nèi)因子。細(xì)胞在中性條件(不加細(xì)胞因子刺激)下培養(yǎng)為Th0細(xì)胞;加入IL-12和抗IL-4(10 mg/L;BD Biosciences)向Th1極化;或者加入IL-4和抗 IFN-γ(10 mg/L;BD Biosciences)向 Th2極化;或者向Th17細(xì)胞極化:轉(zhuǎn)化生長因子β1(transforming growth factor β1,TGF-β1;5 μg/L)、IL-6(20 μg/L)、IL-23(10 μg/L)(均購自 R&D systems)、抗IL-4(10 mg/L)和抗 IFN-γ (10 mg/L)。
3 流式細(xì)胞術(shù)檢測
上述極化后的細(xì)胞,采用IC Fixation緩沖液(BD Biosciences)固定后,采用透膜緩沖液透膜,使用小鼠的抗體,PE-anti-IL-17、APC-anti-IL-4、APC-anti-IFN-γ和PE-Cy5.5-anti-CD4抗體進(jìn)行細(xì)胞內(nèi)染色,在FACSCalibur和 LSRFortessa(BD Biosciences)進(jìn)行流式細(xì)胞術(shù)檢測。
4 實(shí)驗(yàn)性腸炎模型的建立
按照文獻(xiàn)[11-12]的方法進(jìn)行T細(xì)胞轉(zhuǎn)染的結(jié)腸炎模型的建立,簡而言之,按照分選純化 WT和IRF8-/-小鼠的naive CD4+CD45RBhiT細(xì)胞和IRF8-/-CD4+CD25+Treg細(xì)胞,使用1×PBS 200 μL、經(jīng)過腹腔注射給RAG1-/-受體鼠(每組6只),注射的細(xì)胞數(shù)每只均為5×105。每周監(jiān)測受體鼠的體重及臨床表現(xiàn),第5周后處死受體鼠,結(jié)腸組織在10%的甲醛緩沖液中固定、石蠟包埋,切成5 μm后蘇木精伊紅(HE)染色,按照評(píng)分標(biāo)準(zhǔn)[11]進(jìn)行結(jié)腸病理評(píng)分,實(shí)驗(yàn)分組如下:(1)IRF8-/-對(duì)實(shí)驗(yàn)性腸炎的影響:根據(jù)供體鼠實(shí)驗(yàn)分為:WT組和IRF8-/-組;(2)IRF8-/-CD4+CD25+Treg細(xì)胞對(duì)實(shí)驗(yàn)性腸炎的抑制作用:按照注射細(xì)胞的來源分為WT-CD4+CD45RBhiT組;②WT-CD4+CD45RBhiT+WT Treg組;③WT-CD4+CD45RBhiT+IRF8-/-Treg組。
5 統(tǒng)計(jì)學(xué)處理
計(jì)量資料用均數(shù)±標(biāo)準(zhǔn)差(mean±SD),組間比較采用t檢驗(yàn)、Mann-Whitney U檢驗(yàn)或ANOVA。以P<0.05為差異有統(tǒng)計(jì)學(xué)意義。
結(jié) 果
1 IRF8對(duì)小鼠Th1、Th2和Th17分化的影響
小鼠naive CD4+T細(xì)胞在Th17極化條件下,IL-17+CD4+細(xì)胞比例在IRF8-/-小鼠顯著高于WT小鼠(P<0.01),而在Th1和Th2極化條件下,Th1和Th2細(xì)胞比例在IRF8-/-和WT小鼠中無顯著差異(P >0.05),見圖1。
2 CD4+CD45RBhiT細(xì)胞轉(zhuǎn)染實(shí)驗(yàn)性結(jié)腸炎模型
分別采用 WT或者 IRF8-/-小鼠的 CD4+CD45RBhiT細(xì)胞,經(jīng) RAG1-/-小鼠(n=6)腹腔注射,每周觀察小鼠體重的變化,結(jié)果顯示注射IRF8-/-小鼠CD4+CD45RBhiT細(xì)胞的RAG1-/-小鼠體重顯著低于注射WT小鼠CD4+CD45RBhiT細(xì)胞的RAG1-/-小鼠(P<0.05),見圖2;連續(xù)觀察5周后,處死小鼠,注射IRF8-/-小鼠CD4+CD45RBhiT細(xì)胞的小鼠結(jié)腸病理評(píng)分顯著高于WT組(P<0.05),見圖3;腸系膜淋巴結(jié)中,IL-17+CD4+T細(xì)胞比例IRF8-/-組顯著高于WT組(P<0.01),而Th1(IFN-γ+CD4+)和 Treg(Foxp3+CD4+)細(xì)胞比例無顯著差異(P>0.05),見圖4。
3 IRF8-/-CD4+CD25+Treg細(xì)胞對(duì)實(shí)驗(yàn)性腸炎的抑制作用
單獨(dú)注射WT小鼠CD4+CD45RBhiT細(xì)胞后,與注射Treg細(xì)胞2組比較,體重明顯下降(P<0.05),而無論同時(shí)注射IRF8-/-或者WT小鼠的Treg細(xì)胞,受體鼠體重均未明顯下降,且兩者之間無顯著差異(P >0.05),見圖5。
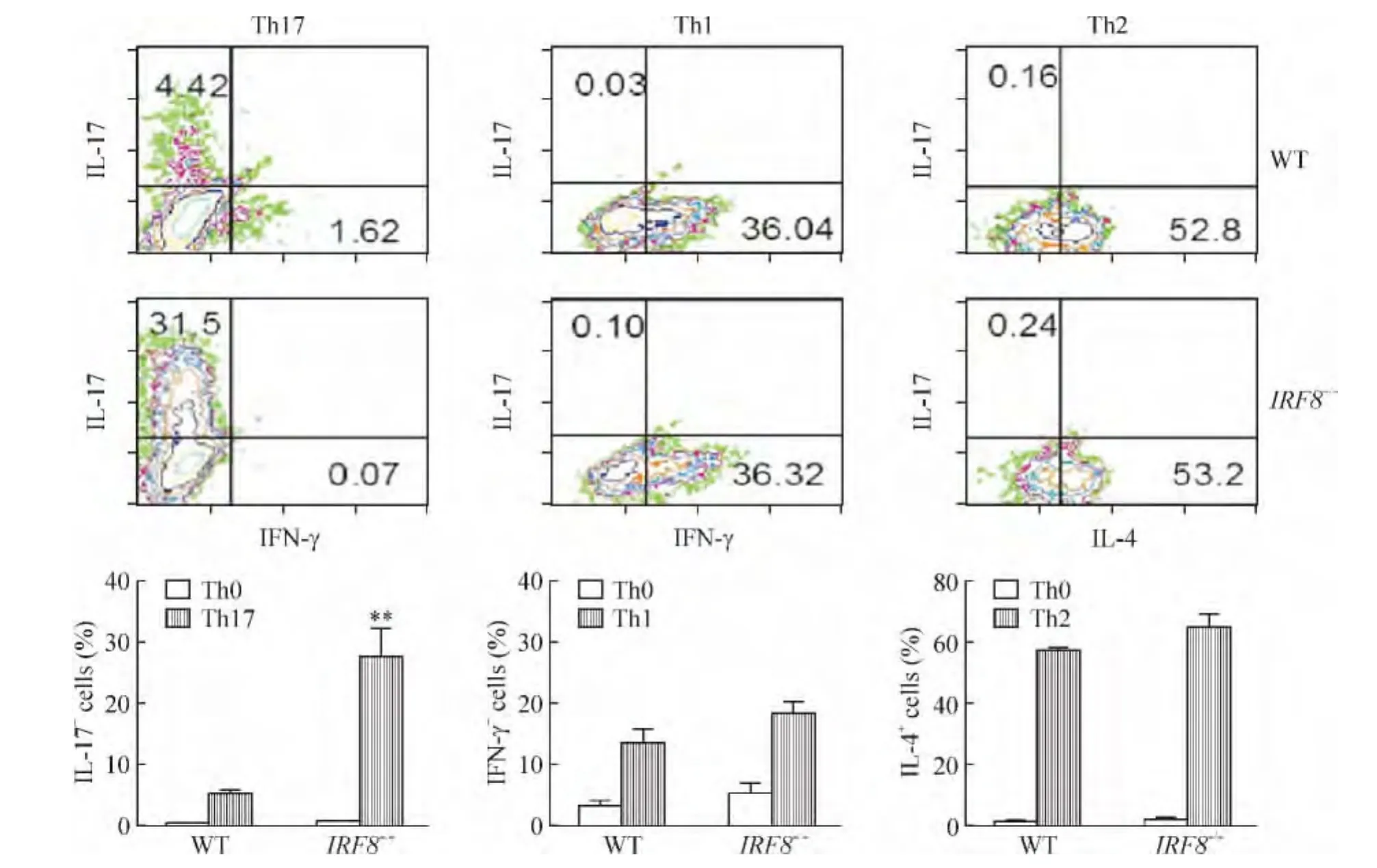
Figure 1.Naive CD4+T cells from IRF8-/-or WT mouse spleens were cultured under polarized conditions in vitro.Mean±SD.n=6.**P <0.01 vs WT.圖1 小鼠脾臟naive CD4+T細(xì)胞體外極化培養(yǎng)
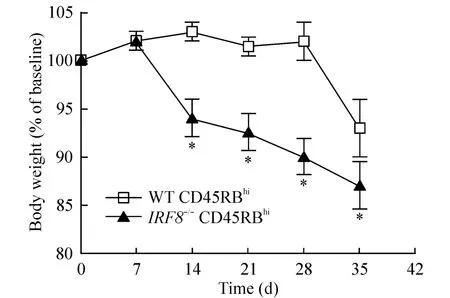
Figure 2.Changes of body weight of RAG1-/-mice after injected with WT or IRF8-/-CD4+CD45RBhiT cells.Mean±SD.n=6.*P<0.05 vs WT CD45RBhi.圖2 RAG1-/-小鼠注射CD4+CD45RBhiT細(xì)胞后體重的變化
討 論
近年來研究發(fā)現(xiàn)初始CD4+T細(xì)胞在不同細(xì)胞因子和轉(zhuǎn)錄因子的調(diào)控下,除分化出 Th1、Th2和Treg細(xì)胞之外,還分化出新型的輔助性T細(xì)胞,產(chǎn)生IL-17,即Th17細(xì)胞,其除在黏膜防護(hù)和病原菌清除中的作用外,在自身免疫性疾病中的作用也得到了較深入的認(rèn)識(shí)[10]。其中Th17及IL-17和炎癥性腸病[2-3]和異基因造血干細(xì)胞移植后并發(fā)的移植物抗宿主病[13-14]密切相關(guān)。RORγt是 Th17細(xì)胞分化的決定性轉(zhuǎn)錄因子,但是Th17細(xì)胞分化也受到一些正反饋和負(fù)反饋調(diào)節(jié),如最近報(bào)道的IL-21、IL-23R、IL-10和IL-27調(diào)節(jié)反饋圈的調(diào)節(jié)[15-18],提示可能存在固有的基因程序激發(fā)和沉默Th17細(xì)胞的發(fā)育,多種轉(zhuǎn)錄因子包括RORγt、RORα、STAT3和IRF4與Th17細(xì)胞的分化密切相關(guān)[10,15],但是沉默 Th17發(fā)育的機(jī)制目前仍然未完全闡明。
在本研究中,我們闡明了IRF8作為內(nèi)部沉默因子,阻止了初始CD4+T細(xì)胞向Th17細(xì)胞分化。我們采用了IRF8全基因敲除小鼠研究發(fā)現(xiàn),IRF8基因缺失促進(jìn)初始CD4+T細(xì)胞向Th17細(xì)胞分化,而對(duì)Th1和Th2細(xì)胞的分化無影響。我們進(jìn)一步通過免疫介導(dǎo)小鼠炎癥性腸病的模型研究IRF8對(duì)炎癥性腸病的影響,發(fā)現(xiàn)轉(zhuǎn)染IRF8-/-的 CD4+CD45RBhiT細(xì)胞給RAG1-/-小鼠較WT誘導(dǎo)出更為嚴(yán)重的結(jié)腸炎,在腸系膜淋巴結(jié)的T細(xì)胞重建中IRF8-/-的供體鼠較WT供體鼠顯示出更高的Th17細(xì)胞比例,表明IRF8抑制Th17的免疫反應(yīng)與減輕實(shí)驗(yàn)小鼠結(jié)腸炎的發(fā)生有關(guān)。
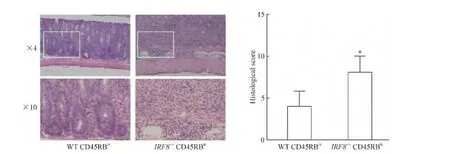
Figure 3.Colonic pathological changes in RAG1-/-mice after injected with WT or IRF8-/-CD4+CD45RBhiT cells.Mean±SD.n=6.*P<0.05 vs WT CD45RBhi.圖3 RAG1-/-小鼠注射CD4+CD45RBhiT細(xì)胞后結(jié)腸病理變化

Figure 4.Percentages of T cell subtypes in RAG1-/-mouse mesenteric lymph nodes after injected with WT or IRF8-/-CD4+CD45RBhiT cells.Mean±SD.n=6.**P <0.01 vs WT CD45RBhi.圖4 注射CD4+CD45RBhiT細(xì)胞后RAG1-/-小鼠腸系膜淋巴結(jié)中T細(xì)胞亞群比例
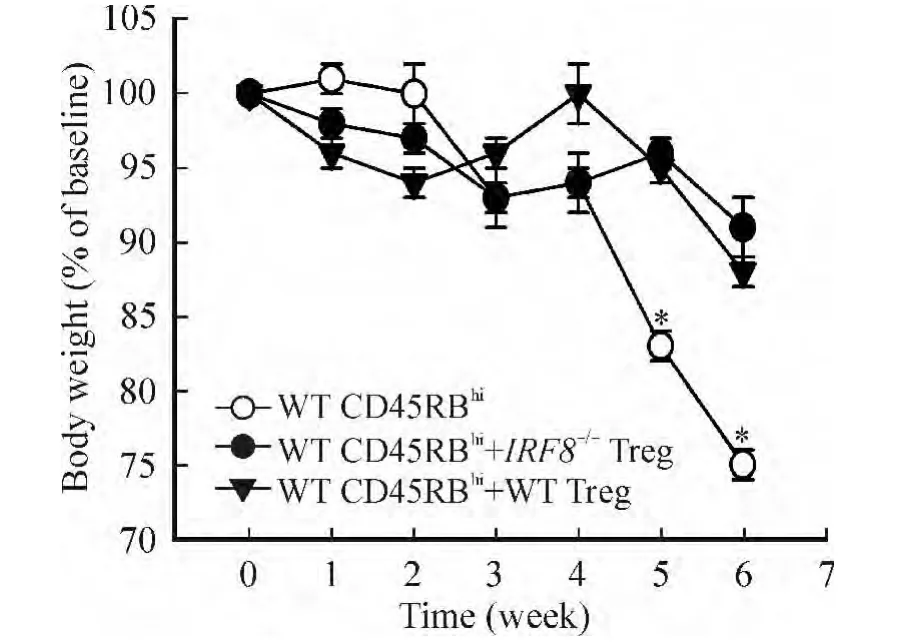
Figure 5.Immunosuppressive effect of IRF8-/-CD4+CD25+Treg cells on experimental colitis in mice.Mean±SD.n=6.*P<0.05 vs other groups.圖5 IRF8-/-CD4+CD25+Treg對(duì)小鼠實(shí)驗(yàn)性腸炎的免疫抑制作用
最近在人IBD結(jié)腸標(biāo)本的研究發(fā)現(xiàn),IRF家族中IRF1、IRF5和IRF8表達(dá)無顯著增加,而IRF4顯著增加;在鼠的動(dòng)物模型中,進(jìn)一步證實(shí)IRF4與IL-17啟動(dòng)子結(jié)合,誘導(dǎo)IL-17產(chǎn)生,IL-17誘導(dǎo)表達(dá)IL-17R的細(xì)胞產(chǎn)生IL-6,促進(jìn)T細(xì)胞RORγt表達(dá),從而誘導(dǎo)炎癥性腸病發(fā)生[19]。IRF8作為轉(zhuǎn)錄激活劑或者抑制劑依靠靶向DNA序列、并與PU.1或E47不同的伙伴蛋白以及IRF其它家族成員相互作用[6]。最近基因組掃描Meta分析顯示IRF8為多發(fā)性硬化患者的易感基因,更加證明了IRF8在免疫調(diào)控的炎癥性疾病中的作用[20]。
Tregs在維持機(jī)體免疫平衡中作用不可或缺,其不僅可避免IBD的發(fā)生,而且可以逆轉(zhuǎn)已發(fā)生的腸炎[21]。如果體內(nèi) Tregs與 Th17之間失平衡或者Tregs缺乏,抗原的免疫刺激可導(dǎo)致結(jié)腸黏膜的炎性反應(yīng)。動(dòng)物實(shí)驗(yàn)表明,給T細(xì)胞缺陷的小鼠注入不含有Tregs的幼稚T細(xì)胞,可誘發(fā)其對(duì)腸道共生菌群的高反應(yīng)性,導(dǎo)致嚴(yán)重的自身免疫性結(jié)腸炎;同時(shí)輸入Tregs則可抑制這類炎癥反應(yīng)[22]。另有研究表明,剔除小鼠的Treg細(xì)胞會(huì)使其 T細(xì)胞介導(dǎo)的炎癥性疾病(如腸炎)惡化[23]。本研究將WT小鼠CD4+CD45RBhiT細(xì)胞轉(zhuǎn)染給RAG1-/-小鼠時(shí)分別同時(shí)轉(zhuǎn)染W(wǎng)T或者IRF8-/-Treg,探討IRF8-/-Treg對(duì)炎癥性腸病的抑制作用,發(fā)現(xiàn)IRF8-/-Tregs發(fā)揮了正常的抑T細(xì)胞活性。
(致謝:本研究在美國紐約大學(xué)西奈山醫(yī)學(xué)院熊華保副教授悉心指導(dǎo)和大力支持下完成,深表感謝!)
[1] Rietdijk ST,D′Haens GR.Recent developments in the treatment of inflammatory bowel disease[J].J Dig Dis,2013,14(6):282-287.
[2] Wedebye Schmidt EG,Larsen HL,Kristensen NN,et al.TH17 cell induction and effects of IL-17A and IL-17F blockade in experimental colitis[J].Inflamm Bowel Dis,2013,18(8):1567-1576.
[3] Hundorfean G,Neurath MF,Mudter J.Functional relevance of T helper 17(Th17)cells and the IL-17 cytokine family in inflammatory bowel disease[J].Inflamm Bowel Dis,2012,18(1):180-186.
[4] 周宏斌,陳志華,李 雯.Th17細(xì)胞及白細(xì)胞介素17A在慢性氣道炎癥性疾病中的作用[J].中國病理生理雜志,2012,28(3):560-564.
[5] 韓麗娜,張亞晶,楊庭樹,等.自身免疫性心肌炎大鼠Th1、Th2、Th17亞群免疫反應(yīng)狀態(tài)[J].中國病理生理雜志,2010,26(10):2033.
[6] Tamura T,Yanai H,Savitsky D,et al.The IRF family of transcription factors in immunity and oncogenesis[J].Annu Rev Immunol,2008,26:535-584.
[7] Brüstle A,Heink S,Huber M,et al.The development of inflammatory TH-17 cells requires interferon-regulatory factor 4[J].Nat Immunol,2007,8(9):958-966.
[8] Weaver CT,Hatton RD,Mangan PR,et al.IL-17 family cytokines and the expanding diversity of effector T cell lineages[J].Annu Rev Immunol,2007,25:821-852.
[9] Park H,Li Z,Yang XO,et al.A distinct lineage of CD4 T cells regulates tissue inflammation by producing interleukin 17[J].Nat Immunol,2005,6(11):1133-1141.
[10]Korn T,Bettelli E,Oukka M,et al.IL-17 and Th17 cells[J].Annu Rev Immunol,2009,27:485-517.
[11]Totsuka T,Kanai T,Nemoto Y,et al.IL-7 is essential for the development and the persistence of chronic colitis[J].J Immunol,2007,178(8):4737-4748.
[12]Powrie F,Leach MW,Mauze S,et al.Phenotypically distinct subsets of CD4+T cells induce or protect from chronic intestinal inflammation in C.B-17 scid mice[J].Int Immunol,1993,5(11):1461-1471.
[13] Teshima T,Maeda Y,Ozaki K.Regulatory T cells and IL-17-producing cells in graft-versus-host disease[J].Immunotherapy,2011,3(7):833-852.
[14]Yi T,Chen Y,Wang L,et al.Reciprocal differentiation and tissue-specific pathogenesis of Th1,Th2,and Th17 cells in graft-versus-host disease[J].Blood,2009,114(14):1301-1312.
[15] Ivano II,Mckenzie BS,Zhou L,et al.The orphan nuclear receptor RORγt directs the differentiation program of proinflammatory IL-17+helper cells[J].Cell,2006,126(6):1121-1133.
[16] Yang L,Anderson DE,Baecher-Allan C,et al.IL-21 and TGF-beta are required for differentiation of human Th17 cells[J].Nature,2008,454(7202):350-352.
[17]McGeachy MJ,Chen Y,Tato CM,et al.The interleukin-23 receptor is essential for the terminal differentiation of interleukin 17-producing effector T helper cells in vivo[J].Nat Immunol,2009,10(3):314-324.
[18] Stumhofer JS,Laurence A,Wilson EH,et al.Interleukin-27 negative regulates the development of interleukin 17-producing T helper cells during chronic inflammation of the central nervous system[J].Nat Immunol,2006,7(9):937-945.
[19] Mudter J,Yu J,Zufferey C,et al.IRF4 regulates IL-17A promoter activity and controls RORγt-dependent Th17 colitis in vivo[J].Inflamm Bowel Dis,2011,17(6):1343-1358.
[20] De Jager PL,Jia X,Wang J,et al.Meta-analysis of genome scans and replication identify CD6,IRF8 and TNFRSF1A as new multiple sclerosis susceptibility loci[J].Nat Genet,2009,41(7):776-782.
[21] Fahlen L,Read S,Gorelik L,et al.T cells that cannot respond to TGF-beta escape control by CD4+CD25+regulatory T cells[J].J Exp Med,2005,201(5):737-746.
[22] O′Garra A,Vieira P.Regulatory T cells and mechanisms of immune system control[J].Nat Med,2004,10(8):801-805.
[23] Veltkamp C,Ruhwald R,Giesem T,et al.CD4+CD25+cell depletion from the normal CD4+T cell pool prevents tolerance toward the intestinal flora and leads to chronic colitis in immuno-deficient mice[J].Inflamm Bowel Dis,2006,12(6):437-446.

