注射用七葉皂苷鈉無菌檢查方法學驗證
杭州澳亞生物技術有限公司(310018)徐全華 陳青連 李紅菊
七葉皂苷鈉是從七葉樹科植物天師栗的干燥成熟種子中提取得到的皂苷鈉鹽,具有消腫、抗炎和改善血液循環的作用。用于腦水腫、創傷或手術后引起的腫脹,也用于靜脈回流障礙性疾病。
根據中國藥典2010年版二部無菌檢查法的規定[1],建立藥品無菌檢查方法時,應該進行方法學驗證,以證明方法的適用性。為確保該產品檢查方法科學、結果準確,本文建立了注射用七葉皂苷鈉無菌檢查方法,并對檢查方法進行了驗證。
1 儀器與材料
XG1.DWXD-0.36型脈動真空滅菌器(山東新華醫療器械廠);HTY-Ⅲ型智能集菌儀(杭州泰林生物技術設備有限公司);KDGB220、KDGB330型一次性全封閉集菌培養器(杭州泰林生物技術設備有限公司);LRH-250-Ⅱ型、LRH-250型生化培養箱(廣東省醫療器械廠)。
注射用七葉皂苷鈉(規格:5mg,杭州澳亞生物技術有限公司生產,批號:1106145、1106184、1106185)。
試驗用菌株:金黃色葡萄球菌(Staphylococcus aureus)[CMCC(B)26003];銅綠假單孢菌(Pseudomonas aeruginosa)[CMCC(B)10104];枯草芽孢桿菌(Bacillus subtilis)[CMCC(B)63501];生孢梭菌(Clostridium sporogenes)[CMCC(B)64 941];大腸埃希菌(Escherichia coli)[CMCC(B)44 102];白色念珠菌(Candida albicans)[CMCC(F)980 01];黑曲霉(Aspergillus niger)[CMCC(F)98003]。上述菌種由中國藥品生物制品檢定所提供。
驗證用培養基:硫乙醇酸鹽流體培養基;改良馬丁培養基;營養肉湯培養基;營養瓊脂培養基;玫瑰紅鈉瓊脂培養基;改良馬丁瓊脂培養基。上述培養基由杭州微生物試劑有限公司提供。
稀釋液和沖洗液:0.1%蛋白胨水溶液(杭州澳亞生物技術有限公司質檢部配制)。
2 方法與結果
2.1 菌液制備 取金黃色葡萄球菌、銅綠假單孢菌、枯草芽孢桿菌、大腸埃希菌的新鮮培養物,用白金耳接種至營養肉湯培養基中,取生孢梭菌的新鮮培養物,用白金耳接種至硫乙醇酸鹽流體培養基中,32.5℃培養24h。取白色念珠菌的新鮮培養物接種至改良馬丁培養基中,25.5℃培養24h。上述培養物用0.9%無菌氯化鈉溶液制成每1ml含菌數小于100cfu的菌懸液。
取黑曲霉斜面的新鮮培養物接種至改良馬丁瓊脂斜面培養基上,25.5℃培養5d使大量孢子成熟,加5ml含0.05%(ml/ml)聚山梨酯80的0.9%無菌氯化鈉溶液,用白金耳輕輕將孢子洗脫,用管口帶紗布的無菌毛細吸管吸出孢子懸液至無菌試管內,用含0.05%(ml/ml)聚山梨酯80的0.9%無菌氯化鈉注射液制成每1ml含孢子數小于100cfu的孢子懸液。
2.2 菌液計數 分別取金黃色葡萄球菌、銅綠假單孢菌、枯草芽孢桿菌、大腸埃希菌、生孢梭菌各1ml于培養皿中,每種菌做兩個平皿,加營養瓊脂培養基;取白色念珠菌、黑曲霉菌各1ml于培養皿中,每種菌做兩個平皿,加玫瑰紅鈉瓊脂培養基,按規定條件培養,結果見附表1。由附表1可知,各菌種在相應的稀釋度下,每毫升菌落計數結果符合規定。
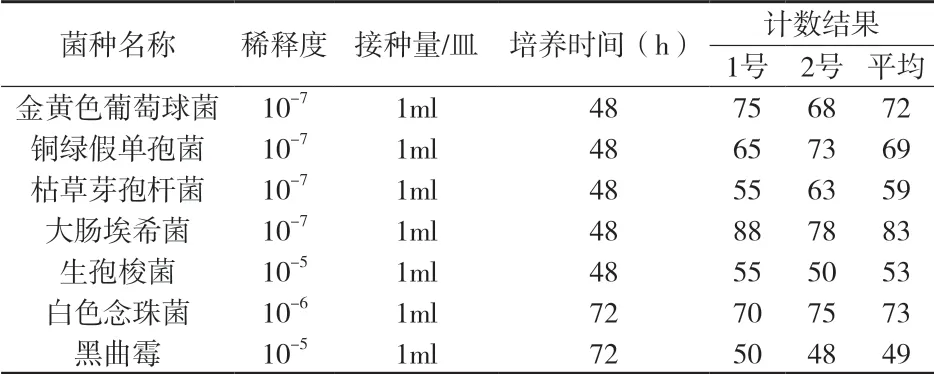
附表1 微生物計數結果
2.3 培養基的無菌性試驗 取硫乙醇酸鹽流體培養基和改良馬丁培養基各8支,在相應培養條件下培養14d,結果顯示兩種培養基的無菌性符合規定,見附表2。(注:“+”代表有菌生長,“-”代表無菌生長,以下表格符號意義相同)
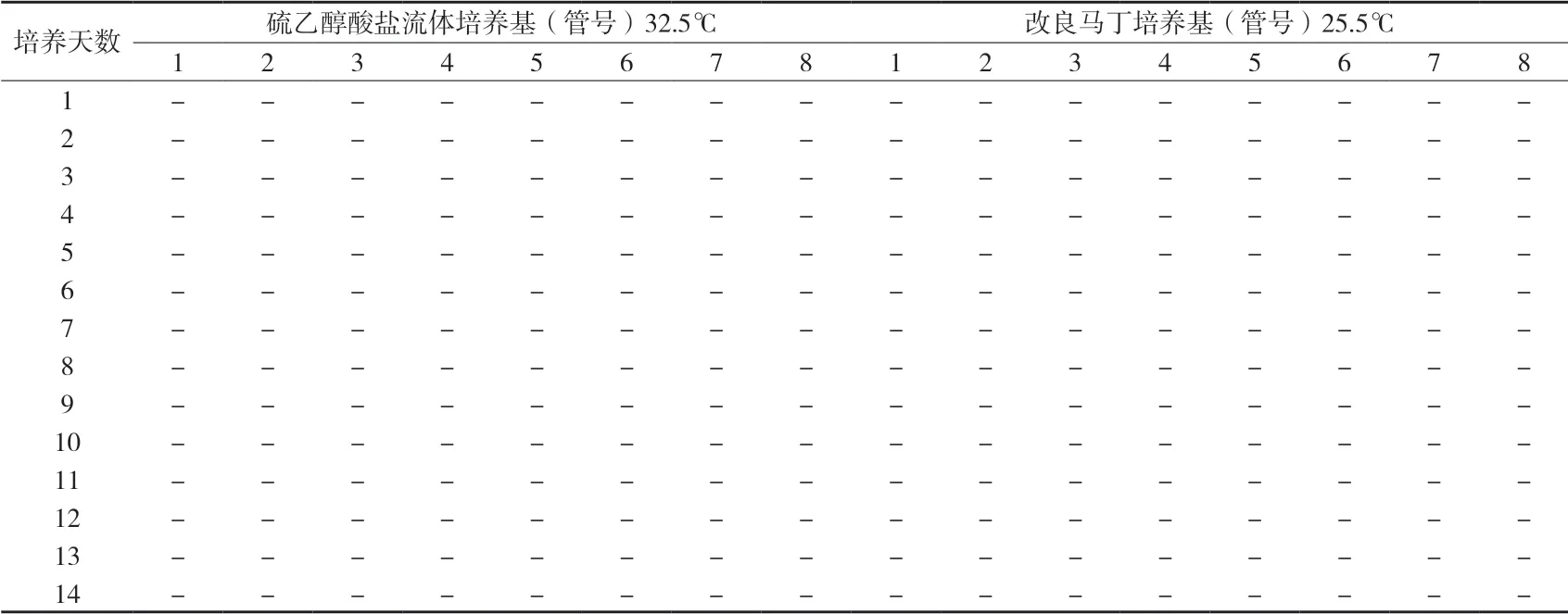
附表2 培養基的無菌性檢查結果
2.4 培養基的靈敏度試驗 取每管裝量為12ml的硫乙醇酸鹽流體培養基9支,分別接種小于100cfu的金黃色葡萄球菌、銅綠假單孢菌、枯草芽孢桿菌、生孢梭菌各2支,另1支不接種作為空白對照,按相應條件培養3d。取每管裝量為9ml的改良馬丁培養基5支,分別接種小于100cfu的白色念珠菌、黑曲霉各2支,另1支不接種作為空白對照,按相應的條件培養5d。每天觀察記錄,結果見附表3。由附表3可知,培養基的靈敏度試驗結果符合規定。

附表3 培養基的靈敏度試驗結果
2.5 薄膜過濾法方法學驗證 每批取供試品180支,用0.1%蛋白胨緩沖液溶解供試品,每10支為一組,分成18組,每組使用一個過濾器,其中6組未用沖洗液沖洗,另6組沖洗量為100ml,再6組沖洗量為200ml,在最后一次沖洗液中加入每1ml小于100cfu的試驗菌1ml,過濾后,將相應的培養基100ml加至各濾筒內作為供試品陽性對照(PPC)。另取集菌培養器,不過濾供試品,其他操作同上,作為陽性對照(PC)。按規定溫度培養3~5d,各試驗菌同法操作,結果見附表4、附表5、附表6。由附表4~6可知,三批產品在設定沖洗量為未沖洗、100ml和200ml條件下,對6種菌株而言供試品陽性對照和陽性對照均生長良好,且無明顯差異,均無抑菌作用,因此確定該產品無菌檢查方法為:取本品,用0.1%蛋白胨水溶液溶解,采用薄膜過濾法過濾,無需經沖洗液沖洗,直接加相應的培養基培養。
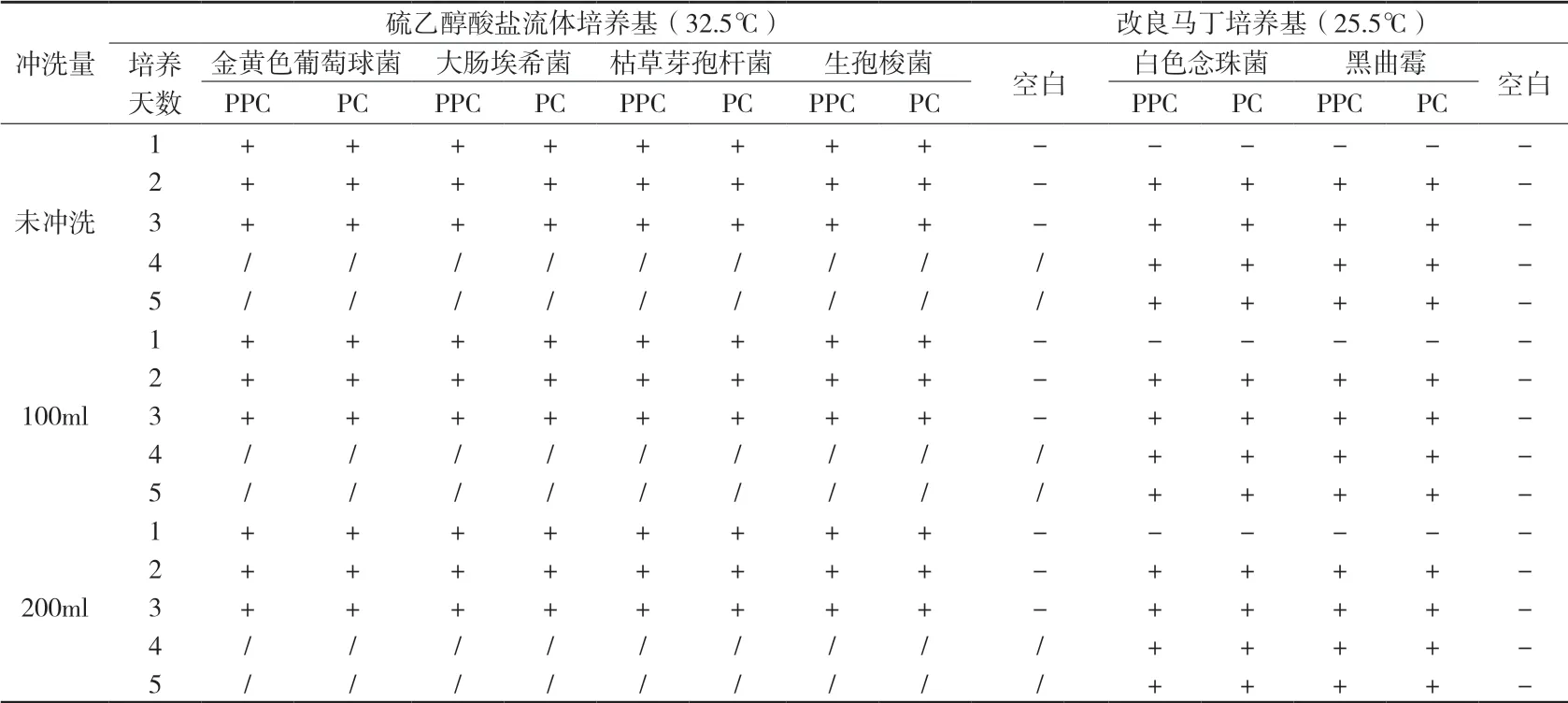
附表4 注射用七葉皂苷鈉方法學驗證結果(批號:1106145)
2.6 樣品的無菌檢查 每批取供試品30支,用0.1%蛋白胨水溶液溶解供試品,取三聯管全封閉集菌培養器直接過濾,其中一管加入100ml硫乙醇酸鹽流體培養基,另一管加入100ml改良馬丁培養基,第三管加入100ml硫乙醇酸鹽流體培養基并接種小于100cfu的金黃色葡萄球菌菌液作供試品陽性對照,另取稀釋液,同法操作,作為陰性對照,按規定溫度培養14d,結果見附表7。由附表7可知,三批產品按驗證確定的方法進行檢查,供試品陽性對照和陰性對照均成立,產品符合無菌要求。

附表5 注射用七葉皂苷鈉方法學驗證結果(批號:1106184)
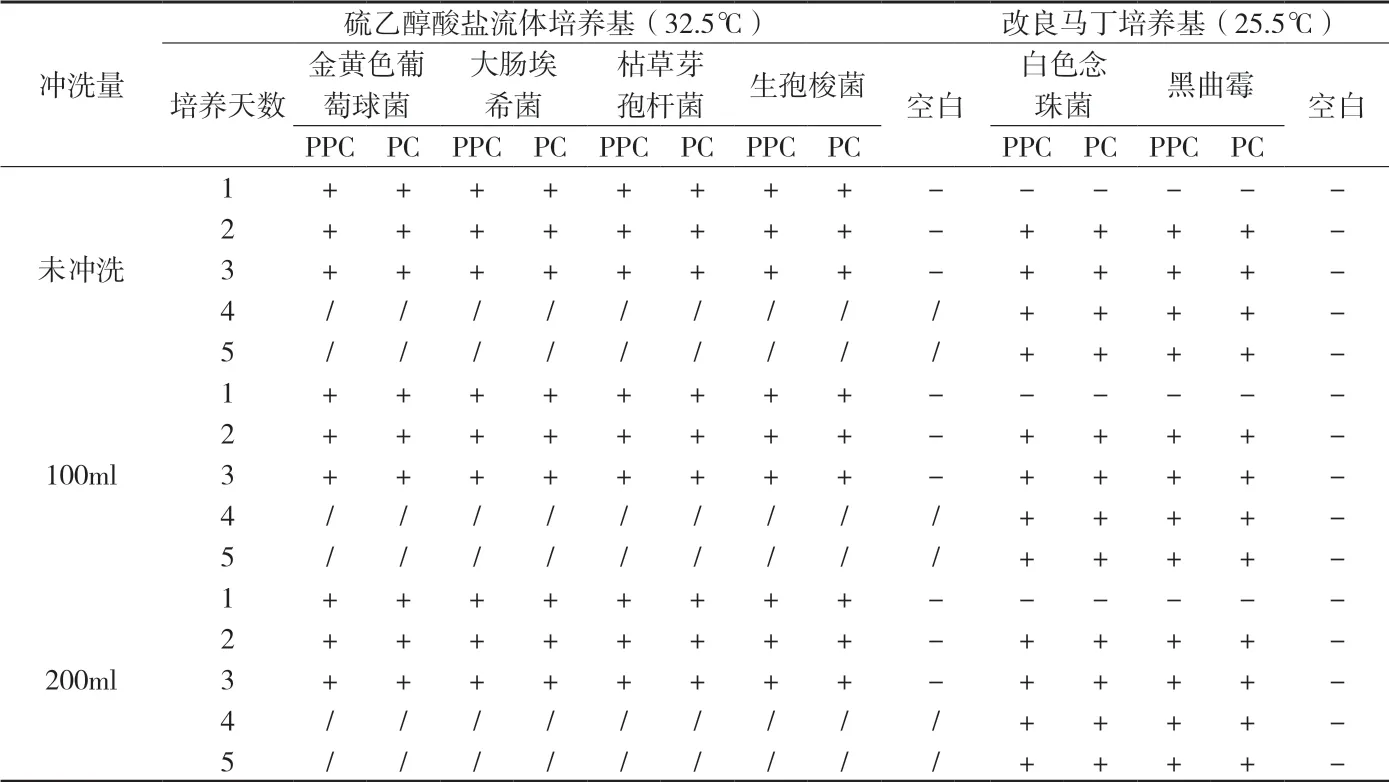
附表6 注射用七葉皂苷鈉方法學驗證結果(批號:1106185)
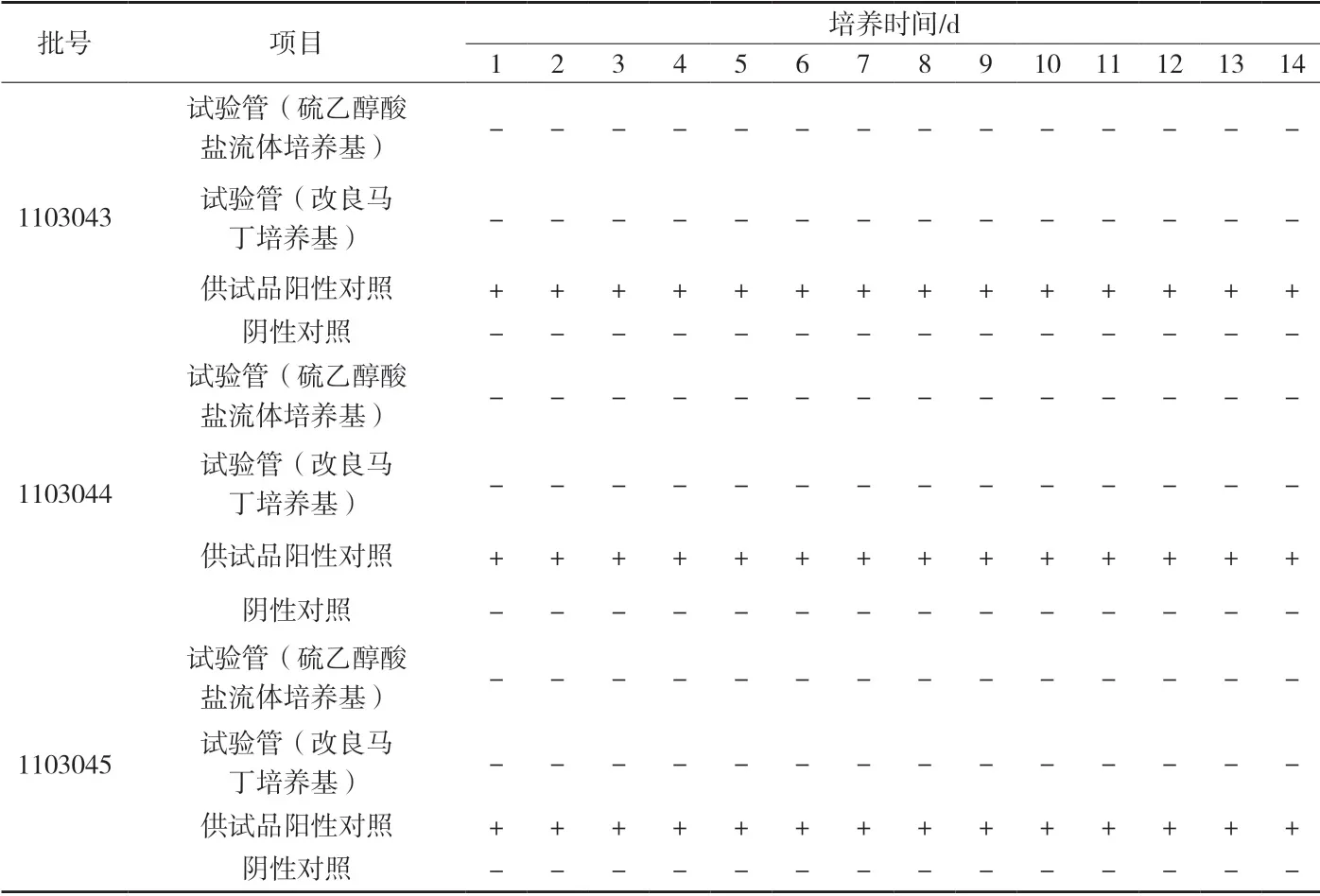
附表7 樣品無菌檢查試驗結果
3 討論
根據《中國藥典》二部附錄Ⅺ無菌檢查法的要求,無菌檢查法包括薄膜過濾法和直接接種法,只要供試品性狀允許,應采用薄膜過濾法,因此本品采用薄膜過濾法進行了相應的研究。此外,由于注射用七葉皂苷鈉為非抗菌藥物,因此,選擇金黃色葡萄球菌作陽性對照菌。研究結果表明:注射用七葉皂苷鈉在試驗菌液計數及所用培養基無菌性、靈敏度符合規定條件下,三批產品經驗證各陽性對照組生長情況均成立,未經沖洗和沖洗量為100ml和200ml的供試品陽性對照組生長情況與陽性對照組均生長良好,并且無明顯差異,無抑菌作用。三批樣品經檢查,符合無菌要求。因此,確定該產品無菌檢查方法為:取本品,用0.1%蛋白胨水溶液適量使溶解,用薄膜過濾法處理后,無需沖洗液進行沖洗,依法檢查,應符合規定。通過上述驗證所建立的方法可用于注射用七葉皂苷鈉的無菌檢查,結果準確、可靠。

