食管癌調強放療腫瘤退縮規律及其臨床價值
唐華燕 唐朝暉 黃洪林
食管癌是臨床常見的惡性腫瘤之一,臨床發病率和死亡率較高,多數患者確診后即已至晚期,生存時間較短[1]。目前放射治療是治療中晚期食管癌的主要手段。現回顧性分析我院行調強放療的食管癌患者放療過程中腫瘤退縮的規律,為提高放療準確性、降低周圍組織受量提供研究依據,報告如下。
1 資料與方法
1.1 一般資料
選取2012年5月至2013年5月我院收治的38例食管癌患者作為研究對象。所有患者均符合中國抗癌協會食管癌專業委員會出版的《食管癌規范化診治指南》[2]中食管癌相關診斷標準。患者年齡為42~76歲,平均年齡為(57.85±6.77)歲。原發腫瘤參照食管癌TNM分期標準[3]進行非手術T分期,為T2~T4期。排除合并其他惡性腫瘤或不能夠完成放療或新輔助聯合放化療計劃者。38例中男性30例,女性8例;病理類型:鱗狀細胞癌37例,小細胞癌1例;腫瘤部位:頸+胸上段17例,胸中段18例,胸下段3例;X線分型:髓質型33例,潰瘍型4例,蕈傘型1例;非手術T分期:T2期13例,T3期16例,T4期9例;治療方式:單純放療13例,同期放化療25例;病變長度:<5 cm 17例,≥5 cm 21例。
1.2 方法
1.2.1 CT定位 所有患者放療前均取仰臥位,使用GE64排螺旋CT掃描儀進行模擬定位。掃描范圍為鎖骨上至肝門水平區域,間隔5 mm重建后將信息傳遞至Varian-TPS三維治療計劃系統[4]。
1.2.2 確定靶區、擬定放療計劃 使用3D-TPS逐層勾畫GTV及周圍危及器官(包括心臟、肺部等),明確病變部位、長度及原發范圍,并使用3D-TPS對放療前GTV大小進行計算[5]。將GTV左右各擴展0.5~0.8 cm,上下各擴展2.0~3.0 cm作為臨床靶區(clinical target volume,CTV),同時參考轉移腫大淋巴結所累及區域和解剖結構對靶區進行適當調整。將CTV左右各擴展0.5~0.8 cm,上下各擴展1.0~1.5 cm作為計劃靶區(planning target volume,PTV)。
1.2.3 處方劑量及危及器官限量 常規分割,1.8~2.3 Gy/次,5次/周,處方劑量為50~62 Gy,中位劑量為54 Gy。兩肺V20≤30%,V30≤20%;脊髓最大劑量≤45 Gy;心臟V50≤50%[6]。
1.3 觀察指標
所有患者均于外照射前、照射至中位劑量32 Gy時、放療結束時、放療后6個月內分別進行CT及X線鋇餐造影檢查,記錄患者GTV變化情況,并以此計算放療前半程、放療后半程和放療全程VRR。
計算公式:VRR=(pGTV-iGTV)/pGTV[7]。pGTV為放療前大體腫瘤體積;iGTV為放療后大體腫瘤體積。
1.4 統計學分析
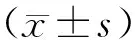
2 結果
2.1 不同放療時段患者GTV變化情況
所有患者外照射前、照射至中位劑量32 Gy時、放療結束時及放療后6個月GTV見表1。隨著放療進行,患者GTV逐漸縮小。完成6個月隨訪的32例患者中6例較放療結束時GTV有所增加,18例有所減小,8例基本不變。

表1 不同放療時段患者GTV變化情況/ml
2.2 患者放療過程中腫瘤VRR
根據VRR計算公式得到放療前半程、放療后半程和放療全程VRR值(表2)。放療前半程患者VRR明顯高于后半程,差異具有統計學意義(P<0.05)。

表2 患者放療過程中腫瘤VRR/%
注:*為與放療前半程VRR比較,P<0.05。
3 討論
臨床研究表明,食管癌患者腫瘤容積效應與放射性抵抗、乏氧及遠處轉移均有緊密聯系,腫瘤負荷增加產生的副作用是影響腫瘤控制率的重要因素[8]。腫瘤體積也是影響預后的主要因素,患者腫瘤體積越小,表明治療效果越好,局部控制率和長期生存率較高。患者GTV越大,表示腫瘤細胞數量越多,更易引起腫瘤內血運障礙、乏氧細胞增加甚至腫瘤中心壞死,而乏氧細胞增多會引發腫瘤侵襲性增加,對放療的抗拒增加,影響治療效果[9]。本研究中38例患者,隨著放療的逐步進行,腫瘤體積不斷縮小,與上述文獻報道相似,表明放射治療對減小腫瘤體積具有顯著效果。
腫瘤的體積變化情況不僅是放射治療的監測指標,也是診斷食管癌臨床分期和評估放療效果的重要指標。臨床研究表明,患者GTV縮小后腫瘤橫徑及前后徑均會產生變化,此時仍按照放療前測定的靶區和劑量采取常規調強放射治療,易造成沉淀劑量明顯改變[10],需要重新進行CT模擬定位,調整靶區治療計劃。螺旋CT增強掃描和容積掃描能夠準確顯示患者食管壁厚度、食管外浸潤、淋巴結轉移以及食管壁異常增強,不僅能夠為放療前食管癌診斷和TNM分期提供依據,還能為設計放療計劃和評估放療效果提供參考。本研究中使用螺旋CT掃描技術為放療進行指導,同時也為放療患者的療效進行評估。
隨著自適應放療觀念被臨床醫師廣泛認可,將影像學設備與放療結合,隨時修整靶區和劑量,以減少周圍正常組織受照劑量和并發癥發生率已經成為了臨床研究的熱點。臨床研究表明,食管癌患者放療過程中同時存在腫瘤退縮和靶區移位的情況,尤其是當照射劑量超過40 Gy時中心移位率更高[11]。采用自適應放療提高了放療的準確性,更加適應放療過程中腫瘤和危及器官區的變化情況。
本研究結果顯示,放療前半程患者VRR明顯高于后半程,差異具有統計學意義,表明患者腫瘤退縮主要發生在放療前半程,放療師需及時根據影像學檢查結果調整靶區及放射劑量,保證在靶區高劑量照射的同時降低周圍組織受量。
[1] 孫蘇平,楊鴻鵬,黎 功,等.中國非手術治療食管癌研究進展〔J〕.癌癥進展,2008,6(1):30-35,52.
[2] 中國抗癌協會食管癌專業委員會.食管癌規范化診治指南〔M〕.北京:中國協和醫科大學出版社,2011:8-12.
[3] 陳龍奇.制訂2009第7版食管癌TNM分期標準〔J〕.中國胸心血管外科臨床雜志,2008,15(1):52-55.
[4] 施 怡,顏志勇,謝伯軍,等.食管癌CT表現及其對放療的預測價值〔J〕.實用癌癥雜志,2013,28(1):73-76.
[5] 張先穩,張西志,花 威,等.AAA算法和PBC算法在食管癌調強放療中的驗證評估〔J〕.實用癌癥雜志,2013,28(3):282-284.
[6] 葛小林,孫新臣,陳文湛,等.胸上段食管癌調強放療和三維適形放療劑量學研究〔J〕.中國醫學物理學雜志,2010,27(2):1708-1711,1720.
[7] Hsu WH,Hsu PK,Hsieh CC,et al.The metastatic lymph node number and ratio are independent prognostic factors in esophageal cancer〔J〕.J Gastrointest Surg,2009,13(11):1913-1920.
[8] 王 軍,韓 春,李曉寧,等.食管癌調強放射治療初期療效分析〔J〕.癌癥,2009,28(11):1138-1142.
[9] 程 巖,王麗梅,張雪彬,等.食管癌調強放療療效和預后因素分析〔J〕.疾病監測與控制,2013,7(8):505-506.
[10] Yang SN,Liao CY,Chen SW,et al.Clinical implications of the tumor volume reduction rate in head-and-neck cancer during definitive intensity-modulated radiotherapy for organ preservation〔J〕.Int J Radiat Oncol Biol Phys,2011,79(4):1096-1103.
[11] 孫 軍,張 強,祝 晨,等.胸中段食管癌調強放療近期療效觀察〔J〕.腫瘤防治研究,2012,39(3):318-320.

