FCC汽油S Zorb反應吸附脫硫過程中不飽和烴加氫反應的研究
余 賀,趙基鋼,侯曉明,2,沈本賢
(1.華東理工大學化學工程聯合國家重點實驗室,上海 200237;2.中國石化上海高橋分公司)
FCC汽油S Zorb反應吸附脫硫過程中不飽和烴加氫反應的研究
余 賀1,趙基鋼1,侯曉明1,2,沈本賢1
(1.華東理工大學化學工程聯合國家重點實驗室,上海 200237;2.中國石化上海高橋分公司)
S Zorb工藝可以將FCC汽油的硫質量分數降至小于10 μgg,但在脫硫過程中,由于反應體系中引入了H2,在吸附劑表面既發生了硫化物的脫硫反應,也不可避免地存在導致汽油辛烷值損失的不飽和烴的加氫反應。對比分析了中國石化上海高橋分公司S Zorb原料汽油和產品汽油的組成,從熱力學和動力學角度分析了這些加氫反應對體系組分變化的影響,計算了標準壓力下不同溫度下的反應平衡常數K和Gibbs反應自由能,并采用四階龍格-庫塔法計算了每個反應的反應速率常數,這些數據可以為SZorb裝置工藝參數的進一步優化提供參考。
吸附脫硫 加氫反應 反應速率 熱力學 動力學
我國車用汽油的主要調合組分為FCC汽油,FCC汽油約占我國成品汽油總量的70%~80%。FCC汽油具有高硫、高烯烴含量的特點,烯烴體積分數為40%~60%,硫質量分數為160~1 600μgg[1]。目前我國絕大多數煉油廠都是采用加氫脫硫(HDS)的工藝處理FCC汽油,傳統加氫脫硫的主要歷程為:在壓力5.6~8.4MPa的條件下,硫化物與氫氣在CoMoAl2O3或NiMoAl2O3催化劑作用下發生氫解或加氫反應生成H2S,進而達到脫除油品中硫化物的目的。傳統HDS技術在大量脫除汽油中硫化物的同時,由于其苛刻的反應條件致使汽油中的不飽和烴加氫飽和,造成汽油辛烷值下降。SZorb技術是ConocoPhillips公司開發,中國石油化工股份有限公司買斷并實施工業應用的FCC汽油吸附脫硫技術[2-4],在臨氫條件下可以將汽油的硫質量分數降到10μgg以下,具有氫耗低、反應活性穩定、運轉周期長和能耗低的優點。FCC汽油是一種包含不同碳數烷烴、烯烴、芳烴和含硫、含氮化合物的多組分物質,在臨氫條件下進行吸附脫硫反應的同時,體系不可避免地會發生烯烴等不飽和烴的加氫反應,不飽和烴的種類與含量不同,加氫飽和后辛烷值損失的程度也不同,因此,汽油中烴類分子的大小、結構和含量對辛烷值有著決定性的影響[5-6]。目前關于該技術的研究報道主要集中在如何開發新型高效、高穩定性的吸附劑[7]以及脫硫反應機理,而對于FCC汽油SZorb反應吸附脫硫前后組成變化的研究則很少報道。
本課題根據SZorb工藝過程中原料汽油和產品汽油的烴組成差異,分析SZorb反應吸附脫硫過程中可能存在的加氫反應,研究這些反應的熱力學和動力學規律,以期為SZorb工藝條件的優化提供借鑒。
1 實 驗
1.1 原 料
SZorb原料汽油和產品汽油均取自中國石化上海高橋分公司,基本性質見表1。
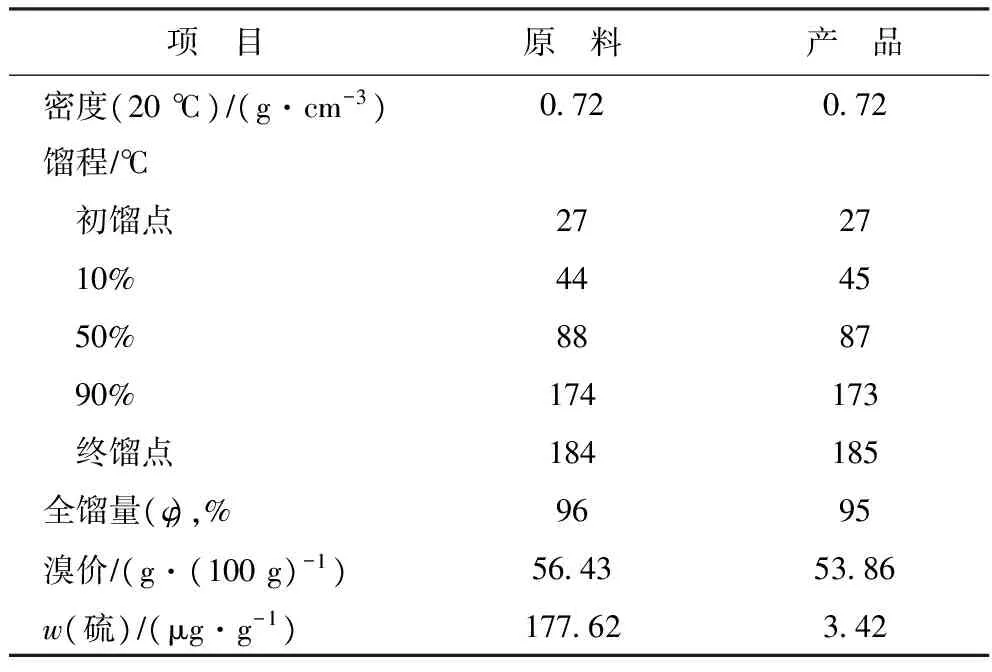
表1 S Zorb原料和產品的基本性質
1.2 組成分析
采用上海海欣色譜儀器有限公司生產的GC-920氣相色譜儀和CDMC色譜工作站分析FCC原料汽油和產物的族組成,氫火焰離子化檢測器,色譜柱為高彈性石英毛細管柱和PONA柱石英毛細管柱,固定液為OV-101,柱長為50 m,內徑為0.2 mm。色譜柱溫度35 ℃,停留時間10 min,升溫速率2 ℃/min,終溫200 ℃,汽化室溫度200 ℃,檢測器溫度200 ℃,進樣量2 μL。
2 FCC汽油S Zorb吸附脫硫前后的組成變化分析
由PONA分析得到FCC汽油經S Zorb脫硫工藝處理前后的族組成,結果見表2。由表2可知:脫硫后正構烷烴、異構烷烴含量有所增加,其中正構烷烴增加幅度最大,達2.32百分點,而環烷烴和芳烴含量分別降低0.31百分點和3.26百分點,異構烷烴含量增加是異構烯烴飽和所致;吸附脫硫后C4~C6烯烴含量減少,表明FCC汽油中這些烯烴在吸附劑表面較容易發生加氫反應。
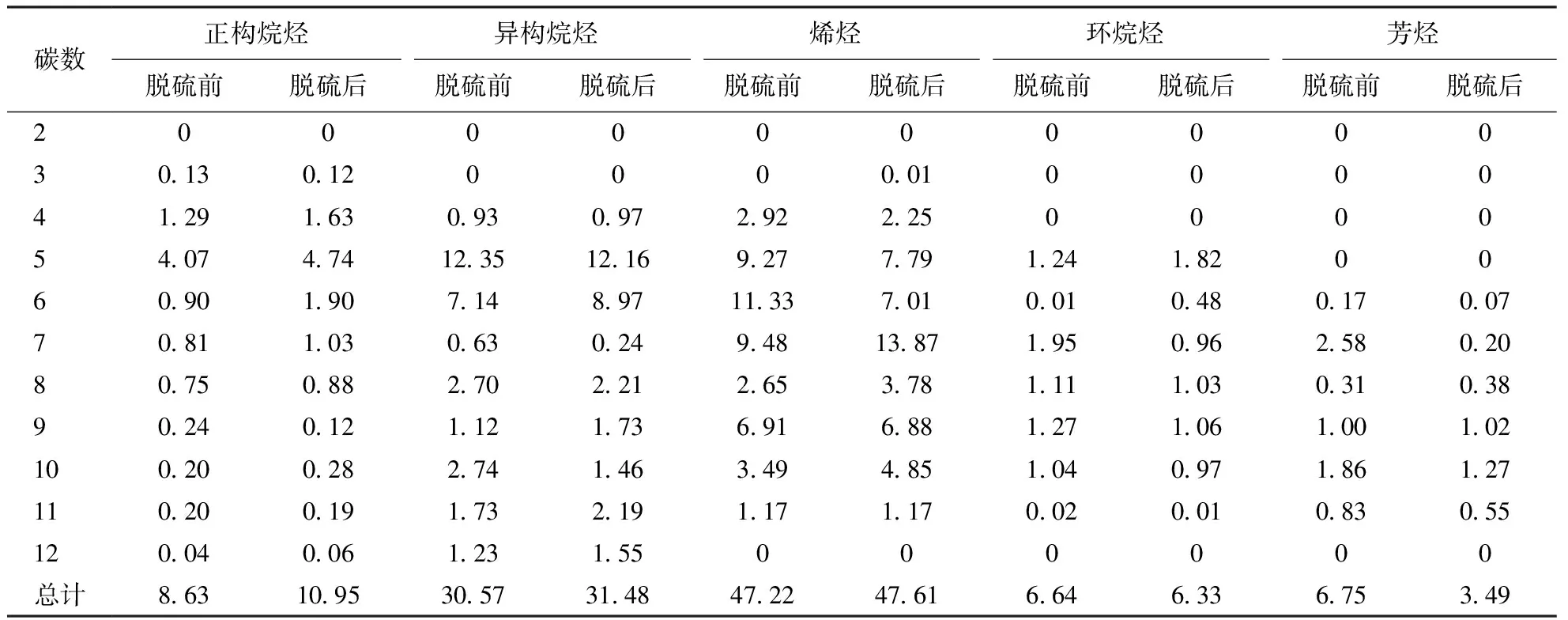
表2 FCC汽油經S Zorb脫硫工藝處理前后的族組成數據 w,%
表3列出了FCC汽油S Zorb吸附脫硫前后含量變化較大的16種烴類,表4為S Zorb吸附脫硫過程中可能存在的8個有代表性的加氫反應。

表3 16種烴類在S Zorb原料和產品中的含量 w,%
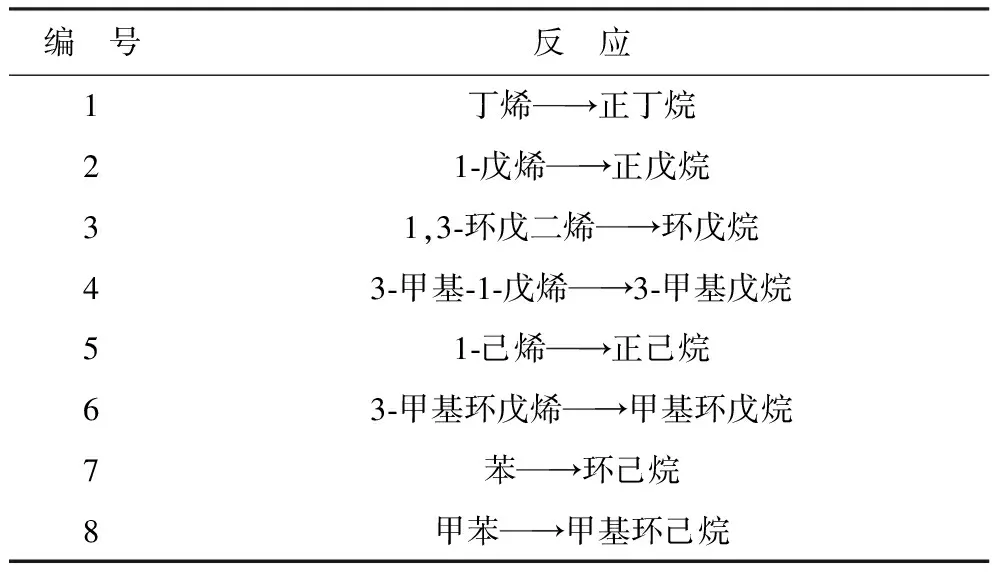
表4 S Zorb吸附脫硫過程中可能存在的代表性加氫反應
3 熱力學計算與分析
3.1 基團貢獻法
采用基團貢獻法Benson法估算FCC汽油中各組分的物性參數,其特點是考慮鄰近基團的影響,幾乎適用于全部的有機物,溫度范圍較寬,精確度較高。基本原則是:以原子或原子團為中心,并考慮到與此原子或原子團相連接的原子或原子團的不同來劃分基團,在確定基團參數時考慮了次相鄰原子間的影響,對于那些不能在基團參數中反映出來的因素,如順反異構、位置異構、交叉異構等則另設修正項[8]。Benson法的計算式為:
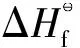
3.2 計算方法
熱容與溫度的關系式為:
Cp,m=a+bT+cT2
(1)
式中:a,b,c是反應體系中與各物質本性有關的常數,T為反應溫度。
各反應式的ΔCp為:
ΔCp=Δa+ΔbT+ΔcT2
(2)
式中:Δa=∑(υa),Δb=∑(υb),Δc=∑(υc),v為化學計量數。
(3)
式中:ΔH0為積分常數,將某一溫度以及該溫度下的標準摩爾反應焓代入求得。
根據van’t Hoff方程的微分式:
(4)
對式(4)進行積分,便可得到反應平衡常數K與溫度的關系:
(5)
式中:I為積分常數,可由某一溫度T下的K值代入式(5)求得。
3.3 計算過程及分析
反應體系中所涉及物質的熱力學參數由基團貢獻法估算,結果見表5。
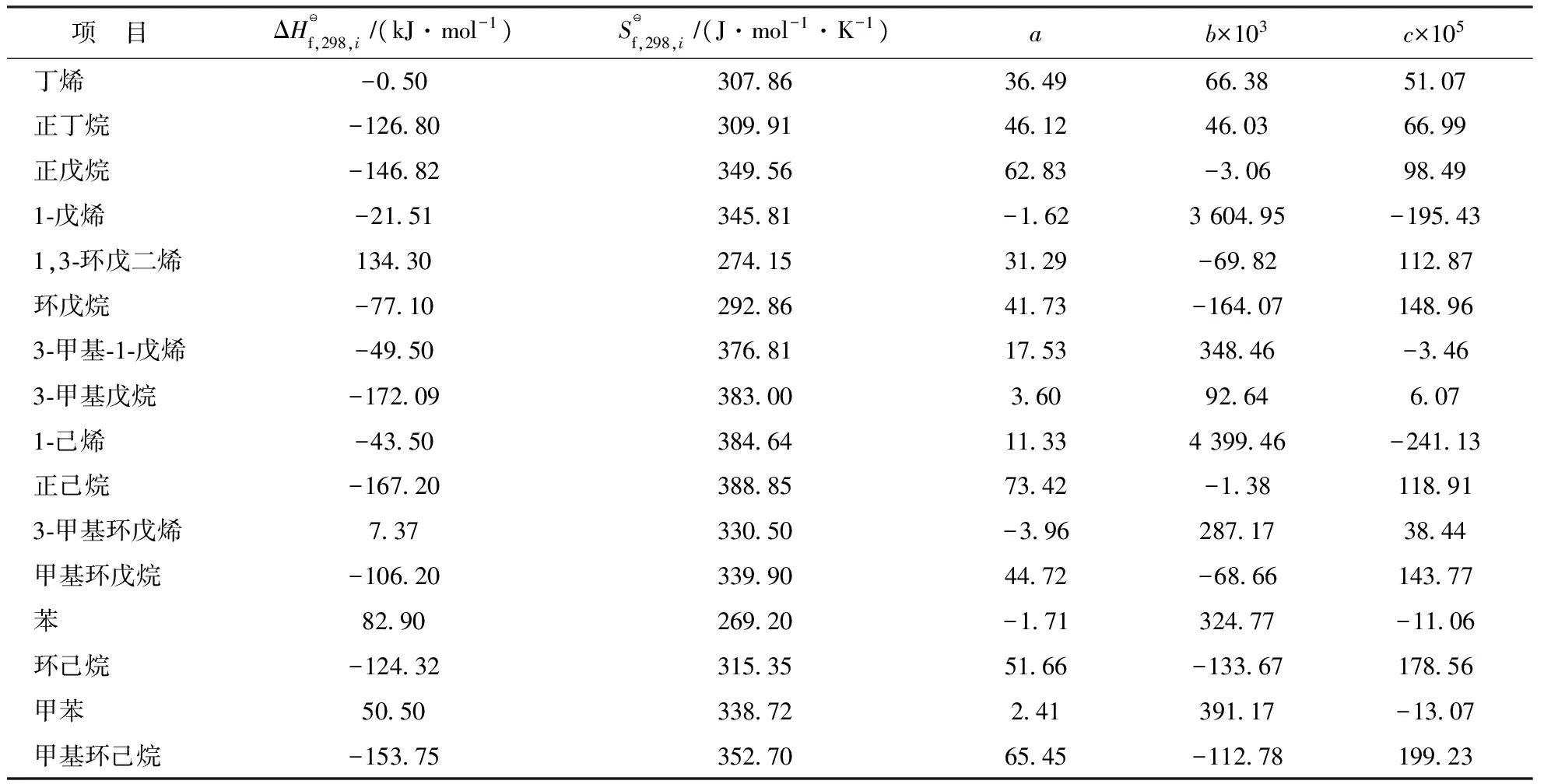
表5 標準狀態下16種烴類的熱力學參數
在表5數據的基礎上進行標準狀態下反應可行性的熱力學分析[9],計算標準摩爾反應焓、熵以及Gibbs自由能,結果見表6。
標準摩爾反應焓:
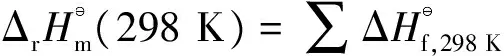
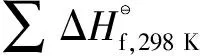
(6)
標準熵變:
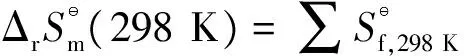
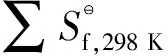
(7)
標準Gibbs自由能:
(8)
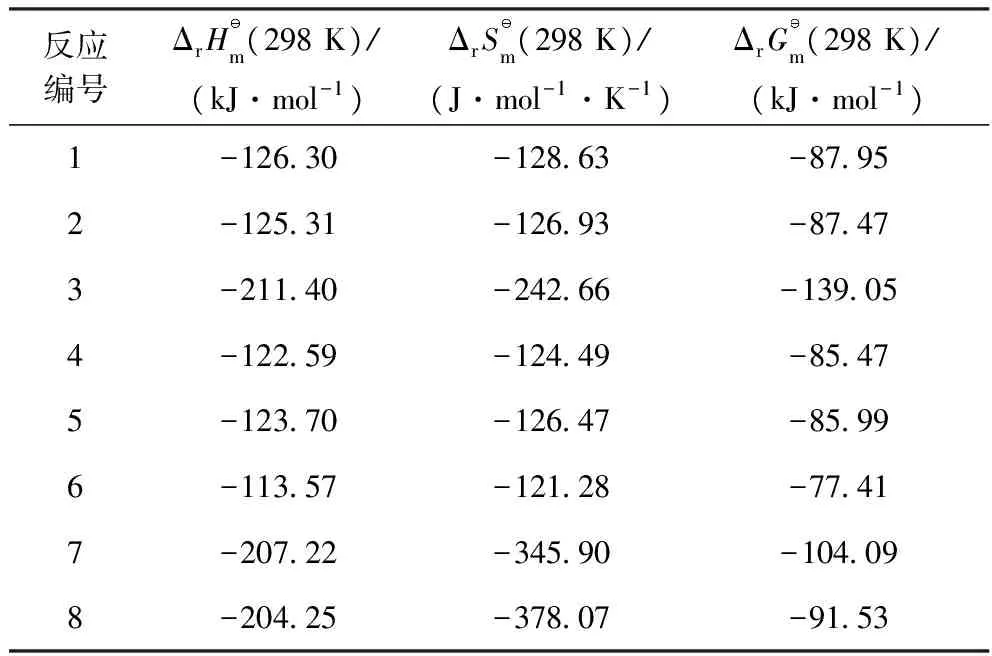
表6 標準狀態下的反應焓、反應熵和反應Gibbs自由能
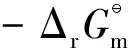
由表7可知:在所討論的溫度范圍內,每一個反應的平衡常數都隨溫度的升高而下降,說明加氫反應屬于放熱反應,且對溫度的變化較敏感;在相同條件下,直鏈烯烴中丁烯加氫反應的平衡常數最大,1-戊烯次之,1-己烯最小,表明隨著烯烴碳數的增大,加氫反應的平衡常數越來越小;在相同碳數下,支鏈烯烴3-甲基-1-戊烯加氫反應的平衡常數大于1-己烯;在芳烴反應體系中,苯加氫反應的平衡常數大于甲苯;另外,1,3-環戊二烯加氫反應的平衡常數最大,表明對于不同結構的烯烴,在相同條件下環狀二烯烴相對于其它烯烴更容易發生加氫飽和反應。羅翔等[10]的研究也得到了與上述結果類似的觀點。
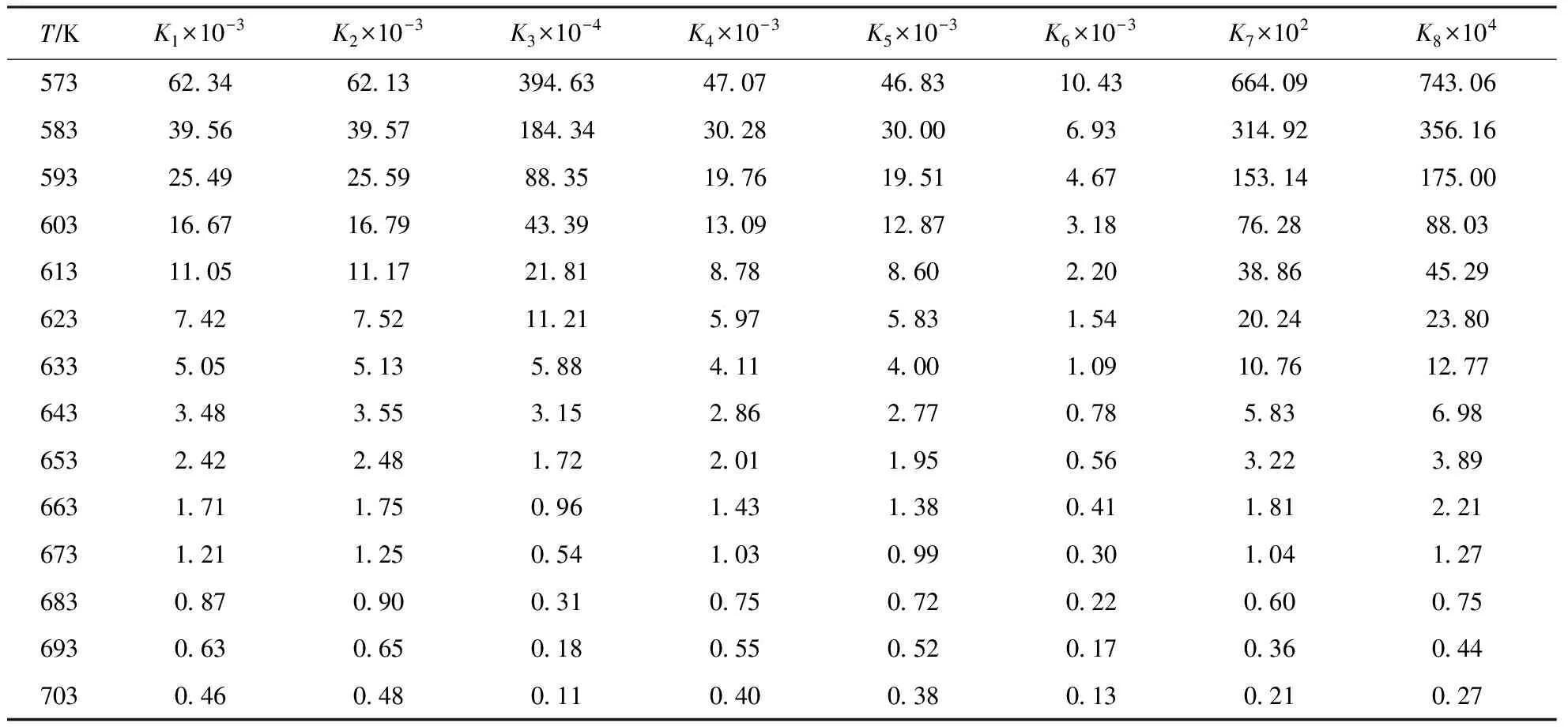
表7 不同溫度下的反應平衡常數
烯烴碳數、有無支鏈、是否環狀等是影響加氫反應進行的主要因素,為了方便了解汽油中各烯烴加氫反應與汽油烴類組成的關系,將烯烴分為直鏈烯烴、支鏈烯烴、環烯烴和芳烴4大類。圖1~圖4為0.1 MPa時各烯烴加氫反應的Gibbs自由能與溫度的關系曲線。
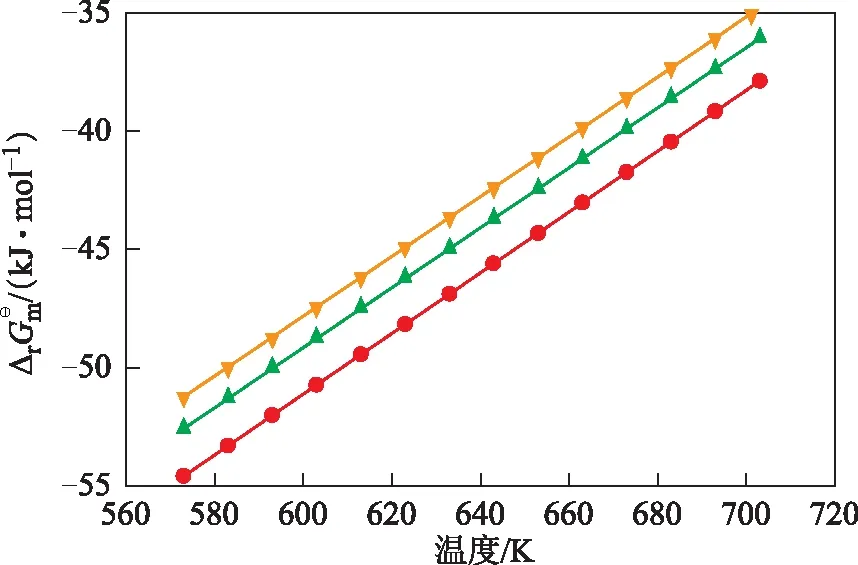
圖1 直鏈烯烴體系各反應的Gibbs自由能與溫度的關系●—反應1; ▲—反應2; 反應5
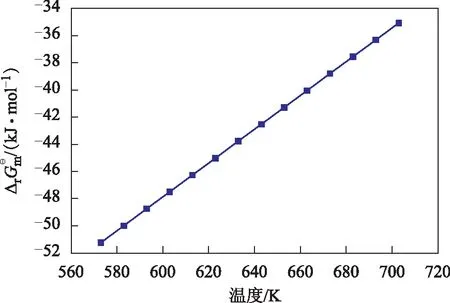
圖2 支鏈烯烴體系反應的Gibbs自由能與溫度的關系■—反應4
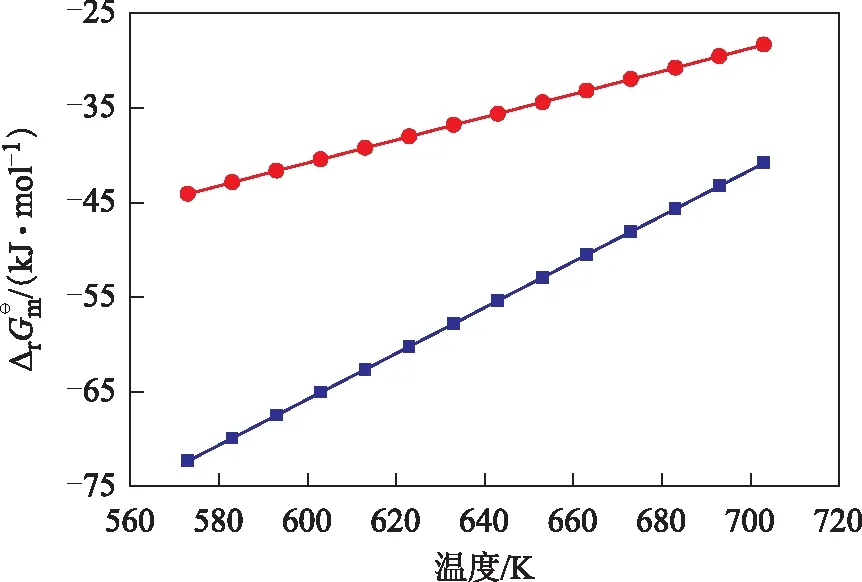
圖3 環烯烴體系各反應的Gibbs自由能與溫度的關系■—反應3; ●—反應6
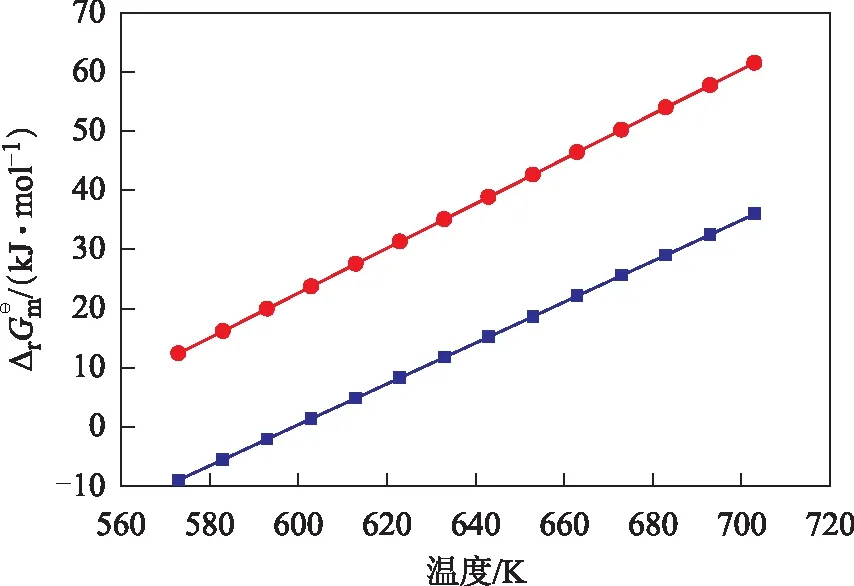
圖4 芳烴體系各反應的Gibbs自由能與溫度的關系■—反應7; ●—反應8

4 動力學分析
反應動力學參數的計算方法有很多種,所采用的方法不同,計算結果會有很大的差異,根據文獻[11]報道,四階龍格-庫塔法和數值積分法在計算過程中不會引入明顯的誤差,計算結果可靠。國內外學者也針對烯烴的加氫反應動力學進行了大量的研究,丁建軍等[12]研究了FCC汽油中烯烴在鎳基催化劑上的加氫反應,認為烯烴的反應級數均為1。
本課題在Matlab環境下根據四階龍格-庫塔法求解表4中8個反應的反應速率常數(k)。計算框圖見圖5,結果見表8。
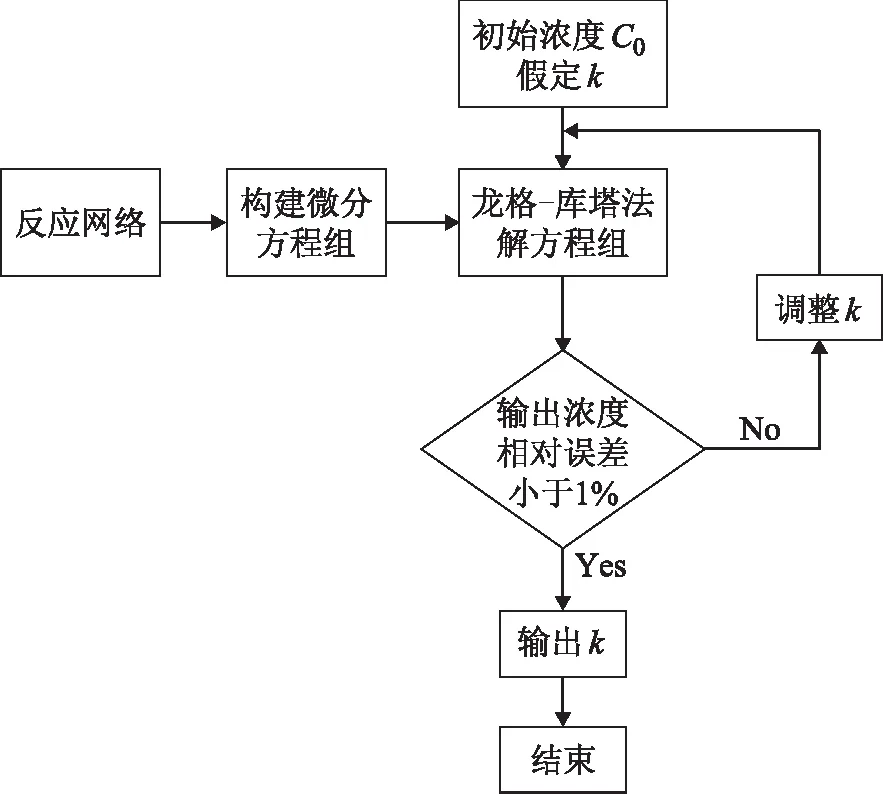
圖5 反應速率常數計算框圖
在圖5所示的計算框圖里,先假定一組反應速率常數,然后根據設計的程序求出假定反應速率常數下生成物的摩爾組成,若其與實際產品摩爾組成的相對誤差大于1%,則調整反應速率常數,直到計算得到的生成物摩爾組成與實際產品摩爾組成的相對誤差小于1%,那么計算得到的反應速率常數便是該加氫反應的反應速率常數。由表8可知,各烯烴加氫反應速率常數由高到低的順序為:1,3-環戊二烯>3-甲基環戊烯>1-己烯>3-甲基-1-戊烯>丁烯>戊烯-1>甲苯>苯。
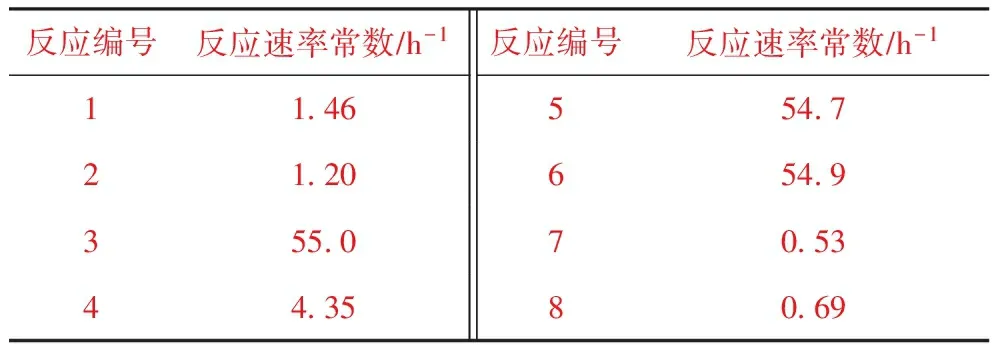
表8 四階龍格-庫塔法得到的反應速率常數
將在Matlab環境下求得生成物摩爾組成與實際結果進行對比,如表9所示。由表9可以看出,根據四階龍格-庫塔法計算得到的生成物摩爾組成與實際值比較接近,相對誤差不到1%,因此,表8中的反應速率常數可滿足要求,這就為進一步求解化學反應動力學方程提供了基礎數據。
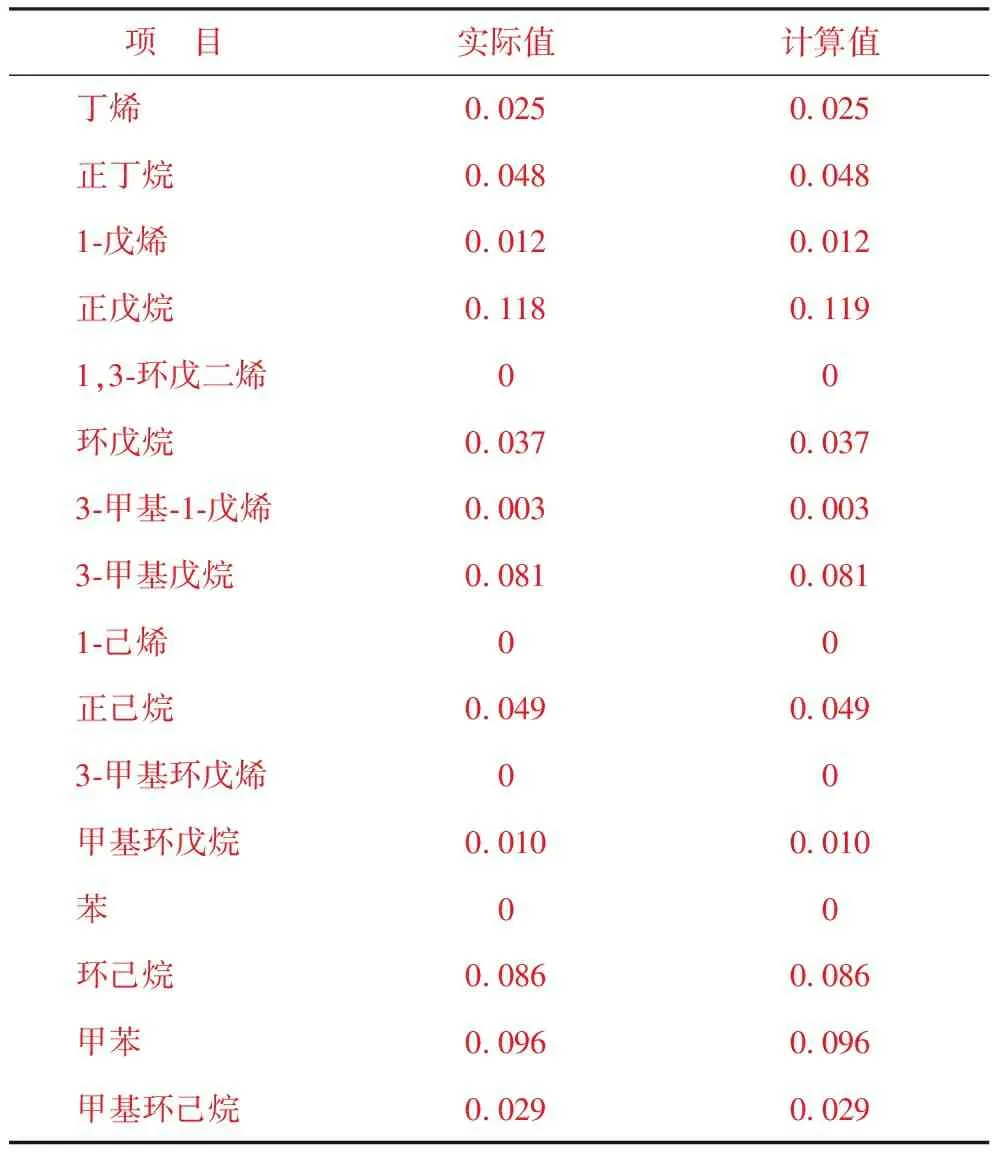
表9 生成物摩爾組成的實際值與計算值對比
5 結 論
(1) FCC汽油烴類組成是決定汽油辛烷值的主要因素,在S Zorb反應吸附脫硫過程中,反應體系會發生不飽和烴的加氫反應,導致辛烷值的損失。烯烴結構和含量不同時,加氫反應的程度和反應速率不同,辛烷值損失也會有所差異。
(2) FCC汽油中的烯烴加氫反應屬于放熱反應,多集中在C4,C5,C6餾分中,反應溫度是影響辛烷值損失的重要因素,反應平衡常數對溫度比較敏感,即低溫對加氫反應有促進作用,高溫對加氫反應有抑制作用。在相同條件下,各烯烴加氫反應平衡常數由高到低的順序為:1,3-環戊二烯>丁烯>1-戊烯>3-甲基-1-戊烯>1-己烯>3-甲基環戊烯>苯>甲苯。

(4) 根據四階龍格-庫塔法確定不同烯烴的加氫速率由高到低的順序為:1,3-環戊二烯>3-甲基環戊烯>1-己烯>3-甲基-1-戊烯>丁烯>1-戊烯>甲苯>苯。
[1] 趙樂平,胡永康,龐宏,等.FCC汽油加氫脫硫降烯烴新技術的開發[J].工業催化,2004,12(4):24-26
[2] 姚智,楊遠行,王萬新,等.國產吸附劑在S Zorb汽油吸附脫硫裝置上的工業應用[J].石油煉制與化工,2013,44(5):43-46
[3] 胡躍梁,孫啟明.S Zorb吸附脫硫裝置運行過程中存在的問題分析及應對措施[J].石油煉制與化工,2013,44(7):69-72
[5] 王寧.汽油燃料的化學組成和結構與抗爆性能關系的研究[J].石油煉制與化工,1996,27(2):41-46
[6] 彭樸,陸婉珍.汽油辛烷值和組成的關系[J].石油煉制,1981,12(6):27-38
[7] 徐莉,鄒亢,徐廣通,等.S Zorb工業吸附劑結構、組成及再生行為研究[J].石油煉制與化工,2013,44(6):44-48
[8] 董新法,方利國,陳礪.物性估算原理和計算機計算[M].北京:化學工業出版社,2006:180-199
[9] 劉俊吉,周亞平,李松林.物理化學[M].北京:高等教育出版社,2009:35-72
[10]羅翔,肖尚辰,侯凱湖.FCC汽油加氫脫硫過程的熱力學分析[J].石油與天然氣化工,2010,39(3):210-212
[11]熊杰明,張麗萍,呂九琢.反應動力學參數的計算方法與計算誤差[J].計算機與應用化學,2003,20(1):159-162
[12]丁建軍,黃興亮.催化裂化輕汽油中烯烴加氫反應宏觀動力學[J].化學工程,2011,39(9):61-65
STUDY ON HYDROGENATION OF UNSATURATED HYDROCARBON DURING FCC GASOLINE DESULFURIZATION BY S Zorb PROCESS
Yu He1, Zhao Jigang1, Hou Xiaoming1,2, Shen Benxian1
(1.StateKeyLaboratoryofChemicalEngineering,EastChinaUniversityofScienceandTechnology,Shanghai200237; 2.SINOPECShanghaiGaoqiaoCompany)
The S Zorb process can reduce the sulfur content of gasoline to less than 10 μgg. However, the hydrogenation reactions of olefins and aromatics occur inevitably during S Zorb adsorption desulfurization, leading to some octane number loss. In order to optimize the S Zorb operation, the comparative analysis of the compositions of feed and product of S Zorb unit of Shanghai Gaoqiao branch was conducted to see the influence of hydrogenation reactions on change of compositions from the point of view of thermodynamics and kinetics. The equilibrium constants and Gibbs free energies at different temperatures were calculated under the normal pressure. And the reaction rate constants were figured out by the 4thorder Runge-Kutta method.
S Zorb; hydrogenation reaction; reaction rate; thermodynamics; kinetics
2013-12-02; 修改稿收到日期: 2014-03-23。
余賀,碩士研究生,從事FCC汽油S Zorb工藝反應過程的研究工作。
趙基鋼,E-mail: zjg@ecust.edu.cn。

