L-亮氨酸產(chǎn)生菌的代謝工程改造及其發(fā)酵效率
黃欽耿
(1. 福建省麥丹生物集團(tuán)有限公司福州研究中心,福建 福州 350008;2. 福建師范大學(xué)工業(yè)微生物發(fā)酵技術(shù)國家地方聯(lián)合工程研究中心,福建 福州 350107)
L-亮氨酸為哺乳動物8種必需氨基酸之一,廣泛應(yīng)用于食品、飼料、醫(yī)藥等行業(yè),市場需求量逐年增多[1]。迄今為止,L-亮氨酸工程菌株主要有大腸桿菌和棒狀桿菌。其中以谷氨酸棒桿菌和黃色短桿菌為出發(fā)菌株的研究最多[2]。谷氨酸棒桿菌是一類重要的工業(yè)氨基酸生產(chǎn)菌株,已成為一個工業(yè)生物技術(shù)及轉(zhuǎn)化的平臺菌株,每年生產(chǎn)數(shù)百萬噸的氨基酸[3],其中包括作為風(fēng)味增強(qiáng)劑的L-谷氨酸(350萬噸/年)和作為飼料和食品添加劑的L-賴氨酸(250萬噸/年)等[3]。谷氨酸棒桿菌在氨基酸的發(fā)酵方面,除了L-谷氨酸和L-賴氨酸這類大宗氨基酸之外,還包括許多的小品種氨基酸,如三類支鏈氨基酸(branched-chain amino acid,BCAAs):L-纈氨酸、L-異亮氨酸及L-亮氨酸[4-6],其每年需求量約在1000~3000噸,其中L-亮氨酸的需求量約在500~800噸/年,特別在飼料行業(yè)中,L-亮氨酸作為動物營養(yǎng)有著特殊的作用,因此受到研究者的廣泛關(guān)注。隨著其應(yīng)用的不斷拓展,市場也在持續(xù)攀升[2]。
目前,發(fā)酵法生產(chǎn)L-亮氨酸的,日本企業(yè)占主導(dǎo)地位,尤以日本味之素公司,其在亮氨酸產(chǎn)量和品質(zhì)均具有明顯優(yōu)勢,大罐產(chǎn)酸能力達(dá)30~35 g/L,糖酸轉(zhuǎn)化率為22%~28%,可達(dá)70%以上的提取率,合計年產(chǎn)量400~500噸。迄今為止,工業(yè)化L-亮氨酸生產(chǎn)菌主要通過傳統(tǒng)誘變篩選獲得的,這種經(jīng)典育種方法雖可獲得L-亮氨酸相對高產(chǎn)的優(yōu)良菌株,但該法也會引入有害突變,使目標(biāo)菌株生長緩慢,雜酸增多。另外,這種方式工作量大,周期長,很難在短期內(nèi)進(jìn)一步提高目標(biāo)物產(chǎn)量。為了克服這些問題,理性化代謝工程育種正成為氨基酸高產(chǎn)菌株獲得的主要方式。
代謝工程是在對代謝網(wǎng)絡(luò)系統(tǒng)分析的基礎(chǔ)上,從合成生物學(xué)的視角出發(fā),采用基因工程技術(shù)修飾代謝途徑,定向改造細(xì)胞合成系統(tǒng)、轉(zhuǎn)運(yùn)系統(tǒng)和細(xì)胞調(diào)控系統(tǒng),以提高產(chǎn)物得率或改進(jìn)細(xì)胞性能的目的[2]。本研究以先期通過傳統(tǒng)復(fù)合誘變手段、結(jié)合結(jié)構(gòu)類似物的篩選方法獲得的一株具有L-甲硫氨酸及L-賴氨酸原養(yǎng)型,高濃度α-噻唑丙氨酸及α-氨基亮氨酸結(jié)構(gòu)類似物抗性的產(chǎn)L-亮氨酸菌株——谷氨酸棒桿菌MD106(CorynebacteriumglutamicumMD106)為出發(fā)菌株,利用谷氨酸棒桿菌模式菌株ATCC13032基因組序列為模板,采用自殺載體pk18mobsacB介導(dǎo)的基因重組手段,失活panBC基因以及alaT基因,減少L-亮氨酸合成前體物丙酮酸和α-酮基異戊酸消耗,增強(qiáng)L-亮氨酸代謝流,實現(xiàn)對L-亮氨酸合成途徑的優(yōu)化,為進(jìn)一步代謝工程優(yōu)化改造L-亮氨酸菌株獲得高產(chǎn)L-亮氨酸的工程菌奠定基礎(chǔ)。
1 材料和方法
1.1 材料
1.1.1 菌株和質(zhì)粒 谷氨酸棒桿菌MD106(CorynebacteriumglutamicumMD106)為本室選育并保存;載體克隆受體菌EscherichiacoliJM109購自TAKARA;自殺載體pk18mobsacB質(zhì)粒為中國科學(xué)院微生物研究所李寅研究員贈送。
1.1.2 主要工具酶和試劑 限制性內(nèi)切酶、DNA聚合酶、T4連接酶等均購自TAKARA;基因組提取試劑盒、PCR產(chǎn)物回收試劑盒、膠回收試劑盒等均購自上海生工。其他藥品均為國產(chǎn)分析純。
1.1.3 引物 根據(jù)Genbank的谷氨酸棒桿菌模式菌株ATCC13032基因組序列,分別設(shè)計panBC基因以及alaT基因的融合重疊延伸PCR引物。其中,劃線部分序列重疊延伸互補(bǔ)序列,方框中的序列分別為EcoRⅠ和SalⅠ酶切位點。
panBC基因的融合延伸引物設(shè)計如下:

panBC-2:5′- AACTACAGACCTAGAACCTAAGCATCAACAATGCGTCGAATC-3′
panBC-3:5′- TAGGTTCTAGGTCTGTAGTTGCTTATCGACGCCCTCCTCC-3′

alaT基因的融合延伸引物設(shè)計如下:

alaT-2:5′-AACTACAGACCTAGAACCTATTGAGGAGTGCTTGGGTGGTCATG-3′
alaT-3:5′-TAGGTTCTAGGTCTGTAGTTACTGGACCAAAGCAATACGCACGTGG-3′

1.1.4 培養(yǎng)基 LB培養(yǎng)基:配方參閱參考文獻(xiàn)[7];LB+10%蔗糖培養(yǎng)基:LB培養(yǎng)基的基礎(chǔ)上添加10%的蔗糖;LBG培養(yǎng)基:LB培養(yǎng)基添加0.5%的葡萄糖;菌株的種子及發(fā)酵培養(yǎng)基:企業(yè)內(nèi)部資料(略)。
1.2 方法
1.2.1panBC基因及alaT基因上下游片段的擴(kuò)增 采用細(xì)菌基因組提取試劑盒提取谷氨酸棒桿菌MD106,并以此為模板,采用panBC-1、panBC-2引物對與alaT-1、alaT-2引物對擴(kuò)增panBC和alaT基因的上游片段,panBC-3、panBC-4引物對與alaT-3、alaT-4引物對擴(kuò)增panBC基因的下游片段。
反應(yīng)體系為50 μL:ddH2O 33 μL,10×Ex buffer 5 μL,dNTP 5 μL,引物1、2(或3、4)各2 μL,MD106基因組1 μL,ExTaq酶2 μL,混合后進(jìn)行PCR擴(kuò)增。
PCR反應(yīng)程序:95℃預(yù)變性5 min;94℃變性40 s,55℃退火40 s,72℃延伸40 s,30個循環(huán);72℃最后延伸10 min。反應(yīng)結(jié)束后,膠回收試劑盒回收目的片段。
1.2.2 ΔpanBC基因與ΔalaT基因的融合擴(kuò)增及亞克隆 采用上述獲得的回收目的片段,分別以panBC和alaT的上下游片段通過融合PCR擴(kuò)增獲得截短的panBC基因(ΔpanBC)及截短的alaT基因(ΔalaT)。
PCR擴(kuò)增的反應(yīng)體系為50 μL:ddH2O 30 μL,10×Ex buffer 5 μL,dNTP 5 μL,引物1、4各2 μL,回收的上游片段及下游片段各2 μL,ExTaq酶2 μL,混合后進(jìn)行PCR擴(kuò)增。
PCR反應(yīng)程序:95℃預(yù)變性10 min;94℃變性40 s,55℃退火40 s,72℃延伸1 min,30個循環(huán);72℃最后延伸10 min。反應(yīng)結(jié)束后,膠回收試劑盒回收目的片段。
回收獲得的目的片段進(jìn)行T-A連接,并轉(zhuǎn)化感受態(tài)JM109細(xì)胞,菌落PCR篩選獲得陽性克隆,并送交上海生工進(jìn)行測序。
1.2.3 自殺敲除組件pk18ΔpanBC及pk18ΔalaT的構(gòu)建 將ΔpanBC與ΔalaT的陽性克隆質(zhì)粒與敲除載體pk18mobsacB同時用限制性內(nèi)切酶EcoRI、SalI進(jìn)行雙酶切。
雙酶切體系60 μL:ddH2O 33μL,ΔpanBC、ΔalaT、pk18mobsacB質(zhì)粒15 μL(約1 μg),10×H buffer 6 μL,EcoRI、SalI 各3 μL,37℃水浴過夜酶切。
雙酶切產(chǎn)物切膠回收后用于后續(xù)連接反應(yīng),連接反應(yīng)體系20 μL:ddH2O 3 μL,雙切回收ΔpanBC、ΔalaT片段12 μL,pk18mobsacB 2 μL,10×ligase buffer 2 μL,T4 DNA ligase 1 μL,16℃過夜連接。
連接反應(yīng)結(jié)束后轉(zhuǎn)化大腸桿菌JM109感受態(tài)細(xì)胞,37℃,120 r/min復(fù)蘇1 h,取300 μL涂布于含卡那霉素終濃度50 μg/mL的LB平板上,置于37℃恒溫培養(yǎng)箱中倒置培養(yǎng)約20 h。挑單菌落接種至含終濃度50 μg/mL卡那霉素的LB液體培養(yǎng)基中,37℃,250 r/min培養(yǎng)過夜,提質(zhì)粒篩選陽性克隆并進(jìn)行酶切鑒定。
1.2.4 谷氨酸棒桿菌MD106的panBC基因的失活 將獲得的pk18ΔpanBC重組載體電擊轉(zhuǎn)入谷氨酸棒桿菌MD106感受態(tài)細(xì)胞[采用艾本德(Eppendorf)電轉(zhuǎn)儀,電擊條件為:1800 V,電擊時間約為4~5 ms]。重組質(zhì)粒電擊轉(zhuǎn)入宿主之后,首先進(jìn)行第一次重組,即通過單交換的方式整體插入線性插入染色體中,此步可通過含25 μg/mL卡那霉素的LBG平板進(jìn)行篩選,平板上生長的克隆可視為成功進(jìn)行一次重組的克隆,對獲得的已經(jīng)進(jìn)行一次重組的單克隆進(jìn)行LB液體搖菌過夜,并劃線含10%蔗糖的LB平板,再分別點植LBG及LBG+卡那霉素(25 μg/mL)平板,進(jìn)行二次重組篩選,并對能夠再LBG平板生長,不能在LBG+卡那霉素(25 μg/mL)平板生長的克隆進(jìn)行PCR驗證,并進(jìn)行測序驗證染色體panBC基因是否被ΔpanBC替換。
1.2.5 谷氨酸棒桿菌MD106(ΔpanBC)的alaT基因的失活 在獲得的panBC失活菌株的基礎(chǔ)上,進(jìn)一步進(jìn)行染色體alaT基因的失活,將pk18ΔalaT重組載體電轉(zhuǎn)導(dǎo)入谷氨酸棒桿菌MD106(ΔpanBC),方法同pk18ΔpanBC的電轉(zhuǎn)及篩選操作。篩選陽性克隆進(jìn)行PCR驗證,并進(jìn)行測序驗證染色體alaT基因是否被ΔalaT替換。獲得谷氨酸棒桿菌MD106(ΔpanBC-ΔalaT)。
1.2.6 搖瓶發(fā)酵培養(yǎng) 將谷氨酸棒桿菌MD106(ΔpanBC/ΔalaT)與對照菌株谷氨酸棒桿菌MD106,進(jìn)行搖瓶的二級發(fā)酵:一級種子30℃,200 r/min培養(yǎng)18 h,15%移種量轉(zhuǎn)接發(fā)酵搖瓶,30℃,200 r/min發(fā)酵40 h,測定菌體密度及分析L-亮氨酸及雜酸類型和含量。
2 結(jié)果與分析
2.1 ΔpanBC基因及ΔalaT基因的融合擴(kuò)增及驗證
以谷氨酸棒桿菌MD106基因組為模板,分別進(jìn)行panBC基因及alaT基因上下游序列的擴(kuò)增(圖1-A),獲得基因片段大小與理論預(yù)測的基本一致。
以獲得的上下游片段互為模板,通過重疊延伸PCR的方法獲得中間缺失了427 bp基因序列的panBC基因(ΔpanBC基因)和中間缺失412 bp基因序列的alaT基因(ΔalaT基因),其大小與理論預(yù)測基本一致(圖1-B)。測序結(jié)果顯示:融合的ΔpanBC基因和ΔalaT基因與ATCC13032的相關(guān)序列幾乎完全一致,證明融合片段構(gòu)建成功。
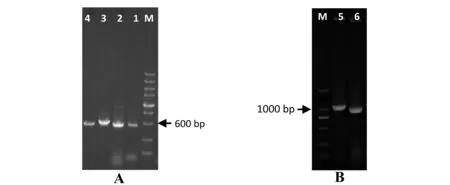
A:M為200bp leader marker,1、2為panBC基因的上下游片段,3、4為alaT基因的上下游片段B:M為DL2000 DNA leader marker,5為ΔpanBC基因融合片段,6為ΔalaT基因融合片段
圖1 ΔpanBC基因及ΔalaT基因的融合擴(kuò)增
2.2 自殺敲除組件pk18ΔpanBC及pk18ΔalaT的構(gòu)建
EcoRⅠ與SalⅠ雙切的ΔpanBC與ΔalaT片段與同樣的酶切并回收的載體pk18mobsacB線性片段連接產(chǎn)物轉(zhuǎn)化感受態(tài)JM109,并提取質(zhì)粒進(jìn)行酶切驗證(圖2)。結(jié)果顯示,自殺敲除組件pk18ΔpanBC及pk18ΔalaT的構(gòu)建成功。

M:λ-EcoT14 DNA leader marker;1:陰性對照(pk18mobsacB雙切);2:pk18ΔpanBC載體的雙切;3:pk18ΔalaT載體的雙切
圖2 pk18ΔpanBC及pk18ΔalaT重組載體的酶切驗證
2.3 重組載體轉(zhuǎn)化MD106及變株的篩選、驗證
自殺敲除組件pk18ΔpanBC及pk18ΔalaT轉(zhuǎn)化出發(fā)菌株谷氨酸棒桿菌MD106后,因載體含有KmR基因,在含25 μg/mL的卡那霉素培養(yǎng)基進(jìn)行初次篩選,獲得一次重組的菌株,一次重組的克隆不多,效率不高,總共不到10個克隆,這與pk18mobsacB載體本身特性有關(guān)。一次重組菌中的染色體中還含有sacB基因,利用蔗糖進(jìn)行反篩選,以蔗糖為基質(zhì)進(jìn)行再次篩選,過濾掉一次抗性平板篩選過程中存在的游離載體,選擇性進(jìn)行保留二次重組的菌株。根據(jù)pk18mobsacB重組特性,在進(jìn)行二次重組的過程中,可能出現(xiàn)回復(fù)變株,其概率在50%左右,所以需要對二次重組的克隆需要進(jìn)行進(jìn)一步的PCR驗證,以菌落為模板,分別以panBC-1、panBC-4引物對和alaT-1、alaT-4引物對為引物,進(jìn)行PCR篩選和驗證,結(jié)果見圖3。結(jié)果顯示,陽性克隆的PCR產(chǎn)物較對照(以原始MD106基因組為模板)明顯要小,而且對截短的PCR產(chǎn)物進(jìn)行測序分析,確認(rèn)基因panBC及alaT基因分別被ΔpanBC和ΔalaT基因替換。

M:200 bp DNA leader marker,1:ΔpanBC基因替換驗證,2:陰性對照(MD106菌落PCR驗證),3:MD106(ΔpanBC)菌株P(guān)CR驗證,4:panBC缺失基礎(chǔ)上的ΔalaT基因替換驗證
圖3panBC及alaT基因缺失菌株的菌落PCR驗證
2.4 panBC、alaT基因失活對MD106發(fā)酵產(chǎn)L-亮氨酸的影響
以初步優(yōu)化的培養(yǎng)基,采用搖瓶二級發(fā)酵的方式,對panBC、alaT基因失活菌株及原始MD106菌株進(jìn)行發(fā)酵實驗,考察雙基因缺失對菌株生長、L-亮氨酸產(chǎn)率以及雜酸合成的影響。結(jié)果(表1)顯示:(1)panBC、alaT雙基因失活的重組菌株的生物量較對照菌株差別不大,說明在現(xiàn)有培養(yǎng)基的情形下,雙基因的缺失基本不會對菌體生長造成較為明顯的影響。(2)panBC、alaT雙基因的失活有利于增強(qiáng)L-亮氨酸的代謝流,提高L-亮氨酸產(chǎn)酸率。(3)alaT基因的失活,大大減少了MD106菌株的丙氨酸合成能力,其丙氨酸的合成量減少超過80%。(4)panBC、alaT雙基因失活菌株,其發(fā)酵總雜酸明顯較對照菌株要低,而且幅度不僅僅只局限于丙氨酸的減少上,說明雙基因的缺失對于L-亮氨酸的生物合成帶來影響的同時,也對其他氨基酸的合成帶來了調(diào)控,而且這種調(diào)控對于積累L-亮氨酸合成來說是有益的。

表1 panBC、alaT雙基因缺失菌株與對照菌株的部分發(fā)酵指數(shù)
3 討論
丙酮酸是合成三支鏈氨基酸的共同前體物,α-酮基異戊酸既是L-纈氨酸的直接前體物,又是合成L-亮氨酸的間接前體物。因此,在進(jìn)行L-亮氨酸代謝工程改造時,應(yīng)在增加丙酮酸合成代謝流的同時,使丙酮酸的代謝流盡可能的流向α-酮基異戊酸,另外,在分支途徑中還應(yīng)使α-酮基異戊酸主要流向L-亮氨酸。
丙酮酸的支路代謝主要包含:通過轉(zhuǎn)氨合成丙氨酸,這一路經(jīng)很容易實現(xiàn),而且對丙酮酸的消耗巨大,催化合成這一過程主要包括兩個轉(zhuǎn)氨酶,即AvtA(avtA基因編碼)和AlaT(alaT基因編碼),其中AlaT對丙氨酸的合成貢獻(xiàn)更大,有研究[8]表明,失活A(yù)laT之后,細(xì)胞的丙氨酸的合成大大降低,而且由于AvtA的氨基供體為L-纈氨酸,所以,通過失活alaT基因,不僅大量減少丙氨酸合成,減少丙酮酸的消耗,且還相對能促進(jìn)L-纈氨酸的消耗,并提供L-亮氨酸合成的間接前體物α-酮基異戊酸的量,這一點在本研究當(dāng)中也得到驗證,失活alaT基因之后丙氨酸的量降低超過80%,且雜酸比例也大大降低。
D-泛酸的合成以α-酮基異戊酸為直接前體,經(jīng)羥基酮泛酸甲基轉(zhuǎn)移酶(panB基因編碼)和泛酸合成酶(panC基因編碼)等催化,最終合成泛酸。通過失活泛酸合成的相關(guān)酶系,增加L-亮氨酸合成前體物,增強(qiáng)L-亮氨酸代謝流[9]。
本研究在傳統(tǒng)方法選育獲得一定遺傳標(biāo)記的產(chǎn)L-亮氨酸菌株MD106的基礎(chǔ)上,采用代謝工程手段L-亮氨酸的前體物丙酮酸及α-酮基異戊酸的消耗路徑進(jìn)行了修飾,使得L-亮氨酸的產(chǎn)率明顯提高,而且雜酸比例大大減少,為下一步的菌種構(gòu)建提供了保障,證明代謝工程的技術(shù)路線完全適應(yīng)于L-亮氨酸的菌種改造,為進(jìn)一步構(gòu)建高產(chǎn)L-亮氨酸工程菌打下了基礎(chǔ)。
參考文獻(xiàn):
[1] LEE J W, NA D, PARK J M, et al. Systems metabolic engineering of microorganisms for natural and non-natural chemicals[J]. Nat. Chem. Biol, 2012(8): 536-546.
[2] HAN M W, J B PARK. Recent progress in development of synthetic biology platforms andmetabolic engineering of Corynebacterium glutamicum[J]. Journal of Biotechnology, 2014(180):43-51.
[3] BECKER J, WITTMANN C. Bio-based production of chemicals, materials and fuels-Corynebacterium glutamicum as versatile cell factory[J]. Curr. Opin. Biotechnol, 2012(23):631-640.
[6] SATOSHI H, MASAKO S, KIMIO U, et al. Engineering ofCorynebacteriumglutamicumfor High Yield L-Valine Production under Oxygen Deprivation Conditions[J]. Appl. Environ. Microbiol, 2013, 79(4):1250-1257.
[7] 薩姆布魯克J,拉塞爾D W.分子克隆實驗指南:第三版[M].北京:科學(xué)出版社,2002.
[8] JAN M, LOTHAR E. Metabolic Function of Corynebacterium glutamicum Aminotransferases AlaT and AvtA and Impact on L-Valine Production[J]. Appl. Environ. Microbiol, 2008, 74(24): 7457-7462.
[9] HERMANN S, LOTHAR E. d-Pantothenate Synthesis inCorynebacteriumglutamicumand Use ofpanBCand Genes Encoding L-Valine Synthesis for d-Pantothenate Overproduction[J]. Appl. Environ. Microbiol, 1999, 65(5):1973-1979.
- 臺灣農(nóng)業(yè)探索的其它文章
- 新時期福建省農(nóng)產(chǎn)品供給能力評價與分析
- 日本農(nóng)業(yè)女性參與農(nóng)業(yè)及農(nóng)村發(fā)展的現(xiàn)狀與分析
- 江西省農(nóng)村金融發(fā)展對城鄉(xiāng)收入差距影響的實證研究
- 我國水產(chǎn)養(yǎng)殖業(yè)環(huán)境成本信息披露的現(xiàn)狀與對策
- 新型農(nóng)村金融機(jī)構(gòu)的市場定位研究
——以福建省為例 - GPON網(wǎng)絡(luò)在設(shè)施農(nóng)業(yè)上的應(yīng)用
——以福建省農(nóng)業(yè)科學(xué)院漁溪現(xiàn)代循環(huán)農(nóng)業(yè)科技示范園為例

