經皮左心室重建術治療前壁心肌梗死后室壁瘤合并心功能不全一例
丁風華,方躍華,楊文潔,楊震坤,張建盛,張奇,胡健,張瑞巖,沈衛峰
·病例報告Case report·
經皮左心室重建術治療前壁心肌梗死后室壁瘤合并心功能不全一例
丁風華,方躍華,楊文潔,楊震坤,張建盛,張奇,胡健,張瑞巖,沈衛峰
經皮左心室重建術;室壁瘤;心功能不全
心力衰竭是心血管疾病死亡的主要原因之一[1]。其原因主要為發生心肌梗死,20%~50%患者會在隨后的數年內發展為心力衰竭[2]。研究表明,前壁心肌梗死患者更容易發展為心力衰竭。由于前壁梗死面積相對較大、曲面形態和心尖部心肌相對薄弱,因此重構發生更加明顯,病程進展更快。雖然,常用的血管緊張素轉換酶抑制劑、血管緊張素受體拮抗劑和β受體阻斷劑均用于心肌梗死的二級預防和抑制左室重構,但仍有部分患者最終出現室壁瘤甚至心力衰竭[3-4]。外科手術是室壁瘤重要的治療方法,術式包括室壁瘤線性切除修補術和成形術等,但臨床效果不盡如人意[5]。
近年來,國內外病例報道和小樣本研究表明,通過介入治療方法置入一種在鎳鈦合金材料制成附有聚四氟乙烯薄膜的傘狀左室隔絕裝置(ventricular partitioning device,VPD)可作為心力衰竭的另一種非藥物微創治療選擇,具有較好的安全性和可行性[6-9]。然而,左心室形態的全面評估和隔絕裝置尺寸的選擇是手術成敗的關鍵。以往選擇的左室隔絕裝置直徑為75 mm和85 mm兩種。我中心為1例急性前壁心肌梗死后巨大室壁瘤形成伴有心力衰竭患者施行經皮穿刺左心室重建術(percutaneous ventricular restoration,PVR),而植入左室隔絕裝置直徑達95 mm,手術獲得圓滿成功,現報道如下。
1 臨床資料
患者男,64歲,身高170 cm,體質量93 kg。7個月前反復出現心前區壓榨樣疼痛,偶伴有冷汗,發作時間長短不等,當時未及時就診。5個月前,患者仍時有胸悶發作,且出現活動后氣促癥狀,運動耐量明顯下降,就診檢查心電圖顯示V1~5 ST段弓背型抬高(無動態演變),心臟超聲檢查顯示左心室擴大伴室壁瘤形成、左心功能不全。初步診斷冠心病,陳舊性前壁心肌梗死伴室壁瘤形成,慢性心力衰竭C期,紐約心臟病協會(NYHA)心功能分級Ⅲ級。為進一步診治,隨后行冠脈造影,顯示左前降支90%狹窄,于病變處置入依維莫司藥物涂層支架2枚(Xience V 2.25×28mm,Xicence V 3.5× 23mm),術后繼續口服阿司匹林、氯吡格雷雙聯抗血小板聚集,培哚普利、美托洛爾和阿托伐他汀等藥物心血管二級預防治療。支架植入后,患者主訴胸悶癥狀顯著改善,活動后氣促癥狀略好轉,復查心臟超聲顯示心臟大小未明顯改變,左室射血分數低下(表1)。且仍有活動后氣促癥狀。
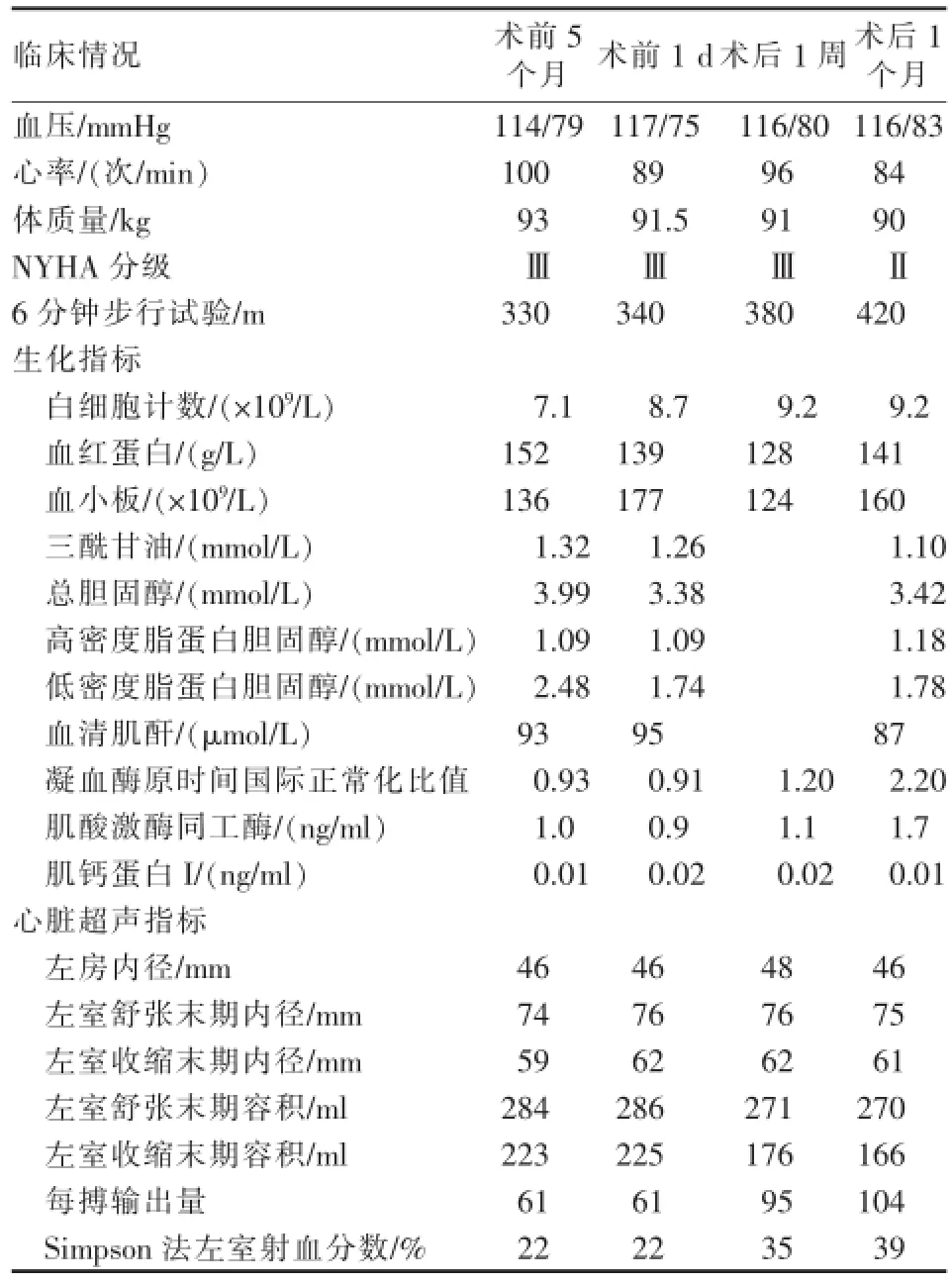
表1 患者經皮左室重建術前、術后各項臨床、生物化學和心超指標變化
2 經皮左室重建術
2.1 術前評估
患者靜息血壓115/75 mmHg(1 mmhg=0.133 kPa),心率90次/min,NYHA心功能分級為羅馬數級,6分鐘步行試驗距離330 m。患者術前再次評估心超顯示,冠脈介入治療后5個月,心臟各項超聲指標與冠脈介入治療前無明顯改善(表1)。
2.2 手術過程
患者取平臥位,在雙側腹股溝區域2%利多卡因局部麻醉。Seldinger法成功穿刺雙側股動脈后,左側置入6 F股動脈鞘管(Glidesheath,泰尓茂公司,日本),右側置入16 F動脈鞘(Ultimum,圣尤達公司,美國)。6 F豬尾導管從左側股動脈鞘管內送入,沿主動脈上行,通過主動脈瓣送至左心室室壁瘤內。根據術前左心室CT造影顯示的室壁瘤的位置,選擇最佳體位(右前斜31°)進行左心室造影充分暴露心尖、瘤體和瘤頸的位置。以相同方法從右側股動脈送入另一6 F豬尾導管進入左心室,交換Amplatz 0.035英寸260mm超硬導絲,沿超硬導絲送入16 F輸送鞘和預先折疊收入鞘內的95mm PARACHUTE左心室隔絕傘(CardioKinetix公司,美國)到達心尖部,造影和床旁心臟超聲確認位置,逐步回撤輸送鞘釋放隔絕傘。隨后膨脹預置于隔絕傘內球囊,使傘面撐開,球形錨固定于心肌內。最后解旋釋放隔絕傘,造影顯示室壁瘤被完全隔絕,隔絕裝置位置良好(圖1)。手術順利,手術時間70m in,X線曝光時間15 min,對比劑用量120m l。
2.3 術后隨訪
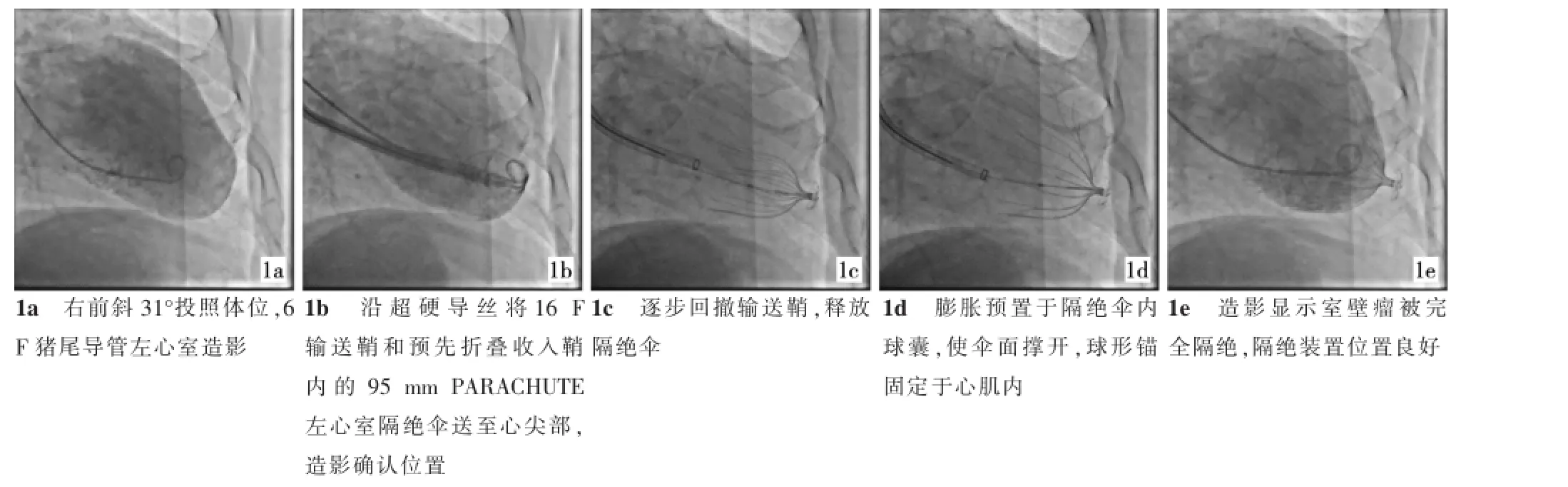
圖1 左室隔絕裝置(VPD)放置前后圖像
術后患者無并發癥發生,心肌標志物和血清肌酐與術前相比無變化。12 h后,患者可自行下床活動。術后給予阿司匹林(100mg/d),氯吡格雷(75mg/d)雙聯抗血小板聚集和口服華法林抗凝治療(調整INR于2.0~3.0)。術后1周,患者自覺運動耐量明顯上升,6分鐘步行試驗距離提升至380m,心臟超聲顯示左室射血分數由22%上升至35%(表1)。1個月后,患者登3層樓無明顯氣促,6分鐘步行試驗距離420m,左室射血分數39%。
3 討論
本研究成功地完成了國內首例巨大室壁瘤左心室重建術,手術順利,圍手術期無并發癥,術后患者運動耐量和左心功能得到顯著改善。
缺血性心肌病導致的心力衰竭可通過冠脈血運重建,改善心肌供血,從而改善心功能。然而,對于心肌梗死后心功能不全或室壁瘤患者,血運重建不能提升心臟功能,因此對提高患者運動耐量和改善患者預后效果不佳。目前常用的冠心病的二級預防治療手段尚不能有效抑制疾病的加重。通過外科手術切除壞死心肌,對左心室進行解剖重建,可能使部分患者臨床獲益[5]。然而,患者的嚴格篩選和對外科手術水平的依賴,是重建術能否使患者獲益的關鍵。
近年來研究初步證實,PVR可治療心功能不全或心肌梗死后室壁瘤形成患者,術后心功能普遍改善,生活質量明顯提高[6-9]。其治療原理是通過左室隔絕裝置將室壁瘤隔絕:①避免瘤體繼續擴大而使心功能進一步惡化;②使瘤腔內無效血容量被重新分配、利用,增加左心輸出量,從而改善心功能和運動耐量。目前,PVR主要適應證為:①年齡≥18歲;②陳舊前壁心肌梗死合并前壁無運動或反常運動;③左室射血分數<40%伴左心室擴大;④NYHA心功能分級Ⅱ級以上。主要排除標準:①3個月內急性心肌梗死;②心肌缺血需要血運重建;③30 d內血運重建史;④明顯的瓣膜疾病;⑤左心室血栓[8]。目前,經皮左室重建術還不能用于左心室結構復雜患者,因此術前心臟超聲和左心室CT造影尤為重要。如果CT檢查發現乳頭肌及腱索靠近左心室心尖部則不適合該手術;擴張型心肌病左室整體擴張伴室壁變薄也不適合該手術;由于器械規格限制,目前左室隔絕裝置僅有65 cm、75 cm、85 cm和95 cm 4種規格,因此乳頭肌水平左室舒張末期內徑超過7 cm或小于4 cm也不適合。對于左心室射血分數小于15%,或年齡大于80歲的患者應整體評估手術風險后實施手術。
PVR的主要并發癥包括:術中術后并發室性心律失常甚至心跳驟停、圍手術期和術后出血并發癥、圍手術期心肌梗死、心臟穿孔和心臟壓塞、裝置栓塞/移位/斷裂可能需要緊急心外科手術、心內膜炎、裝置侵蝕穿透左心室、顯著裝置周圍泄漏、外周血管栓塞/血栓/肺栓塞、對比劑腎病、腦卒中或短暫性缺血性發作和瓣膜損傷(二尖瓣關閉不全惡化或主動脈瓣損傷)。術中操作注意事項:①維持ACT≥250 s;②在預置PARACHUTE時需充分排氣,以免術中發生氣體栓塞;③隔絕裝置后,避免在任一方向旋轉導引導管超過180°,以免隔絕傘過度折疊;④在有瓣膜狹窄或存在機械主動脈瓣膜假體的情況下穿過主動脈瓣時要小心操作,避免損傷;⑤在釋放隔絕傘之前,不能過度旋轉導管,也不能旋轉PARACHUTE分離旋鈕;⑥球囊擴張隔絕傘時,推薦注入對比劑或0.9%氯化鈉溶液,預混液不能超過20m l。
總之,針對心肌梗死后室壁瘤合并心功能不全,經皮左心室重建術是繼外科手術以后較為安全和有效的治療手段,由于其具有創傷小、費用低、手術并發癥少、術后恢復快等優點,更易于被患者接受,因而有望成為室壁瘤患者的主要治療手段。然而,其臨床有效性還有待于更大規模的臨床研究來證實。
[1]中國心力衰竭診斷和治療指南2014[J].中華心血管病雜志,2014,42:98-122.
[2]Roger VL,Go AS,Lloyd-Jones DM,et al.Heart disease and stroke statistics—2011 update:a report from the American Heart Association[J].Circulation,2011,123:e18-e209.
[3]Flather MD,Yusuf S,Kober L,et al.Long-term ACE-inhibitor therapy in patients with heart failure or left-ventricular dysfunction:a systematic overview of data from individual patients[J].Lancet,2000,355:1575-1581.
[4]Brophy JM,Joseph L,Rouleau JL.Beta-blockers in congestive heart failure[J].Ann Intern Med,2001,134:550-560.
[5]Athanasuleas CL,Buckberg GD,Stanley AW,et al.Surgical ventricular restoration:the RESTORE Group experience[J].Heart Fail Rev,2004,9:287-297.
[6]馬為,洪濤,李建平,等.經皮心室重建術——附兩例病例報告[J].中國介入心臟病學雜志,2013,21:274-276.
[7]Skowasch M,Robertson GC,Wunderlich N,etal.Percutaneous ventricular restoration in a chronic heart failure patient[J].EuroIntervention,2006,2:128-131.
[8]Sagic D,Otasevic P,Sievert H,etal.Percutaneous implantation of the left ventricular partitioning device for chronic heart failure:a pilot study with 1-year follow-up[J].Eur JHeart Fail,2010,12:600-606.
[9]Bozdag-Turan I,Bermaoui B,Paranskaya LA,et al.Challenges in patient selection for the parachute device implantation[J].Catheter Cardiovasc Interv,2013,82:E718-725.
Percutaneous left ventricular restoration for ventricular aneurysm associated w ith cardiac insufficiency follow ing anterior myocardial infarction:report of one case
DING Feng-hua,FANG Yue-hua,YANGWen-jie,YANG Zhen-kun,ZHANG Jian-shen,ZHANG Qi,HU Jian,ZHANG Rui-yan,SHEN Wei-feng.Department of Cardiology,Affiliated Ruijin Hospital,School of Medicine,Shanghai Jiaotong University,Shanghai200025,China(JIntervent Radiol,2014,23:886-888)
ZHANGRui-yan,E-mail:zhangruiyan@263.net
percutaneous ventricular restoration;ventricular aneurysm;cardiac insufficiency
R541.1
D
1008-794X(2014)-10-0886-03
2014-07-23)
(本文編輯:李欣)
10.3969/j.issn.1008-794X.2014.10.012
200025上海交通大學醫學院附屬瑞金醫院心內科(丁風華、方躍華、楊震坤、張建盛、張奇、胡健、張瑞巖、沈衛峰),放射科(楊文潔)
張瑞巖E-mail:zhangruiyan@263.net

