陜西省實施2012年版《藥品經營質量管理規范》存在的問題及對策
(陜西省食品藥品監督管理局藥品認證中心,陜西 西安 710065)
2012年版《藥品經營質量管理規范》(GSP)于2013年6月1日起正式施行。與2000年版GSP相比,新版GSP全面提升了企業經營的軟硬件標準和要求。在軟件方面,GSP明確要求企業建立質量管理體系,并對質量管理制度、崗位職責、操作規程、記錄、憑證等一系列質量管理體系文件提出詳細要求,強調了文件的執行和實效;提高了相關人員特別是質量管理人員的資質要求。在硬件方面,GSP全面推行計算機信息化管理,著重規定計算機管理的設施、網絡環境、數據庫及應用軟件功能要求;明確規定企業應對藥品倉庫采用溫濕度自動監測系統,對倉儲環境實施持續、有效的實時監測;對儲存、運輸冷藏、冷凍藥品要求配備特定的設施設備[1]。筆者結合GSP對藥品批發企業軟硬件建設等方面要求的變化和陜西省實施GSP工作中存在的問題,以發放調查問卷和現場調研的方式,對藥品批發企業的現狀及實施GSP存在的突出問題進行了調研,并提出相關對策。
1 基本情況
截至2013年6月,我省現有藥品批發企業549家,零售連鎖56家,藥品零售企業8877余家(含藥品零售連鎖門店)。按經營規模分類,詳見表1。按經營范圍等分類,含二類精神藥品93家(16.94%),含生物制品256家(46.63%),疫苗專營19家(3.46%),體外診斷試劑81家(14.75%),基層藥品配送16家(2.91%),縣級醫療機構配送54家(9.84%)。調研工作中,共發放調查問卷350份,收回295份(84.29%),其中276份(93.56%)以傳真形式反饋,19份(6.44%)為現場調研收回。問卷發放范圍覆蓋省、市、縣各級各類藥品批發企業。
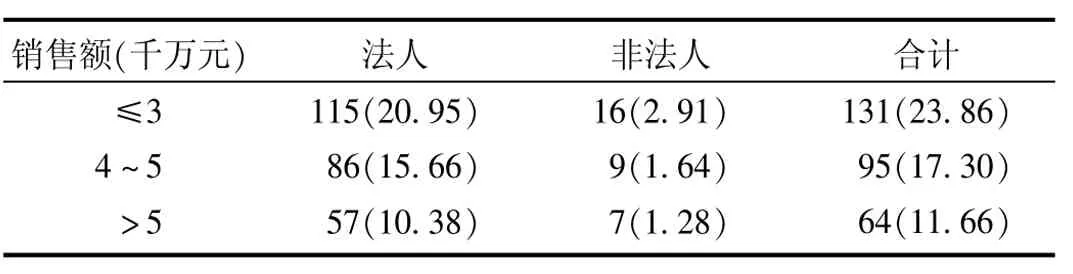
表1 陜西省藥品批發企業按經營規模分類情況表[家(%)]
2 企業實施新版GSP存在的問題
2.1 執業藥師配備
從調查情況看,企業反映最集中的是執業藥師配備問題。目前,我省共有549家藥品批發企業,8877家藥品零售企業。GSP要求每家批發企業需配備2名執業藥師,零售藥店至少配備1名執業藥師[2],全省藥品經營企業共需近萬名執業藥師。截至2013年10月,我省共4446人取得執業藥師資格,在我省注冊的僅2023人,與GSP執業藥師配備的要求有較大差距,這將導致陜西省近半數藥品批發企業、4/5的藥品零售企業因執業藥師配備問題不能通過GSP認證,詳見表2。
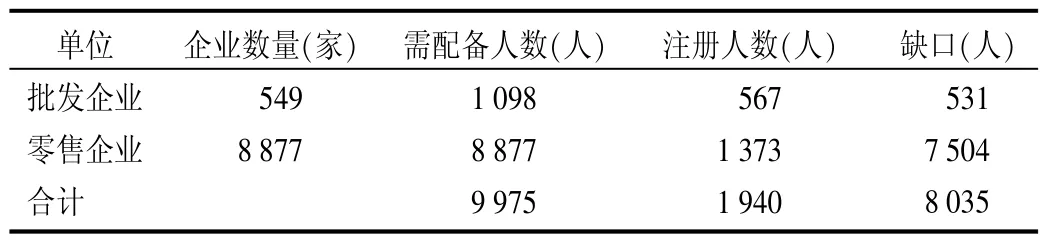
表2 陜西省藥品經營企業執業藥師缺口分析
2.2 庫房改造及相關設施設備配備
由調研情況可見,企業反映最突出的問題是改造時間和資金。2013年6月至2014年初,我省有近100家藥品批發企業需重新取得GSP認證證書,要在半年多時間內完成庫房改造及設施設備的配備,時間非常緊迫。
GSP要求企業庫房配備溫濕度調節系統、24 h溫濕度自動監測和記錄系統。目前,我省僅有7家企業在新址自建庫房(磚混結構),其他企業庫房均為租賃,80%以上企業庫房為彩鋼結構,保溫效果不好,由于庫房本身結構和條件限制,要在溫度最高的7~10月使庫房內溫濕度達到藥品儲存要求,有一定難度。除部分自建庫房的企業使用中央空調外,多數企業都使用大功率普通空調,增大了溫濕度調控的運行成本,但調控溫濕度的效果并不佳。
企業對庫房改造的不積極還有其他3個方面的原因:一是溫濕度自動監測系統在醫藥流通行業尚未普遍采用,無經驗可借鑒,缺乏改造樣板;二是GSP實施細則遲遲未出臺,企業擔心附錄出臺后對相關設施設備有更具體的要求,加之近年來城市改造速度加快,企業租賃的庫房隨時可能被拆遷,造成重復建設;三是我省藥品經營企業普遍規模不大,缺乏GSP改造的能力、動力和實力。
2.3 計算機系統
計算機系統是GSP新增的內容。目前,我省藥品批發企業已全部配備了計算機系統,但與GSP的要求還有較大差距。企業所建立的計算機系統普遍以日常業務管理和財務管理為主,質量控制在計算機系統應用中所占比例很小。這就導致企業計算機系統的升級費用大,少則十幾萬,多則上百萬。而且,計算機系統的升級不可能一氣呵成,需要軟件開發商結合藥品經營過程中的質量管理狀況、企業的質量管理文件不斷加以改進。升級完成后的計算機系統除GSP要求的功能外,還要與原系統、冷鏈藥品的管理、庫房溫濕度自動監測系統、實施電子監管藥品的管理等對接,以上這些都需要時間和資金的支撐。
2.4 設備驗證
設備驗證也是GSP新增的內容。驗證的目的是確認相關設施設備及系統能符合規定的設計標準和要求,可安全、有效地正常運行和使用,確保藥品在儲存、運輸過程的質量。驗證對象主要包括冷庫、冷藏運輸車輛、冷藏箱、保溫箱和冷藏儲運溫濕度監測系統。驗證類型主要有使用前驗證、定期驗證和停用時間超過規定時限的驗證。
由調研情況可見,我省涉及驗證工作的藥品批發企業全都選擇了委托驗證這條捷徑,但這會導致企業相關人員無法真正融入到相關設施設備的驗證工作中,使企業的驗證工作與整個質量管理體系脫節。造成企業將驗證工作委托的原因有3個方面:一是企業相關人員沒有接觸過驗證工作,對新增的驗證內容非常陌生,對驗證方法及驗證要求無從下手,對驗證數據不知道如何處理和應用;二是企業缺少驗證需要的相關設備;三是委托驗證省時省力,同時設備供應商為銷售設備,驗證費用相對便宜。
2.5 收貨與驗收環節
收貨是GSP為核實藥品購銷渠道新增的環節。我省藥品批發企業反映較集中的問題是增加了工作環節,就要增加相應的工作崗位,而收貨環節又是一個動態過程。藥品到貨時,收貨員要對照采購記錄、隨貨同行單和藥品實物逐一進行核實,這就要用到可移動電腦,在計算機系統軟件功能支持的前提下通過無線網絡來完成。企業目前配備的計算機系統、軟件功能和硬件設施,不能完全適應動態收貨的過程。
另外,驗收環節還增加了“查驗同批號藥品檢驗報告書”的要求。上游客戶藥品檢驗報告書的存檔和管理、下游客戶檢驗報告書的復印,都需要耗費大量的人力、物力和財力。雖然GSP允許企業可以電子數據的形式傳遞和保存檢驗報告書,但目前的計算機系統和軟件功能尚不能保證其合法性和有效性。
在企業實際收貨核查隨貨同行單的工作環節中,個別企業還存在先入庫、后完成收貨和驗收工作環節的現象,隨貨同行單還存在內容不全、未加蓋出庫專用章原印章、內容與實物不符、有手寫或涂改的現象。
2.6 冷鏈藥品的質量管理
我省藥品批發企業經營范圍含“生物制品”的企業共256家,疫苗專營企業19家,近半數藥品經營企業涉及冷鏈藥品的質量管理。目前,我省藥品批發企業對冷鏈藥品的儲存環境已基本達到GSP的硬件要求,都配備了冷庫和雙回路電源(或發電機組),冷庫具備外部顯示溫度功能和聲、光報警功能,但冷鏈藥品運輸過程中的溫度管理還有較大差距。我省冷鏈藥品在購銷環節的普遍現象是頻次多、批量少,而運輸冷鏈藥品的工具主要有冷藏車、保溫箱和冷藏箱,這就導致冷藏車運輸冷鏈藥品的成本加大,保溫箱、冷藏箱的流轉不能滿足冷鏈藥品的業務需求。個別企業甚至用普通泡沫箱代替保溫箱,用冰凍礦泉水代替專業蓄冷劑運輸冷鏈藥品。多數企業只在出貨和進貨等環節對冷鏈藥品的溫度進行人工確認,而對運輸過程中的溫度變化不能實時監控和數據采集,溫度數據不連續。
3 藥品監管部門實施GSP存在的問題
3.1 檢查員培訓
GSP正式施行后,陜西省食品藥品監督管理局通過嚴格的考試選拔出374名新版GSP檢查員,但就新版GSP與2000年版GSP對經營企業軟、硬件要求變化而言,新版GSP檢查員對現場檢查中諸如計算機系統、冷藏冷凍藥品的管理及設施設備的驗證等相關檢查內容的把握方面還有所欠缺。
3.2 企業申報GSP時限集中,實施GSP時間緊、任務重
根據陜西省食品藥品監督管理局《關于印發新修訂藥品經營質量管理規范實施方案的通知》精神,2013年6月1日后《藥品經營企業許可證》或《GSP認證證書》任何一證到期的,均以新修訂藥品GSP為標準組織驗收,但2013年12月31日前證書到期不能及時完成改造的,可以申請延期至2014年6月30日。到2014年12月31日為止,我省將有261家藥品批發企業《GSP認證證書》到期,還有2013年6月1日后《GSP認證證書》到期申請延期的40多家藥品批發企業,2014年全年將有300家以上藥品批發企業申報GSP認證,平均每天完成1家企業的GSP認證工作,時間緊,任務重。
4 對策及建議
4.1 加強針對性培訓和政策鼓勵,充分發揮職能部門作用
應充分發揮相關部門職能作用,加強執業藥師的宣傳和培訓:近年來,我省執業藥師考試通過率一直維持在10%左右,低于全國平均水平。《國家藥品安全“十二五”規劃》和GSP提高了執業藥師在藥品經營環節中的要求,陜西省食品藥品監督管理局信息培訓中心可充分發揮職能作用,將執業藥師考前培訓列入日常培訓,邀請相關專家針對執業藥師考試編制教材,提高培訓質量和效果。各級執業藥師管理部門要對通過考試的執業藥師注冊加強管理,防止認證“槍手”的出現。
出臺相關政策,鼓勵企業向集約化發展:陜西省食品藥品監督管理局可結合我省執業藥師數量的實際情況,制訂相關政策解決執業藥師不足的問題。如鼓勵發展連鎖企業,引導有規模、有實力的藥品零售企業發展連鎖經營,實行標準化統一配送,提高藥品零售連鎖企業的市場占有率;允許連鎖總部設立執業藥師中心,按門店比例配備一定數量的執業藥師,通過現代信息技術實現對處方的遠程實時審核。
4.2 整合資源,聯合發展
政府倡導,解決企業庫房改造中的困難:應充分發揮政府職能部門的作用,倡導企業在倉庫改造、建造的過程中向規模化、標準化、集中化發展。如西安市食品藥品監督管理局已組織部分藥品批發企業與戶縣相關部門進行協商,集中建立藥品倉庫,雖然一次性投入較大,但日常的運行成本、管理費用將大大降低,也有利于食品藥品監管部門的日常監管。
加強政策宣傳,支持企業聯合重組:降低成本、提高效益是企業發展的目標。只有實現規模經營,才會帶來規模效益。醫藥物流合理化將作為“第三利潤”的源泉得到進一步開發,這也是醫藥流通領域企業發展的基本趨勢。對基礎設施條件過硬、資金充裕、專業人才齊備和市場占有份額較高的藥品流通企業來說,實施新版GSP是其重新布局、占領市場的機遇。但對確屬無力進行新版GSP認證改造的的企業,省局可以搭建平臺,推動藥品經營資源整合,鼓勵具有藥品現代物流條件的藥品批發企業通過兼并、重組、聯合發展,促進規范化、規模化,逐步形成以區域核心批發企業為物流配送中心的醫藥商品流通主渠道;批準有實力的企業從事醫藥物流,允許其接受委托進行藥品的儲存、配送服務業務,減少企業重復建設,提高社會資源利用率。
4.3 發揮行業協會作用,體現“團購”效應
我省藥品批發企業的計算機系統升級改造成本千差萬別,少則十幾萬,多則上百萬。企業的目標是既滿足GSP對計算機系統的要求,又要把改造成本降到最低。相關協會可發揮行業作用,組織企業對軟件開發商統一進行遴選,在滿足GSP要求的基礎上,各公司結合自身實際,對軟件系統做適當調整,節約開發升級成本,體現“團購”效應。
4.4 加強驗證培訓,使其融入企業質量管理工作
驗證管理為全新引入的理念,也是藥品流通質量管理標準接近國際規范的要求,但企業對驗證管理感覺無從下手。要解決驗證管理與整個GSP管理體系脫節的問題,可采取以下措施:一是加強對企業相關人員的專題培訓,必要時進行現場驗證觀摩;二是要鼓勵有實力的企業、單位配備相關驗證設施設備,并允許其從事相關設備租賃活動;三是部分企業聯合購買相關驗證設備,共同完成各企業的驗證工作,并在驗證過程中取長補短,共同提高;四是逐步限制冷藏冷凍設施設備的委托驗證。
4.5 加強冷鏈藥品監管,提升冷鏈藥品儲運集中度
冷藏、冷凍藥品儲存、運輸環節的溫度控制是冷鏈藥品質量管理核心。針對目前冷藏、冷凍藥品在儲運環節中存在的斷鏈現象、冷鏈設施不足等問題,一是要加強對冷藏、冷凍藥品的監管,增加監管措施,如增加對經營冷藏、冷凍藥品經營企業的檢查力度和頻率,通過GPS定位等現代化手段對冷藏、冷凍藥品在儲運環節的實時跟蹤;二是要提升冷藏、冷凍藥品經營的集中度。鼓勵有實力的企業增加冷藏、冷凍藥品的儲運設施設備,政策上允許他們接受委托冷藏、冷凍藥品的儲存與配送,提升冷鏈藥品的儲運集中度。
4.6 加強檢查員培訓,提高其業務水平
GSP檢查員是實施藥品GSP認證的關鍵環節。新版GSP實施以來,我省僅對GSP檢查員進行了1次新版GSP規范的培訓,檢查員對新版GSP現場檢查的經驗相對欠缺。通過分梯次對檢查員進行新版GSP現場檢查專題培訓、現場觀摩研討、赴已開展新版GSP認證工作的省份學習等多種方式,提高GSP檢查員的業務能力,可充分做好開展GSP認證工作的準備。
4.7 出臺相關鼓勵政策,解決企業集中申報問題
目前,我省大多藥品批發企業對實施新版GSP認證持觀望態度,都期待借鑒通過新版GSP認證企業的經驗,吸取教訓。這就造成企業在規定認證期限將至時集中申報,造成GSP認證工作的被動。建議陜西省食品藥品監督管理局加快我省GSP認證相關文件修訂,并出臺相關鼓勵政策,消除企業“害怕通不過認證”的顧慮。如對前期申報認證的企業,檢查組現場檢查只找問題、不下結論,對企業存在缺陷完全整改完成后進行復查,做到零缺陷通過認證。只有讓企業通過認證有盼頭,通過認證嘗到甜頭,才能有效避免發生“井噴式”報送和“泄洪式”認證的壓力,同時也可為檢查員積累檢查經驗,為2014年GSP認證工作的順利開展打下基礎。
5 結語
GSP作為我國藥品經營質量管理工作的基本準則,將會更好地促進藥品經營企業依法經營和依法管理,有利于凈化藥品流通市場,確保人民群眾用藥安全有效。同時,實施新版GSP既是對監管部門政策水平的一次檢驗,也是對藥品經營企業執行相關政策能力的考驗,需要勇氣,更需要智慧。
參考文獻:
[1]李國慶.《藥品經營質量管理規范》修訂內容解讀[N].中國醫藥報,2013-02-25.
[2]奚軍偉,王 維.2012年版與2000年版《藥品經營質量管理規范》對比分析[J].中國藥業,2014,23(6):11-13.

