參花婦康膠囊中丹參醇提取工藝研究
周 健 ,宋 岐 ,金向群
(1.吉林輝南三和制藥有限公司,吉林 通化 135100; 2.吉林大學藥學院,吉林 長春 130021)
參花婦康膠囊是中藥6類新藥(臨床批件號為2011L01664),由當歸、丹參、芍藥、川芎、香附、紅花、苦參 7味中藥提取而制成的膠囊劑。處方中丹參的化學成分為脂溶性和水溶性兩部分,前者為丹參酮類,主要有丹參酮Ⅰ(tanshinoneⅠ)、丹參酮ⅡA(tanshinoneⅡA)、丹參酮ⅡB(tanshinoneⅡB)、隱丹參酮(crytotanshinone)、羥基丹參酮(hydroxytanshinone)、丹參羥基酯(methyltanshinonenate)、二氫丹參酮Ⅰ(dinydrotanshinoneⅠ)及異丹參酮Ⅰ、異丹參酮Ⅱ、異隱丹參酮、二氫異丹參酮Ⅰ,后者主要為酚酸類,包括丹參素、原兒茶醛和丹參酸甲、乙、丙。為了保證其療效,丹參的提取應先采用醇提取,醇提取后的殘渣再與其他藥物進行煎煮。本試驗中以干膏率及干膏中含丹參酮ⅡA的量為指標,優選丹參藥材乙醇提取的最佳工藝。
1 儀器與試藥
微壓循環煎藥機(北京東華醫療設備有限責任公司);旋轉蒸發儀(上海申生科技有限公司);萬分之一電子分析天平(上海梅特勒-托利多儀器有限公司);電熱真空干燥箱(上海實驗儀器廠有限公司),LC-10A型高效液相色譜儀(日本島津公司);KQ-250D型數控超聲波清洗器(昆山市超聲儀器有限公司)。藥材均購于吉林省藥材公司;丹參酮ⅡA對照品(批號為 0766-9909,中國藥品生物制品檢定所);甲醇、乙腈為色譜純(Fisher Scientific);水為二蒸水,其余試劑均為分析純。
2 方法與結果
2.1 丹參酮ⅡA含量測定
2.1.1 色譜條件與系統適用性試驗
色譜柱:Agilent zorbax NH2柱(150 mm ×4.6 mm,5 μm),十八烷基硅烷鍵合硅膠為填充劑;流動相:甲醇-水(72∶28);檢測波長:270 nm;流速:1.0 mL /min。理論板數按丹參酮ⅡA峰計算應不低于 2 000。
2.1.2 線性關系考察
精密稱取丹參酮ⅡA對照品適量,加流動相制成每1 mL含0.033 mg的對照品溶液,分別精密吸取該對照品溶液 1,2,3,4,5 μL,注入高效液相色譜儀,依法測定。以進樣量(X)為橫坐標、峰面積值(Y)為縱坐標作圖,得近似通過原點的直線。回歸方程為 Y=199 353.5 X+10 709.17,r=0.999 8(n=6)。結果表明,丹參酮ⅡA進樣量在 0.033~0.165 μg范圍內與峰面積呈良好的線性關系。
2.1.3 供試品溶液制備
取干膏0.7 g,研細,精密稱定,置50 mL容量瓶中,加入甲醇40 mL,超聲處理1 h,取出,放至室溫,加甲醇定容至刻度,搖勻,濾過,濾液用微孔濾膜(0.45 μm)濾過,取續濾液,即得。
2.1.4 含量測定方法
精密吸取2.1.3項下方法制備的供試品溶液10 μL,注入高效液相色譜儀,按擬訂色譜條件測定,每份樣品測定2次,峰面積取2次平均值。
2.2 提取工藝考察
2.2.1 因素水平確定
為了尋求丹參藥材乙醇提取的最佳工藝條件,擬以正交試驗表 L9(34)進行試驗,其中提取次數為因素A,乙醇用量為因素B,乙醇濃度為因素C,提取時間為因素D,因素水平表見表1。
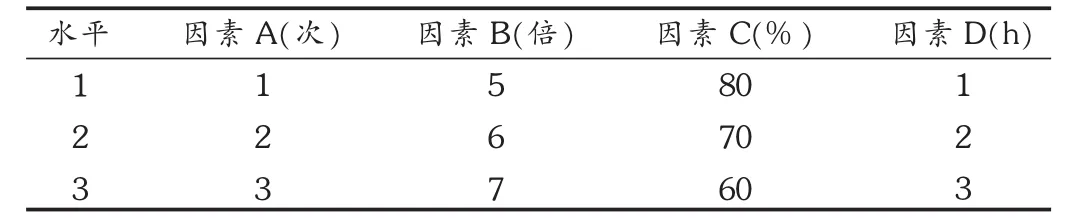
表1 因素水平表
2.2.2 考察指標
由于丹參中主要有效成分為丹參酮ⅡA,故確定以出膏量、干膏中含丹參酮ⅡA的量為考察指標。干膏率(%)=干膏質量/提取的藥材量×100%,干膏中丹參酮ⅡA的量=干膏重×百分含量(%)=干膏重×(樣品峰面積×對照品進樣量×對照品質量濃度×定容體積)/(對照品峰面積×樣品進樣量×稱樣量)×100%。
2.2.3 正交試驗與結果
準確稱取5倍處方量藥材9份,每份800 g,按表1進行提取,合并提取液,濾過,濾液濃縮并減壓干燥(真空度為0.08 MPa,溫度為 80℃),粉碎,稱量,取一定量的干膏粉,按 2.1.3項下方法制備供試品溶液,按2.1.4項下方法進行含量測定,按正交試驗軟件設計表格,并進行試驗。結果見表2和表3。可見,以干膏得量為指標進行方差分析所得的最佳條件是A2B2C2D3,以干膏中含丹參酮ⅡA的量為指標進行方差分析所得的最佳工藝條件也是A2B2C2D3,所得結果一致。由這兩個結果可見,影響乙醇提取的主要因素是提取次數及溶劑量,其次是提取時間和乙醇濃度。因此,最終確定的最佳工藝是,乙醇濃度為70%,溶劑量為6倍,提取時間為3 h,提取次數為2次。
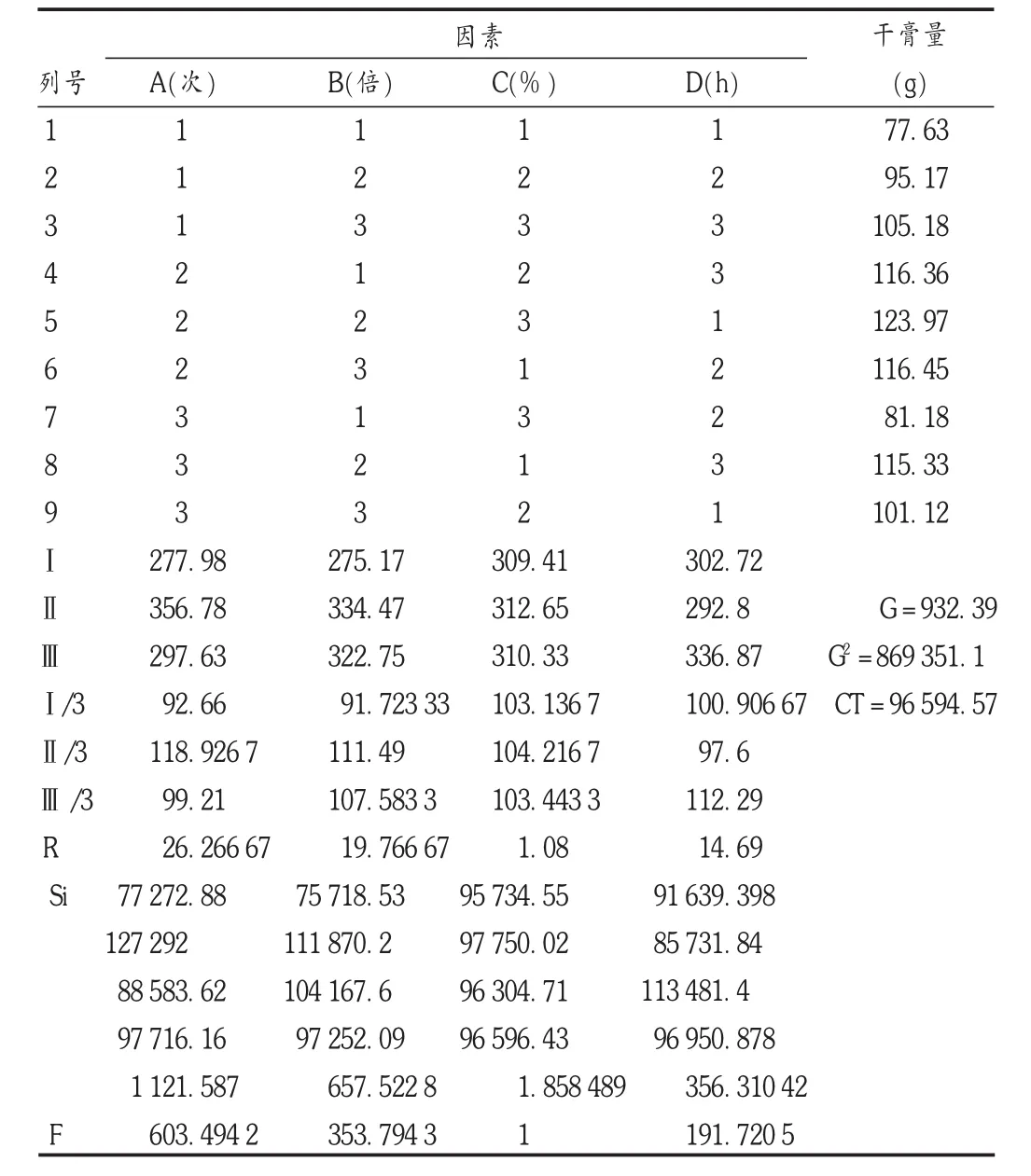
表2 乙醇提取正交試驗設計與結果(干膏量)
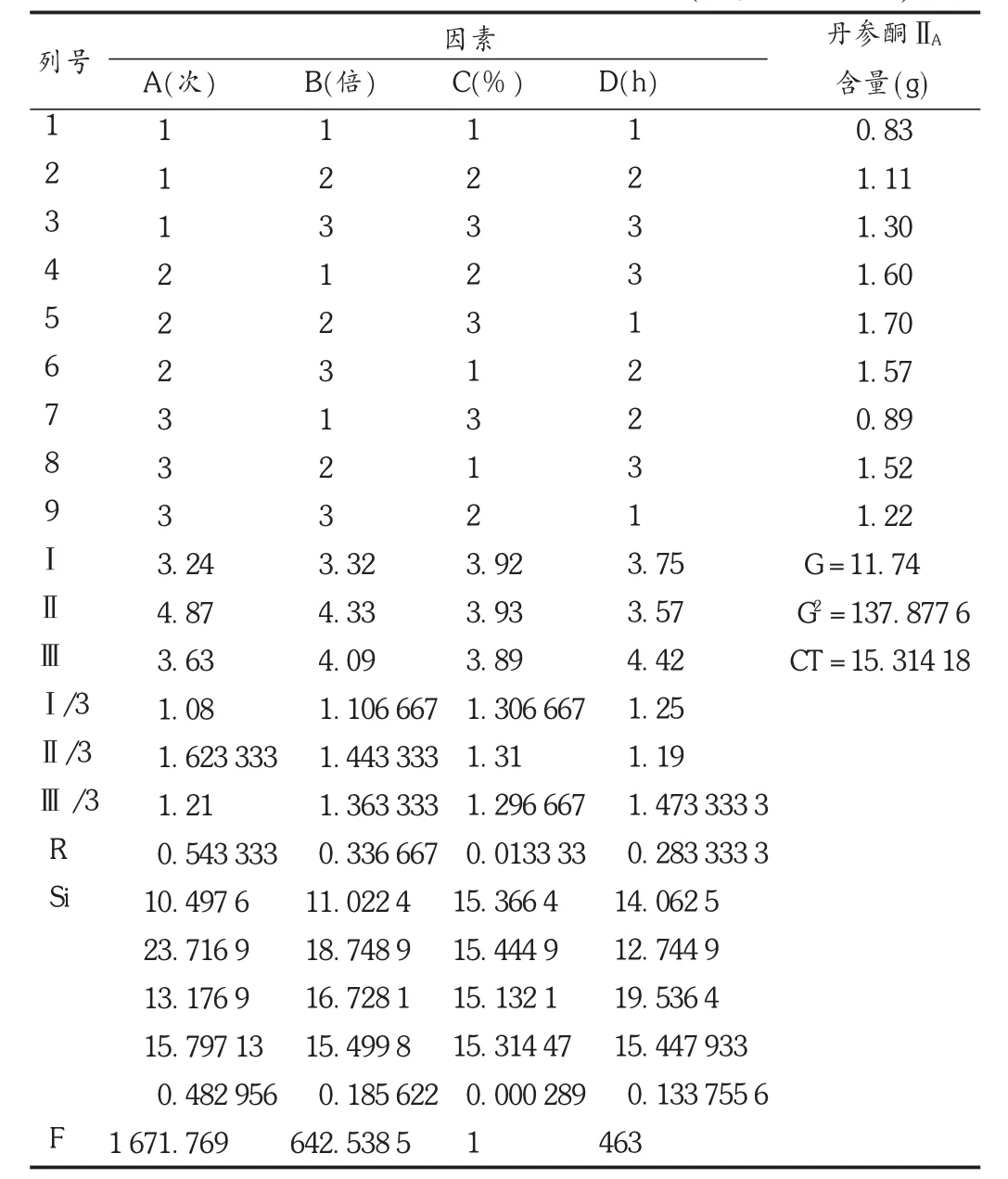
表3 乙醇提取正交試驗設計表與結果分析(丹參酮ⅡA含量)
2.2.4 工藝驗證試驗
為了進一步驗證所選工藝條件A2B2C2D3,進行如下試驗。取丹參8 000 g共3份,分別按上述工藝條件A2B2C2D3進行提取,合并提取液,濃縮并減壓干燥得干膏,稱定干膏量并測定干膏中含丹參酮ⅡA量。結果見表4。可見,丹參乙醇最佳提取工藝條件可行。

表4 最佳提取工藝驗證試驗結果(g)
3 討論
丹參酮ⅡA為處方中丹參的脂溶性指標性成分,具有較好的生理活性[1],主要有抗炎、抑菌、改善血循環、抗癌等作用[2-7]。本試驗中以干膏量及干膏中含丹參酮ⅡA的量為考核指標,較以單一成分為指標考察更能全面地體現中藥復方藥效物質的作用。
考慮到大生產時提取時間太短,有效成分不易提取完全;提取時間太長,又費時,且會提高成本。因此,提取時間選擇為1,2,3 h 3種水平。
稱取丹參藥材適量,加5倍量乙醇就可浸沒藥材;加溶劑量太大,不但浪費溶劑,而且會使成本過高。因此,選擇溶劑量為5,6,7 倍。
參考文獻:
[1]李玉萍,顧 兵,劉建濤,等.丹參酮ⅡA的研究進展[J].時珍國醫國藥,2010,21(7):1 170 - 1 172.
[2]關翠雯,金 晶,李 佳,等.丹參酮ⅡA激活Nrf2/ARE通路保護雷公藤甲素所致急性肝損傷[J].藥學學報,2013,48(9):1 397 -1 403.
[3]陳 曦,趙永芳.丹參酮ⅡA對異丙腎上腺素至心肌缺血大鼠apelin及受體的影響[J].中國藥物應用與檢測,2012,9(1):18 -21.
[4]蘇洪義.丹參酮ⅡA磺酸鈉注射劑對急性腦梗死患者血液流變學影響分析[J].中國實用醫藥,2011,6(30):31 - 32.
[5]翟昌林,黎 莉,張 運.丹參酮ⅡA對大鼠心肌缺血預適應保護中脂聯素表達的影響[J].中華中醫藥學刊,2012,30(8):1 859 -1 851.
[6]肖建勇,譚宇蕙,張廣獻.丹參酮ⅡA對腎癌786-O細胞生長抑制作用及其分子機制[J].中國新藥與臨床藥理,2012,23(2):136 -139.
[7]王曉露,解方為,晨 曦,等.丹參酮ⅡA對大鼠移植性肝癌的抑制作用[J].現代生物學進展,2011,11(11):2 062 - 2 064.

