細胞因子誘導的殺傷細胞治療中晚期泌尿生殖系統腫瘤效果觀察
李 霞,趙穩興,蔡 琳,蔡學敏,崔 靜,王媛媛,徐文漭
泌尿生殖系統惡性腫瘤由于病程發展較快,患者就診時已屬中晚期。過繼免疫治療是繼手術、放療、化療之外治療腫瘤的方法。細胞因子誘導的殺傷細胞(cytokine-induced killer cells,CIK)在體外可大量擴增,有較強的生物學效應,CIK治療是有效的過繼免疫療法之一[1-2]。成都軍區昆明總醫院2005年6月—2010年2月為38例中晚期泌尿生殖系統惡性腫瘤進行了CIK治療,效果滿意,現報告如下。
1 對象與方法
1.1 病例選擇標準 納入標準:①Karnofsky評分[3]≥60分;②心、肝、腎功能及血常規大致正常,白細胞數>2.1×109;③接受CIK治療前均未接受其他免疫治療或免疫抑制治療。排除標準:①正在接受放、化療或其他全身抗腫瘤治療者;②合并傳染性疾病者;③對生物制品過敏反應者。本研究通過醫院倫理委員會批準,患者均簽署治療知情同意書。
1.2 一般資料 本組38例,男25例,女13例;年齡28~75歲。均經影像學及病理學等確診為惡性腫瘤,根據國際抗癌聯盟(UICC)分期標準[4]進行臨床分期:Ⅱ期4例,占10.5%;Ⅲ ~Ⅳ期34例,占89.5%;膀胱癌4例,前列腺癌9例,腎癌12例,宮頸癌3例,子宮內膜癌5例,卵巢癌5例。患者均僅接受手術治療,因各種原因自動放棄放、化療。
1.3 治療方法
1.3.1 CIK制備:手術后2周用Pules-3000血細胞分離機(美國百特公司)采集患者外周血單個核細胞(PBMC),再采用淋巴細胞分離液(北京鼎國生物技術有限責任公司)進一步分離純化 PMBC,用AIM-V培養基(GIBCO公司)調整細胞密度為(1~2)×106個/ml細胞接種于培養瓶后置于37℃、5%CO2培養箱(Therm公司)。0 h培養加1000 U/mlγ干擾素(γ-IFN)(上海克隆生物高技術有限公司),24 h后加1000 U/ml白介素(IL)-2(山東泉港藥業有限公司)、50 ng/ml CD3單克隆抗體(CD3 McAb)(美國BD公司)繼續培養。4~5 d細胞傳代培養用僅含1000 U/ml IL-2的AIM-V培養基維持。每日用倒置顯微鏡觀察細胞生長情況。
1.3.2 CIK回輸:細胞培養7~10 d經微生物檢測陰性、活性檢測>80%時收集部分細胞,先用生理鹽水50 ml洗滌細胞2次,然后懸于200 ml生理鹽水中通過靜脈回輸,連續3 d為1個療程。輸注前、后均用生理鹽水沖管,避免與其他藥物混合,嚴格控制滴速,先慢后快。每次回輸細胞數>1×109,每療程細胞數(5~10)×109。3個月重復1次治療。
1.4 免疫細胞化學染色 收集培養7 d后的細胞,0.9%氯化鈉溶液洗滌2次,再用PBS液洗滌2次后懸浮細胞涂片,細胞數量約1×107。應用EnvisionTM二步法進行免疫細胞化學染色,DAB顯色。
1.5 流式細胞儀檢測 分別于治療前、第2療程結束通過流式細胞儀(BD公司)檢測外周靜脈血CD56+、CD3+、CD3+CD56+T細胞。均于清晨空腹采集患者2 ml靜脈血,EDTA抗凝。取不同熒光標記的單克隆抗體各20μl,分別加入100μl抗凝外周血中,室溫下孵育15 min后加入紅細胞裂解液,PBS液洗滌2次后檢測,應用Cellquest軟件分析數據,記錄陽性細胞百分率。
1.6 觀測指標及療效判定 觀測指標包括瘤體變化、腫瘤標志物、生存期、生存質量及毒性反應等。療效參照WHO對實體瘤療效判定標準[4]進行評價:以患者治療前及完成2個療程治療后CT及B超結果進行對照比較,分為完全緩解(CR)、部分緩解(PR)、輕度緩解(MR)、穩定(SD)、進展(PD),緩解率(%)=(CR+PR+MR)例數/總例數×100%。同時評估臨床癥狀,復查胸部CT、血常規、肝腎功能等;臨床癥狀、生存質量及毒性反應以患者主訴為依據,其中生存質量采用 Karnofsky評分評價[5],提高>10分為改善,下降>10分為惡化,提高或下降≤10分為穩定,Karnofsky評分總提高率(%)=(改善+穩定)例數/總例數×%。
1.7 統計學處理 應用SPSS 17.0軟件進行統計學分析,數據以均數±標準差(x±s)表示,采用配對t檢驗,α=0.05為檢驗水準。
2 結果
2.1 CIK細胞表面標記 免疫細胞化學染色發現,培養7 d的CIK CD3和CD56呈強陽性,見圖1。
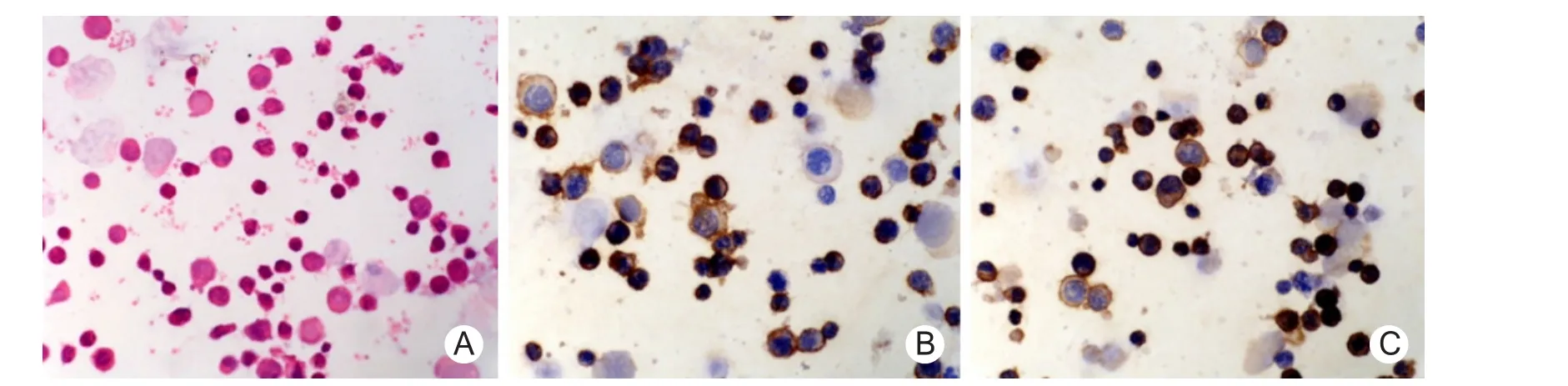
圖1 培養7 d后的CIKCIK.細胞因子誘導的殺傷細胞;A.CIK體積較大,核圓形,胞漿豐富(HE×200);B.CIK細胞膜CD3染色陽性(DAB×200);C.CIK細胞膜CD56染色陽性(DAB×200)
2.2 機體免疫狀態變化 CIK細胞回輸后監測血常規、腎功能、γ谷氨酰轉移酶(γ-GT)和丙氨酸轉氨酶(ALT)未見異常;第2療程后患者外周血免疫指標較治療前明顯改善,差異均有統計學意義(P<0.05)。見圖 2、表 1。
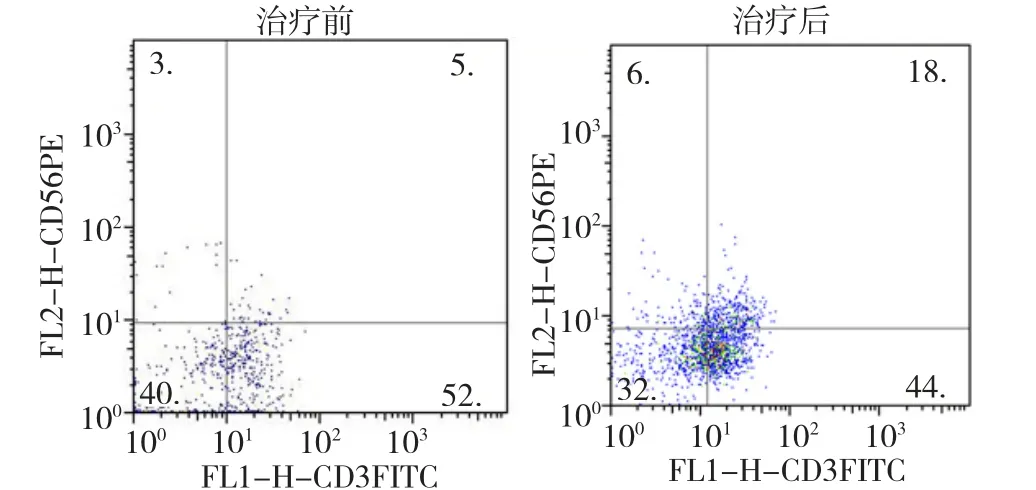
圖2 38例中晚期泌尿生殖系統惡性腫瘤患者細胞因子誘導的殺傷細胞治療前后流式細胞檢測圖

表1 38例中晚期泌尿生殖系統惡性腫瘤患者CIK治療前后機體免疫狀態變化(x ± s,%)
2.3 臨床療效及毒性反應 本組4例接受6個療程、10例接受4個療程 、15例接受3個療程 、9例接受2個療程治療。2個療程后,CR 20例,PR 11例,MR 5例,SD 2例,緩解率為94.7%。復查胸部CT均未見異常。本組均獲隨訪,隨訪時間2~8年,存活5年以上者17例,其中前列腺癌8例,腎癌9例。本組僅1例女性腎癌患者回輸CIK時出現發熱,經對癥處理后體溫恢復正常。
2.4 腫瘤標志物變化 與治療前比較,治療2個療程后癌胚抗原(CEA)、癌抗原(CA)125、乳酸脫氫酶(LDH)及前列腺特異性抗原(PSA)水平均顯著下降(P <0.01),見表2。
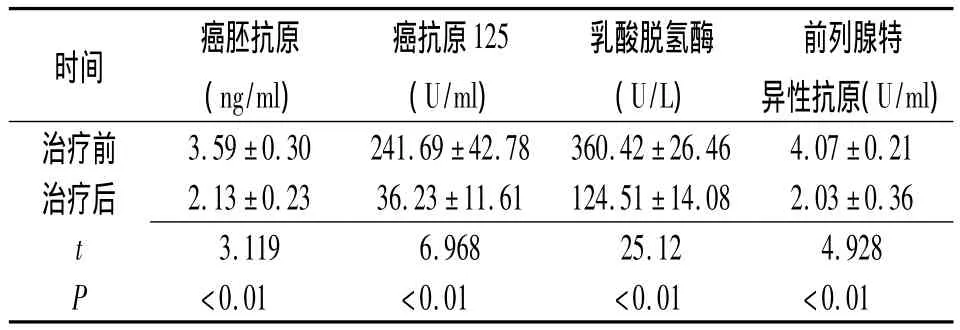
表2 38例中晚期泌尿生殖系統惡性腫瘤患者CIK治療前后腫瘤標志物變化(x±s)
2.5 生存質量變化 本組治療后Karnofsky評分提高10~20分,其中改善34例,穩定2例,Karnofsky評分提高率為94.7%。治療后患者體質量平均增加1~2 kg。2年無病生存21例,無病生存率(disease free survival,DFS)為55.3%,5年無病生存17例,DFS為44.7%。
3 討論
3.1 CIK作用機制 腫瘤生物治療主要有細胞因子治療、單克隆抗體治療、基因治療、過繼細胞免疫治療和腫瘤疫苗治療5類[6-9]。CIK治療被認為是具有較好應用前景的過繼細胞免疫治療方法[10-11]。CIK是存在于人體外周血中的,經抗CD3McAb、γ-IFN、IL-2等聯合作用后產生的一類對惡性腫瘤細胞具有高度殺傷能力的T淋巴細胞[12],兼具T淋巴細胞強大的抗腫瘤活性和自然殺傷細胞(NK)非組織相容性抗原(MHC)限制性殺瘤細胞特性,且增殖能力強,同時還能分泌 IL-2、IL-6、腫瘤壞死因子 α(TNF-α)等細胞因子,增強細胞毒作用,或調節腫瘤細胞對免疫效應細胞的敏感性,間接殺傷腫瘤細胞[13]。體內回輸CIK可在不損傷機體免疫系統功能的前提下直接殺傷腫瘤細胞,還能調節和增強機體的免疫功能。此外,CIK還是對多重耐藥腫瘤細胞敏感的廣譜抗瘤免疫活性細胞[14]。因此,CIK免疫治療因低毒、有效的特點越來越受到重視[15-18]。
3.2 泌尿生殖系統腫瘤的治療現狀 女性器官位于盆腔深部,由于位置特殊,婦科惡性腫瘤目前缺少有效的診斷方法,患者出現癥狀時往往已是中晚期,喪失徹底切除腫瘤的機會。婦科惡性腫瘤治療仍以放化療及手術為基本手段,但腫瘤患者的細胞免疫功能狀態直接影響患者的預后。卵巢癌雖然對化療敏感,但由于化療毒性作用較大,很多患者無法耐受全程化療。放療與腔內照射+化療為局部晚期宮頸癌標準的一線治療方案,但急性不良反應較嚴重,能最終完成治療的患者不足50%[19]。前列腺癌及泌尿系統腫瘤發病率約占實體瘤的9%,且近年來有不斷上升的趨勢。將近一半的患者首次就診時已屬晚期或有遠處轉移,約50%的患者術后復發或轉移,未接受治療者3年存活率低于5%。腎癌是免疫原性較強的腫瘤之一,轉移性腎癌預后極差,化療作用有限,總反應率僅為5% ~15%[20],但對生物免疫治療比較敏感,以往采用細胞因子類藥物治療,有研究將CIK用于治療局限性腎癌、轉移性腎癌,取得了較好的臨床效果[21-22]。對于中晚期前列腺癌,放、化療及內分泌治療雖有一定效果,但毒性反應較大,易復發,細胞過繼免疫治療有較好效果[23]。
3.3 CIK治療注意事項 CIK治療作為一種新的生物治療方法,在給腫瘤患者帶來希望的同時,也會導致患者及其家屬產生疑惑、恐懼心理[24-26]。治療前應盡可能與患者及其家屬多溝通交流,客觀介紹CIK治療的效果及可能發生的毒性反應,可介紹治療成功的患者,消除患者及其家屬的疑惑、恐懼心理,使其全力配合治療。同時向患者及家屬講明該方法療效存在個體差異,幫助患者調整好心態,避免因達不到預期療效而出現心理落差。細胞輸注過程中除嚴格按照輸血程序無菌操作外,還要嚴密觀察生命體征,對心肺功能不全者滴速應盡量緩慢,輸入液體量應嚴格限制。回輸后患者最常見的毒性反應是發熱,可能是腫瘤熱或CIK攻擊腫瘤所致,本組僅出現1例,經對癥處理后體溫恢復正常。
綜上所述,放、化療后間隔2~4周、機體免疫力有所恢復時輸入CIK,可提高泌尿生殖系統腫瘤患者的緩解率。本組行手術后結合CIK治療,2個療程后緩解率為94.7%,相關腫瘤標志物呈下降趨勢,而相關免疫活性細胞呈上升趨勢,Karnofsky評分提高10~20分,體質量增加1~2 kg。表明CIK療法是治療中晚期泌尿生殖系統腫瘤的有效方法。
[1] Hontscha C,Borck Y,Zhou H,et al.Clinical trials on CIK cells:first report of the international registry on CIK cells(IRCC)[J].J Cancer Res Clin Oncol,2011,137(2):305-310.
[2] 秦莉,王志華.CIK細胞的體外培養與細胞毒作用[J].醫學分子生物學雜志,2007,4(1):82-85.
[3] 周際昌.實用腫瘤內科學[M].北京:人民衛生出版社,2003:28-48.
[4] 孫燕,湯釗猷.UICC臨床腫瘤學手冊[M].8版.北京:人民衛生出版社,2006:425-501.
[5] 孫燕,周際昌.臨床腫瘤內科手冊[M].北京:人民衛生出版社,2003:102-113.
[6] Hobeika A C,Morse M A,Osada T,et al.Depletion of human regulatory Tcells[J].MethodsMol Biol,2011,707:219-231.
[7] Kim Y J,Lim J,Kang J S,et al.Adoptive immunothe of human gastric cancer with ex vivo expanded Tcells[J].Arch Pharm Res,2010,33(11):1789-1795.
[8] Schoenfeld J,Jinushi M,Nakazaki Y,et al.Active immunotherapy induces antibody responses that target tumor angiogenesis[J].Cancer Res,2010,70(24):10150-10160.
[9] Gomes A Q,Martins D S,Silva-Santos B.TargetingγδT lymphocytes for cancer immunotherapy:from novel mechanistic insight to clinical application[J].Cancer Res,2010,70(24):10024-10027.
[10]舒心,李幸.胃癌CIK細胞治療的研究現狀及進展[J].武警醫學,2013,24(6):526-528.
[11]Olioso P,Giancola R,Di Riti M,et al.Immunotherapy with cytokine induced killer cells in solid and hematopoietic tumours:a pilot clinical trial[J].Hematol Onco1,2009,27(3):130-139.
[12]Kim H M,Lim J,Yoon Y D,et al.Anti-tumor activity of ex vivo expanded cytokine-induced killer cells against human hepato-cellular carcinoma[J].Int Immunopharmacol,2007,7(13):1793-1801.
[13]王堅,何敏,王穎,等.ICOS基因轉染對CIK細胞殺傷膽管癌細胞作用的研究[J].中華消化外科雜志,2008,7(3):213-217.
[14]Linn Y C,Lau SK,Liu B H,et al.Characterization of the recognition and functional heterogeneity exhibited by cytokine-induced killer cell subsets against acute myeloid leukaemia target cell[J].Immuology,2009,126(3):423-435.
[15]李霞,趙穩興,蔡琳,等.化療聯合CIK免疫療法治療晚期消化道腫瘤86例觀察[J].解放軍醫藥雜志,2014,26(5):38-40,61.
[16]Helms M W,Prescher JA,Cao Y A,et al.IL-12 enhances efficacy and shortens enrichment time in cytokine-induced killer cell immun-otherapy[J].Cancer Immunol Immunother,2010,59(9):1325-1334.
[17]安東建,柴琴,田垣,等.DC/CIK細胞治療152例腫瘤的副反應觀察[J].中國當代醫藥,2013,20(1):6-8.
[18]Kimura H,Iizasa T,Ishikawa A,et al.Prospective phase II study of post-surgical adjuvant chemo-immunotherapy using autologous dendritic cells and activated killer cells from tissue culture of tumor-draining lymph nodes in primary lung cancer patients[J].Anticancer Res,2008,28(2B):1229-1238.
[19] Ikushima H,Osaki K,FuruIani S,et al.Chemoradiation therapy for cervical cancer:toxicity of concurrent weekly cisplatin[J].Radiat Med,2006,24(2):115-121.
[20]楊琳,丁英俊,石磊,等.索拉非尼治療晚期腎癌患者33例長期臨床觀察[J].疑難病雜志,2012,11(10):757-759.
[21]李霞,徐文漭,崔靜,等.CIK細胞治療局限性腎癌的療效[J].腫瘤防治研究,2011,38(8):950-953.
[22]Olioso P,Giancola R,Di Riti M,et al.Immunotherapy with cytokine induced killer cells in solid and hematopoietic tumours:a pilot clinical trial[J].Hematol Oncol,2009,27(3):130-139.
[23] J?hnisch H,Füssel S,Kiessling A,et al.Dendritic cellbased immunotherapy for prostate cancer[J].Clin Dev Immunol,2010,2010:517493.
[24]葉穎江,王杉.胃癌免疫治療的新進展[J].中華消化外科雜志,2010,9(4):247-249.
[25]陳新華,李姍姍,李曉雪.CIK細胞治療消化道惡性腫瘤的臨床護理[J].武警醫學,2013,24(1):81-82.
[26]張效東,周寧新,徐迎新,等.聯合免疫治療肝門部膽管癌根治術后皮膚多發轉移[J].中華消化外科雜志,2010,9(4):316-317.

