超聲對150例甲狀腺微小癌的診斷分析*
毛明鋒,楊順實△,戴 晴,江 玲
(1.武漢市中心醫院超聲科,武漢430014;2.北京協和醫院超聲科,北京100005)
甲狀腺微小癌(thyroid microcarcinoma,TMC)是指腫瘤直徑小于或等于10mm的甲狀腺癌[1],臨床上常無任何癥狀,有少數TMC雖原發灶大小無變化,卻發生遠處轉移或向未分化癌轉化,因此,TMC早診斷、早治療十分重要。TMC常與甲狀腺其他疾病并存,術前誤診、漏診率高。本研究回顧性分析經手術及病理證實的150例患者的206個TMC結節的二維超聲和彩色多普勒超聲特征,旨在進一步提高超聲對TMC的診斷及鑒別診斷。
1 資料與方法
1.1 一般資料 選擇武漢市中心醫院2008年5月至2012年12月經手術和病理證實的150例患者為研究組,其中男58例,女92例,年齡18~62歲,平均(40.0±5.8)歲;其中癌結節單發105例,多發45例(34例為2個結節,11例為3個結節),共206個結節;無自覺癥狀體檢發現122個,結節性甲狀腺腫復查者51個,甲狀腺癌術后復發者6個,橋本甲狀腺炎患者復查發現者27個。同期在武漢市中心醫院手術并經病理確診為良性結節患者69例共83個結節設為對照組,其中男8例,女61例,年齡19~71歲,平均(46.0±5.2)歲。
1.2 儀器與方法 采用Philips HD11XE及iu22彩色多普勒超聲診斷儀,探頭頻率為5~12MHz。患者取仰臥位,充分暴露頸部,仔細檢查甲狀腺內結節部位、大小、數目、邊界、內部回聲、血流、有無鈣化及結節與甲狀腺包膜關系。同時檢測雙側頸部淋巴結有無異常,記錄淋巴結的形狀、大小、數目、內部回聲特征及血流情況。結節回聲水平分為3級[2]:(1)低回聲,低于甲狀腺前方頸前肌肉回聲;(2)中等回聲,與甲狀腺病灶周圍正常腺體回聲相近;(3)高回聲,高于甲狀腺病灶周圍正常腺體回聲。計算縱橫比,將任何切面結節前后徑大于或等于橫徑均定義為縱橫比大于或等于1,其余為縱橫比小于1[3]。鈣化分為4類[4]:(1)微小鈣化,散在分布的砂粒樣強回聲,伴或不伴聲影,≤2mm;(2)粗大鈣化,不規則強回聲,后方伴聲影,>2 mm;(3)蛋殼樣鈣化,鈣化位于結節周邊并伴聲影。
1.3 統計學處理 采用SPSS 17.0軟件進行數據分析。以病理學結果為標準,研究組與對照組良性甲狀腺結節的聲像圖特點比較采用χ2檢驗。計算各超聲征象的靈敏度、特異度、陽性預測值、陰性預測值,以P<0.05為差異有統計學意義。
2 結 果
2.1 超聲表現 超聲檢測病灶大小3~10mm,檢出最小病灶為3mm×3mm。聲像圖特征:所有癌結節均為實性結節,研究組中TMC結節內部回聲、縱橫比、血流、內部鈣化及鈣化大小、分布及類型與良性結節比較見表1。
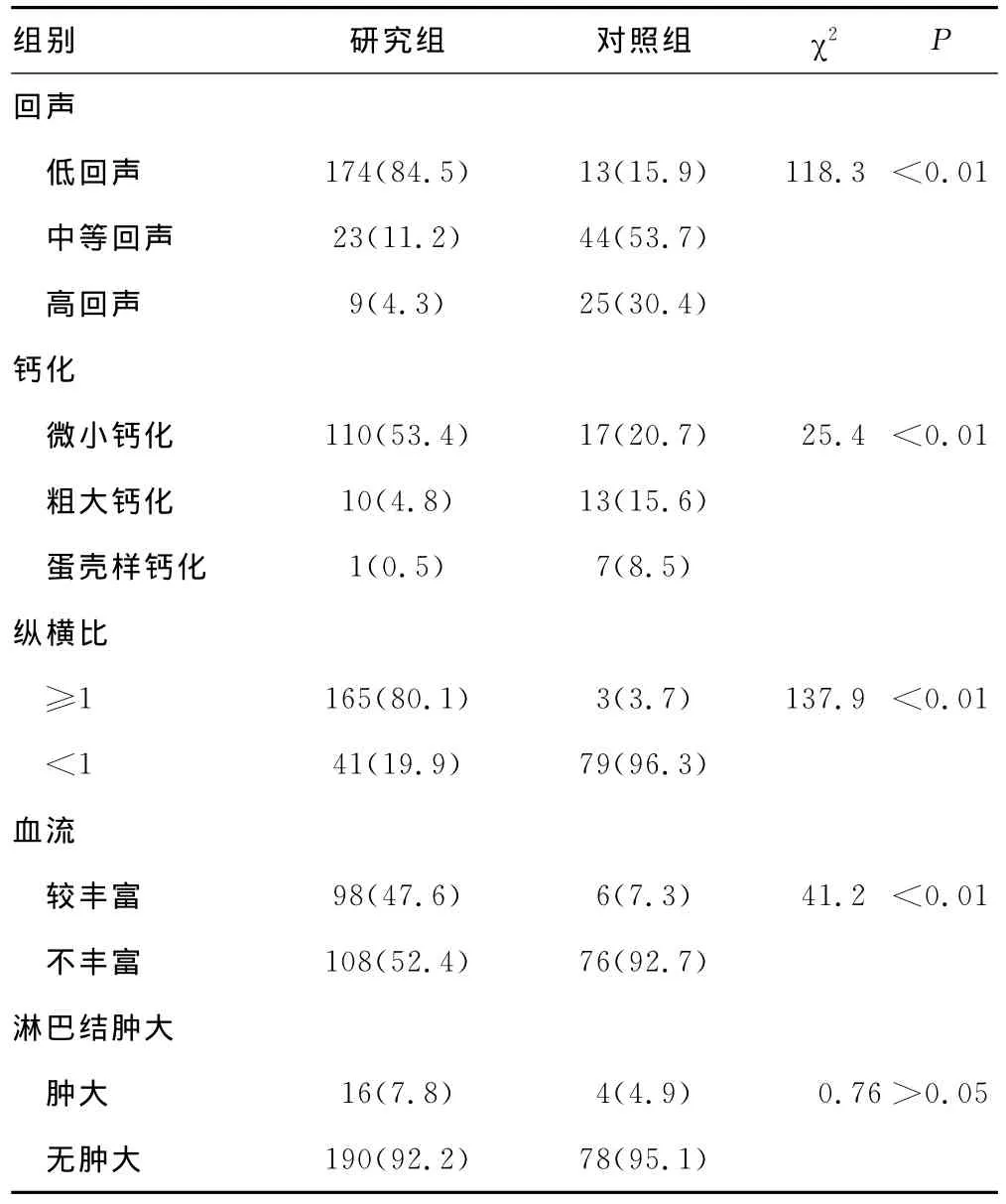
表1 研究組和對照組的二維超聲表現[n(%)]
所有癌結節均無包膜回聲,邊緣不規則,大部分邊界不清,有細小毛刺樣改變。研究組中37例(24.7%)超聲發現頸部淋巴結轉移,二維超聲表現為髓質消失或偏心,縱橫比大于0.55,形態不規則,內部微小鈣化或液化;彩色多普勒血流顯示內部血流豐富,分布不規則達皮質,病理均證實為轉移性淋巴結。150例患者同時合并有結節性甲狀腺腫21例,腺瘤10例,橋本甲狀腺炎27例。此外,其他特征包括42個結節凸向甲狀腺表面,甲狀腺包膜回聲的連續性中斷。
χ2檢驗表明,低回聲、微小鈣化、縱橫比大于或等于1、血流及淋巴結腫大方面,研究組均明顯高于對照組(P<0.01)。超聲對TMC的診斷靈敏度為86.9%,特異度為80.7%,陽性預測值為92.3%,陰性預測值為71.3%。超聲診斷與病理診斷結果見表2。
血流豐富,表現為血流由周邊部進入結節或結節內部的點片狀血流信號,局部可見粗大穿支血流。研究組顯示98病灶內均能測及彩色血流信號,血供較豐富,分布不規則,局部可見粗大血流分布。PW可探及動脈頻譜,收縮期峰值流速(8.5~32.0)cm/s,阻力指數0.62~0.82。超聲聲像圖見圖1。
2.2 病理類型 乳頭狀癌188例,濾泡狀癌14例,髓樣癌4例。
2.3 超聲診斷與手術病理結果 206個TMC中,179個超聲診斷正確,診斷準確率為86.9%;其余27個中,18個誤診為甲狀腺腺瘤,9個誤診為結節性甲狀腺腫腺瘤樣增生。
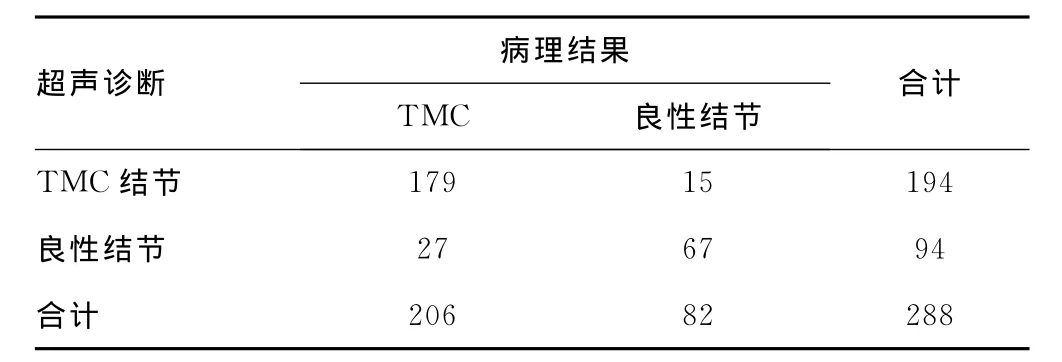
表2 二維超聲診斷結節性質與病理組織學檢查結果比較(n)

A:TMC縱橫比大于1,呈實性極低回聲,邊緣模糊;B:TMC縱橫比大于1,邊緣模糊,結節內見有多個微小鈣化(白箭),分布不規則,凸向甲狀腺右側包膜,包膜連續性中斷;C:TMC示內部血供豐富,可見粗大血流,血流信號分布不規則;D:TMC頸部淋巴結轉移,淋巴結內見豐富血流信號,分布雜亂
3 討 論
世界衛生組織組織學分類標準規定最大徑小于或等于10 mm的甲狀腺癌為TMC。TMC在每個年齡階段都可以發生,以青年女性多見,病理以乳頭狀癌為主,極少數為濾泡癌或髓樣癌[5]。隨著超聲和病理檢查水平的不斷提高,甲狀腺手術不斷增加,使TMC的發現率逐年增高。世界各地報道TMC占甲狀腺癌的比例差異較大,約為6%~35%。因此,大多數TMC病灶是在甲狀腺良性疾病手術中偶然發現或術后病理檢查才發現。
本研究發現TMC的超聲診斷主要以下幾點。(1)結節多數為實性低回聲,少數為等回聲。本研究中TMC結節多為實性低回聲,占所有結節的84.5%(174/206)。蔡勝等[6]提出將低回聲進一步細分為極低回聲(低于頸前肌肉)和低回聲(高于頸前肌肉但低于甲狀腺正常腺體回聲),極低回聲診斷意義更大。(2)實性結節內微小鈣化,一般分布在實性結節內部,聲影不明顯,直徑小于或等于0.5mm,反映病理中的砂粒體[7]。此細小點狀強回聲是甲狀腺癌中特有的砂粒體的聲像圖表現。張武等[8]和王瑛等[9]均認為砂粒體鈣化在甲狀腺癌的診斷中很有意義,對甲狀腺癌的診斷具有很高的特異度,但靈敏度不高,約29%~59%[10]。超聲聲像圖上還有一種微小鈣化為結晶樣鈣化,為良性病變的特異性表現,超聲特點為點狀強回聲,后伴彗星尾征,主要分布在結節壁上或者分布在結節內囊性成分上,病理上為膽固醇結晶或膠體濃縮。(3)結節的前后徑和橫徑的比值大于或等于1,一般認為此征象是診斷TMC的特異性指標[11]。前后徑和橫徑的比值大于或等于1,主要是由于惡性腫瘤可突破向不同組織層縱向生長,而良性結節生長則在一個組織層內[5]。但是他對于診斷大于1cm的甲狀腺癌意義不大,>1cm的腫瘤生長常不規則。(4)大部分TMC形態不規則,邊界模糊,部分不規則暈環。良性結節也可以顯示暈環,但邊界清晰,寬度均勻,而惡性結節暈環邊界不清,寬度不均勻,易中斷[12]。另外,本組42個(20.4%)TMC顯示結節凸向甲狀腺包膜,包膜連續性中斷,提示惡性腫瘤浸潤,進一步發展可能侵犯周邊肌層及頸動脈。
由于甲狀腺位置表淺,高分辨率彩色多普勒超聲可較敏感探測到TMC的血流信號,本組47.6%TMC較大病灶均能檢出豐富血流,大部分分布不規則。對于有些較小結節,放大結節圖像,靈敏度可能更高。本組良性結節6例檢出豐富血流信號,病理為濾泡樣腺瘤,血流分布特點為周邊血流環繞,內部豐富,血流分布比較規則。有關甲狀腺癌的收縮期峰值流速及血流阻力指數值爭議較大,之前有研究認為由于高代謝和腫瘤組織快速生長,血管形成較多,而新生血管缺乏平滑肌組織,管壁薄,在彩色多普勒超聲血流成像上顯示血流速度增高,阻力指數偏低的頻譜圖,但病灶均為10mm以上,在小于5mm病灶內及周邊無彩色血流增多、增速的跡象,所以TMC較小結節彩色多普勒超聲血流成像特點與良性結節差異不大。本組資料中癌灶內收縮期峰值流速范圍也較大,約8.5~32.0cm/s,故峰值流速對良惡性的診斷價值有待探討,但血流阻力值增高可能有參考價值。
淋巴結轉移是大部分惡性腫瘤的共性,特別是甲狀腺乳頭狀癌,本組中37例(37/150,24.7%)發生頸部淋巴結轉移。從頸部淋巴結轉移來看,氣管旁Ⅵ區發現最多,其次為Ⅱ、Ⅲ、Ⅳ區,Ⅰ、Ⅴ區少有淋巴結轉移[13]。轉移性淋巴結有一個重要特點,他在聲像圖上與甲狀腺癌原發灶表現類似,內可出現微小鈣化、液化、等回聲光團等。他與非轉移性淋巴結鑒別如下:(1)非轉移性淋巴結形態規則,呈橢圓形,前后徑和橫徑的比值小于0.55,而轉移性淋巴結呈圓形或類圓形,前后徑和橫徑的比值大于或等于0.55;(2)非轉移性淋巴結皮髓質分界清晰,而轉移性淋巴結髓質消失或偏心,內部出現液化、微小鈣化或中等團塊回聲;(3)非轉移性淋巴結血流由淋巴門進入,分布規則,呈樹枝狀,很少達皮質,而轉移性淋巴結血流豐富,分布不規則,達皮質。本組良性結節僅發現4例頸部淋巴結腫大,病理為反應性淋巴結增生,二維超聲表現形態規則,皮髓質分界清晰,僅皮質增厚,前后徑和橫徑的比值小于0.55。
綜上所述,TMC的超聲表現具有一定特征性,仔細檢查結節的形態、回聲、邊界、鈣化、內部血流信號是關鍵。特別是頸部淋巴結出現異常,即使甲狀腺內未發現結節,也需要進一步檢查,必要時超聲引導下細針穿刺以及時診斷和手術。綜合多項聲像圖特征對TMC早期診斷和鑒別有重要意義。
[1]曾書娥,黃建國.高頻超聲對甲狀腺微小癌瘤的診斷價值[J].腫瘤防治研究,2007,34(12):981.
[2]蔡勝,張一體,李建初,等.甲狀腺微小癌的超聲征象及其診斷價值[J].中華超聲影像學雜志,2008,17(8):704-708.
[3]李泉水,張家庭,鄒霞,等.甲狀腺微小癌超聲顯像特征的研究[J].中國超聲醫學雜志,2009,25(10):940-943.
[4]Wang N,Xu Y,Ge C,et al.Association of sonographically detected calcification with thyroid carcinoma[J].Head Neck,2006,28(12):1077-1083.
[5]Baloch ZW,Livolsi VA.Microcarcinoma of the throid[J].AdvAnat Pathol,2006,13(2):69-75.
[6]蔡勝,張一休,李建初,等.甲狀腺微小癌的超聲征象及其及診斷價值[J].中華超聲影像學雜志,2008,17(8):704-708.
[7]Das DK,Mallik MK,Haji BE,et al.Psammoma body and its precursors in papillary thyroid carcinoma:a study by fine-needle aspiration cytology[J].Diagn Cytopathol,2004,31(6):380-386.
[8]張武,梁建平.甲狀腺疾病的超聲診斷進展[J].中華超聲影像學雜志,1998,7(1):55-57.
[9]王瑛,王武.甲狀腺囊性乳頭狀癌超聲特征[J].中國超聲醫學雜志,1998,14(2):20-22.
[10]Reading CC,Charboneau JW,Hay ID,et al.Sonography of thyroid nodules:a“classic pattern”diagnostic approach[J].Ultrasound Q,2005,21(3):157-165.
[11]褚潔,楊麗春.甲狀腺微小乳頭狀癌的超聲診斷及進展[J].中國醫學影像技術,2010,26(10):1996-1998.
[12]張春梅,吳長君,張雪菊,等.超聲在甲狀腺良惡性結節診斷中的應用[J].中國醫學影像技術,2007,23(3):385-387
[13]龔龍,易春華,陳文奎,等.分化型甲狀腺癌頸淋巴結轉移特點的回顧性分析[J].腫瘤防治研究,2012,39(1):48-50.

