不同生物載體對雌酮的吸附性能
楊小麗 黃克虎
(東南大學土木工程學院,南京 210096)
近年來,關于環境雌激素干擾人類和動物的內分泌系統、影響健康和生殖的研究與日俱增,以雌酮(E1)、17β雌二醇(E2)和17α乙炔基雌二醇(EE2)為代表的類固醇雌激素(steroid estrogens, SE)尤其引人關注.E1,E2,EE2的雌情活性是其他各種疑似環境雌激素的104~ 105倍,且這3類SE在濃度低至ng/L時仍能夠影響許多脊椎動物甚至人類的內分泌系統,因此被公認為是最具風險性的環境雌激素[1].許多國家及國際組織研究者調查發現,污水處理廠出水是自然水體中SE的重要來源[2],其中殘留的SE濃度往往超過預測無效應濃度(1.0 ng/L)數十倍[3],成為向自然水體釋放SE的重要來源之一.我國人口密度高且人均用水量低,污水中SE濃度較高,而現有污水處理工藝的主要去除對象是有機物、氮磷等大量營養物,其對SE等微量有機物的去除只是大量有機物去除的伴生結果.筆者對南京3座污水處理廠調查發現,出水中E1,E2和EE2平均值分別為9.2 ~ 20.5,8.4 ~ 22.1和5.3 ~ 18.6 ng/L[4].國內學者[5-6]也指出,我國城市污水處理廠出水SE污染水平處于中等或偏高水平,對水生生物繁殖、生態安全甚至人民健康都存在著極大的潛在威脅.
目前,對雌激素的去除機理尚沒有取得一致的結論,但普遍認為雌激素的去除主要基于吸附和生物降解2種途徑.活性污泥的吸附作用對雌激素的去除貢獻較生物降解大,進水中雌激素濃度較低是造成其生物轉化速率較低的原因.同時,生物膜法具有生物濃度高、抗沖擊負荷能力強、生物相豐富等特點,對包括雌激素在內的微量有機物呈現出明顯的去除優勢,日益受到關注.而生物載體在生物膜系統中起著關鍵作用,其對雌激素的吸附可為后續雌激素的生物降解提供條件,因此有必要研究不同生物載體對雌激素的吸附去除效果.
本文以天然類固醇雌激素雌酮(estrone, E1)為研究對象,重點考察了活性炭、沸石、竹炭和玉米芯4種不同類型的水處理生物載體對E1的吸附性能,并分析吸附去除機制.為如何挖掘現有城市污水處理工藝的潛力、不增設深度處理工藝單元而達到以較低成本強化雌激素去除的目的,提供理論依據和實踐指導,對解決已逐步提上議事日程的雌激素污染問題、降低水生生態風險、改善水環境具有重要的意義.
1 材料和方法
1.1 試劑與儀器
雌酮標準樣品為色譜純,購自美國Sigma公司,用乙腈配制成1 mg/L標準液保存.使用時用純水稀釋為1,10,100,500 μg/L的E1溶液.HPLC級甲醇和乙腈購自國藥集團化學試劑有限公司.4種生物載體經球磨后過30目篩并烘干備用,并采用ASAP 2020型自動吸附儀分析其表面物理性質,結果見表1.

表1 4種生物載體的表面物理性質
高效液相色譜儀購自島津公司,配有LC-20AB型梯度泵、SIL-20A型自動進樣器、SPD-20型紫外檢測器、RF-10AXL型熒光檢測器及LC solution色譜工作站.Agilent ZorbaxExtend-C18 色譜柱購自安捷倫公司.SPE自動萃取工作臺購自Caliper公司.萃取小柱購自Dusseldorf公司.恒溫培養搖床型號為THZ-100.此外,試驗中還需要超聲波清洗器、氮吹儀等設備.
1.2 吸附試驗
吸附試驗在恒溫調速搖床上進行,搖床轉速為125 r/min,溫度為25 ℃.采用容量為500和1 000 mL的2種錐形瓶進行吸附試驗.錐形瓶中依次加入濃度分別為1,10,100,500 μg/L的E1溶液和不同種類的生物載體(載體投加量均為2 g),混勻后放入恒溫搖床震蕩,定期取樣分析,時間間隔為5,15,30,60,120,180 min.
1.3 分析方法
1.3.1 樣品預處理
混合液樣品直接在3000 r/min的轉速下離心5 min,上清液用直徑為0.7 μm的玻璃纖維膜(GF/F)過濾,移入其他容器,用于檢測或者進行固相萃取.采用固相萃取對水樣中的E1進行濃縮:首先用7 mL乙腈、10 mL甲醇、10 mL純水依次對固相萃取小柱進行活化,再將水樣以10 mL/min的速度通過該柱,完成上樣后,分別用質量分數為5%的甲醇溶液和純水淋洗C18小柱,然后用氮氣真空吹干,最后用10 mL乙腈作為洗脫劑洗脫待測物.在微氮氣流中吹干,加入1 mL色譜純乙腈溶解,利用0.22 μm的玻璃纖維膜過濾,用于HPLC檢測.
1.3.2 E1分析測試條件
采用高效液相色譜分析E1,檢測條件如下:流速為0.8 mL/min;超純水為流動相A,乙腈為流動相B, 0 ~ 5 min時,流動相A與流動相B(體積比為55∶45)等度洗脫,隨后進行梯度洗脫,5~10 min時,流動相B的體積分數從45%變為50%,10~13 min時,流動相B的體積分數從50%變為45%;紫外檢測波長為200 nm;柱溫為30 ℃;進樣量為20 μL;色譜系統采用外標法進行校準,以保留時間進行定性,通過峰面積進行定量.
2 實驗結果與討論
2.1 E1初始濃度對吸附作用的影響
在E1初始濃度分別為1,10,100,500 μg/L的條件下,4種生物載體對E1的吸附去除率隨吸附時間的變化見圖1.由圖可見,4種生物載體對E1吸附是一個快速吸附過程,1 h左右達到平衡;不同E1初始濃度下,4種載體達到吸附平衡的時間大致相同.因此,E1初始濃度對吸附平衡時間影響較小.
吸附平衡時,隨著E1初始濃度的增加,活性炭對E1的吸附去除率依次為73.07%,75.04%,91.07%和92.08%;沸石對E1的吸附去除率依次為57.64%,65.75%,89.13%和87.85%;玉米芯對E1的吸附去除率依次為39.59%,38.36%,48.12%和59.57%.可見,E1初始濃度為1~500 μg/L時,活性炭、沸石和玉米芯對E1的吸附去除效果均隨著E1初始濃度的增加而增加.分析認為,較高的初始濃度會在溶液和生物載體之間形成一個較大的濃度梯度,從而促進生物載體對E1的吸附.不同E1初始濃度下,玉米芯對E1的吸附去除率均低于60%,這可能是由于玉米芯為天然生物材料,與E1結合強度不夠.研究還發現,不同E1初始濃度下,吸附平衡時竹炭對E1的吸附去除率接近,分別為73.42%,75.35%,76.14%和78.66%,可見竹炭吸附能力受E1初始濃度的影響較小,這可能是由于竹炭中較大的平均孔徑所致.結合4種生物載體的表面物理性質(見表1)可知,具有較大比表面積、孔容及微孔數量的生物載體對E1表現出較好的吸附效果,因此,可以優先選擇作為生物膜法的生物載體.
從圖1還可看出,4種生物載體吸附過程中均呈現初期快速吸附、吸附速率減緩、慢速吸附、趨于平衡4個階段.在E1初始濃度為1,10,100,500 μg/L的條件下,吸附時間為5 min時活性炭對E1的吸附去除率可分別達44.28%,62.2%,70.18%和59.17%,沸石和竹炭對E1的吸附去除率也在40%以上,玉米芯對E1的吸附去除率為平衡時的67.33%,79.95%,83.91%和86.52%.吸附時間為30 min時, 4種載體的吸附量均達到其對應最大吸附量的90%以上.可見,E1可以通過生物載體的初期吸附使其濃度迅速降低.李青松[7]在研究活性炭吸附去除水中的17α乙炔基雌二醇(EE2)時,也發現類固醇雌激素通過活性炭的初期吸附作用去除率可達50%以上.此外,在吸附平衡時間附近,吸附量會上下波動,部分載體吸附量甚至小幅下降,表明E1出現脫附現象.這種脫附現象可能是由于震蕩作用使某些結合不牢固的吸附位點處E1脫落,重新返回到溶液中,使載體吸附量降低;但隨著吸附時間的延長,E1不斷進入載體的內部孔徑,吸附逐漸達到飽和,最終吸附和解吸達到動態平衡,溶液中的E1溶度也趨于穩定.

圖1 不同生物載體對E1的吸附去除率隨時間的變化
2.2 E1吸附規律解析
表面吸附可以用Freundlich公式來描述[8],即

(1)
式中,qe為吸附平衡后物質在載體中的E1吸附量,μg/g;Ce為物質溶解于水相的濃度,μg/L;KF與1/n為Freundlich吸附常數.
溫度為25 ℃時不同E1初始濃度下4種生物載體對E1的Freundlich吸附等溫線擬合結果見表2.由表可知,4種生物載體對E1的吸附均符合Freundlich吸附模型,吸附模型的決定系數R2均達到了極顯著水平.活性炭、沸石和玉米芯對E1的吸附等溫方程參數中的1/n接近1,表明該過程是線性吸附,吸附為恒定的分配吸附機制;而竹炭對E1的吸附等溫方程參數中n=0.712,表明竹炭對E1的吸附是非線性吸附,這可能是因為竹炭的平均孔徑相對較大,對E1的吸附呈現出多層吸附.Fukuhara等[9]研究了活性炭對E1的吸附作用,發現在E1初始濃度為1 μg/L的條件下,吸附平衡時活性炭對其的吸附量為25.6~73.5 μg/g,并且吸附符合Freundlich 吸附模型.Fuerhacker等[10]研究了3種活性炭對E2的吸附特性,發現在不同濃度的E2溶液中,E2被快速吸附,50~180 min后達到吸附平衡;當初始濃度為1~100 ng/L時,平衡濃度為初始濃度的49%~81%,這與本文研究結果相似.

表2 Freundlich吸附等溫模型和相關參數
溶液中的吸附是一個較復雜的過程,吸附質從液相被吸附轉移到吸附劑顆粒中,可分為吸附劑周圍流體界膜中吸附質的遷移(外擴散)、吸附劑顆粒內擴散和吸附劑內的吸附反應等幾個過程[11].為了實現高效的SE吸附,傳質過程和吸附動力學分析十分重要.吸附過程中的擴散現象可以用顆粒內擴散模型進行解釋,顆粒內擴散模型通常適用于完全混合溶液,即
qt=kpt0.5
(2)
對于溶液中的吸附,常采用偽一級和偽二級動力學模型,即
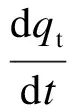
(3)
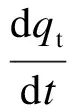
(4)
式中,kp為顆粒間速率常數,μg/(g·min0.5);k1為吸附偽一級反應速率常數,1/min;k2為吸附偽二級反應速率常數,μg/(g·min);t為吸附時間,min;qe,qt分別為吸附平衡、吸附時間為t時的載體吸附量,μg/g.
分別采用顆粒內擴散模型、偽一級和偽二級動力學模型對不同E1初始濃度下的活性炭吸附過程進行擬合,結果見表3.

表3 吸附動力學方程及相關參數
由表3可知,顆粒內擴散模型不能較好地描述活性炭對E1的吸附過程.顆粒內擴散動力學模型擬合的直線不經過原點,故顆粒內擴散不是控制活性炭吸附E1速率的唯一因素,吸附速率同時還受顆粒外擴散過程等因素影響,整個吸附過程是由多種動力學機理共同作用的結果.偽一級吸附動力學的決定系數R2均小于0.95,而偽二級吸附模型能夠較好地擬合活性炭對E1的吸附,不同E1初始濃度的動力學決定系數R2都大于0.99,因此偽二級吸附模型能夠較真實地反映E1在活性炭上的吸附機理,并且吸附速率常數K隨E1濃度增加而減小.這可能是由于E1的初始質量濃度越高,其分子之間相互碰撞的幾率越大,故E1與活性炭上的吸附點位結合所需的時間越長.李若愚等[12]分析顆粒活性炭對雙酚A的吸附行為也符合偽二級吸附模型,且吸附速率常數隨雙酚A初始濃度的增加而減小.
采用相同的方法研究了不同E1初始濃度下沸石、竹炭和玉米芯對E1的吸附傳質過程.結果表明,顆粒內擴散模型也不能較好地描述沸石、竹炭和玉米芯對E1的吸附過程,這可能是由于顆粒內擴散模型認為液膜擴散是可以忽略的[12],而實驗結果顯示生物載體對E1的初期吸附速率非常快,液相和固相之間較大的濃度差產生了液膜擴散,這與模型假設的液膜擴散可以忽略不符,因此顆粒內擴散模型不能用來描述整個吸附過程規律.另外,顆粒內擴散動力學模型擬合的直線不過原點這一現象也進一步證實,顆粒內擴散不是控制吸附速率的唯一因素[13].同樣,偽二級動力學模型能夠較真實地反映E1在沸石、竹炭和玉米芯上的吸附過程,說明生物載體對E1的吸附以化學吸附為主[14],并且吸附速率常數K均隨E1濃度增加而減小.
3 結論
1) 活性炭、沸石、竹炭和玉米芯4種生物載體對E1的吸附是一個快速過程,1 h左右即可達到吸附平衡,且吸附平衡時間受E1初始濃度影響較小.在E1初始濃度為1~500 μg/L的條件下,吸附30 min后,4種載體的吸附量均達到其對應最大吸附量的90%以上.
2) 4種生物載體中,活性炭、沸石和玉米芯的吸附能力均隨著E1初始濃度的增加而增加;竹炭對E1的吸附能力受E1初始濃度影響較小.
3) 不同E1初始濃度下,4種載體對E1的吸附均符合Freundlich吸附模型.活性炭、沸石和玉米芯對E1的吸附是線性吸附,竹炭對E1的吸附是非線性吸附.偽二級動力學模型能夠較好地描述4種生物載體對E1的吸附規律,且4種生物載體對E1的吸附速率常數均隨著E1初始濃度增加而減小.
)
[1] Johnson A C, Sumpter J P. Removal of endocrine-disrupting chemicals in activated sludge treatment works [J].EnvironmentalScience&Technology, 2001,35(24): 4697-4703.
[2] Liu Z H, Kanjo Y, Mizutani S. Removal mechanisms for endocrine disrupting compounds(EDCs) in wastewater treatment-physical means, biodegradation, and chemical advanced oxidation [J].ScienceoftheTotalEnvironment, 2009,407(2): 731-748.
[3] Butwell A J, Gardner M J, Gordon W S J, et al. Scoping study for a national demonstration program on EDC removal: report of UK WIR [R]. London: UK Water Industry Research, 2005.
[4] Yang X L, Li G P, Chen M, et al. Occurrence and removal of steroid estrogens in three sewage treatment plants in Nanjing, China [J].FreseniusEnvironmentalBulletin,2012,21(12): 3836-3841.
[5] 陽春, 胡碧波, 張智. 類固醇雌激素在生活污水處理中的去除過程[J]. 中國給水排水,2008,24(10): 11-15.
Yang Chun, Hu Bibo, Zhang Zhi. Removal of steroid estrogens during sewage treatment [J].ChinaWater&Wastewater, 2008,24(10): 11-15. (in Chinese)
[6] Zhou H, Huang X, Wang X, et al. Behaviour of selected endocrine-disrupting chemicals in three sewage treatment plants of Beijing, China[J].EnvironmentalMonitoringandAssessment, 2010,161(1/2/3/4): 107-121
[7] 李青松. 水中甾體類雌激素內分泌干擾物去除性能及降解機理研究[D]. 上海: 同濟大學環境科學與工程學院, 2007.
[8] Andersen H R, Hansen M, Kj?lholt J, et al. Assessment of the importance of sorption for steroid estrogens removal during activated sludge treatment [J].Chemosphere, 2005,61(1): 139-146.
[9] Fukuhara T, Iwasaki S, Kawashima M, et al. Adsorbability of estrone and 17β-estradiol in water onto activated carbon [J].WaterResearch, 2006,40(2): 241-248.
[10] Fuerhacker M, Düra S, Jungbauer A. Adsorption isotherms of 17β-estradiol on granular activated carbon(GAC) [J].Chemosphere, 2001,44(7): 1573-1579.
[11] 鐘倩倩, 岳欽艷, 李倩, 等.改性麥草秸稈對活性艷紅的吸附動力學研究[J]. 山東大學學報:工學版, 2011, 41(1): 133-139.
Zhong Qianqian, Yue Qinyan, Li Qian, et al. Kinetics of the adsorption of reactive brilliant red K-2BP onto modified wheat residue [J].JournalofShandongUniversity:EngineeringScience, 2011,41(1): 133-139. (in Chinese)
[12] 李若愚, 高乃云, 徐斌, 等. GAC對水中內分泌干擾物雙酚A的吸附特性及動力學研究[J]. 給水排水, 2007, 33(2): 13-19.
Li Ruoyu, Gao Naiyun, Xu Bin, et al. GAC adsorption characteristics and kinetics of EDCs-bisphenol A in water [J].Water&Wastewater, 2007,33(2): 13-19. (in Chinese)
[13] Azza K, Nemr A E, Amany E S, et al. Removal of direct N Blue-106 from artificial textile dye effluent using activated carbon from orange peel: adsorption isotherm and kinetic studies [J].JournalofHazardousMaterials, 2009,165(1/2/3): 100-110.
[14] Wan N W S, Kamari A, Koay Y J. Equilibrium and kinetics studies of adsorption of copper (Ⅱ) on chitosan and chitosan/PVA beads [J].InternationalJournalofBiologicalMacromolecules, 2004,34(3): 155-161.

