鈦對(duì)ZA35合金在堿溶液中電化學(xué)行為的影響
劉敬福,楊 光,崔 佳
(遼寧工程技術(shù)大學(xué) 材料科學(xué)與工程學(xué)院,阜新 123000)
0 引言
ZA 鋅合金具有優(yōu)良的力學(xué)性能和耐磨性能,可替代銅及銅合金作為礦山、冶金設(shè)備中的滑動(dòng)軸承、軸瓦和模具用材料[1]。此外,因其優(yōu)異的加工性能和較高的性價(jià)比,ZA 鋅合金在電子通訊、制鎖和廚衛(wèi)等領(lǐng)域中也有一定應(yīng)用。但是,ZA 鋅合金易因腐蝕導(dǎo)致老化失效,限制了其應(yīng)用領(lǐng)域[2-3]。為改善ZA 鋅合金的耐蝕性能,可通過添加合金元素及控制合金組織等途徑來實(shí)現(xiàn)[3-4]。在合金化元素中,鈦的加入可提高ZA 鋅合金的力學(xué)性能[4],但是關(guān)于鈦對(duì)ZA 鋅合金在堿液中電化學(xué)腐蝕行為影響的研究尚未見報(bào)道。而鋅合金特別是ZA 系鋅合金作為手機(jī)中堿性電池的負(fù)極材料、保護(hù)混凝土結(jié)構(gòu)(堿性)的犧牲陽極材料以及接觸堿液的廚房刀具材料在使用時(shí)常會(huì)與堿性介質(zhì)接觸。為此,作者通過電化學(xué)工作站測定不同含鈦量的ZA35合金在5%NaOH 溶液中的開路電位和極化曲線,分析鈦對(duì)ZA35合金在堿液中耐腐蝕性的影響規(guī)律,為其在實(shí)際工程應(yīng)用提供參考。
1 試樣制備與試驗(yàn)方法
試驗(yàn)用ZA35合金冶煉主要原材料為純鋅、純鎂和純鋁,合金元素銅和鈦分別以Al-50%Cu 和Al-10%Ti中間合金的形式加入,合金熔煉在井式電阻爐中進(jìn)行。熔煉過程:將井式電阻爐升溫至830 ℃后,按配比放入裝有鋁錠、兩種中間合金的坩堝,原料全部熔化后,溫度降為700℃時(shí),放入鋅錠;將經(jīng)預(yù)熱后用鋁箔包好的鎂壓入坩堝底部,用ZnCl2精煉去氣;精煉后扒渣在金屬型中澆注,將鑄錠線切割成φ25mm×100mm 圓柱體。4種試驗(yàn)合金的化學(xué)成分見表1。
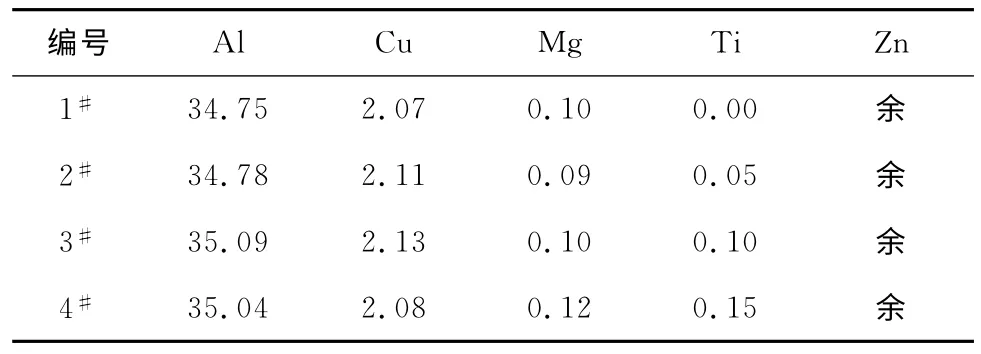
表1 試驗(yàn)合金的化學(xué)成分(質(zhì)量分?jǐn)?shù))Tab.1 Chemical compositions of test alloys(mass)%
在CS310型電化學(xué)工作站上測定試驗(yàn)合金的開路電位和極化曲線。采用常規(guī)的三電極體系,待測合金為工作電極,鉑電極為輔助電極,飽和甘汞電極為參比電極;腐蝕電位測量時(shí)間為30 min,掃描速率為2mV·s-1。
電化學(xué)試驗(yàn)介質(zhì)為質(zhì)量分?jǐn)?shù)5%的NaOH 溶液。開路電位值均是在堿液中浸泡50 min后穩(wěn)定的數(shù)值。合金弱極化時(shí)的極化曲線分析采用Corrtest軟件,得到相關(guān)參數(shù)。合金組織在日立S-3400N型掃描電鏡上觀察。
2 試驗(yàn)結(jié)果與討論
2.1 開路電位
試驗(yàn)合金在不同溫度NaOH 溶液中的開路電位均隨時(shí)間延長而略微正移,到30~40min后趨于穩(wěn)定。由圖1可以看出,隨著堿液溫度升高,合金的開路電位負(fù)移,溫度相同時(shí),添加鈦的2#,3#和4#合金開路電位均較未添加鈦的1#合金開路電位高,其中含0.1%鈦的3#合金開路電位最高。
開路電位可以反映合金在溶液中的溶解傾向。在腐蝕條件相同時(shí),合金電極開路電位值低表明其還原能力強(qiáng),易氧化溶解(1#合金),而合金電極開路電位值高表明其還原能力弱,不易被腐蝕(3#合金)。可以定性認(rèn)為,適量鈦加入可以改善ZA35合金的耐堿液腐蝕性。堿液溫度升高合金的開路電位數(shù)值都下降的原因是溫度升高,OH-活性也提高,與基體反應(yīng)加劇,氧化膜溶解迅速,電極反應(yīng)速率加快,導(dǎo)致腐蝕速率增加。溫度升高還能增強(qiáng)溶液之間的對(duì)流和擴(kuò)散,降低電解液電阻,減弱合金的鈍化行為,也使開路電位變負(fù)[5]。

圖1 試驗(yàn)合金在不同溫度NaOH 溶液中的開路電位Fig.1 Open-circuit potentials of test alloys in NaOH solution at different temperatures
2.2 極化曲線
由圖2可看出,試驗(yàn)合金在NaOH 介質(zhì)中的極化曲線呈不同的規(guī)律。當(dāng)電位掃描區(qū)間在-1.40~-1.20V 范圍時(shí),合金的陽極極化為活化極化,極化曲線存在明顯直線段;在-1.20 V 以上的范圍時(shí),合金發(fā)生鈍化。鋅合金在弱極化時(shí)活化溶解的腐蝕機(jī)理較復(fù)雜,電極反應(yīng)過程可能受到電子傳遞步驟和擴(kuò)散傳質(zhì)步驟等的控制[6];根據(jù)Zn-H2O 系電位-pH 圖,在弱極化區(qū)及pH >8的堿性環(huán)境中,材料處于不穩(wěn)定區(qū),是鋅合金陽極活化、鈍化轉(zhuǎn)變頻繁之處。此時(shí)鋅及鋅合金的耐蝕性主要取決于表面保護(hù)膜的性質(zhì),在5%NaOH 溶液中合金生成的腐蝕產(chǎn)物ZnO 比較疏松,易脫落,從而使陽極表面始終暴露在堿性溶液中,持續(xù)不斷地被腐蝕[7]。鋅合金在強(qiáng)極化時(shí)發(fā)生鈍化,是由于合金的陽極溶解產(chǎn)物與溶液中OH-反應(yīng),生成鋅酸根離子吸附在電極表面,進(jìn)一步以Zn(OH)2形式成膜,導(dǎo)致合金的鈍化[7-8]。由于試驗(yàn)合金中鋁元素含量很高,鋁與堿液反應(yīng)最終的腐蝕產(chǎn)物是Al2O3,會(huì)進(jìn)一步提高鈍化效果。
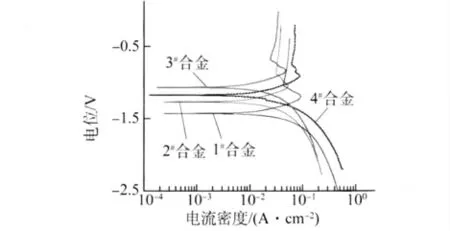
圖2 試驗(yàn)合金在NaOH 溶液中的極化曲線Fig.2 Polarization curves of test alloys in NaOH solution
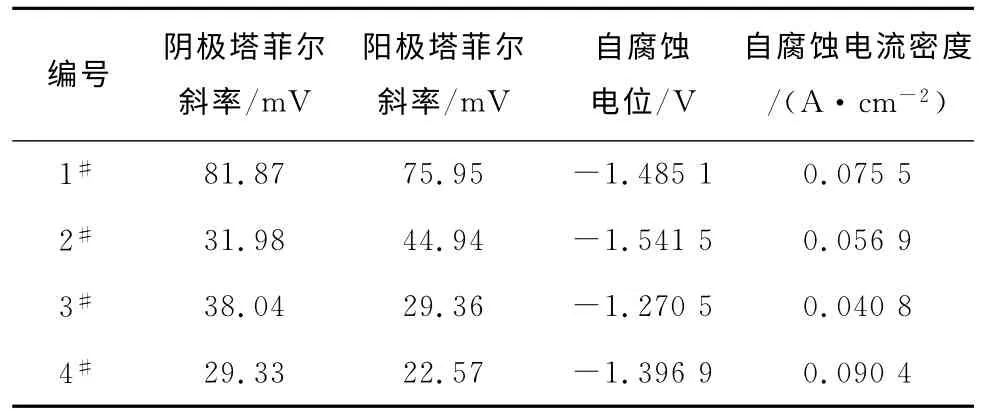
表2 試驗(yàn)合金極化曲線的擬合結(jié)果Tab.2 Fitted polarization curves of test alloys
利用Corrtest軟件計(jì)算出合金在弱極化時(shí)的腐蝕 參數(shù),結(jié)果見表2。由表2可知,隨鈦含量增加,合金的自腐蝕電位變化規(guī)律不明顯,而自腐蝕電流密度呈先下降后上升的變化規(guī)律。加入0.1%鈦的3#合金自腐蝕電位最大,自腐蝕電流密度最小,和未添加鈦的1#合金相比,自腐蝕電流密度下降了46%,體現(xiàn)為耐堿液腐蝕性能增強(qiáng)。由于影響因素多,合金的自腐蝕電位和自腐蝕電流密度之間不存在對(duì)應(yīng)關(guān)系。但加入0.1%鈦的3#合金和未添加鈦的1#合金相比,3#合金中η相和α相的陽極極化增大了,和合金中析出的富銅相等陰極相組成的腐蝕微電池相間電位差減小,因此腐蝕程度降低。進(jìn)一步增大鈦含量,合金組織中會(huì)有富鈦相析出,腐蝕微電池?cái)?shù)量增加,會(huì)惡化合金的耐蝕性,如4#合金,含鈦量為0.15%,自腐蝕電流密度比未加鈦的1#合金增加了19.7%。
合金在強(qiáng)極化時(shí)均進(jìn)入鈍化態(tài),由圖2 可知,1#~4#合金進(jìn)入較穩(wěn)定鈍化態(tài)時(shí)的自腐蝕電流密度依次為0.08,0.07,0.06,0.08 A·cm-2,添加0.1%鈦的3#合金在強(qiáng)極化時(shí)耐蝕性能也最好。
加入適量鈦可改善ZA35合金電化學(xué)性能與其顯微組織變化密切相關(guān)。由于與1#合金相比,3#合金耐電化學(xué)腐蝕性能最優(yōu),因此主要比較這兩種合金的組織,如圖3所示。
ZA35合金主要組成相為η 相、α 相和CuZn3相[9]。由圖3 可見,ZA35 合金組織的樹枝晶很發(fā)達(dá),初生α相的組織特征明顯,為方向性很強(qiáng)的樹枝狀。當(dāng)添加0.1%的鈦時(shí),合金己經(jīng)觀察不到明顯的枝晶方向性,晶粒變小,組織形態(tài)分布變得均勻,初生相顯得更細(xì)小分散。這是由于凝固時(shí),鈦以細(xì)小而均勻分布的Al3Ti相成為α-Al的結(jié)晶核心,二者具有良好的晶界共格關(guān)系,原子間的結(jié)合力大[4],以Al3Ti 為形核基底,促使晶粒得到細(xì)化。在NaOH 介質(zhì)中發(fā)生電化學(xué)腐蝕時(shí),ZA35 合金中的η-Zn相和α-Al相作為陽極溶解,形成具有保護(hù)特性的腐蝕產(chǎn)物Al2O3,保護(hù)基體。Al2O3阻塞晶界,阻止堿液進(jìn)一步滲入,晶粒越細(xì)小,阻塞作用越明顯。ZA35合金中加入0.1%的鈦后合金晶粒細(xì)化顯著,因此耐電化學(xué)腐蝕性能相應(yīng)提高。

圖3 1#和3#試驗(yàn)合金的顯微組織Fig.3 Microstructure of 1#(a)and 3#(b)test alloys
由圖4可以看出,1#合金表面有腐蝕產(chǎn)物脫落形成的蝕孔,3#合金表面的腐蝕產(chǎn)物分布連續(xù),只有輕微腐蝕坑,耐腐蝕能力明顯比1#合金強(qiáng),這也和電化學(xué)極化試驗(yàn)得到的結(jié)果相符合。

圖4 1#和3#試驗(yàn)合金的腐蝕表面形貌Fig.4 Morphology of corrosion surfaces of 1#(a)and 3#(b)test alloys
3 結(jié)論
(1)隨NaOH 溶液溫度升高,合金開路電位負(fù)移,加入0.1%Ti的ZA35合金的開路電位最高。
(2)在NaOH 溶液中,合金在弱極化時(shí)活化溶解,在強(qiáng)極化時(shí)發(fā)生鈍化;在弱極化時(shí)加入0.1%Ti的ZA35合金較未添加鈦的ZA35合金自腐蝕電流密度下降46%。
(3)在ZA35合金中添加0.1%的鈦后合金晶粒及枝晶細(xì)化效果明顯,是提高合金在堿液中耐腐蝕性能的重要原因。
[1]劉敬福,李榮德,王盈.噴射沉積ZA35-3.5%Mn合金力學(xué)和磨損性能[J].機(jī)械工程材料,2008,32(2):57-60.
[2]郝小軍,宋詩哲.鋁鋅合金在3%NaCl溶液中的電化學(xué)行為[J].中國腐蝕與防護(hù)學(xué)報(bào),2005,25(4):213-217.
[3]李逸泰,范鵬,曾建民,等.硅和錫對(duì)ZA27鋅基合金耐腐蝕性能的影響[J].機(jī)械工程材料,2006,30(12):27-29.
[4]郭亞希,謝敬佩,王文焱,等.Ti、B對(duì)ZA27合金組織及力學(xué)性能的影響[J].熱加工工藝,2009,38(5):39-40.
[5]舒方霞,王兆文,高炳亮,等.Al-In-Mg系鋁合金陽極在NaOH溶液中的電化學(xué)行為[J].輕合金加工技術(shù),2004,32(10):39-42.
[6]陳文汨,張利.鋅合金在KOH 溶液中腐蝕性能的研究[J].腐蝕與防護(hù),2000,21(11):485-487.
[7]楊熙珍,楊武.金屬腐蝕電化學(xué)熱力學(xué):電位-pH 圖及其應(yīng)用[M].北京:化學(xué)工業(yè)出版社,1991:106-107.
[8]王志林,章小鴿,林昌健,等.鋅-銦合金電極在濃KOH 溶液中的電化學(xué)行為[J].電化學(xué),2007,13(4):407-410.
[9]劉敬福,李榮德,謝懿,等.噴射成形高錳ZA35合金的工藝及組織研究[J].材料工程,2010(6):63-67.

