催化劑種類對液相氫還原法制備超細鎳粉的影響*
李博捷 ,趙家春 ,董海剛 ,,范興祥 ,,吳躍東 ,吳曉峰 ,劉 楊 ,童偉鋒
(1.貴研鉑業(yè)股份有限公司,云南昆明 650106;2.稀貴金屬綜合利用新技術國家重點實驗室;3.昆明貴金屬研究所)
鎳是一種具有磁性、導電性和較好化學穩(wěn)定性、高溫穩(wěn)定性、機械穩(wěn)定性的金屬。超細鎳粉具有一系列特殊效應及特殊性質,廣泛應用于金剛石工具、硬質合金、電工合金、屏蔽材料、電池材料等行業(yè)[1-4],市場需求量大[5-10]。超細鎳粉的制備方法主要有氣相法、液相法和固相法。氣相法包括羰基鎳分解法、蒸發(fā)-冷凝法、濺射法[11]。液相法包括多元醇法、水合肼還原法、氫還原法、聯(lián)氨還原法、電解法、草酸鎳熱分解法、微乳液相法等[12]。固相法主要為機械破碎法及金屬還原法等[13]。液相氫還原法操作簡單,成本較低,便于在工業(yè)上推廣,加之近年來高壓設備逐漸成熟,該方法具有較為廣闊的應用前景。氫還原法制備超細鎳粉需要使用催化劑來保證鎳的還原效果。因此,筆者擬以工業(yè)硫酸鎳為主要原料,研究不同種類及濃度的催化劑對液相氫還原法制備超細鎳粉的作用效果,以期獲得適宜的催化劑類型,從而優(yōu)化硫酸鎳液相氫還原法制備超細鎳粉的工藝。
1 實驗部分
1.1 實驗原料與試劑
工業(yè)硫酸鎳[(NiSO4·6H2O),w(Ni)≥22.2%];氫氧化鈉,分析純;瓶裝工業(yè)氫[w(H2)≥99.95%];瓶裝工業(yè)氮[w(N2)≥99.2%];催化劑:RuCl3·3H2O、PdCl2、蒽醌,均為分析純;活性鎳粉[w(Ni)≥99.5%]。
1.2 反應過程分析
將綠色NiSO4·6H2O晶體加水溶解,加入NaOH溶液攪拌調漿后生成含氫氧化鎳和硫酸鈉的漿液,反應過程:
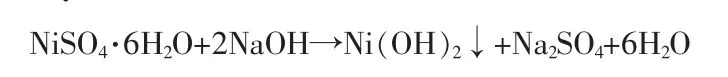
含氫氧化鎳和硫酸鈉漿液氫還原制備超細鎳粉的過程可按下式表示:
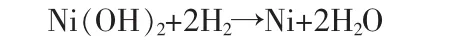
1.3 研究方法
將硫酸鎳加水溶解,加入堿溶液后調漿攪拌。分別加入活性鎳粉、PdCl2、RuCl3及蒽醌等4種催化劑調配。將調配好的溶液移至3 L高壓釜內,密封高壓釜后用氮氣將釜內空氣置換除去,升溫至預定溫度后,使用液相通氫的方法使高壓釜內壓力升至預定壓力,進行液相氫還原反應。反應結束后,降溫泄壓,取出反應產物,使用真空泵、抽濾漏斗過濾,烘干。采用X射線衍射和化學分析,分析所得粉末中的氧含量,計算出未還原氫氧化鎳的含量和還原率,對比使用不同催化劑在不同反應時間下鎳粉的還原率。圖1為該工藝的流程示意圖。
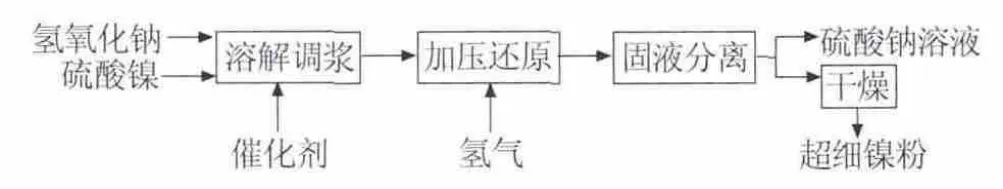
圖1 超細鎳粉制備工藝流程示意圖
2 實驗結果與討論
2.1 與不加催化劑的對比實驗
實驗控制反應條件為溫度90℃,保持壓力為3.8 MPa。為與后續(xù)實驗對比,在無催化的條件下進行液相加氫還原反應作為空白實驗。圖2為無催化劑實驗與2 mg/L的PdCl2作為催化劑在不同時間下對鎳還原率的影響。由圖2可以看出,在不加入催化劑的條件下,反應100 min后,鎳還原率僅為25%左右;使用2 mg/L的PdCl2作為催化劑進行實驗,鎳還原率明顯提高。因此為縮短反應時間,提高單位時間內Ni(OH)2的還原率,需添加催化劑以促進液相氫還原反應的進行。
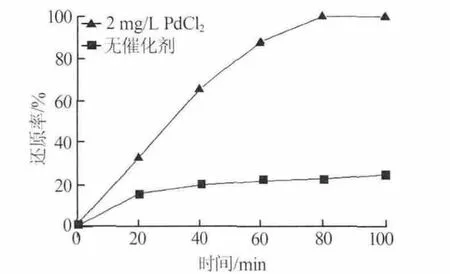
圖2 無催化劑及催化劑下鎳還原率與時間的關系
2.2 活性鎳粉的影響
活性鎳粉擁有尺寸小、比表面積大、表面活性位多等特點,現(xiàn)已成為一種新型的高效催化劑。實驗使用活性鎳粉作為液相加氫還原反應催化劑,考察了不同濃度活性鎳粉對氫氧化鎳還原率的影響,結果見圖3。由圖3可以看出,使用活性鎳粉作為催化劑有一定的催化效果,配料時加入25 g/L活性鎳粉催化劑,反應100 min時得到的鎳還原率最高(72%),但仍有部分 Ni(OH)2未被還原。
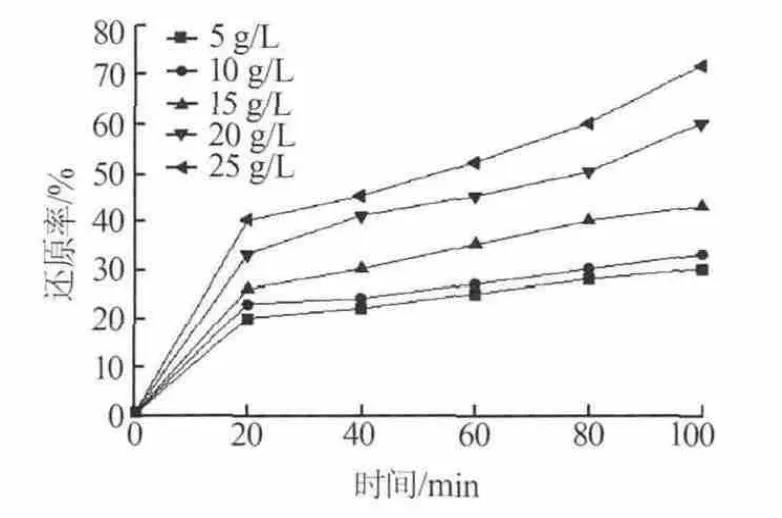
圖3 不同濃度活性鎳粉催化劑下還原率與時間的關系
2.3 RuCl3的影響
RuCl3作為均相反應催化劑被廣泛應用。實驗采用RuCl3作為超細鎳粉制備液相加氫加壓還原反應的催化劑,考察了不同濃度的RuCl3對Ni(OH)2還原率的影響,結果見圖4。由圖4可以看出,在RuCl3催化劑作用下,液相氫還原超細鎳粉的反應過程中還原率有所提高,但相比未使用催化劑時反應還原率提高不大,無法使Ni(OH)2在100 min內還原完畢。
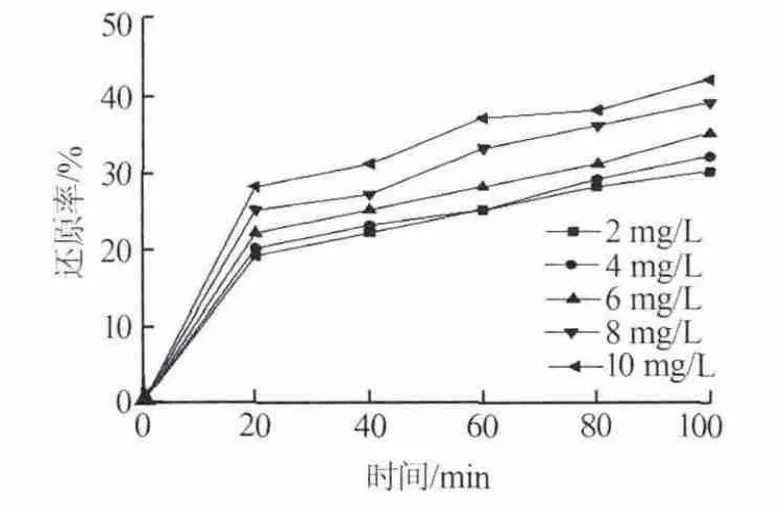
圖4 不同濃度RuCl3下鎳還原率與時間的關系
2.4 蒽醌的影響
蒽醌是一種優(yōu)良的水熱加氫還原制備鎳粉的催化劑,它與H2反應生成氫化蒽醌,并在前期反應所得的Ni(OH)2表面形成活化點,隨即反應形成鎳粉,同時氫化蒽醌反應生成蒽醌,并進行反復反應,直至全部Ni(OH)2還原為鎳粉。實驗考察了不同濃度的蒽醌對Ni(OH)2還原率的影響,結果見圖5。由圖5可以看出,使用蒽醌作為催化劑,鎳還原率得到了明顯提升。當蒽醌質量濃度為10 g/L時,反應80 min時溶液中的Ni(OH)2即幾乎全部被還原為鎳粉。
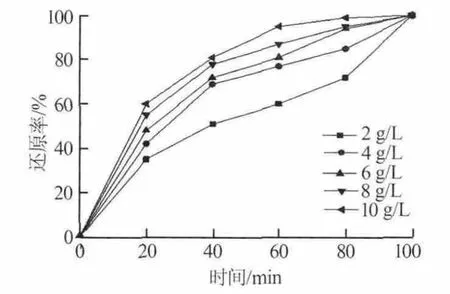
圖5 不同濃度蒽醌催化劑下鎳還原率與時間的關系
2.5 PdCl2的影響
單質Pd具有吸附氫氣的特性,氫氣在Pd表面裂解成氫原子,氫原子具有很強的反應活性,當PdCl2溶液與氫氣接觸,只要有微量的Pd生成,短時間內就可以吸附氫氣,再將氫氣裂解成氫原子,氫原子反應效率遠大于氫氣分子,促使鎳粉液相氫還原反應速率加快,達到催化反應的效果。實驗采用PdCl2作催化劑進行調漿配料,考察了不同濃度的PdCl2對 Ni(OH)2還原率的影響,結果見圖 6。由圖 6可以看出,使用PdCl2作為催化劑,在相同時間下,鎳還原率都得到了明顯提高,尤其在PdCl2質量濃度為10 mg/L、反應時間為50 min時,鎳還原率基本已達到100%。
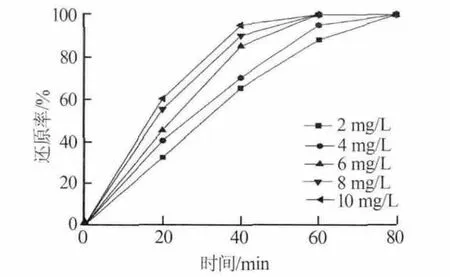
圖6 不同濃度PdCl2催化劑下還原率與時間的關系
通過對比實驗可知,活性鎳粉、PdCl2、RuCl3及蒽醌等4種催化劑都可對硫酸鎳液相氫還原制備超細鎳粉反應起到一定的催化作用;采用活性鎳粉及RuCl3作為催化劑時,反應100 min后仍有部分Ni(OH)2未能被還原;而采用蒽醌及PdCl2作為催化劑時,單位時間內還原率提高明顯。當催化劑蒽醌質量濃度為10 g/L時,反應基本在80 min左右時結束。當PdCl2質量濃度為10 mg/L時,反應基本在50 min左右時結束。對比可知,4種催化劑中PdCl2的效果最好,效率最高。
3 結論
通過研究催化劑對液相氫還原反應的影響,得到結論:1)添加催化劑調漿可以促進液相氫還原反應的進行,縮短反應時間,提高單位時間內Ni(OH)2漿液還原成金屬鎳粉的還原率;2)對比活性鎳粉、PdCl2、RuCl3及蒽醌這4種催化劑,使用質量濃度為10 mg/L的PdCl2作為催化劑進行配料時,可以使硫酸鎳液相氫還原反應制備超細鎳粉在最短時間內得到最大的還原率。
[1]牛明勤,吳介達.超細鎳粉的制備進展[J].精細化工,2003,20(12):715-717.
[2]Hou Y,Kondoh H,Ohta T,et al.Size-controlled synthes is of nickel nanoparticles[J].Appl.Sur.Science,2005,241(1/2):218-222.
[3]龔紅春,田俊濤,吳志申,等.磁場對超細鎳粉的磁性能及電磁屏蔽性能的影響[J].無機化學學報,2008,24(6):964-970.
[4]伍賀東,陳為亮,孟德龍,等.超細鎳粉制備技術研究進展[J].冶金叢刊,2007(1):37-41.
[5]陳立寶,賀躍輝,鄧意達.鎳鈷粉末生產現(xiàn)狀及發(fā)展趨勢[J].粉末冶金技術,2004,22(3):173-177.
[6]Cho H J,Choi G M.Fabrication and characterization of Ni-supported solid oxide fuel cell[J].Solid State Ionics,2009,180(11/12/13):792-795.
[7]田俊濤,龔春紅,余來貴,等.超細鎳粉/微米鎳粉復合電磁屏蔽涂料的研究[J].功能材料,2008,39(10):1615-1617.
[8]Kim M H,Hong M Z,Kim Y S,et al.Cobalt and cerium coated Ni powder as a new candidate cathode material f or MCFC [J].Electrochimica Acta,2006,51(27):6145-6151.
[9]劉紅,丁培培,菅盤銘.納米鎳粉的固相合成及其催化活性研究[J].工業(yè)催化,2007,15(1):67-70.
[10]Zhang Haijun,Liu Yun,Jia Quanli,et al.Fabrication and micromicrowave properties of Ni hollow powders by electroless plating and template removing method[J].Powder Technology,2007,178(1):22-29.
[11]孫偉民,金壽日,楊賀.合金法制備鎳超微粉[J].沈陽工業(yè)大學學報,1997,19(6):55-60.
[12]喻克寧,胡嗣強,毛銘華,等.Ni(OH)2水熱氫還原制備超細Ni粉[J].材料研究學報,1995,9(3):223-227.
[13]韋欽,劉雄飛,曹建,等.納米Ni的制備與微觀結構[J].中南礦冶學院學報,1994,25(1):137-139.

