微波水熱法制備二氧化錳/石墨烯復合材料
陳 仲,李建玲,陳 宇
(北京科技大學冶金與生態工程學院,北京 100083)
微波水熱法制備二氧化錳/石墨烯復合材料
陳 仲,李建玲,陳 宇
(北京科技大學冶金與生態工程學院,北京 100083)
用微波水熱法,以乙醇作為還原劑,在60℃下加熱4 h,一步制備二氧化錳(MnO2)/石墨烯復合材料。通過 XRD、場發射掃描電子顯微鏡(FESEM)和透射電鏡(TEM)等方法對產物進行分析,發現MnO2較好地分散在石墨烯表面。通過循環伏安和恒流充放電研究了產物的電化學性能:以100 mA/g的電流在0~0.8 V(vs.SCE)循環,制備的MnO2/石墨烯復合材料在1 mol/L的Li2SO4中的比電容為195 F/g。
石墨烯; 復合材料; 超級電容器材料; 二氧化錳(MnO2)
二氧化錳(MnO2)的制備方法簡單、價格低廉及對環境友好[1],可作為貴金屬氧化物二氧化釕(RuO2)的替代品,用作超級電容器電極材料。MnO2電極的電化學工作窗口較寬、比電容較高,是相關研究的重要方向。石墨烯的厚度只有0.335 nm,比表面積可達 2 650 m2/g[2],相應的比電容為550 F/g。石墨烯具有優異的電學、光學、力學、熱學和化學特性,在傳感器、儲能器件和微電子器件等方面應用廣泛[3]。
制備相關石墨烯與MnO2的復合材料的方法,大多分為兩步:先制得石墨烯,再通過相關的反應制取復合材料[4]。本文作者采用較簡單且環保的方法,將氧化石墨和KMnO4的混合液經乙醇還原,制備MnO2/石墨烯的復合材料,將制備的復合材料制成超級電容器電極,用恒流充放電、循環伏安測試和交流阻抗測試了其電化學性能。
1 實驗
1.1 樣品的制備和分析
采用改進的Hummer法制備氧化石墨:將1 g鱗片石墨(青島產)加到溶有 1 g硝酸鈉(國藥集團,AR)的23 ml濃硫酸(國藥集團,AR)中,攪拌均勻,再緩慢加入3 g高錳酸鉀(國藥集團,AR),控制溶液溫度不超過20℃,反應90 min;再升溫至35℃,恒溫反應90 min之后,緩慢加入40 ml去離子水,升溫至 95℃,繼續反應 30 min;加入 5 ml 30%H2O2(國藥集團,AR),溶液變為棕黃色,用5%稀鹽酸(國藥集團,AR)和去離子水交替洗滌至無SO42-,最后在60℃下真空(真空度為-0.1 M Pa,下同)干燥48 h,制備氧化石墨。
將1.583 4 g(約0.01 mol)高錳酸鉀溶于70 ml去離子水中,加入78.8 mg氧化石墨,超聲分散1 h,然后加入50 ml乙醇(國藥集團,AR),攪拌均勻后,在微波反應釜中、60℃下微波加熱4 h,用蒸餾水過濾、洗滌數次,最后在80℃下真空干燥12 h,制備MnO2/石墨烯復合材料。
用Zeiss SuprATM 55場發射掃描電子顯微鏡(FESEM,德國產)和 Tecnai G2 F20透射電子顯微鏡(TEM,美國產)對樣品進行形貌觀察;用MXP21 VAHF X射線衍射分析儀(日本產)對樣品進行物相分析,Cu靶,λ=0.154 06 nm,管壓40 kV 、管流 30 mA,掃描速度為 5(°)/min,步長為 0.02°。
1.2 電化學性能測試
將質量比7∶2∶1的活性物質、導電劑Super P(錦州產,電池級)和粘結劑聚偏二氟乙烯(錦州產,電池級)在 N-甲基-2-吡咯烷酮(國藥集團,CP)中混合均勻,制備漿料,再涂覆在1 cm×1 cm的泡沫鎳(錦州產)集流體上,于 80℃下真空干燥8 h,制備成工作電極(約含7 mg活性物質)。
以飽和甘汞電極為參比電極,鉑片為對電極,用三電極體系,分別以1 mol/L Na2SO4(國藥集團,AR)和 1 mol/L Li2SO4(國藥集團,AR)兩種中性溶液為電解液,在VMP2電化學工作站(美國產)上進行電化學性能測試。恒流充放電的電位均為0~0.8 V(vs.SCE),電流分別為 100 mA/g、200 mA/g和500 mA/g;循環伏安測試的掃描速度分別為10 mV/s、20 mV/s和50 mV/s;交流阻抗譜(EIS)測試的頻率為100 kHz~ 10 mHz。
2 結果與討論
2.1 結構和形貌
圖1為氧化石墨、石墨烯和復合材料的XRD圖。
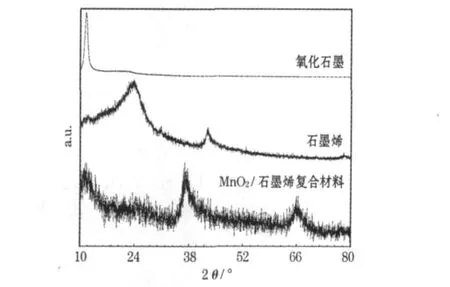
圖1 氧化石墨、石墨烯和復合材料的XRD圖Fig.1 XRD patterns of graphite oxide,graphene and the composite
從圖1可知,所制備的復合材料在13°、37°和 66°處出現了較明顯的MnO2特征峰(JCPDS:18-802),分別對應于M nO2的(002)、(006)和(119)晶面;在 24°左右出現了較弱的(002)衍射峰,表明氧化石墨還原成石墨烯還不很完全,原因是乙醇為弱還原劑,反應所得產物有較多的含氧官能團。
復合材料的FESEM圖和TEM圖分別為圖2和圖3。

圖2 復合材料的FESEM圖Fig.2 Field emission scanning electron microscopy(FESEM)photographs of the composite
從圖2a和圖2b可知,復合材料為顆粒狀,粒度不均勻,并有團聚。

圖3 復合材料的TEM圖Fig.3 Transmission electron microscope(TEM)photograph of the composite
從圖3可知,MnO2顆粒較好地分散在片狀石墨烯的表面,片狀石墨烯形成一個相互連接的結構,在增強復合材料的導電性的同時,有利于陰陽離子的擴散和吸脫附。
2.2 電化學性能
圖4是復合材料的恒流測試充放電曲線。
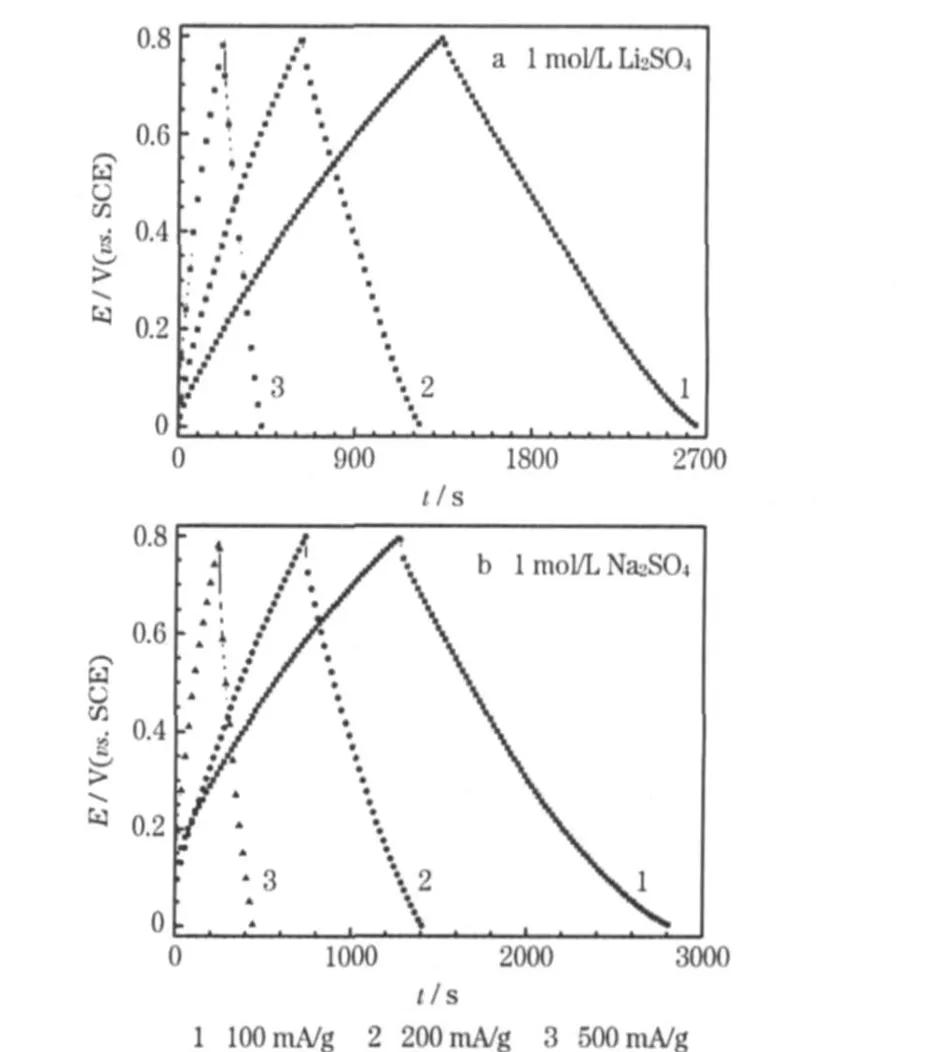
圖4 復合材料的恒流充放電曲線Fig.4 Glavanostatic charge/discharge curves of the composite
從圖4可知,充放電曲線呈現出較好的三角形對稱,表現出良好的充放電效率。根據圖4的數據,由式(1)計算活性物質的比電容Cm。

式(1)中:I為充放電電流(A);t為充放電持續的時間(s);m為電極活性物質的質量(g);ΔU為充放電電壓差(V)。計算可知,當電流為100 mA/g、200 mA/g和500 mA/g時,活性物質在1 mol/L Li2SO4中的比電容分別為195 F/g、166 F/g和126 F/g,在 1 mol/L Na2SO4中的比電容分別為165 F/g、150 F/g和123 F/g,與在Na2SO4溶液中相比,在電流較小(100 mA/g以下)時,復合材料電極在Li2SO4溶液中的比電容較高,可能是由于Li+擴散系數大于Na+擴散系數,影響傳質的速度;且Li+半徑比Na+的小,周圍可以吸引更多的水分子。
復合材料的循環伏安曲線見圖5。
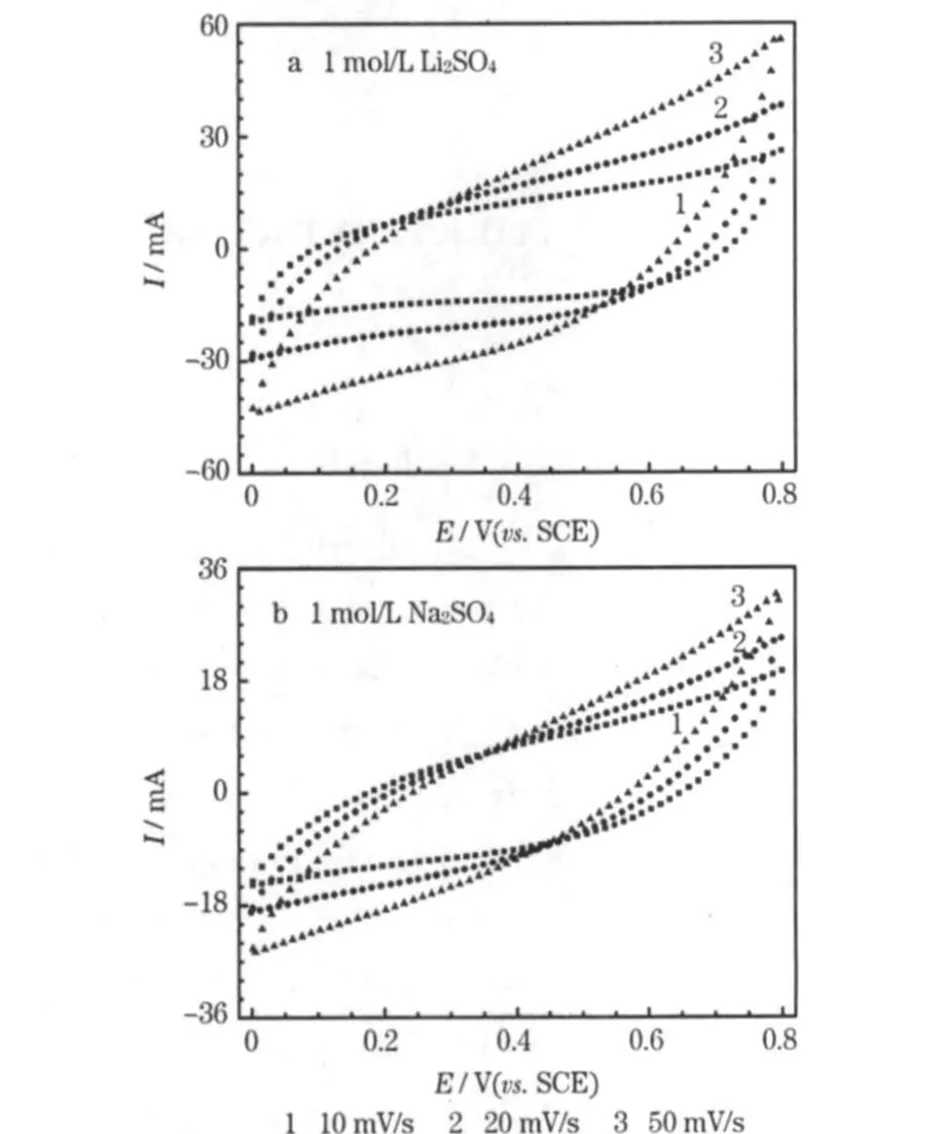
圖5 復合材料的循環伏安曲線Fig.5 CV curves of the composite
從圖5可知,在 1 mol/L Li2SO4和 1 mol/L Na2SO4中,復合材料的循環伏安曲線呈近似矩形對稱,在端電位電勢方向時的電流響應很快,顯示出材料有較好的電容行為;且在相同的掃描速度下,在Li2SO4中有更高的比電容。
復合材料的交流阻抗譜見圖6。
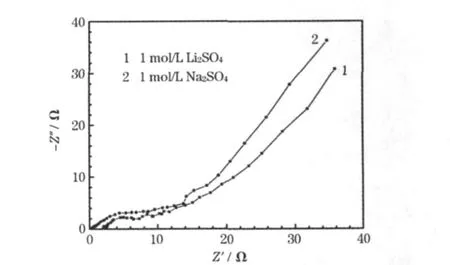
圖6 復合材料的交流阻抗譜Fig.6 A.C.impedance plots of the composite
圖6中,高頻區的半圓表示電極與電解液界面的電化學阻抗;中低頻區表現為明顯的Warburg特征 45°斜線,體現出電解液在電極內的響應轉變為擴散控制;高頻區半圓圓弧越大,說明電極材料的阻抗越大。從圖6可知,復合材料制備的電極在1 mol/L Na2SO4中的阻抗比在1 mol/L Li2SO4中大,與恒流充放電計算出的復合材料的比電容對應。
3 結論
本文作者采用微波加熱,在60℃下處理4 h,一步還原制得MnO2/石墨烯復合材料,并在不同電解液中測試了產物的電化學性能。
在電解液1 mol/L Li2SO4中,復合材料的比電容較高,在電流為100 mA/g時為195 F/g;在電解液1 mol/LNa2SO4中,相同條件下的比電容為165 F/g。這可能是由于Li+擴散系數大于Na+擴散系數,影響傳質的速度,且Li+的半徑比Na+的小,周圍可吸引更多的水分子。
[1] ZHANG Fei(張菲),HU Hui-li(胡會利),GAO Peng(高鵬).超級電容器用過渡金屬氧化物的研究進展[J].Battery Bimonthly(電池),2009,39(5):291-293.
[2] Chae H K,Siberio-Perez D Y,Kim J,et al.A route to high surface area,porosity and inclusion of large molecules in crystals[J].Nature,2004,427(6 974):523-527.
[3] Du X,Skachko I,Barker A,et al.Approaching ballistic transport in suspended grapheme[J].Nature Nanotechnology,2008,3(8):491-495.
[4] Yan J,Fan Z J,Wei T,et al.Fast and reversible surface redox reaction of graphene-MnO2composites as supercapacitor electrodes[J].Carbon,2010,48(13):3 825-3 833.
Preparating manganese dioxide/graphene composite by microwave-hydrothermal method
CHEN Zhong,LI Jian-ling,CHEN Yu
(School of Metallurgical and Ecological Engineering,University of Science and Technology Beijing,Beijing100083,China)
Manganese dioxide(MnO2)/graphene was prepared via one step by microwave-hydrothermal method at 60℃for 4 h with alcohol as reductant.The product was analyzed by XRD,field emission scanning electron microscopy(FESEM)and transmission electron microscope(TEM).It was found that M nO2was well dispersed on the surface of graphene.The electrochemical performance of product was studied by cyclic voltammetry and galvanoststic charge-discharge.When cycled in 0~0.8V(vs.SCE)with the current of 100 mA/g,the specific capacitance of prepared MnO2/graphene composite in 1 mol/L Li2SO4was 195 F/g.
graphene; composite; supercapacitor material; manganese oxide(MnO2)
TM533
A
1001-1579(2013)01-0015-03
陳 仲(1987-),男,湖北人,北京科技大學冶金與生態工程學院碩士生,研究方向:超級電容器電極材料;
李建玲(1971-),女,河北人,北京科技大學冶金與生態工程學院教授,研究方向:新能源材料,本文聯系人;
陳 宇(1987-),男,吉林人,北京科技大學冶金與生態工程學院碩士生,研究方向:鋰離子電池材料。
新世紀優秀人才支持計劃(NCET-09-0215)
2012-08-29

