α-硫辛酸聯合甲鈷胺治療糖尿病周圍神經病變的臨床觀察
葉飛 朱亭
糖尿病周圍神經病變(diabetic peripheral neuropathy,DPN)是糖尿病最常見的并發癥,多為對稱性表現,下肢重于上肢,表現為指端感覺異常,往往伴有感覺過敏、疼痛,后期可出現運動神經受累,肌力減低甚至肌萎縮和癱瘓[1],危害性大。本研究收集了在我科住院的2型糖尿病合并周圍神經病變患者78例,觀察α-硫辛酸聯合甲鈷胺治療DPN的療效。
1 資料與方法
1.1 一般資料 選擇在我科自2009年10月至2011年10月住院的2型糖尿病合并周圍神經病變患者78例,臨床表現主要為四肢麻木疼痛及感覺異常。將患者隨機分為觀察組和對照組,每組各39例,觀察組男19例,女20例,對照組男17例,女22例,2組患者肝腎功能均正常,且在年齡、性別比例、病程、空腹血糖(FBG)水平、糖化血紅蛋白(HbA1c)方面比較無統計學差異(P>0.05),具有可比性。見表1。
表1 2組治療前一般資料比較±s,n=39)
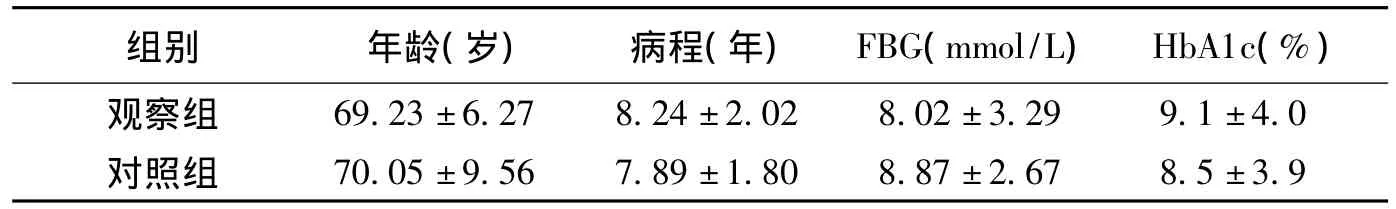
表1 2組治療前一般資料比較±s,n=39)
組別 年齡(歲) 病程(年) FBG(mmol/L) HbA1c(%)69.23±6.27 8.24±2.02 8.02±3.29 9.1±4.0對照組觀察組70.05±9.56 7.89±1.80 8.87±2.67 8.5±3.9
1.2 入組標準 參考美國糖尿病協會(ADA)診斷標準[2],同時符合以下標準的患者入組:(1)四肢感覺異常;(2)膝腱反射減弱或消失;(3)神經電生理檢查顯示:下肢運動神經傳導速度減弱;(4)排除其他周圍神經病變;(5)排除肝腎功能異常;(6)妊娠或哺乳期婦女;(7)征得患者本人或家屬同意。
1.3 方法
1.3.1 治療方法:2組患者住院后測定血糖水平,根據FBG情況予以短效胰島素控制血糖,調整胰島素用量,控制FBG<7.0 mmol/L,餐后血糖 <10.0 mmol/L。觀察組予以α-硫辛酸600 mg+生理鹽水250 ml,靜脈滴注,每日1次,同時予以甲鈷胺1000 μg,靜脈推注,每日 1 次,療程為 2周。對照組:單純予以甲鈷胺1000 μg,靜脈推注,每日1次,療程為2周。
1.3.2 觀察指標及療效判斷標準:觀察指標:分別于治療前后測定FBG、肝腎功能,檢測正中神經、腓總神經、脛神經運動神經傳導速度(motor nerve conduction velocity,MCV)、感覺神經傳導速度(sensory nerve conduction velocity,SCV)的變化。療效判斷標準:(1)顯效:自覺癥狀明顯好轉或消失,腱反射基本恢復正常,MCV和SCV較治療前加快>5 ms或恢復正常;(2)有效:自覺癥狀明顯減輕,腱反射未完全恢復正常,MCV和SCV較治療前加快3~5 ms;(3)無效:自覺癥狀無減輕或加重,腱反射無改善,MCV和SCV無變化。總有效率=顯效率+有效率[3]。
1.4 統計學方法 采用SPSS 13.0進行統計學分析,計量資料采用均數±標準差±s)表示,組間比較采用 t檢驗;計數資料采用百分率表示,組間比較采用卡方檢驗,以P<0.05為差異有統計學意義。
2 結果
2.1 2組治療前后運動和感覺神經傳導速度比較 治療前2組MCV和SCV差異無統計學意義(P<0.05)。治療2周后2組MCV和SCV均較治療前顯著提高,差異均有統計學意義(P<0.05),觀察組在治療后MCV和SCV均高于對照組(P<0.05)。見表2。
表2 2組治療前后運動和感覺神經傳導速度比較±s,ms,n=39)
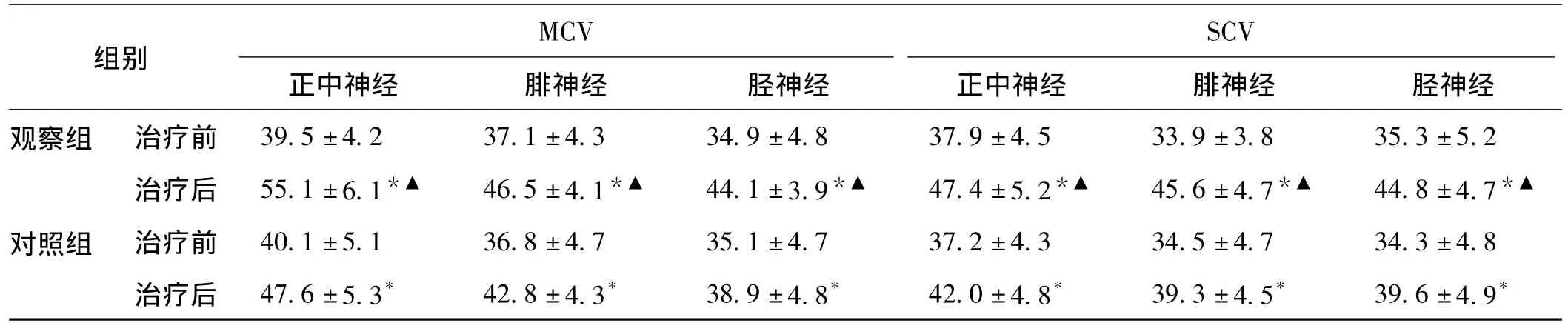
表2 2組治療前后運動和感覺神經傳導速度比較±s,ms,n=39)
注:與治療前比較,*P<0.05;與對照組比較,▲P<0.05
MCV SCV正中神經 腓神經 脛神經 正中神經 腓神經 脛神經觀察組 治療前 39.5±4.2 37.1±4.3 34.9±4.8 37.9±4.5 33.9±3.8 35.3±5.2治療后 55.1±6.1*▲ 46.5±4.1*▲ 44.1±3.9*▲ 47.4±5.2*▲ 45.6±4.7*▲ 44.8±4.7組別*▲對照組 治療前 40.1±5.1 36.8±4.7 35.1±4.7 37.2±4.3 34.5±4.7 34.3±4.8治療后 47.6±5.3* 42.8±4.3* 38.9±4.8* 42.0±4.8* 39.3±4.5* 39.6±4.9*
2.2 2組療效比較 觀察組顯效26例,有效 11例,無效 2例,總有效率達94.87%;對照組顯效17例,有效7例,無效15例,總有效率為62.53%,2組相比,觀察組明顯高于對照組,差異有統計學意義(P<0.01)。
2.3 不良反應 有2例患者在輸注過程中感覺局部疼痛,放慢輸注速度后,疼痛癥狀消失。所有入選患者治療前后肝腎功能均正常。
3 討論
DPN為2型糖尿病最為常見的并發癥,其發病機制尚不明確,目前認為高血糖性代謝紊亂、微血管疾病、神經因子減少是其主要相關因素[4-5]。此外,血糖長期過高,神經末梢組織氧供給不足,高血糖激活多元醇通路,神經細胞內山梨醇的含量增加,氧化應激增強,自由基形成過多,體內高血糖和高氧化狀態是末梢神經組織損傷,脫髓鞘變性的主要病因[6]。因而對于DPN的治療,應在控制血糖的基礎上營養神經和改善氧化應激。
α-硫辛酸是一種水溶性或脂溶性的代謝抗氧化物,是丙酮酸脫氫酶的輔助因子,在體內可轉化成二氫硫辛酸,清除多種氧化應激產物,螯合重金屬離子,再生成還原性谷胱甘肽、維生素C、維生素E、硫氧化蛋白等其他抗氧化劑,進一步清除生理和病理過程中產生的各種自由基[7-8]。研究表明,α-硫辛酸能夠抑制細胞中過氧化物誘導的核因子激活,下調細胞黏附因子-1(ICAM-l)、血管細胞黏附分子-1(VCAM-l)的表達,抑制炎癥反應,營養周圍神經[9]。此外,α-硫辛酸強大的抗氧化效應,能夠逆轉或阻斷各種途徑的氧化反應,作用于發病機制的上游途徑,直接減少超氧化物的生成,對抗高血糖誘發的氧化應激,改善微循環狀態,從而增加神經營養血管的血流量,治療DPN[10]。
甲鈷胺是甲基維生素B12的衍生物,參與體內甲基轉移,促進神經細胞的核酸、蛋白質和脂質代謝,并參與神經組織軸突結構蛋白的合成及受傷神經纖維的修復。能夠促進髓鞘的形成和軸突的再生,促進損傷的髓鞘修復,改善神經傳導速度[11]。
在我們的觀察中,α-硫辛酸和甲鈷胺聯合治療DPN,2周后運動和感覺神經的傳遞速度明顯提高,患者的自主癥狀有顯著好轉,相對于單純應用甲鈷胺效果明顯。這提示我們,氧化應激在DPN的發生發展中可能起著關鍵的作用,抗氧化應激治療可能成為治療DPN新的靶點。而α-硫辛酸與甲鈷胺聯合應用,不僅阻止了神經細胞的進一步損傷,而且還促進神經細胞的修復,對DPN有著顯著的效果,值得臨床推廣。
[1]Pinzur MS.Diabetic peripheral neuropathy[J].Foot Ankle Clin,2011,16(2):345-349.
[2]寧光.糖尿病周圍神經病變研究進展[J].中國實用內科雜志,2007,27(7):487-489.
[3]李靜.糖尿病周圍神經病變藥物治療進展[J].藥學與臨床研究,2011,19(1):51-54.
[4]Morales-Vidal S,Morgan C,McCoyd M,et al.Diabetic peripheral neuropathy and the management of diabetic peripheralneuropathic pain[J].Postgrad Med, 2012, 124(4):145-153.
[5]樊華,戎娟.老年2型糖尿病合并大血管病變患者血液流變學指標臨床觀察[J].實用老年醫學,2011,25(6):513-515.
[6]Tesfaye S,Selvarajah D.Advances in the epidemiology,pathogenesis and management of diabetic peripheral neuropathy[J].Diabetes Metab Res Rev,2012,28(1):8-14.
[7]辛月穎.α-硫辛酸治療糖尿病周圍神經病變的療效觀察[J].中國現代醫生,2009,47(34):45-46.
[8]谷雪靜,王燕,樊海英.α-硫辛酸治療2型糖尿病周圍神經病變22例療效觀察[J].實用老年醫學,2012,26(1):47-49.
[9]Stevens MJ,Obrosova I,Cac X,et al.Effects of alpha-lipoic acid on peripheral nerve conduction,blood flow,energy metabolism and oxidative stress in experimental diabetic neuropathy[J].Diabetes,2009,49(6):1006-1115.
[10]Han T,Bai J,Liu W,et al.A systematic review and meta-analysis of α-lipoic acid in the treatment of diabetic peripheral neuropathy[J].Eur JEndocrinol2012,167(4):465-471.
[11]Miranda-Massari JR,Gonzalez MJ,Jimenez FJ,et al.Metabolic correction in the management of diabetic peripheral neuropathy: improving clinical results beyond symptom control[J].Curr Clin Pharmacol,2011,6(4):260-273.

