HPLC法測定地奧司明原料藥及片劑的含量和有關物質
趙 喆,唐素芳(天津市藥品檢驗所,天津 300070)
地奧司明臨床上用于治療與靜脈、淋巴功能不全相關的各種疾病(如靜脈性水腫、軟組織腫脹、四肢沉重等)及急性痔發作,其制劑主要有地奧司明片。目前,地奧司明原料藥及制劑尚未載入2010年版《中國藥典》,而執行的標準是國家食品藥品監督管理局暫行標準(國標)[1]。現版的國外藥典中如《歐洲藥典》(EP7.0)[2]和《英國藥典》(BP)2012年版[3]僅收載地奧司明的原料藥,均未收載制劑。根據國家藥典委員會2011年基本藥物標準提高的任務分工,我所對該品種質量標準進行了修訂,對質量標準中性狀、鑒別、檢查和含量測定等項目均進行了試驗研究,并結合樣品的檢驗情況,擬訂了質量標準。其中有關物質的研究工作參考了EP7.0有關物質的檢查方法并結合國內產品的生產工藝等實際情況,對本品的雜質情況進行了研究和考察,建立了有效可控的有關物質檢查方法,并采用同一色譜系統對含量進行了測定,完善了質量標準,有效控制了本品的質量,本文對此報道如下。
1 材料
1200系列高效液相色譜(HPLC)儀,包括泵、脫氣機、二極管陣列檢測器、自動進樣設備、柱溫箱等(美國Agilent公司);AE 240型分析天平(瑞士Mettler Toledo儀器公司)。
地奧司明對照品(某藥廠提供,批號:120501,純度:98.1%);橙皮苷對照品(中國食品藥品檢定研究院,批號:110721-201115,純度:95.3%);地奧司明系統性試驗對照品(購自歐洲藥品質量管理局,為包含地奧司明和6種雜質的混合對照品);地奧司明原料藥(四川某公司,批號:C006G110301、C006G110601、C006G110602;江蘇某公司,批號:100908、100909、100910;純度:均>90%);地奧司明片(江蘇某公司,批號:120606、120607、120608;武漢某公司,批號:110207、110302、110303,規格:均為每片0.45g);乙腈、甲醇均為色譜純,水為純化水。
2 有關物質測定
2.1 色譜條件
色譜柱:Phenomenex C18(100mm×4.6mm,3μm);流動相:水-甲醇-冰醋酸-乙腈(66∶28∶6∶2,V/V/V/V),流速:0.7ml/min;檢測波長:275nm;柱溫:40℃;進樣量:10μl。
2.2 溶液的制備
系統適用性溶液:稱取系統適用性對照品5mg,加二甲基亞砜(DMSO)5ml溶解,即得。
橙皮苷對照品貯備液:精密稱取橙皮苷對照品10mg,置于10ml量瓶中,加DMSO溶解并稀釋至刻度,搖勻,即得。
供試品溶液a(有關物質):精密稱取原料藥(或片粉)適量,加DMSO溶解并制成1mg/ml的溶液,搖勻(片劑溶液過濾,取續濾液),即得。
對照溶液(有關物質):精密量取橙皮苷對照品貯備液1ml和供試品溶液a 3ml,置于100ml量瓶中,加DMSO稀釋至刻度,搖勻,即得。
供試品溶液b(含量測定):精密稱取原料(或片粉)適量,加DMSO溶解并制成0.2mg/ml的溶液,搖勻(片劑溶液過濾,取續濾液),即得。
輔料溶液:按照江蘇某公司提供的處方比例,按供試品溶液b配制方法配制不含主成分的輔料溶液。
2.3 系統適用性試驗
量取系統適用性溶液10μl注入色譜儀,考察分離效果。結果顯示,系統適用性溶液中的6個雜質(A、B、C、D、E、F)全部檢出并達到基線分離,橙皮苷峰與主峰的分離度為8.0,理論板數按主峰計為3700,詳見圖1。

圖1 系統適用性溶液色譜圖1.雜質A;2.雜質B(橙皮苷);3.雜質C;4.地奧司明;5.雜質D;6.雜質E;7.雜質F;8.溶劑Fig 1 HPLC chromatogram of system suitability test1.impurity A;2.impurity B(hesperidin);3.impurity C;4.diosmin;5.impurity D;6.impurity E;7.impurity F;8.solvent
系統適用性對照品目前國內無法提供,只能購自歐洲藥品質量管理局,且價格昂貴,而中國食品藥品檢定研究院僅能夠提供橙皮苷對照品。為適應國內的檢驗條件,本次試驗選擇了3根不同品牌的色譜柱Phenomenex、Inertsil ODS-3、Waters Atlantis T3[分別編號①、②、③,規格均為(100mm×4.6mm,3μm)],分別取系統適用性溶液進樣考察,擬通過限定橙皮苷峰與主峰的分離度作為系統適用性試驗的條件,確保所有雜質的分離和檢出,結果分離度分別為8.0、5.3、4.6,理論板數分別為3700、7000、6500。表明系統適用性溶液中的6個雜質如能全部檢出并達到基線分離,橙皮苷峰與主峰的分離度應至少>4.6。不同色譜柱的理論板數差異較大,結合試驗數據將理論板數定為不低于3000。根據試驗結果,擬定色譜條件與系統適用性試驗為“2.1”項下色譜條件,量取對照溶液注入色譜儀,記錄色譜圖,橙皮苷峰與主峰的分離度應不低于4.6,理論板數按主峰計算應不低于3000。
2.4 有關物質的測定方法及限度的確定
量取對照溶液適量,用DMSO稀釋20倍作為靈敏度測試溶液,注入色譜儀,調節檢測靈敏度,使主峰的信噪比不小于10;再精密量取供試品溶液a與對照溶液分別注入色譜儀,記錄色譜圖至主峰保留時間的5倍。雜質的限度和計算方法經參考EP7.0中地奧司明的雜質限度,并結合收集到的樣品有關物質的測定結果,修訂為:已知雜質橙皮苷按外標法計算,限度不得過5.0%;其他單個雜質按主成分自身對照法計算,含量在1.0%~3.0%的雜質不得多于3個,剩余的其他單個雜質不得過1.0%。總雜質(含橙皮苷)按主成分自身對照法計算,原料藥限度不得過10.0%;片劑考慮其生產及貯存過程中雜質可能增加的情況,并結合收集到的樣品的有關物質的測定結果,修訂為“不得過13.0%”。
2.5 專屬性試驗
分別取地奧司明原料藥(批號:C006G110301)25mg、片粉(批號:120606)40mg和輔料10mg各4份,分別加DMSO 15ml進行如下處理。(1)酸破壞:加1mol/L的鹽酸溶液4ml,80℃水浴加熱10min,放冷,用氫氧化鈉試液調至pH為7,加DMSO稀釋至25ml(片粉和輔料溶液需過濾,以下同)。(2)堿破壞:加氫氧化鈉試液1ml,放置2h,用1mol/L鹽酸溶液調至pH為7,加DMSO稀釋至25ml。(3)氧化破壞:加30%過氧化氫溶液1ml,80℃水浴加熱30min,放冷,加DMSO稀釋至25ml。(4)高溫破壞:80℃水浴加熱30min,放冷,加DMSO稀釋至刻度,搖勻。(5)光照破壞:加DMSO稀釋至刻度,搖勻,直接光照5d。分別取上述5種溶液,進樣測定,結果表明在上述條件下,除高溫和光照條件下溶液比較穩定,色譜圖基本無變化外,其余條件下主峰均有降解,但降解的雜質均可與主峰達到基線分離。說明擬定的色譜條件專屬性較好,輔料溶液基本無變化,對測定無干擾,詳見圖2。
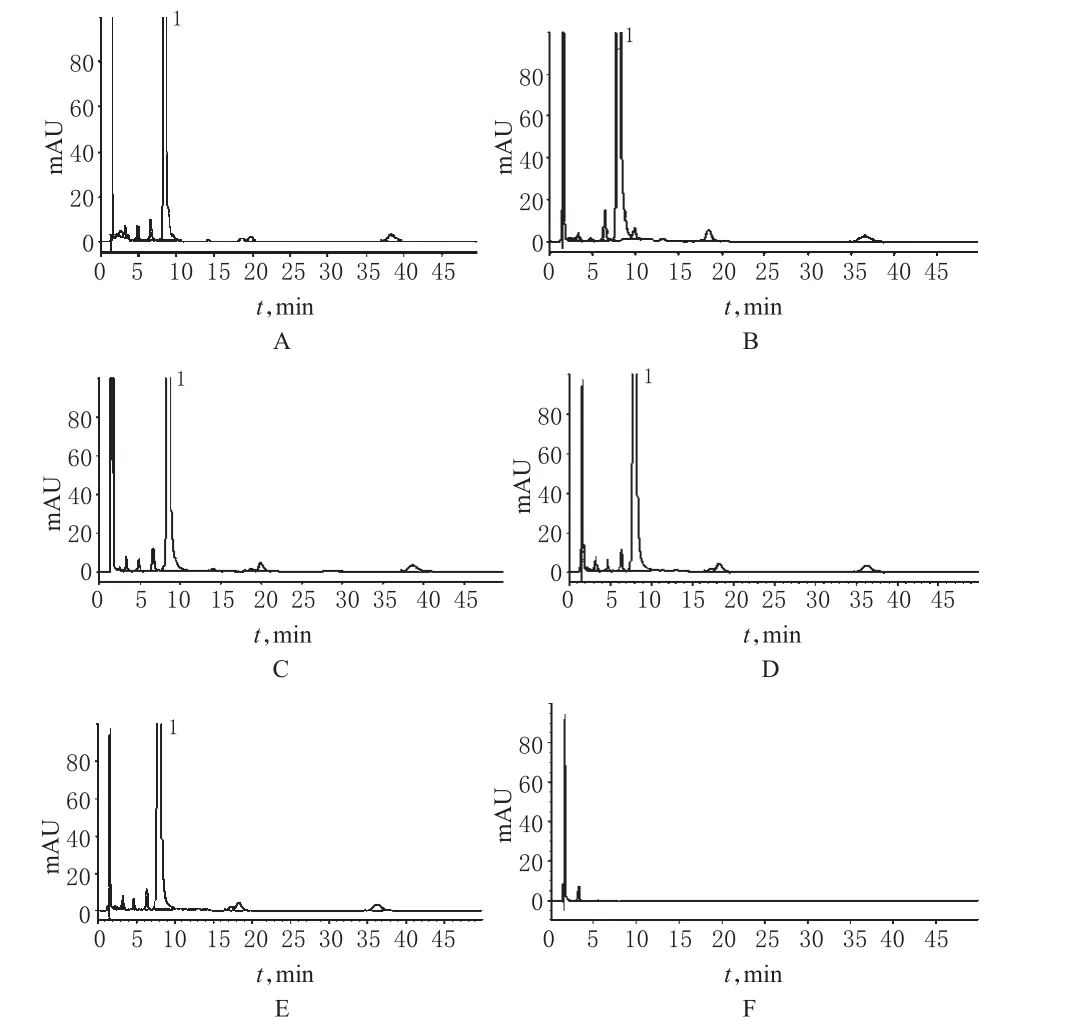
圖2 專屬性試驗高效液相色譜圖A.酸破壞樣品;B.堿破壞樣品;C.氧化破壞樣品;D.高溫破壞樣品;E.光照破壞樣品;F.輔料;1.地奧司明Fig 2 HPLC chromatograms of specificity testA.samples destroyed by acid;B.samples destroyed by alkali;C.samples destroyed by oxidant;D.samples destroyed by high temperature;E.samples destroyed by strong light;F.excipients;1.diosmin
2.6 線性關系試驗
精密稱取橙皮苷和地奧司明對照品適量,用DMSO稀釋制成二者質量濃度均為0.5、1.0、2.0、5.0、10.0、30.0、50.0、100.0μg/ml的系列溶液,分別注入色譜儀,記錄色譜圖;分別以橙皮苷和地奧司明的質量濃度(c)為橫坐標,以相應的峰面積(A)為縱坐標,進行線性回歸。結果,橙皮苷線性方程為A=1.99×10c-1.404(r=0.9999,n=7)(相應的雜質限度范圍為0.1%~10.0%),檢測質量濃度線性范圍為0.996~99.7μg/ml;地奧司明線性方程為A=1.64×10c-12.449(r=0.9999,n=6)(相應的雜質限度范圍為0.25%~10.0%),線性范圍為2.47~98.9μg/ml。
2.7 檢測限確定
取“2.6”項下溶液適量,采用逐步稀釋法稀釋,進樣測定,結果信噪比為3時,地奧司明、橙皮苷的檢測限分別為15、5ng。
2.8 系統精密度試驗
取對照溶液和供試品a溶液(批號:C006G110301)適量,分別重復進樣6次,對照溶液中橙皮苷、地奧司明峰面積RSD分別為0.4%、0.5%,供試品溶液a中地奧司明峰面積RSD為0.2%,表明本系統精密度良好。
2.9 方法精密度試驗
按照“2.2”項下方法配制6份供試品(批號:C006G110301)溶液進樣測定,計算,結果基本一致,詳見表1。
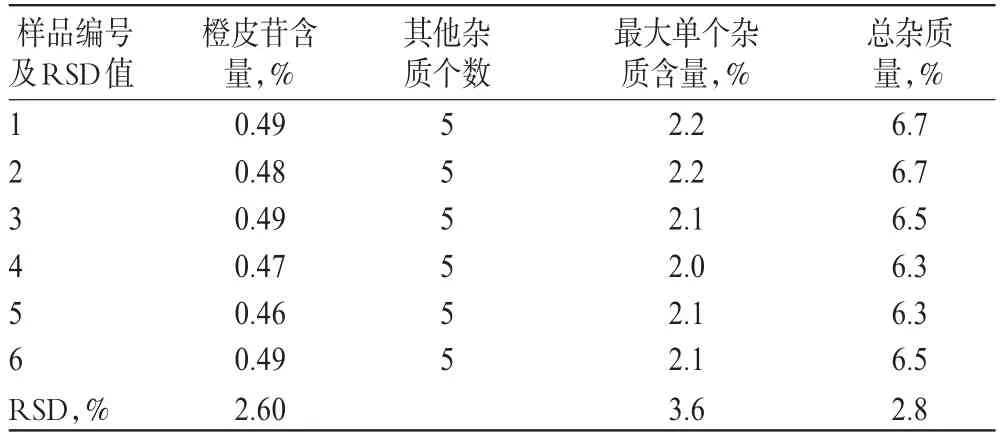
表1 有關物質精密度試驗結果Tab 1 Results of precision test of related substances
2.10 穩定性試驗
取對照溶液及供試品溶液a適量在室溫下分別放置0、4、8、12、24h,測定。結果對照溶液中橙皮苷峰面積的RSD為0.5%,供試品溶液中地奧司明、橙皮苷峰面積的RSD分別為0.5%、2.6%。表明溶液在24h內基本穩定。
2.11 橙皮苷加樣回收率試驗
分別精密稱取地奧司明原料藥(批號:C006G110301)7份(其中1份作為空白),每份100mg,置于100ml量瓶中,加DMSO適量,使溶解,精密加入橙皮苷對照品貯備液1ml,加DMSO稀釋至刻度,搖勻,注入色譜儀,記錄色譜圖;空白溶液同法測定橙皮苷,扣除峰面積后計算回收率。結果平均回收率為98.8%,RSD為1.1%(n=6)。
2.12 耐用性試驗
本次試驗采用3種不同型號的色譜柱,對不同廠家的同一批樣品進行耐用性考察,按“2.3”項下色譜柱編號進行試驗,結果基本一致,詳見表2。
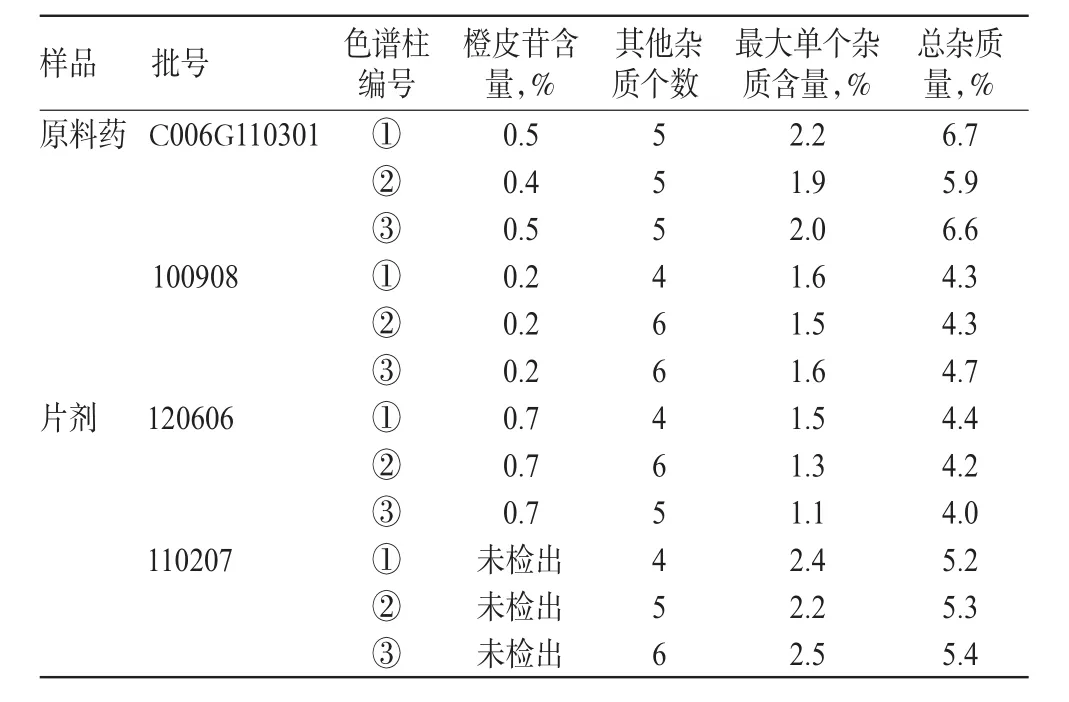
表2 耐用性試驗結果(n=3)Tab 2Results of durability test(n=3)
上述結果顯示,采用不同的色譜柱測定,檢出雜質個數基本相同,最大單一雜質和總雜質量的測定結果基本一致,橙皮苷的測定結果也基本一致。表明本方法的耐用性較好,不同型號的C18色譜柱均適用。
2.13 有關物質測定結果
精密量取對照溶液與供試品溶液a,按照“2.4”項下方法,對6批原料藥和6批片劑進行有關物質測定,結果見表3、圖3。
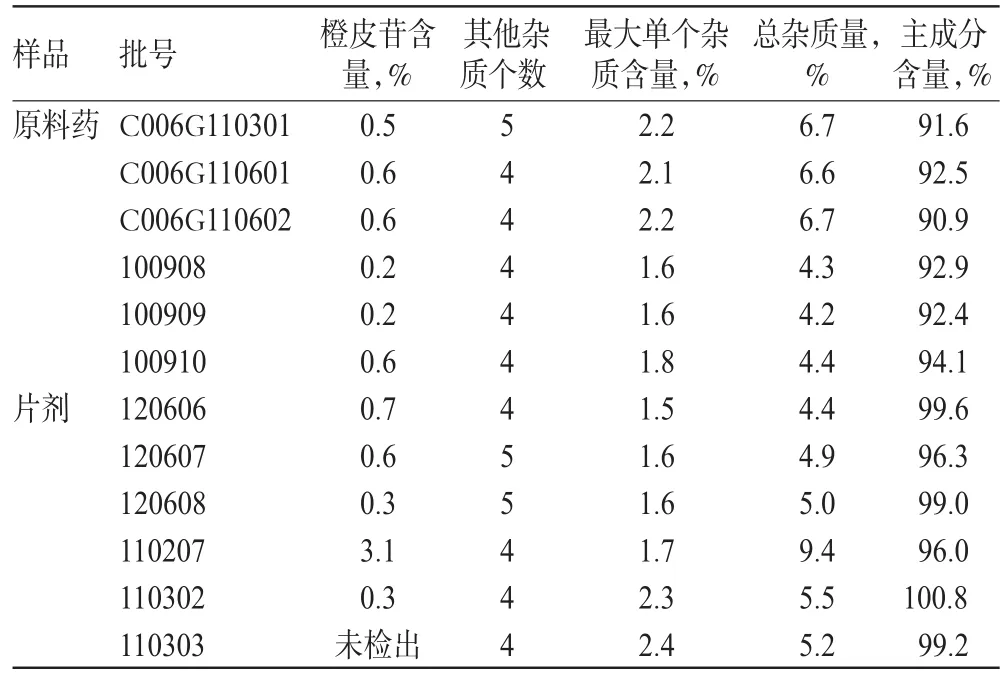
表3 樣品測定結果(n=2)Tab 3Results of content determination of samples(n=2)
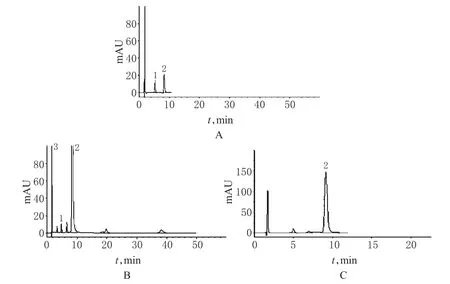
圖3 樣品測定高效液相色譜圖A.對照溶液;B.供試品溶液a;C.供試品溶液b;1.橙皮苷;2.地奧司明;3.溶劑Fig 3 HPLC chromatograms of samplesA.control solution;B.test solution a;C.test solution b;1.hesperidin;2.diosmin;3.solvent
3 主成分含量測定
采用有關物質項下的色譜系統,供試品溶液的質量濃度修訂為0.2mg/ml。經試驗,地奧司明線性方程為A=1.62×10c-1.05×10(r=0.9999,n=5),檢測質量濃度線性范圍為99.63~298.9μg/ml,平均回收率為 99.2%(RSD=0.5%,n=6)。按照擬定方法測定6批原料藥和6批片劑中主成分的含量,結果見表3、圖3。
4 討論
4.1 色譜系統的選擇
前期試驗中采用國家標準中色譜系統對系統適用性溶液進行試驗,結果其中的6個雜質(A、B、C、D、E、F)在該色譜系統中未能全部檢出,而在EP7.0的色譜系統中能全部被檢出,表明EP7.0的流動相系統優于現有國家標準。
4.2 色譜柱的選擇(5μm和3μm色譜柱的選擇)
本文建立的方法采用色譜柱為C18(100mm×4.6mm,3μm),規格較特殊,在日常檢驗工作中不常使用。因此,對可否用常規的色譜柱替代,筆者做了如下比對試驗:選用了3根不同品牌的常規C18(250mm×4.6mm,5μm),用系統適用性溶液分別進樣,考察分離效果。結果顯示,5μm色譜柱中,只有1根(Phenomenex)色譜柱能全部檢出6個雜質,但雜質B與雜質C未達到基線分離,且雜質的相對保留時間與EP7.0中標注的完全不同,其他2根色譜柱均不能完全分出6個雜質;而不同品牌的3μm內徑的色譜柱能將6個雜質全部分離出來,且雜質的相對保留時間與EP7.0基本相同。表明內徑3μm色譜柱的分離效果明顯優于5μm的色譜柱,更有利于雜質的全部檢出。故擬定標準中規定選用特殊規格的色譜柱。
綜上所述,本文的色譜系統能完全有效地檢出并分離地奧司明原料藥及片劑的有關物質,可有效地控制本品的質量,優于國家現行質量標準。
[1] 國家食品藥品監督管理局.YBH01832009地奧司明[S].2009-02-10.
[2] Directorate for the Quality of Medicines&Healthcare of the Council of Europe(EDQM).European Pharmacopoeia[S].7.0.Strasbourg :Council of Europe,2010:1864-1865.
[3] British Pharmacopoeia Commission.British Pharmacopoeia[S].2012edition.London:Stationary Office,2011:729-730.

