DNA酶傳感器的研究進展
王敏娟
(寶雞文理學院化學化工學院,陜西 寶雞721013)
DNA屬于生物聚合物當中的一類,是最重要的遺傳信息載體。20世紀90年代初,人們發現一部分DNA分子也表現出催化活性,稱之為脫氧核酶(DNA酶,DNAzyme)。目前,DNA酶和適體統一被稱為功能化的DNA,可以通過體外篩選、擴增技術得到。
雖然DNA酶有催化功能,但是當它單獨存在時,其催化作用很弱;只有在可與其特異性結合的輔助因子共存時,才能激活DNA酶的活性而表現出催化性能,這些輔助因子包括氨基酸、核酸、金屬離子和小的有機分子等。基于此原理,DNA酶被作為識別物質廣泛應用于一系列金屬離子(如 Hg2+、Cu2+、Pb2+等)的識別和檢測。
1 DNA酶的特點
(3)與蛋白質相比,DNA酶發生多次的復性、變性之后,其結合力或者活性仍然不受影響,因此,可以在相當苛刻的條件下使用和儲存。
(4)DNA 酶可以用于光纖和微陣列技術[3,4],可以用于實時或者多種金屬離子的同時檢測。
2 DNA酶的作用機理
與金屬離子特異性識別的DNA酶由兩部分組成:第一部分是特異性識別金屬離子的環狀部分;第二部分是與底物鏈雜交的部分。當底物鏈與酶鏈雜交之后,如果有與酶鏈特異性識別的金屬離子存在,酶鏈就會被激活,底物鏈的rA處被水解而斷裂。因此,DNA酶作為生物識別物質廣泛應用于多種金屬離子的檢測。
DNA酶作為生物探針具有以下特點:
(1)DNA酶的制備不依賴于動物和細胞,而是可以通過體外篩選或指數富集配體系統進化技術來得到,而且其序列一旦確定,就可以通過化學的方法進行合成。因此,同批生產的DNA酶幾乎沒有批間誤差,而且組成確定,純度高。
(2)DNA酶是單鏈的DNA序列,比較容易合成,大約在1~2d內即可完成,而且比RNA的合成便宜。在生理條件下,DNA的穩定性比蛋白質高1000倍,比RNA高10萬倍[1]。近期發現,DNA酶經常以球狀蛋白的形式存在[2],所以不易被核酸內切酶識別。
3 DNA酶傳感器在光學分析中的研究進展
金屬中毒,是指人體內某種金屬的含量過多而引起的慢性或急性中毒,并非過量攝入有害的金屬離子才會導致人體中毒,人體需要的金屬離子攝入過量也會導致金屬中毒。通常情況下,重金屬一旦攝入人體將無法排出體外。因此如何快速、準確地檢測某種金屬離子是否超標已經成為研究熱點。
目前,金屬離子的檢測方法主要有原子吸收光譜法[5]、電 感 耦 合 等 離 子 體 質 譜 法[6-8]、陽 極 溶 出 伏 安法[9,10]、毛細管電泳法[11]等,這些方法 大多需要精密的儀器和熟練的操作人員,而且樣品需要預處理,難以實現對金屬離子的實時檢測。因此人們建立了基于DNA酶的生物傳感方法用于檢測金屬離子。下面就主要介紹DNA酶在光學傳感器中的應用進展。
3.1 基于DNA酶的熒光傳感器
熒光傳感器的構建是基于分子識別物質與目標物作用前后體系熒光信號的變化來對目標物進行檢測的。早在2000年,Li等[12]就篩選出了與Pb2+特異性結合的DNA酶(17E),同時構建了檢測Pb2+的熒光傳感器。在底物鏈(17DS)的5′端標記了熒光物質TAMRA,在酶鏈(17E)的3′端標記了猝滅劑 Dabcyl,當標記有熒光物質的底物鏈單獨存在于溶液中時,體系的熒光信號很強;當加入酶鏈之后,由于底物鏈和酶鏈雜交成雙螺旋結構,使得熒光物質和猝滅物質間發生了熒光共振能量轉移(FRET),TAMRA的熒光被猝滅,體系熒光信號大大減弱;向體系中加入Pb2+后,Pb2+作為酶的輔助因子,使得酶的活性被激活,底物鏈在切割點被切斷,熒光猝滅現象被消除,TAMRA的熒光信號恢復,體系熒光信號增強,此方法在4℃下的檢出限為10nmol·L-1。雖然此方法能夠高靈敏度、高選擇性地檢測Pb2+,但是必須在4℃下進行,如果溫度升高到室溫就會導致底物鏈從酶鏈上解旋下來而產生過高的背景信號。為了解決這個問題,Liu等[13]建立了一種基于分子內和分子間同時猝滅的雙猝滅新型熒光檢測方法來降低背景信號,原理如圖1所示。
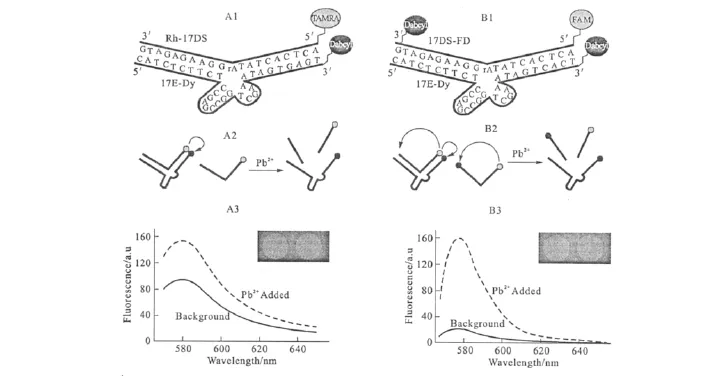
圖1 基于DNA酶檢測Pb2+的單猝滅(A)與雙猝滅(B)熒光傳感器對比Fig.1 Comparison of the single-(A)and double-quencher(B)DNAzyme-based Pb2+ sensor designs
由圖1可看出,雙猝滅效應對高的背景信號產生了明顯的抑制作用,并且可以在較寬的溫度范圍內對Pb2+進行檢測且不影響選擇性。2005年,Swearingen等[14]又建立了非均相檢測Pb2+的熒光法。將一端修飾有猝滅劑、另一端修飾有巰基的酶鏈(HS-17E-Dy)通過巰基自組裝固定到金表面,再與標記有熒光物質的底物鏈(17DS-Fl)雜交,不存在Pb2+時,熒光基團與猝滅基團較接近,熒光信號被猝滅;與Pb2+反應后,底物鏈被切斷,熒光信號恢復,同樣根據加入Pb2+前后體系熒光信號的變化來對Pb2+進行定量檢測。與均相熒光法相比,非均相的檢測方法使得固定在金表面的酶鏈可以再生和長期保存,而且檢出限(1nmol·L-1)比均相檢出限降低了一個數量級。
雖然之前構建的基于DNA酶的金屬離子傳感器響應速度快,但是須對酶鏈或者底物鏈進行標記,因而對酶的活性有一定的影響,且成本較高。
2009年,Xiang等[15]將dSpacer位點引入到傳感器的構建當中,他們在DNA雙鏈區的酶鏈上引入了一個dSpacer位點,以熒光小分子2-氨基-5,6,7-三甲基-1,8-萘啶(ATMND)為信號物質,建立了基于DNA酶的無標記型熒光法用于檢測Pb2+。單獨的ATMND溶液的熒光信號很強,但是當它嵌入到有dSpacer位點的雙鏈中形成配合物時,熒光信號被猝滅。Pb2+的存在使得酶鏈被激活而將底物鏈切斷,雙螺旋結構被破壞,小分子被釋放出來,熒光信號增強,在優化的條件下,這種無標記的方法對溶液中4nmol·L-1的Pb2+也能產生特異性的響應。
2010年,Zhang等[16]又將高猝滅效率的分子信標模型和酶催化檢測Pb2+模型聯合起來,建立了一種檢測Pb2+的催化分子信標(CAMB)新模型。此方法與前面的方法相比,有以下幾個優點:第一,催化分子信標背景信號低,改變了信噪比,靈敏度比直線型的底物探針模型高;第二,分子信標的猝滅效率高,使得在操作中可以用比酶鏈濃度較大的底物鏈來達到信號放大的目的;第三,酶鏈無需修飾猝滅物質來起猝滅的作用,可以用來傳感一系列的目標物(金屬離子或有機分子)。該法檢測限(600pmol·L-1)較基于DNA酶的Pb2+檢測方法更低。
隨后,Carmi等[17,18]和 Liu等[19]篩選出了與 Cu2+特意性識別的DNA酶。Liu等[20]采用降低背景信號的雙猝滅方法,構建了檢測Cu2+的熒光傳感器,該傳感器可以對溶液中不低于35nmol·L-1(2.3ppb)的Cu2+進行檢測,且響應速度特別快,在2~4min內就可以完成檢測。此外,Liu等[21,22]還運用DNA酶構建了一系列用于檢測其它金屬離子(如Uo2+、Hg2+)的熒光傳感器。
3.2 基于DNA酶的光度傳感器
光度傳感器的構建是基于分子識別物質與目標物作用前后體系吸光度的變化進行定量檢測,或者根據加入目標物前后,體系最大吸收波長的變化進而引起溶液顏色的變化,來進行目視檢測,即所謂的比色法。
Liu等[22]在這方面也進行了一系列的工作,將之前構建的用于檢測Pb2+的熒光傳感器模型改為光度傳感器[23]。該光度傳感器是將底物鏈兩端延伸,使得延伸的部分正好與自組裝在納米金粒子(13nm)上的單鏈DNA雜交,然后與酶鏈雜交,在沒有與Pb2+作用之前,延伸的底物鏈將溶液中修飾有單鏈DNA的納米金粒子連在一起,納米金團聚,膠體溶液由酒紅色變為藍色;與Pb2+作用后,底物鏈被水解斷裂,納米金再度分散到溶液中,顏色由藍色又變回酒紅色,從而可根據顏色和吸光度的變化來檢測Pb2+。
2008年,Lee等[23]采用檢測Pb2+的比色法模型,構建了基于DNA酶的標記型和非標記型光度傳感器用于檢測UO,原理如圖2所示。
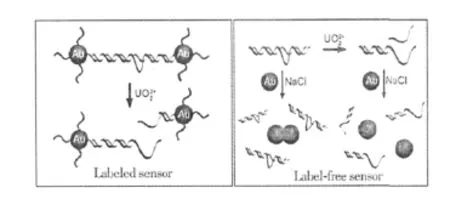
圖2 基于DNA酶的光度傳感器用于檢測UO的研究Fig.2 Scheme of labeled and lable-free colorimetric sensors based on Au nanoparticle in the absence and presence of UO
3.3 基于DNA酶的電化學發光傳感器
近年來,電化學發光分析方法因高的靈敏度和可以重復多次檢測等優點也受到了研究者的關注。Ma等[24]以釕聯吡啶為電化學發光物質,構建了信號增強型電化學發光DNA酶傳感器用于檢測Pb2+的方法。將3′端標有釕聯吡啶的與底物鏈雜交好的DNA酶固定在石墨電極的表面,在沒有加入目標物Pb2+之前,酶鏈與底物鏈以雙螺旋結構存在,由于雙螺旋結構有一定的剛性,使得釕聯吡啶與電極表面的距離增大;加入Pb2+后,Pb2+將底物鏈切斷,DNA的雙螺旋結構被打開,從而使得釕聯吡啶與電極的距離縮小,電化學發光信號增強,根據體系電化學發光信號的變化對目標物Pb2+進行定量檢測,檢測限為1.4pmol·L-1。此方法也可以用于其它金屬離子的檢測。
4 結語
近年來,光學分析法由于靈敏度高、操作簡單和檢測費用低等特點而得到了迅速的發展。由于DNA酶合成較便宜、性質穩定、易于儲存,而且在金屬離子的存在下可以被激活而發生催化作用,因此,研究者們構建了一系列基于DNA酶的光學生物傳感器用于金屬離子的檢測。DNA酶有望用于實時或者多種金屬離子的同時檢測。
[1]Breaker R R.Catalytic DNA:In training and seeking employment[J].Nat Biotechnol,1999,17(5):422-423.
[2]Nowakowski J,Shim P J,Prasad G S,et al.Crystal structure of an 82-nucleotide RNA-DNA complex formed by the 10-23DNA enzyme[J].Nat Struct Biol,1999,6(2):151-156.
[3]Walt D R.Techview:Molecular biology.Bead-based fiber-optic arrays[J].Science,2000,287(5452):451-452.
[4]Taylor L C,Walt D R.Application of high-density optical microwell arrays in a live-cell biosensing system[J].Anal Biochem,2000,278(2):132-142.
[5]Tahan J E,Granadillo V A,Romero R A.Electrothermal atomic absorption spectrometric determination of Al,Cu,Fe,Pb,V and Zn in clinical samples and in certified environmental reference materials[J].Anal Chim Acta,1994,295(1-2):187-197.
[6]Aggarwal S K,Kinter M,Herold D A.Determination of lead in urine and whole blood by stable isotope dilution gas chromatography-mass spectrometry[J].Clin Chem,1994,40(8):1494-1502.
[7]Liu H W,Jiang S J,Liu S H.Determination of cadmium,mercury and lead in seawater by electrothermal vaporization isotope dilution inductively coupled plasma mass spectrometry[J].Spectrochim Acta Part B:Atomic Spectroscopy,1999,54(9):1367-1375.
[8]Bowins R J,McNutt R H.Electrothermal isotope dilution inductively coupled plasma mass spectrometry method for the determination of sub-ng·mL-1levels of lead in human plasma[J].J Anal At Spectrom,1994,9(11):1233-1236.
[9]Feldman B J,Osterloh J D,Hata B H,et al.Determination of lead in blood by square wave anodic stripping voltammetry at a carbon disk ultramicroelectrode[J].Anal Chem,1994,66(13):1983-1987.
[10]Jagner D,Renman L,Wang Y.Determination of lead in microliter amounts of whole blood by stripping potentiometry[J].Electroanalysis,1994,6(4):285-291.
[11]Regan F B,Meaney M P,Lunte S M.Determination of metal ions by capillary electrophoresis using on-column complexation with 4-(2-pyridylazo)resorcinol following trace enrichment by peak stacking[J].J Chromatogr B:Biomed Appl,1994,657(2):409-417.
[12]Li J W,Lu Y.A highly sensitive and selective catalytic DNA biosensor for lead ions[J].J Am Chem Soc,2000,122(42):10466-10467.
[13]Liu J,Lu Y.Improving fluorescent DNAzyme biosensors by combining inter-and intramolecular quenchers[J].Anal Chem,2003,75(23):6666-6672.
[14]Swearingen C B,Wernette D P,Crogek D M,et al.Immobilization of a catalytic DNA molecular beacon on Au for Pb(Ⅱ)detection[J].Anal Chem,2005,77(2):442-448.
[15]Xiang Y,Tong A J,Lu Y.A basic site-containing DNAzyme and aptamer for label-free fluorescent detection of Pb2+and adenosine with high sensitivity,selectivity,and tunable dynamic range[J].J Am Chem Soc,2009,131(42):15352-15357.
[16]Zhang X B,Wang Z D,Xing H,et al.Catalytic and molecular beacons for amplified detection of metal ions and organic molecules with high sensitivity[J].Analytical Chemistry,2010,82(12):5005-5011.
[17]Carmi N,Breaker R R.Characterization of a DNA-cleaving deoxyribozyme[J].Bioorg Med Chem,2001,9(10):2589-2600.
[18]Carmi N,Balkhi H R,Breaker R R.Cleaving DNA with DNA[J].Proc Natl Acad Sci USA,1998,95(5):2233-2237.
[19]Liu J W,Lu Y.A DNAzyme catalytic beacon sensor for paramagnetic Cu2+ions in aqueous solution with high sensitivity and selectivity[J].J Am Chem Soc,2007,129(32):9838-9839.
[20]Liu J W,Brown A K,Meng X L,et al.A catalytic beacon sensor for uranium with parts-pertrillion sensitivity and millionfold selectivity[J].PNAS,2007,104(7):2056-2061.
[21]Liu J W,Lu Y.Rational design of"turn-on"allosteric DNAzyme catalytic beacons for aqueous mercury ions with ultrahigh sensitivity and selectivity[J].Angew Chem Int Ed,2007,46(40):7587-7590.
[22]Liu J W,Lu Y.A colorimetric lead biosensor using DNAzyme-directed assembly of gold nanoparticles[J].J Am Chem Soc,2003,125(22):6642-6643.
[23]Lee J H,Wang Z D,Liu J W,et al.Highly sensitive and selective colorimetric sensors for uranyl(UO):Development and comparison of labeled and label-free DNAzyme-gold nanoparticle systems[J].J Am Chem Soc,2008,130(43):14217-14226.
[24]Ma F,Sun B,Qi H,et al.A signal-on electrogenerated chemiluminescent biosensor for lead ion based on DNAzyme[J].Anal Chim Acta,2011,683(2):234-241.

