百草枯半抗原分子設計合成及表征
管 露, 張銀志*, 楊婷婷, 尤繼明, 李紅梅, 孫秀蘭
(1.食品科學與技術國家重點實驗室 江南大學,江蘇 無錫 214122;2.江蘇蘇微微生物研究有限公司,江蘇 無錫214068;3.國家有機食品質量監督檢驗中心,江蘇 寶應 225800)
百草枯(paraquat,PQ)又名克無蹤、對草快,化學名為1,1'-二甲基-4,4'-聯吡啶陽離子鹽,它是一種廣譜、滅生性有機雜環類除草劑,主要防治玉米、大豆、蔬菜、水稻、果園等地的雜草,也用作谷類、棉花、甘蔗等收割前的脫葉劑,它對植物綠色組織具有較強的破壞作用[1]。百草枯可經胃腸道、皮膚和呼吸道吸收。有研究顯示,使用百草枯除草的農民長期吸入小劑量百草枯易導致肺纖維化[2]。由于百草枯的廣泛應用,有可能會存在于糧油作物和一些食品原料中,即使在非致害水平下,也會對人體健康產生潛在危害。
農藥免疫分析法不但具有與常規分析法相當或更高的靈敏度,而且無須使用昂貴儀器設備,方法簡便快速,在農藥殘留的快速篩選和定量檢測以及現場和快速檢測方面已顯示出獨特的優點,受到環境監測工作者的重視。酶聯免疫吸附測定法檢測百草枯殘留的研究,國外已有報道[3-8],國內相關報道極少[9-10]。百草枯的分子量僅為257 Da,屬于半抗原,只具有反應原性,而無免疫原性。由于百草枯自身沒有可供偶聯的活性官能團(如氨基、羧基等),因此,必須對百草枯分子結構進行修飾,使其具有活性基團——羧基,然后與大分子載體蛋白質交聯,才能刺激動物產生特異性免疫應答。由于百草枯分子結構中,聯吡啶環上兩氮原子均連有甲基,不易直接連入帶有一段碳連的羧基。為此,作者選取百草枯的結構類似物—4,4’-聯吡啶,通過控制反應先在其一側氮原子上加入甲基,然后再在另一氮原子上連入帶有一段碳連的羧基,即為百草枯半抗原,從而為百草枯完全抗原的合成奠定了基礎。
1 材料與方法
1.1 材料與儀器
1.1.1 實驗材料 4,4’-聯吡啶、碘甲烷、N,N二甲基甲酰胺(DMF)、濃 HCl、丙酮、體積分數 95%乙醇等均為分析純,氮氣,3A分子篩。
1.1.2 實驗儀器 Spectronic 1.70紫外可見光分光光度計,意大利GBC產品;WBG 1-4002型旋轉蒸發儀,德國產品;79-1型磁力加熱攪拌器,常州市國立試驗設備研究所提供;DF-101S型集熱式磁力攪拌器,江蘇省金壇市正基儀器有限公司制造;SHB-Ⅲ型循環水真空泵,鞏義市站街光亞儀器廠制造;DZF-6020型真空干燥箱,鞏義市英峪予華儀器廠制造;SX2箱式電阻爐,上海實驗儀器廠有限公司制造;Waters Platform ZMD 4000型液相色譜質譜聯用儀,美國Waters公司產品;BC-W201型恒溫浴鍋,上海貝凱生物化工設備有限公司制造;ALPHA1-4型冷凍干燥機。
1.2 實驗方法
百草枯的分子結構式如圖1,本實驗以4,4’-聯吡啶和碘甲烷為起始原料[4,9],合成了N-甲基-N′-戊酸基-二吡啶二溴化物(簡稱PQ-h),用于制備百草枯的人工抗原。其合成路線如圖2,反應分3步完成。

圖1 百草枯的分子結構式Fig.1 Molecular structural formula of paraquat

圖2 百草枯人工半抗原的合成路線Fig.2 Synthesis route of artificial hapten for paraquat
1.2.1 N-甲基-二吡啶陽離子化合物——Monoquat(MQ)的合成 事先將50 mL的三頸圓底燒瓶通氮氣排除其中的空氣,稱取3 g 4,4’-聯吡啶于圓底燒瓶中,加入30 mL無水丙酮溶解后冷卻至4℃,在磁力攪拌下慢慢加入1.14 mL碘甲烷(CH3I),于暗處反應。反應混合物完全加入后,低溫(4℃左右)攪拌過夜。用無水丙酮洗滌,抽干,得產品MQ,真空干燥,得黃色針狀結晶,然后存放于真空干燥器中,取少量進行鑒定。
1.2.2 N-甲基-N′-戊酸乙酯基-二吡啶陽離子化合物的合成 稱取1.56 g第一步反應得到的MQ于圓底燒瓶中,加入30 mL新鮮蒸餾的無水二甲基甲酰胺(DMF)溶解,然后加入1.6 mL 5-溴戊酸乙酯在120℃油浴磁力攪拌下反應,回流5 h,然后室溫放置過夜。抽濾,用無水DMF洗滌,真空干燥,得黃色片狀結晶,存放于真空干燥器中,取少量進行鑒定。
1.2.3 N-甲基-N′-戊酸基-二吡啶陽離子化合物(PQ-h)的合成 稱取0.3 g第二步得到的N-甲基-N′-戊酸乙酯基-二吡啶陽離子化合物與23 mL濃HCl混合,水浴加熱回流3 h左右。在旋轉蒸發器上蒸去過量的酸和水,保持水浴溫度不超過60℃,蒸干,得固體殘留物。冷卻后,加入少量丙酮結晶(析出白色晶體),過濾,抽干,真空干燥,得粗品,再經體積分數95%乙醇重結晶,真空干燥,存放于真空干燥器中,取少量進行鑒定。
2 結果與分析
取上述每一步合成的百草枯衍生物進行LCMS鑒定和1HNMR鑒定,并將百草枯半抗原進行IR鑒定,結果見圖3—9。
2.1 N-甲基-二吡啶陽離子化合物——Monoquat(MQ)的 LC-MS、1HNMR 鑒定
由圖3知,第一步反應合成的產物純度較高,達95%以上,說明反應比較徹底,基本無副產物生成。經計算產物得率約為86%。由質譜圖可看出產物的相對分子質量為171,這與目標產物——N-甲基-二吡啶陽離子化合物(MQ)的相對分子質量一致。

圖3 N-甲基-二吡啶陽離子化合物(MQ)的LC圖譜和MS圖譜Fig.3 LC spectrum (A)and MS spectrum (B)of N-methyl-4-(pyridine-4-pyridyl)pyridinium(MQ)
由圖 4可知,該物質的1HNMR (500 MHz,D2O):δ為 8.92(d,2H,ArH),8.76(d,2H,ArH),8.39(d,2H,ArH),7.9 (d,2H,ArH),4.5 (s,3H,CH3),所得結構信息與目標物——N-甲基-二吡啶陽離子化合物(MQ)的結構信息相同,從而推斷其為目標產物[9]。

圖4 N-甲基-二吡啶陽離子化合物(MQ)的1HNMR圖譜Fig.4 1HNMR spectrum of N-methyl-4-(pyridine-4-pyridyl)pyridinium(MQ)
2.2 N-甲基-N′-戊酸乙酯基-二吡啶陽離子化合物的LC-MS、1HNMR鑒定
圖5的LC圖出現兩個峰,N-甲基-N′-戊酸乙酯基-二吡啶陽離子化合物在液相色譜上的保留時間為1.62 min,其余為雜質峰,通過積分計算其純度為70%。由質譜圖可以看出,300.5為N-甲基-N′-戊酸乙酯基-二吡啶陽離子化合物的陽離子峰,計算得其相對分子質量為300,與實際相對分子質量相符。

圖5 N-甲基-N′-戊酸乙酯基-二吡啶陽離子化合物的LC圖譜和MS圖譜Fig.5 LC spectrum (A)and MS spectrum (B)of N-(5-ethoxy-5-oxopentyl)-N'-methylbipyridilium
由圖 6可知,該物質的1HNMR (500 MHz,D2O):δ(ppm)9.18 (d,2H,ArH),9.11 (d,2H,ArH),8.61(d,2H,ArH),8.58(d,2H,ArH),4.56(s,3H,NCH3),2.54 (t,2H,CH2),2.18 (t,2H,CH2),1.76(m,2H,CH2),1.29 (t,3H,CH3), 所得結構信息與目標物——N-甲基-N′-戊酸乙酯基-二吡啶陽離子化合物的結構信息相同,從而推斷其為目標產物[9]。
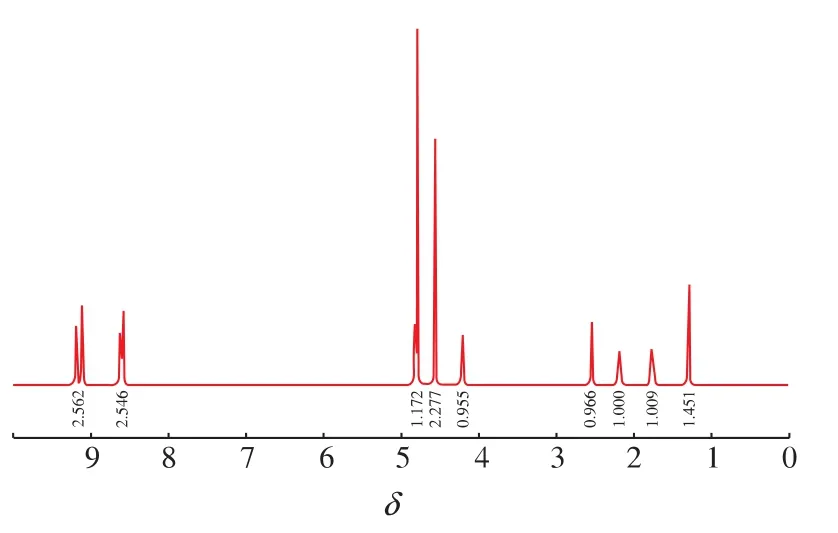
圖6 N-甲基-N′-戊酸乙酯基-二吡啶陽離子化合物的1HNMR圖譜Fig.6 1HNMR spectrum of N-(5-ethoxy-5-oxopentyl)-N'-methylbipyridilium
2.3 N-甲基-N′-戊酸基-二吡啶陽離子化合物(PQ-h)的 LC-MS、1HNMR 鑒定
由圖7可知,酸水解后的產物相對較純,純度達96%。由質譜圖可看出272.5為PQ-h的陽離子峰,計算得其相對分子質量為272,與實際的相對分子質量相符,經計算得率為69%。

圖7 N-甲基-N′-戊酸基-二吡啶陽離子化合物(PQ-h)的LC圖譜和MS圖譜Fig.7 LC spectrum (A)and MS spectrum (B)of N-(5-ethoxy-5-oxopentyl)-N'-methylbipyridilium(PQ-h)
由圖 8可知, 該物質的1HNMR (500 MHz,D2O):δ為 9.18(d,2H,ArH),9.11(d,2H,ArH),8.61(d,2H,ArH),8.57 (d,2H,ArH),4.81 (t,2H,CH2),4.56 (s,3H,CH3),2.54 (t,2H,CH2),2.19 (m,2H,CH2),1.75 (m,2H,CH2), 羧基上的活潑氫被溶劑DO2中的D替換。該所得結構信息與目標物——N-甲基-N′-戊酸基-二吡啶陽離子化合物(PQ-h)的結構信息相同,從而推斷其為目標產物[9]。
2.4 IR鑒定結果及分析
取合成的百草枯半抗原進行IR (KBr壓片)鑒定,結果見圖9。

圖8 N-甲基-N′-戊酸基-二吡啶陽離子化合物 (PQ-h)的1HNMR圖譜Fig.8 1HNMR spectrum of N-(5-ethoxy-5-oxopentyl)-N'-methylbipyridilium(PQ-h)

圖9 百草枯半抗原的IR圖譜Fig.9 IR spectrum of paraquat hapten
由圖9知,3 439.32 cm-1對應的寬的峰為羧酸上的O—H伸縮吸收,3 017.81 cm-1對應的為芳環上C—H的伸縮振動,1 726.93 cm-1為C=O的吸收,1 638.41 cm-1為C=N的吸收(即吡啶環結構),1 397.79、1 447.97、1 508.61、1 559.84 cm-1均 為C=C骨架的振動,826.04 cm-1為芳環上C—H面外彎曲振動吸收。通過以上分析,初步確定為目標產物—PQ-h。
3 結語
在農藥殘留的免疫學分析中,人工抗原的合成是制備抗體和建立免疫分析方法最關鍵的步驟,而半抗原的設計又是合成人工抗原的前提。半抗原的設計要求應盡量使合成的半抗原能刺激機體產生特異性免疫應答,并且產生的抗體應具有預期的活性[11]。因此,應盡量保證半抗原分子具有與待測物分子類似的立體化學特征。一般將半抗原設計成包含一個間隔臂和偶聯基團,并仍具有原農藥分子基本結構的分子。通常認為連接臂的最適長度在3~6個碳原子,連接臂太短不利于半抗原的充分暴露,而連接臂太長又會因疏水作用而造成烷基鏈的折疊,導致半抗原分子仍然被載體蛋白質所掩蓋,不利于抗原遞呈細胞(APC)的識別[12]。
在本研究中,采用百草枯的結構類似物—4,4’-聯吡啶通氮氣保護下經3步化學反應合成了目標產物,并用ESI、1HNMR、IR對其結構進行了鑒定。經分析證明,合成的百草枯中間體純度較高,可以將其與載體蛋白質偶聯制備百草枯人工抗原。
[1]曾銘.共振光散射光譜法機理研究及其在農藥分析中的應用[D].成都:四川師范大學,2006:29.
[2]夏敏,劉建華.百草枯中毒研究現狀[J].四川醫學,1995,16(4):237-239.XIA Min,LIU Jian-hua.Research status quo of paraquat poisoning[J].Sichuan Medical Journal,1995,16 (4):237-239.(in Chinese)
[3]Niewola Z,Walsh S T,Davies G E.Enzyme linked immunosorbent assay (ELISA) for paraquat[J].International Journal of Immunopharmacology,1983,5(3):211-218.
[4]Jeanette Van Emon,Bruce Hammock,James N Seiber.Enzyme-Linked immunosorbent assay for paraquat and its application to exposure analysis[J].Anal Chem,1986,58:1866-1873.
[5]Coxon R E,Rae C,Gallacher G,et al.Development of a simple,fluoroimmunoassay for paraquat[J].Clin Chim Acta,1988,175(3):297-305.
[6]Michele Y Selisker,David P Herzog,Roger D Erber,et al.Determination of paraquat in fruits and vegetables by a magnetic particle based enzyme-linked immunosorbent assay[J].J Agric Food Chem,1995,43:544-547.
[7]Koivunen M E,Gee S J,Park E K,et al.Application of an Enzyme-Linked immunosorbent assay for the analysis of paraquat in Human-Exposure samples[J].Arch Environ Contam Toxicol,2005,48:184-190.
[8]Caroline A Spinks,Wang Bo,Clare Mills E N,et al.Development of an ELISA for paraquat;improvement of antibody characteristics by reversed affinity chromatography[J].Analyst,1999,124:847-850.
[9]馬兆揚,黃金祥.半抗原:N-甲基-N′-戊酸基-二吡啶-二溴化物的合成[J].衛生研究,2004,33(2):220-221.MA Zhao-yang,HUANG Jin-xiang.The synthesis of the hapten:N-(5-ethoxy-5-oxopentyl)-N'-methylbipyridilium[J].Journal of Hygiene Research,2004,33(2):220-221.(in Chinese)
[10]Takatori T,Nagao M,Wu B等.單克隆抗體與百草枯反應的特性與進展[J].中國法醫學雜志,1988,3(3):171 Takatori T,Nagao M,Wu B,et al.The characteristics and progress of the reaction to monoclonal antibody and paraquat[J].Chinese Journal of Forensic Medicine,1988,3(3):171.(in Chinese)
[11]朱國念,吳剛,吳慧明.有機磷殺蟲劑毒死蜱人工抗原的合成與鑒定[J].中國農業科學,2003,36(6):657-662.ZHU Guo-nian,WU Gang,WU Hui-ming.Synthesis and identification of the antigens for the organophosphorus insecticide chlorpyrifos[J].Scientia Agricultura Sinca,2003,36(6):657-662.(in Chinese)
[12]Jung F,Gee S J,Harrison R O,et al.Use of immunochemical techniques for the analysis of pesticides[J].Pestic Sci,1989,26:303-317.

