18F標記噠嗪酮類似物的制備及其在小鼠體內的生物分布
彭 程,牟甜甜,趙祚全,馬云川,張現忠,3
(1.首都醫科大學 宣武醫院 PET中心,北京 100053;2.放射性藥物教育部重點實驗室,北京師范大學 化學學院,北京 100875;3. 分子影像暨轉化醫學研究中心,廈門大學 公共衛生學院,廈門 361005;4. 首都醫科大學附屬北京安貞醫院 核醫學科,北京 100029 )
心肌灌注顯像在冠心病的早期診斷和預后評價中起著非常重要的作用。隨著正電子發射斷層掃描(PET)技術的發展與普及,越來越多的18F標記心肌灌注顯像劑被報道,成為放射性藥物研究的新熱點。
MC-Ⅰ(線粒體復合體Ⅰ)抑制劑類似物在已報道的18F標記的心肌灌注顯像劑中生物性能較為突出[1]。尤其是抑制劑噠螨靈的衍生物,如BMS-747158-02(flurpiridaz)[2-9]、18F-FP1OP[10]等,都是以噠嗪酮為藥效團,具有較高的心肌攝取和良好的靶與非靶組織放射性攝取比(T/NT),具有進一步臨床應用的前景(flurpiridaz已經獲得FDA批準進入III期臨床試驗)。
噠螨靈的結構由“頭盔”、連接鏈以及側鏈組成,其化學結構示于圖1。Purohit等[11]對它的衍生物進行了IC50的測定,做了較深入的構效關系研究。但是上述研究都是基于噠螨靈結構中的噠嗪酮部分或連接鏈部分,并未涉及側鏈中苯環的結構修飾。本課題組[12]于2011年報道了18F-FPTP2,其生物分布結果表明,噠螨靈的苯環具有一定的可修飾性,在苯環上引入雜原子并改變苯環取代基的位置,并不會影響該類化合物的心肌攝取。這說明噠螨靈側鏈中的苯環具有較大的可修飾性。因此,側鏈中的苯環是否屬于影響噠螨靈心肌攝取的核心結構,去掉苯環是否會影響該類化合物在心肌中的攝取,值得進一步研究。另外,已報道的18F-FP1OP和18F-FP2OP[13]的穩定性較差,不利于臨床使用,因此需要設計合成一種更為穩定的化合物。鑒于此,本工作擬嘗試對噠螨靈進行進一步修飾,去掉其側鏈中的苯環,制備結構更為簡單的2-特丁基-4-氯-5-(2-氟[18F]乙氧基)-2H-3-噠嗪酮(18F-FP2),以研究該類標記物的穩定性及苯環的存在對于該類化合物心肌攝取的影響。

圖1 噠螨靈的結構圖Fig.1 The structure of pyridaben
1 主要實驗材料
1.1 主要儀器與裝置
高效液相色譜儀島津LC-20AT:日本島津公司產品;AVATAR 360 紅外光譜:美國Nicolet公司產品;Avance 500核磁共振譜儀:瑞士Bruker A.G.公司產品;RM-905a放射性活度計:中國計量科學研究院產品;Venusil MP-C18半制備色譜柱,250 mm×10 mm,5 μm:美國Agela Technologies公司產品;DYY-Ⅲ電泳儀:北京科學儀器修配廠產品;WALLAC/WIZARD 1470γ計數儀:美國PerkinElmer公司產品。
1.2 主要試劑
18F-:北京宣武醫院提供;乙二醇(99%)、對甲基苯磺酰氯(98%)、正四丁基氟化銨(1 mol/L四氫呋喃溶液)、碳酸銫(99%)、糠醛(98%)、二異丙基乙胺(DIPEA)(99%):Alfa Aesar公司產品;叔丁基肼鹽酸鹽(98%)、4-二甲氨基吡啶(DMAP)(99%):Acros Organics公司產品;Kryptofix2.2.2.(K2.2.2):Sigma-Aldrich公司產品。
2 實驗方法
2.1 19F-FP2的合成
2-特丁基-4-氯-5-(2-氟[19F]乙氧基)-2H-3-噠嗪酮(2-tert-butyl-4-chloro-5-(2-[19F]fluroethoxy)-2H-pyridazin-3-one,19F-FP2)的合成路線示于圖 2。其中,2-特丁基-4,5-二氯噠嗪酮(2-tert-butyl-4.5-dichloro-2H-pyridazin-3-one,DCP)的合成參考文獻[13]。
將0.515 g(2 mmol)DCP、0.372 g(6 mmol)乙二醇、1.955 g(6 mmol)碳酸銫和10 mL DMF于68 ℃油浴反應12 h。冷卻后用100 mL乙酸乙酯稀釋,抽濾。濾液經100 mL水洗滌5次后,用無水MgSO4干燥。抽濾后旋蒸濾液,經200~300目的硅膠柱純化,展開劑為V(石油醚)∶V(乙酸乙酯)=2∶3。得到0.39 g白色固體,即 2-特丁基-4-氯-5-(2-羥基)-2H-3-噠嗪酮(2-tert-butyl-4-chloro-5-(2-hydroxy)-2H-pyridazin-3-one, I-2OH),產率80%。1H NMR (400 MHz, CDCl3)δ: 1.581 (s, 9H, N(CH3)3)、2.142 (s, 1H, CH2OH)、3.946 (t, 2H, CH2OH)、4.268 (t, 2H, CH2CH2OH)、7.707 (s, 1H, N=C-H)。
將0.247 g(1 mmol)I-2OH、0.229 g(1.2 mmol)對甲基苯磺酰氯、0.146 g(1.2 mmol)4-二甲氨基吡啶、0.155 g(1.2 mmol)二異丙基乙胺和50 mL無水二氯甲烷加至100 mL茄形瓶中,室溫攪拌2 h。旋蒸除溶劑后,反應液用100 mL乙酸乙酯溶解,分別用100 mL 0.1 mol/L HCl和100 mL水洗滌。有機相用無水Na2SO4干燥,抽濾后旋蒸濾液,用200~300目的硅膠柱純化,展開劑為V(石油醚)∶V(乙酸乙酯)=3∶1,得到0.25 g白色固體,即2-特丁基-4-氯-5-(2-對甲基苯磺酰基)-2H-3-噠嗪酮(2-tert-butyl-4-chloro-5-(2-tosyl)-2H-pyridazin-3-one, OTs-P2),產率63%。1H NMR (400 MHz, CDCl3)δ: 1.569 (s, 9H, N(CH3)3)、2.383 (s, 3H, phenyl-CH3)、4.312~4.367 (m, 4H, CH2CH2OH)、7.283 (d, 2H, CH3-phenyl)、7.757 (s, 1H, N=C-H)、7.734 (m, 2H, SO3-phenyl);13C NMR (100 MHz,CDCl3)δ: 21.70、 27.84、66.55、67.70、67.82、118.46、124.90、127.95、130.03、132.39、145.39、153.21、158.80;ESI-MS C17H21ClN2O5S: 計算值為400.1,實驗值為401.3; 元素分析C17H21ClFN2O5S: 計算值為C50.93%, H5.28%, N6.99%;實驗值為C50.82%, H4.65%, N6.61%。IR (CH2Cl2,cm-1) v: 1 634 (C=O), 1 274 (=C—O—C);熔點:104~105 ℃。結構分析結果確定產物為目的化合物。
將1 mL 1 mol/L 四正丁基氟化銨的THF溶液加至25 mL反應瓶中,110 ℃氮氣吹干。加入1 mL無水乙腈蒸發至干,重復3次。將0.200 g(0.5 mmol)OTs-P2溶于10 mL無水乙腈,加至反應瓶中,回流40 min。反應液經旋蒸后,用20 mL二氯甲烷溶解,用20 mL水洗滌。有機相用MgSO4干燥,抽濾后旋蒸濾液,經200~300目硅膠柱純化,展開劑為V(石油醚)∶V(乙酸乙酯)=3∶1,得到112 mg白色固體,即19F-FP2,產率65%。1H NMR (400 MHz, CDCl3)δ: 1.626 (s, 9H, N(CH3)3)、3.141 (dt, 2H, CH2CH2F)、4.597~4.829 (m, 6H, CH2CH2-triazolyl-CH2CH2CH2F)、7.656 (s, 1H, N=C—H)、7.729 (s, 1H, triazolyl)。13C NMR (100 MHz,CDCl3)δ: 27.28 (d, J=22 Hz), 27.83、49.43、66.74、68.66;82.33 (d, J=167 Hz)、118.34、124.36、153.03、158.77;熔點:87~88 ℃。結構分析結果表明,產物為目標化合物。
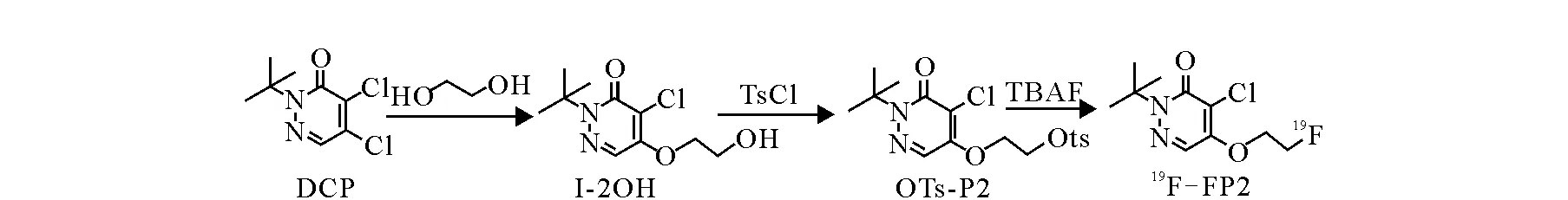
圖2 19F-FP2的合成路線Fig.2 The synthesis route of 19F-FP2
2.2 18F-FP2的合成
18F-FP2的合成路線示于圖 3。
將0.3 mL含有3 mg K2CO3的水溶液和1 mL含有11 mg K2.2.2的乙腈溶液混合,用上述混合液將18F-從QMA柱淋洗至10 mL反應瓶中,110 ℃氮氣吹干。加入0.5 mL無水乙腈蒸發至干,重復3次。將2 mg OTs-P2溶于1 mL 無水乙腈,加至反應瓶中,90 ℃反應30 min。反應結束后冷卻至室溫,注入C18 反相半制備柱,收集保留時間為16.5~17.5 min的組分,即為18F-FP2。HPLC條件為:A相為水,B相為乙腈;淋洗梯度:0~5 min 95%A,5.01~8 min 95%~60%A,8.01~19 min 60%~30%A。

圖3 18F-FP2的合成路線Fig.3 The synthesis route of 18F-FP2
2.3 18F-FP2的穩定性
將1.85 MBq經HPLC純化后的18F-FP2溶于1 mL水中,在室溫下放置3 h,每隔1 h取0.2 mL溶液,采用HPLC檢測其放化純度。
2.4 18F-FP2脂水分配系數的測定
配制0.025 mol/L KH2PO4溶液,加入適量NaOH溶液,調節pH至7.4,得到PBS緩沖溶液,加入與之等體積的正辛醇,充分振蕩后室溫靜置1 d以上。取上層正辛醇0.6 mL,下層PBS液0.58 mL,并取0.02 mL18F-FP2水溶液混合,用渦旋混合器振蕩3~5 min,充分混勻。然后離心5 min,在有機相和水相中分別平行取3個樣,每個樣0.1 mL,用γ計數器測量其放射性活度,每個樣品平行測定3次。計算分配系數lgP值。
2.5 18F-FP2在正常小鼠體內的生物分布
由正常昆明小鼠尾靜脈注射0.1 mL18F-FP2水溶液(0.185 MBq),注射后2、15、30和 60 min將其斷頭處死。取心、肝、脾、肺、肉、骨、血、腎等有關組織和器官,擦凈后稱重,并在γ計數器上測定放射性活度,計算各組織的每克百分注射劑量率(%ID/g)。
3 結果與討論
3.1 18F-FP2的放化產率及放化純度
從18F-起,至純化完畢,制備總時間為70~90 min,衰變校正后的放化產率為53.0%±5.2%。產物的放化純度>98%,比活度約為20 TBq/g。18F-FP2及19F-FP2的HPLC譜圖示于圖4。由圖4可以看出,18F-FP2的保留時間為16.7 min,和相應的參考物質19F-FP2的保留時間16.5 min一致。說明所得到的標記物為目標產物18F-FP2。
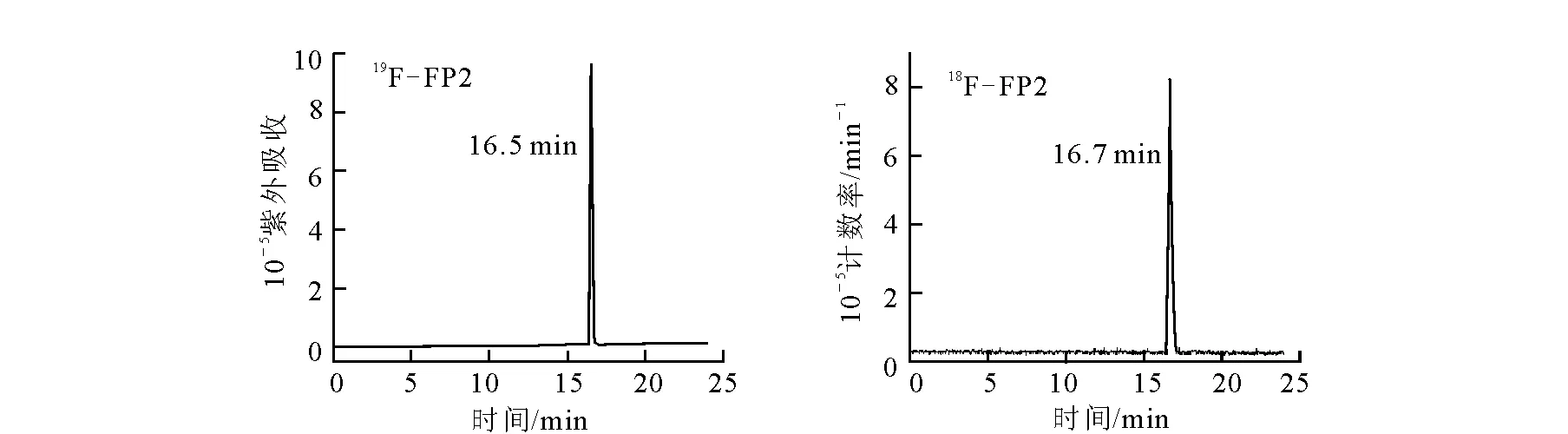
圖4 19F-FP2和18F-FP2的HPLC圖譜Fig.4 The HPLC chromatograms of 19F-FP2 and 18F-FP2
3.2 18F-FP2的穩定性研究
18F-FP2在水溶液中放置3 h后的HPLC譜圖示于圖5。由圖 5可見,18F-FP2在水溶液中的穩定性較好,室溫放置3 h后,放化純度仍>98%。與先前報道的18F-FP1OP[10]、18F-FP2OP[13]相比,其在水溶液中的穩定性有顯著提高。較好的穩定性是藥物臨床推廣使用的前提,也為將來設計穩定的標記化合物提供參考。

圖5 18F-FP2在水溶液中室溫放置3 h后的HPLC譜圖Fig.5 The HPLC chromatograms of 18F-FP2,incubated in water for 3 h
3.3 18F-FP2脂水分配系數的測定
實驗測得18F-FP2的lgP為0.42±0.02,表明其為脂溶性物質。但是其親脂性明顯低于先前報道的化合物(18F-FP1OP[10]和18F-FP2OP[13]),這與標記化合物結構中側鏈苯環的去除有直接關系。
3.4 18F-FP2在正常小鼠體內的生物分布
18F-FP2在正常小鼠體內的生物分布結果列于表1。由表1數據可見,18F-FP2在小鼠肝、肺等器官具有很高的初始攝取,但是清除也很快。在心肌中的初始攝取較低,僅為(4.09±0.53)%ID/g,且清除較快。心肌的低攝取使T/NT較不理想,不符合心肌灌注顯像劑的基本要求。這說明去除噠螨靈結構中的芳環,會嚴重影響化合物在心肌中的攝取。側鏈中的芳環為噠螨靈衍生物保持心肌高攝取的必需基團。
4 結 論
本工作設計并制備了一種18F標記的噠嗪酮類似物18F-FP2,其校正后的放化產率為53.0%±5.2%,放化純度>98%,比活度約為20 TBq/g。18F-FP2為脂溶性化合物,且在水溶液中的穩定性較好,室溫放置3 h放化純度仍>98%。小鼠生物分布結果顯示,該標記物在心肌中的初始攝取較低且清除較快,不適于心肌顯像。
表1 18F-FP2在正常小鼠體內的生物分布
綜上所述,本研究雖然獲得了穩定性更好的標記化合物,但是由于標記側鏈上的苯環去除后大幅降低了心肌攝取,使其不適合用于心肌顯像。鑒于此,建議今后在該類標記物的設計中應保留噠嗪酮側鏈的芳環結構。
參考文獻:
[1] Yu M, Guaraldi M, Kagan M, et al. Assessment of18F-labeled mitochondrial complex I inhibitors as PET myocardial perfusion imaging agents in rats, rabbits, and primates [J]. European Journal of Nuclear Medicine and Molecular Imaging, 2009, 36: 63-72.
[2] Yalamanchili P, Wexler E, Hayes M, et al. Me-chanism of uptake and retention of F-18 BMS-747 158-02 in cardiomyocytes: a novel PET myocardial imaging agent [J]. Journal of Nuclear Cardiology, 2007, 14: 782-788.
[3] Huisman MC, Higuchi T, Reder S, et al. Initial Characterization of an18F-Labeled Myocardial Perfusion Tracer [J]. Journal of Nuclear Medicine, 2008, 49: 630-636.
[4] Yu M, Guaraldi MT, Bozek J, et al. Effects of food intake and anesthetic on cardiac imaging and uptake of BMS747158-02 in comparison with FDG [J]. Journal of Nuclear Cardiology, 2009, 16: 763-768.
[5] Sherif HM, Saraste A, Weidl E, et al. Evaluation of a Novel18F-Labeled Positron-Emission Tomography Perfusion Tracer for the Assessment of Myocardial Infarct Size in Rats / CLINICAL PERSPECTIVE [J]. Circulation: Cardiovascular Imaging, 2009, 2: 77-84.
[6] Yu M, Bozek J, Guaraldi M, et al. Cardiac imaging and safety evaluation of BMS747158, a novel PET myocardial perfusion imaging agent, in chronic myocardial compromised rabbits [J]. Journal of Nuclear Cardiology, 2010, 17: 631-636.
[7] Maddahi J, Czernin J, Lazewatsky J, et al. Phase I, First-in-Human Study of BMS747158, a Novel18F-Labeled Tracer for Myocardial Perfusion PET: Dosimetry, Biodistribution, Safety, and Imaging Characteristics After a Single Injection at Rest [J]. Journal of Nuclear Medicine, 2011, 52: 1 490-1 498.
[8] Maddahi J, Bengel F, Huang SC, et al. Phase 1 rest-stress study of F-18 labeled BMS747158 myocardial perfusion PET tracer: Human safety, dosimetry, biodistribution, and myocardial imaging characteristics [J]. Journal of Nuclear Medicine, 2009, 50: 184-184.
[9] Sherif HM, Nekolla SG, Saraste A, et al. Simplified Quantification of Myocardial Flow Reserve with flurpiridaz F 18: Validation with Microspheres in a Pig Model [J]. Journal of Nuclear Medicine, 2011, 52: 617-624.
[10] Mou T, Zhao Z, Fang W, et al. Synthesis and Preliminary Evaluation of18F-labeled Pyridaben Analogues for Myocardial Perfusion Imaging with Positron Emission Tomography [J]. Journal of Nuclear Medicine, 2012, 53: 472-479.
[11] Purohit A, Radeke H, Azure M, et al. Synthesis and Biological Evaluation of Pyridazinone Analogues as Potential Cardiac Positron Emission Tomography Tracers [J]. Journal of Medicinal Chemistry, 2008, 51: 2 954-2 970.
[12] Mou T, Zhao Z, Yang W, et al. Radiosynthesis and biodistribution of [18F]FPTP2 as potential myocardial perfusion imaging agent [J]. Journal of Labelled Compounds and Radiopharmaceuticals, 2011, 54: S446.
[13] Mou T, Jing H, Yang W, et al. Preparation and biodistribution of [18F]FP2OP as myocardial perfusion imaging agent for positron emission tomography [J]. Bioorganic & Medicinal Chemistry, 2010, 18: 1 312-1 320.

