聯合應用eGFR和Hb濃度對冠狀動脈介入治療CKD合并冠心病患者預后價值的初步評價
唐紅霞,唐 新,賈克剛
(天津泰達國際心血管病醫院檢驗科,天津300457)
慢性腎臟病(CKD)是由于各種原因引起的慢性腎臟損害,具有患病率高、合并心血管疾病率高和死亡率高等特點。很多CKD合并冠心病患者在行經皮冠狀動脈擴張術(PCI)后的治療效果并不樂觀。國外學者研究發現術前檢測患者的血紅蛋白(Hb)水平對CKD患者PCI術后心臟病不良事件發生率有良好的預測作用[1-4],目前國內還未見相關報道。因此,我們評估了估算的腎小球濾過率(eGFR)和Hb對行PCI術的CKD合并冠心病患者住院期間和出院4年內預后的預測價值。
材料和方法
一、對象
選擇2004年1月至2007年12月間在泰達國際心血管病醫院行PCI術的CKD合并心病患者1 005例,其中男704例、女301例。詳細記錄患者的性別、年齡、身高、體重、吸煙、高脂血癥、高血壓、糖尿病、有無心肌梗死病史、病變支數、術前PCI、左室射血分數(LVEF)、心功能分級、術前肌酐、術后住院天數、生存時間(月)以及術后1~4年發生心臟事件等情況。所有患者入院行PCI術前采血測定血清肌酐(SCr),用于計算eGFR。根據2002年美國腎臟病患者生存質量指導組(K/DOQI)指南[5]對CKD患者的最新診斷標準確診CKD。依據eGFR值分為eGFR≥60 mL/min 935例(男660例、女275例),eGFR<60 mL/min 70例(男44例、女26例),同時根據世界衛生組織(WHO)2008年制定的貧血標準[6](男性 <120 g/L、女性<110 g/L)分為4組:A組為eGFR<60 mL/min合并貧血組,共18例,其中男9例、女9例,年齡36~85歲;B組為eGFR<60 mL/min無貧血組,共52例,其中男35例、女17例,年齡45~83歲;C組為eGFR≥60 mL/min合并貧血組,共37例,其中男24例、女13例,年齡40~79歲;D組為eGFR≥60 mL/min無貧血組,共898例,其中男636例、女262例,年齡31~84歲。病例基本情況見表1。
二、方法
1.樣本采集 患者入院行PCI術前清晨空腹采集肘靜脈血3 mL,室溫下靜置30 min后2 000×g離心10 min分離血清,上機檢測。同時采集肘靜脈血2 mL,EDTA-K2抗凝顛倒混勻,上機測定。
2.儀器與試劑 SCr試劑(酶法)為日本和光公司產品,校準品及質控物均為配套產品。Hb用SYSMEX-2100全自動血液分析儀檢測,試劑、校準品及質控物均為Sysmex公司配套產品。
3.檢測方法 在日立7600全自動生化分析儀上采用酶法測定SCr。和光試劑(酶法)的Cr溯源采用美國國家標準與技術研究院(National Institute of Standards Technology,NIST)參考物質(SRM)914a為標準物質,采用氣相色譜-丙基乙二胺-薄層色譜法(GC-PSA-TLC)為Cr定值,未溯源到同位素稀釋質譜法(ID-MS)。但和光公司在日立7600全自動生化分析儀上做了和光酶法試劑和羅氏酶法試劑兩者的相關分析,得出公式:Y=0.890X+1.283,n=48,R2=0.992 6。Y 軸、X軸分別表示和光、羅氏酶法試劑測定的值用上述相關公式換算成可溯源至ID-MS的日立-羅氏Cr檢測系統檢測結果。Hb用Sysmex-2100全自動血液分析儀檢測定值。
4.eGFR的計算 eGFR用簡化的腎病膳食改良實驗(MDRD)方程計算[7-11]:eGFR=175×(SCr/88.4)-1.154×(年齡)-0.203×(0.742女)。
5.隨訪記錄 嚴格記錄所有患者年齡、性別、體重指數(BMI)、術前SCr值、吸煙、高血脂、糖尿病、高血壓、有無心肌梗死病史、病變指數、左室射血分數、心功能分級、術后住院天數和出院后4年內的心臟病事件。所有患者隨訪30 d~4年(中位數為3年;出院患者以電話形式隨訪,記錄心臟事件,包括再入院急性心肌梗死和心源性死亡),相同時間多次發生計1次,不同事件連續發生計最嚴重的事件。

表1 1 005例行PCI術患者的基本情況
三、統計學方法
采用SPSS 17.0統計軟件對實驗數據進行統計學處理。計量資料用±s或中位數(四分位數)表示,比較采用方差分析或秩和檢驗。計數資料分析采用卡方檢驗,病變支數、心功能分級、LVEF(%)采用秩和檢驗,如有超過1/5格子的理論數<5則采用Fisher精確檢驗。P<0.05表示差異有統計學意義。對預后因素的分析采用COX回歸分析,4組間生存曲線的比較使用Kaplan-Meier法,并用對數秩和分析(Log-rank statistic)進行組間生存率的比較。
結 果
一、入選患者的一般情況比較
不同eGFR值4組PCI患者的性別、體重指數(BMI)、術前PCI差異均無統計學意義(P>0.05)。吸煙、高脂血癥、糖尿病、有無心肌梗死病史、病變支數、年齡、高血壓、LVEF(%)在不同eGFR值組中差異有統計學意義(P<0.05),見表1。
二、不同eGFR值4組術后住院天數的比較
4組患者的住院天數呈非正態分布,以中位數(上、下四分位數),即 P25、P50和 P75表示。4組之間術后住院天數差異均有統計學意義(P<0.05),見表2。
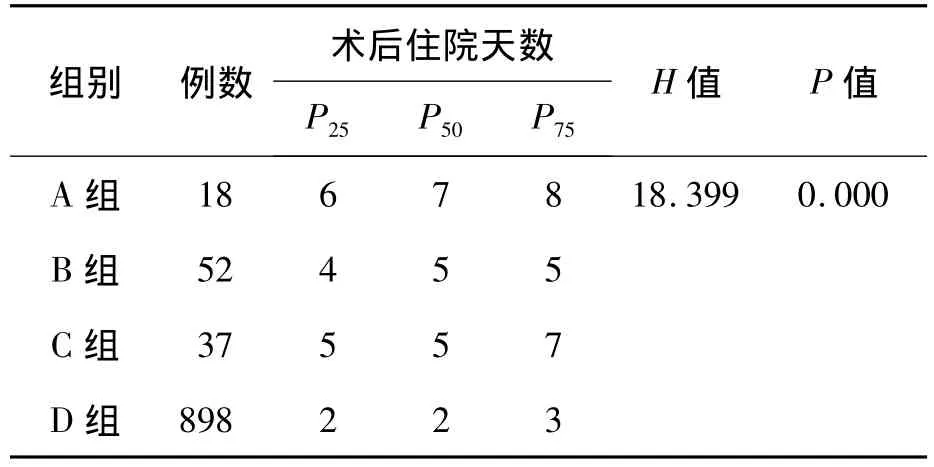
表2 不同eGFR值4組術后住院天數的比較
三、PCI患者的多因素COX回歸分析
多因素分析校正BMI、吸煙、高血壓、高脂血癥、糖尿病、有無心肌梗死病史、病變支數、術前PCI等危險因素及Hb后,發現住院期間和出院4年內,病變支數增加與發生心臟事件的相對危險度(RR)為1.333[95%可信區間(CI):1.023~1.738,P=0.033];本次術前曾行 PCI術與發生心臟事件的RR為3.142(95%CI:1.974~5.001,P=0.000);術前Hb與發生心臟事件的RR 為1.006(95%CI:0.990~1.023,P=0.446),見表3。
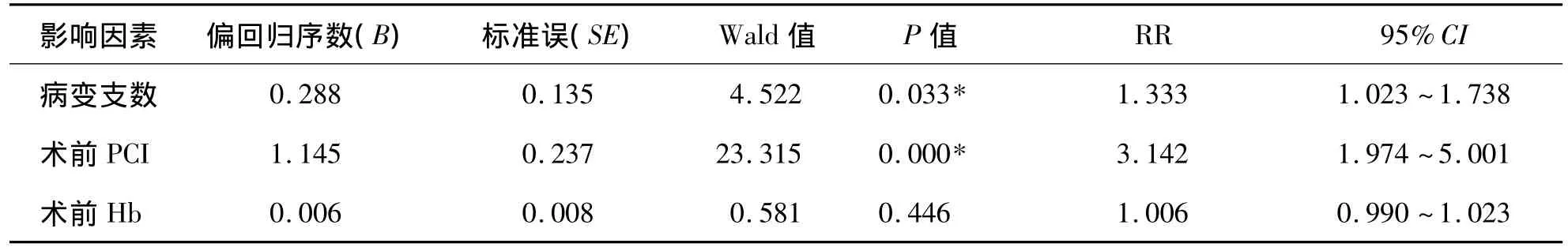
表3 1 005例PCI患者心臟事件的多因素COX回歸分析結果
四、A~D組PCI術后患者的生存率比較
4組患者1、2、3、4年的生存率比較差異有統計學意義(P=1.015),見表4。4組內各自1、2、3、4年的每年生存率也不盡相同。4組患者的生存曲線見圖1。
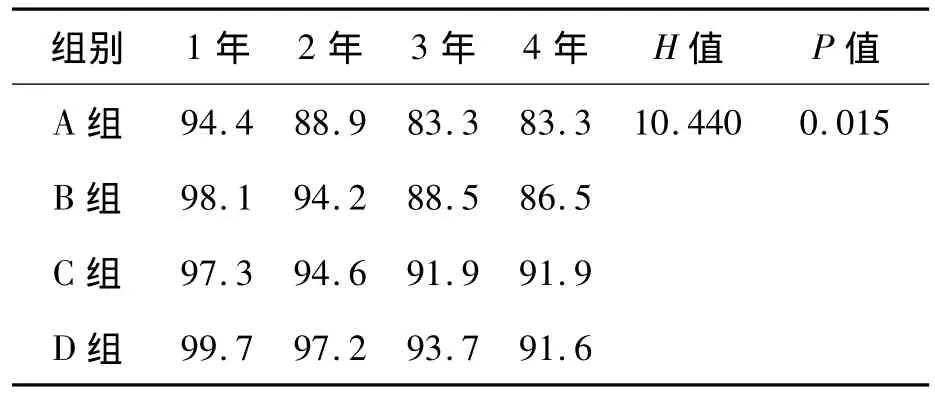
表4 4組患者1~4年間生存率比較 (%)
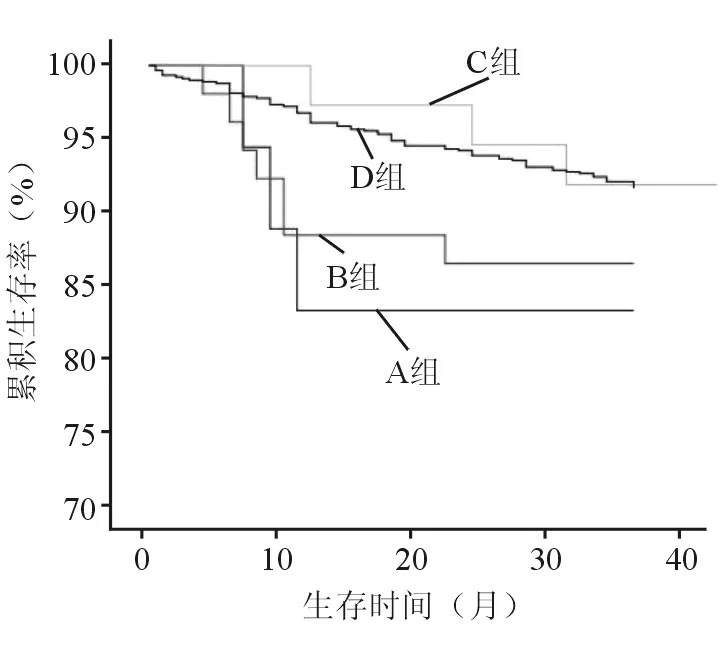
圖1 A~D 4組PCI術后患者的生存曲線
討 論
CKD患者存在不同程度的貧血,原因在于成人促紅細胞生成素85%由腎臟產生(近曲小管、腎臟皮質與髓質小管的內皮細胞)。當腎臟病變達到一定程度時,腎臟生成促紅細胞生成素障礙,紅細胞生成減少就會出現貧血[12-13]。CKD合并心血管病患者Hb濃度可否用于PCI術后的評估是當前研究的熱點。
本研究發現,行 PCI術的 4組(eGFR<60 mL/min合并貧血組、eGFR<60 mL/min無貧血組、GFR≥60 mL/min合并貧血組和eGFR≥60 mL/min無貧血組)患者的性別、BMI、病變支數和術前PCI無明顯差異(P>0.05),年齡、吸煙、高脂血癥、高血壓、糖尿病、有無心肌梗死病史、LVEF(%)在4組間差異有統計學意義(P<0.05),說明除年齡外,高血壓、糖尿病、心肌梗死等的患病率可能會對CKD的疾病譜產生一定的影響。4組患者術后住院天數差異有統計學意義(P<0.05),eGFR≥60 mL/min無貧血組住院天數明顯少于其他3組。
本研究還發現在1 005例患者術后4年隨訪的生存曲線中,4組間生存率差異有統計學意義(P=0.015),且eGFR<60 mL/min合并貧血組生存率明顯低于其他3組。說明CKD合并貧血患者PCI術后的住院死亡率明顯增高。eGFR≥60 mL/min無貧血組生存曲線平緩,生存率高;eGFR<60 mL/min合并貧血組1年以后的生存率維持在較低的水平;而eGFR≥60 mL/min的2組患者不管是否合并貧血,在隨訪的3~4年中其生存率無明顯差異,趨于穩定。Levin等[1]對3 028例老年、eGFR<60 mL/min的CKD患者聯合Hb分組研究發現eGFR越小、Hb越低,患者PCI術后住院時間越長,死亡率也越高;同一水平eGFR值的患者Hb越低,其生存率也越低,差異有統計學意義(P<0.001),證實了CKD患者術前Hb的評價是其住院時間和住院死亡率的獨立危險因素。Ferrari等[2]研究應用MDRD方程評估9 853例老年CKD患者術前eGFR,發現eGFR<60 mL/min在老年人中較普遍,應采用eGFR<45 mL/min作為分級標準;在eGFR<45 mL/min的患者中貧血普遍,有較高的病死率,Hb是CKD患者術后病死率的一個獨立的預示因子,與本研究結果一致。因此,患者行PCI術前評估其eGFR和Hb對于預測住院天數和住院費用有參考價值,特別是術后心臟事件的發生率有意義,可作為評價PCI患者醫院死亡率的一個獨立危險因素,是評估患者治療、預后判斷、住院費用的依據,可指導臨床實踐。
多因素分析結果校正BMI、吸煙、高血壓、高脂血癥、糖尿病、有無心肌梗死病史、病變支數、術前PCI等危險因素后,發現病變支數增加與發生心臟事件的RR為1.333(95%CI:1.023~1.738,P=0.033),說明病變支數增加是患者住院期間和術后4年內發生心臟事件的危險因子。生存分析發現本研究PCI術前曾行PCI術發生心臟事件的RR為3.142(95%CI為1.974~5.001,P=0.000);術前Hb與發生心臟事件的RR為1.006(95%CI為0.990~1.023,P=0.446)。說明 Hb值每降低10 g/L,心臟事件的風險將增加到1.006倍。國外已有報道CKD患者術前Hb值對PCI術治療的預后有一定的評估作用[1-4]。Levin等[1]對3 028例老年、eGFR <60 mL/min的 CKD患者以 eGFR <15、15~29、30~59 mL/min聯合Hb每10 g/L的改變進行分組,得出Hb值每降低10 g/L,心臟事件的風險將增加到1.25倍,增加25%;Hb<100 g/L患者基本上是Hb≥140 g/L的患者2倍。
本研究因受研究例數過少的限制,相對于eGFR>60 mL/min無貧血組898例,其他各組例數較少,其統計學結果顯示Hb值增加與發生心臟事件風險的比例值較低,但聯合患者eGFR值仍然顯示隨著Hb值的增加,患者的生存率升高,發生心臟事件的風險降低,這與Levin等[1]的報道一致。今后將擴大研究病例數、改進eGFR和Hb的分級、分組標準,聯合其他心臟標志物進一步探討聯合患者eGFR研究Hb值的增加與發生心臟事件風險的比例關系。
[1]Levin A,Djurdjev O,Duncan J,et al.Haemoglobin at time of referral prior to dialysis predicts survival:an association of haemoglobin with long-term outcomes[J].Nephrol Dial Transplant,2006,21(2):370-377.
[2]Ferrari P,Xiao J,Ukich A,et al.Estimation of glomerular filtration rate:does haemoglobin discriminate between ageing and true CKD[J].Nephrol Dial Transplant,2009,24(6):1828-1833.
[3]Husemann W,Fobker M,Pohlen M,et al.Impact of haemoglobin concentration and chronic kidney disease in patients with coronary heart disease undergoing percutaneous coronary interventions[J].Nephrol Dial Transplant,2007,22(9):2563-2570.
[4]Nozue T,Michishita I,Iwaki T,et al.Contrast medium volume to estimated glomerular filtration rate ratio as a predictor of contrast-induced nephropathy developing after elective percutaneous coronary intervention[J].J Cardiol,2009,54(2):214-220.
[5]National Kidney Foundation.K/DOQl clinical practice guidelines for chronic kidney disease:evaluation,classification,and stratification[J].Am J Kidney Dis,2002,39(2 Supp 1):S1-S266.
[6]McLean E,Cogswell M,Eqli I,et al.Worldwide prevalence of anaemia,WHO vitamin and mineral nutrition information system,1993-2005[S].Public Health Nutr,2009,12(4):444-454.
[7]吳 炯,王 沖,郭 瑋,等.腎小球濾過率的估算及其臨床應用[J].中華檢驗醫學雜志,2007,30(11):1214-1218.
[8]潘柏申.血肌酐檢測和腎小球濾過率估計[J].中華檢驗醫學雜志,2007,30(11):1205-1206.
[9]賈克剛,韓雪晶,南 芳,等.估算的腎小球濾過率在冠狀動脈旁路移植術預后價值的研究[J].中華檢驗醫學雜志,2009,32(10):1096-1100.
[10]賈克剛,韓雪晶,唐紅霞,等.血清肌酐和估算腎小球濾過率在評價冠狀動脈旁路移植術患者預后的比較研究[J].檢驗醫學,2009,24(9):688-690.
[11]周長邵,韓雪霞,周慧麗,等.肌酐清除率、Cockcroft-Gault公式及MDRD方程評估腎小球濾過率的差異性研究[J].檢驗醫學,2008,23(6):677-678.
[12]孫勁秋,何學紅.腎性貧血機制探述[J].遼寧中醫學院學報,2005,7(5):515-517.
[13]孫雪峰.慢性腎臟病合并腎性貧血的處理策略[J].中國實用內科雜志,2010,30(2):106-108.