尼卡地平、尼莫地平和尼群地平毛細管電泳手性拆分研究
蔡 誠,王園朝,鄧 飛
(杭州師范大學材料與化學化工學院,有機硅化學及材料技術教育部重點實驗室,浙江杭州 310036)
尼卡地平、尼莫地平和尼群地平毛細管電泳手性拆分研究
蔡 誠,王園朝,鄧 飛
(杭州師范大學材料與化學化工學院,有機硅化學及材料技術教育部重點實驗室,浙江杭州 310036)
文章以環糊精及其衍生物為手性試劑,研究了血管擴張型降壓藥鹽酸尼卡地平、尼莫地平和尼群地平手性對映體拆分方法.采用區帶毛細管電泳模式,以高磺化環糊精(HS-CD)為手性識別試劑,考察了手性試劑的類型、濃度及緩沖溶液pH值等對分離度的影響,確定了拆分尼卡地平、尼莫地平和尼群地平手性對映體的最佳條件.結果表明鹽酸尼卡地平在HS-γ-CD手性選擇劑存在下對映體獲得基線分離,尼莫地平和尼群地平分別在HS-β-CD和HS-α-CD手性選擇劑存在下對映體獲得部分分離,并對其分離機理進行了初步探討.
毛細管區帶電泳;高磺化環糊精;手性對映體拆分;鹽酸尼卡地平;鹽酸尼莫地平;鹽酸尼群地平
尼卡地平(Nicardipine,NCD)、尼莫地平(Nimodipine,NMD)和尼群地平(Nitrendipine,NTD)屬第二代1,4-二氫吡啶類鈣拮抗劑(DPHs),通過抑制細胞外Ca的內流、松弛血管平滑肌而起到降壓作用,用于低、中度高血壓病.結構中二氫吡啶環上的4位C為不對稱碳原子(見圖1),存在兩個對映體,因在藥理活性上存在著明顯差異[1-2],對映體分離已引起人們廣泛關注.目前對尼卡地平、尼莫地平和尼群地平的手性分離大多是利用HPLC方法,分離柱手性固定相主要有直鏈淀粉衍生物[3]、大環抗生素類[4]、多糖及纖維素類[5]、卵類粘蛋白[7]和卵類糖蛋白[8]等.毛細管電泳在手性分離方面具有一定的優勢,其手性分離的關鍵是手性試劑的選擇,環糊精因其特殊的空穴結構,廣泛應用于手性物質的分離.在此選擇羥丙基和高磺化兩種類型環糊精衍生物為緩沖溶液手性添加劑,試驗了上述3種結構類似藥物對映體分離條件,基線分離了尼卡地平,部分分離了尼莫地平和尼群地平手性對映體,并對其分離機理進行了初步的討論.
1 實驗部分
1.1 儀器與試劑
Beckman P/ACE MDQ毛細管電泳儀,PDA檢測器,32Karat軟件(美國Beckman公司);熔融石英毛細管裸柱,60cm×50μm,有效長度為49cm(美國Beckman公司).
羥丙基-α,β,γ-環糊精(HP-α,β,γ-CD)(Fluka)、高磺化-α,β,γ-環糊精(HS-α,β,γ-CD)(Beckman);鹽酸尼卡地平、鹽酸尼莫地平和鹽酸尼群地平對照品(中國藥品生物制品檢定所),配成濃度為1.0mg·mL-1的水溶液,1,3,6,8-pyrenetetrasulfonate(PTS)作標記物;其余試劑均為分析純,水為去離子水.
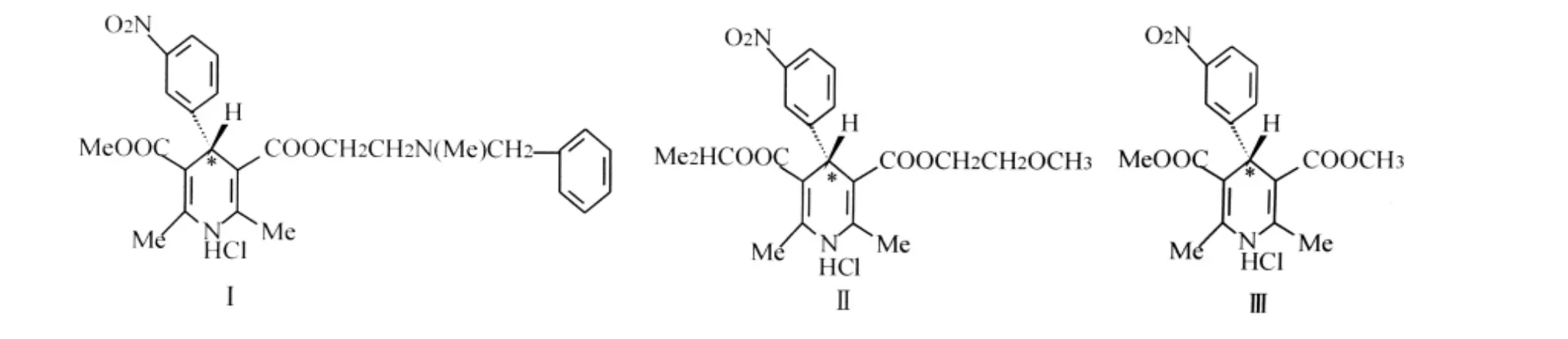
圖1 尼卡地平(Ⅰ)、尼莫地平(Ⅱ)和尼群地平(Ⅲ)的化學結構圖Fig.1 Chemical structures of Nicardipine(Ⅰ)、Nimodipine(Ⅱ)and Nitrendipine(Ⅲ)
1.2 實驗方法
1.2.1 運行緩沖溶液的制備
于一小燒杯中取20%HS-α(β,γ)-CD水溶液5mL,水5mL和100mmol·L-1H3PO4溶液10mL,在pH計上用三乙胺調到所需pH值.即可得到含5%HS-α(β,γ)-CD的50mmol·L-1三乙胺磷酸鹽緩沖溶液.使用前用0.22μm針筒過濾器過濾.
1.2.2 對照品溶液的制備
分別稱取10.0mg鹽酸尼卡地平、鹽酸尼群地平,用少量甲醇溶解后,配成10mL的甲醇/水溶液,即得濃度為1.0mg·mL-1的貯備液,鹽酸尼莫地平貯備液濃度為0.5mg·mL-1.置于冰箱中4℃保存.1.2.3 樣品溶液的制備
分別取200μL濃度為1.0mg·mL-1鹽酸尼卡地平、尼群地平和0.5mg·mL-1尼莫地平貯備液,加入2μL PTS混勻,置于儀器樣品小管中即可.
1.2.4 毛細管柱處理方法
毛細管使用前用0.1mol·L-1NaOH溶液和水分別沖洗2min,運行緩沖溶液沖洗2min.兩次進樣間依次用0.1mol·L-1NaOH溶液、水和緩沖溶液各沖洗1min.
1.2.5 電泳條件
運行緩沖溶液含5%HS-α(β,γ)-CD的50mmol·L-1三乙胺磷酸鹽(pH 2.5);工作電壓:-15kV(反向電壓);檢測波長:200nm,柱溫:25℃;3kPa壓力進樣4s.
2 結果與討論
2.1 手性試劑的選擇
實驗分別選擇了HP-α,β,γ-CD和HS-α,β,γ-CD為手性選擇劑.在加正向分離電壓(8-15kV)和pH6-9范圍內,試驗了HP-α,β,γ-CD對3種手性藥物對映體的拆分效果,結果顯示3種手性藥物對映體均未獲得明顯的手性拆分,而在反相電壓和低pH值條件下,HS-α,β,γ-CD對3種藥物對映體的手性拆分都有明顯的效果,只是分離程度表現不同.其中常溫(25℃)下尼卡地平在HS-γ-CD中手性分離效果最好,但溫度升高時,在HS-α-CD和HS-β-CD中也能獲得較好的手性分離效果;尼莫地平只在HS-β-CD中手性分離效果最好;尼群地平只在HS-α-CD中手性分離效果最好.實驗以尼卡地平為對象,選擇HS-γ-CD為手性試劑,對實驗條件進行了探討.
2.2 緩沖溶液濃度及pH值對對映體分離度的影響
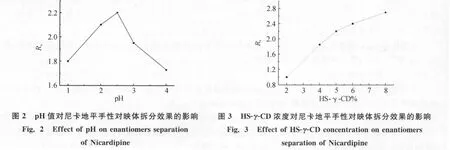
以HS-γ-CD為手性試劑,固定緩沖溶液pH值和磷酸鹽濃度,分別以磷酸鹽、磷酸鹽-tris和磷酸鹽-三乙胺進行試驗,發現單純的磷酸鹽為運行緩沖溶液時電流較大,焦耳熱效應明顯,譜峰拓展峰形拖尾;磷酸鹽-tris為緩沖溶液時,抑制了電流,使峰遷移時間過長,分離效果不理想;磷酸鹽-三乙胺作緩沖溶液時,遷移時間適中,基線穩定,峰形好且分離效果好.在20~70mmol·L-1范圍內,改變緩沖溶液濃度,表明在50mmol·L-1時,對映體分離效果最好.考慮到手性試劑與尼卡地平的充分作用,實驗選擇在較強酸性條件下進行,此時毛細管內壁硅羥基的離解被抑制,基本消除了電滲流,溶質主要依賴于自身電泳速度遷移.試驗了pH值從1~4范圍內變化對RS的影響,見圖2.當pH值較小時,一方面環糊精試劑與尼卡地平作用力加強,使分離變好,另一方面分離時間加長,使譜峰拓寬,分離度減小;當pH值較大時,毛細管壁硅羥基部分離解,有吸附現象基線不好,分離效果變差;當pH為2.5時,基線穩定,且RS最好.故選擇50mmol·L-1三乙胺磷酸鹽(pH2.5)為運行緩沖溶液.
2.3 HS-γ-CD濃度對對映體分離度的影響
HS-γ-CD濃度對鹽酸尼卡地平對映體分離度(RS)的影響見圖3.隨著選擇劑HS-γ-CD濃度的增大,分離度增加,但同時離子強度增加,焦耳熱效應增大.當HS-γ-CD%<5%(W/V)時,試劑與尼卡地平作用力較弱,而且此時緩沖體系粘度較小,遷移時間變短,導致分離不完全;當HS-γ-CD%>5%(W/V)時,濃度對分離度影響程度減弱,濃度太高,緩沖體系粘度較大,分離時間變長,峰形變寬.因此選擇5%HS-γ-CD為最佳手性試劑濃度.
2.4 分離電壓對對映體分離度的影響
柱溫為25℃時,分離電壓在10~25kV范圍內進行實驗,發現當分離電壓大于20kV時,因焦耳熱效應的影響,譜峰變寬,尼卡地平未能達到基線分離;而當電壓低于15kV時,分離時間變長,峰形拖尾,實驗選擇15kV為最佳分離電壓.
2.5 分離譜圖
最佳條件下,鹽酸尼卡地平、鹽酸尼莫地平和鹽酸尼群地平分別在HS-γ-CD、HS-β-CD和HS-α-CD手性選擇劑存在下的對映體分離譜圖(如圖4所示).尼卡地平的兩個手性對映體在HS-γ-CD中獲得了基線分離,而尼莫地平和尼群地平均未獲得基線分離.

圖4 尼卡地平(a)、尼莫地平(b)和尼群地平(c)的手性對映體拆分電泳圖Fig.4 Chiral seperation electropherogram of Nicardipine(a)、Nimodipine(b)and Nitrendipine(c)
2.6 手性識別機理討論
一般認為環糊精對分子手性拆分的機理主要有兩個方面,其一是環糊精杯狀結構內腔尺寸大小的空間匹配作用,其二是環糊精外緣端-OH與手性分子間的氫鍵作用.但在以前的研究中,筆者發現在低pH值條件下叔胺類藥物與高磺化環糊精之間還存在一定的靜電引力作用,有時靜電引力作用對手性對映體的拆分起著決定性的作用[9].該實驗中尼卡地平、尼莫地平和尼群地平分別在HS-γ-CD、HS-β-CD和HS-α-CD中獲得較好的手性拆分效果,這是環糊精與客體空間匹配作用的結果.但尼卡地平在升溫條件下(35℃),以HS-α(β)-CD為手性選擇劑時,也可獲得好的拆分效果,而其它兩種物質沒有此現象.這是因為含有叔氨基的尼卡地平,酸性條件下能獲得一個質子成為季胺鹽而帶正電,可與高磺化環糊精中-SO-3產生靜電引力作用.溫度較高時,分子運動速率加快,主客體間的空間匹配和氫鍵作用影響減弱,靜電引力作用在手性對映體拆分中起主要影響作用.
[1]Jamali F,Mehvar R,Pasutto FM.Enantioselective aspects of drug action disposition:therapeutic pitfalls[J].J Phram Sci,1989,78(9):695-715.
[2]Mast V,Fischer C,Mikus G,etal.Use of pesudoracemic nitrendipine to elucidate the metabolicsteps for stereoselective disposistion of nitrendipine enantiomers[J].Br J Clin Pharmacol,1992,33(1):51-54.
[3]陳仲益,姚彤煒,曾蘇.CHIRALPAK AD柱在14種藥物手性分離中的應用[J].中國藥學雜志,2007,42(7):544-547.
[4]李凌云,錢寶英,高如瑜,等.萬古霉素手性固定相分離幾種藥物對映體[J].分析測試學報,2003,22(6):83-85.
[5]宮麗,賀浪沖,任文艷,等.尼群地平對映體在Chiralcel OJ柱上的拆分特性研究[J].中國藥業,2006,15(3):23-24.
[6]鄒公偉,鄭琦,胡冠九,等.高效液相色譜中的纖維素衍生物手性固定相[J].分析化學,1995,23(4):466-473.
[7]Ohkubo T,Uno T,Sugawara K.Enantiomer separation of dihydropyridine derivative calcium antagonists by high-performance liquid chromatography with chiral stationary phases[J].J Chromatogr,1994,659(2):467-471.
[8]傅強,賀浪沖.卵類糖蛋白手性柱拆分鈣離子拮抗劑尼卡地平對映體[J].分析化學,2005,33(12):1779-1782.
[9]王園朝,金瑛芝,羅經文.10種手性藥物對映體毛細管電泳拆分方法及機理探討[J].分析科學學報,2009,25(1):21-25.
Study on the Enantiomeric Separation of Nicardipine,Nimodipine and Nitrendipine by Capillarary Electrophoresis
CAI Cheng,WANG Yuan-chao,DENG Fei
(College of Material,Chemistry and Chemical Engineering,Key Laboratory of Organosilicon Chemistry and Material Technology of Ministry of Education,Hangzhou Normal University,Hangzhou 310036,China)
Enantioseparation methods of antihypertensive vasodilator nicardipine,nimodipine and nitrendipine were studied using cyclodextrin and its derivatives as chiral reagents.Many factors such as the type of chiral reagent and its concentration,pH of buffer on resolution(Rs)were investigated using high sulfonated cyclodextrin(HS-CD)as chiral recognition reagent with capillary zone electrophoresis,and the optimized conditions of enantioseparation of nicardipine hydrochloride,nimodipine and nitrendipine were defined.The results indicate that nicardipine hydrochloride,nimodipine and nitrendipine are well separated with chiral reagent HS-γ-CD,HS-β-CD and HS-α-CD respectively.The paper discussed their separation mechanisms.
capillary electrophoresis;highly sulfated cyclodextrins;enantioseparation;nicardipine;nimodipine;nitrendipine
R917
A
1674-232X(2012)02-0122-04
11.3969/j.issn.1674-232X.2012.02.006
2011-04-13
浙江省自然科學基金項目(Y406237);浙江省科技廳科技計劃項目(2007F70051).
王園朝(1965—),男,教授,主要從事分子光譜及毛細管電泳分析方法研究.E-mail:wangyc1819@126.com

