改良大泡技術輔助的暴露后彈力層深板層角膜移植術(附視頻)
高華 賈艷妮 宋鵬 丁剛 李素霞 史偉云
角膜移植術是治療角膜盲的主要手術方法。穿透角膜移植術(penetrating keratoplasty,PK)術后發生排斥反應、角膜移植片慢性失功和角膜移植片哆開等風險較高[1]。板層角膜移植術更加安全,但常規板層角膜移植術(保留一部分角膜后部基質)層間界面不規則、清亮度低,影響術后視力恢復及視覺質量提高[2]。大泡技術輔助的暴露后彈力層深板層角膜移植術(deep anterior lamellar keratoplasty,DALK)方法于2002年由Anwar和Teichmann首次描述[3],主要用于治療圓錐角膜[4]。此方法由于能暴露光滑的后彈力層使術后層間界面的問題得到有效解決,但是該方法對手術技術要求高,術中易發生后彈力層破裂[5],限制了其在國內的廣泛開展。我們對大泡技術輔助的暴露后彈力層DALK手術方法進行了改良,用于治療深層感染性角膜炎和斑塊狀角膜營養不良等角膜內皮細胞無明顯病變的疾病(此類患者以往常規選擇PK),減少了術中發生后彈力層穿孔和圍手術期其他并發癥的風險。現將我們近期在臨床實施這一方法后的資料作一總結。
1 對象與方法
1.1 對 象
2011年1月至2012年8月就診于山東省眼科醫院的深層感染性角膜炎患者和角膜基質病變患者屬于下列情況:感染性角膜炎的患者用藥過程中角膜潰瘍加重,潰瘍面積和深度增加,裂隙燈顯微鏡或眼前段光學相干斷層掃描(optical coherence tomography,OCT)檢查角膜潰瘍或浸潤深度超過4/5的深層感染者;斑塊狀角膜營養不良或角膜混濁的患者手術前行角膜OCT檢查和激光共聚焦顯微鏡檢查,后彈力層完整且周邊透明區域角膜內皮細胞密度超過1500個/mm2者納入行DALK,同時作PK準備備用。共37例患者(38只眼)擬行DALK,其中男性23例、女性14例,年齡24~72歲,平均(47.7±12.5)歲。真菌性角膜炎23例、細菌性角膜炎9例、棘阿米巴角膜炎1例、束狀角膜炎1例、斑塊狀角膜營養不良3例(4只眼)。
1.2 手術方法(見視頻1)
1.2.1 術前準備與麻醉
手術前常規準備。2%利多卡因5 mL和羅派卡因5 mL行球周阻滯和眼輪匝肌麻醉,壓迫20~30 min充分降低眶周壓力。
1.2.2 植床準備
(1)切除部分病變角膜:縫合固定上下直肌后,定位病變中心,采用16刀角膜標記器標記,采用負壓環鉆(根據病變范圍,環鉆直徑選擇 7.5~9.5 mm)鉆切角膜深度約250μm,采用角膜板層刀將前部感染或病變的角膜基質切除。
(2)注入空氣分離后彈力層:采用30號穿刺針針頭斜面向下與角膜頂點水平面成10°~30°穿刺進入后部角膜基質,在穿刺過程中避免針尖與角膜表面角度過大穿透角膜植床引起注氣失敗(見圖1)。進入后部角膜基質后快速注入無菌空氣約1 mL,此時可見無菌空氣彌散到角膜基質,角膜基質迅速變白。無菌空氣彌散的力量將后彈力層與基質層分離。此時部分患者可見部分氣體通過房角進入到前房(見圖2)。如因穿刺深度不足一次注氣不成功,可重復注氣直至角膜基質與后彈力層之間形成大氣泡,并部分或全部與后彈力層分離。
(3)繼續切除部分角膜基質:在0.12 mm顯微有齒鑷的輔助下,采用45°角膜刀逐漸向下切除變白的角膜基質。在此過程中應仔細謹慎,直至角膜植床由灰白色變為半透明時,停止向深層切削,水平繼續切除部分角膜基質層。殘留厚約50μm的基質層和后彈力層。
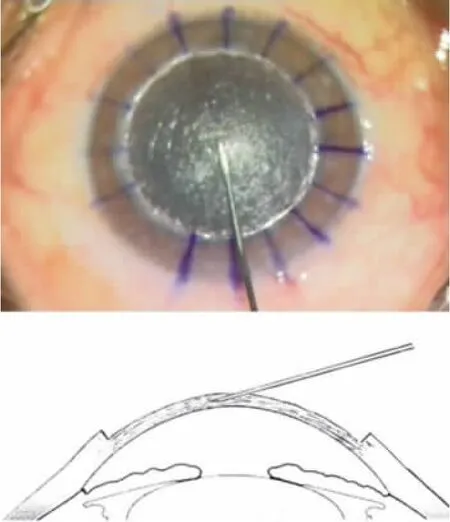
圖1 切除角膜前部基質后,采用30號穿刺針針頭穿刺進入后部角膜基質(下方為示意圖)
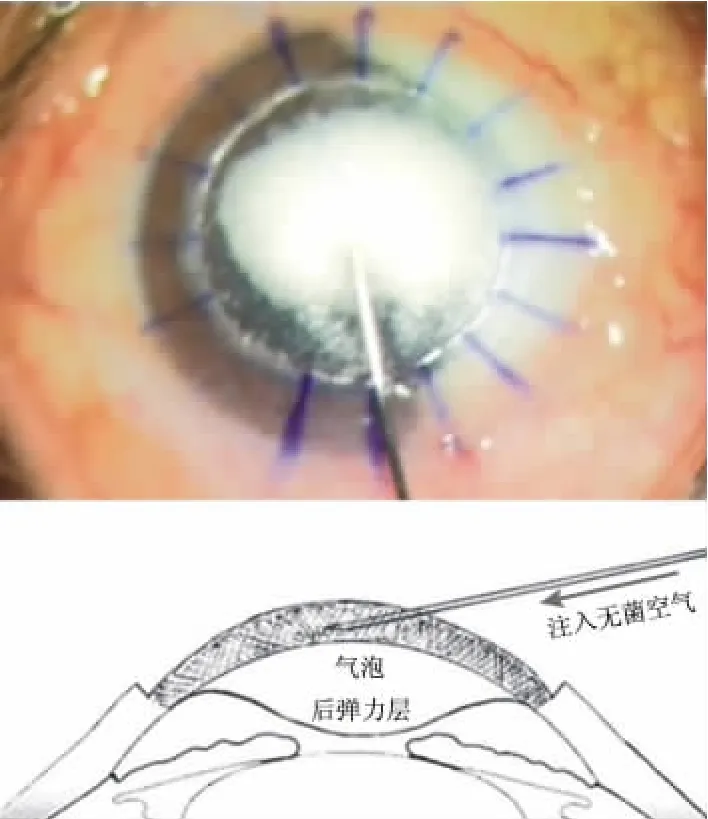
圖2 向角膜基質內快速注入無菌空氣約1 mL,利用快速彌散的空氣將后彈力層與基質層分離并形成大泡(下方為示意圖)
(4)暴露后彈力層:可用兩種方法。其一,左手持0.12 mm顯微有齒鑷輕輕向上提拉角膜基質,觀察并確定角膜基質下方存在氣泡后,右手持角膜刀繼續向下切開角膜基質,當切除接近角膜基質與后彈力層之間的氣泡時,發白的角膜基質逐漸透見后彈力層和前房透亮的氣體。此時采用角膜刀將角膜基質輕輕切穿放出氣體,見到基質層下方透亮的后彈力層。其二,采用30號穿刺針穿刺放出后部角膜基質與后彈力層之間的氣體,同時將針尖向上挑,利用針尖將后部角膜基質切開一個0.5~1.0 mm小切口,暴露出下面光亮的后彈力層。然后采用虹膜恢復器通過切口,輕柔地探到后部角膜基質與后彈力層之間并輕輕上抬,使兩者之間形成空隙,再采用45°角膜刀將后部角膜基質切開,擴大切口。之后采用顯微有齒鑷提拉角膜基質,用角膜刀將后彈力層前的角膜基質自上而下輕輕下壓完全切除干凈,暴露出后彈力層(見圖3)。在切除的過程中,在角膜環鉆標記的最外緣保留了約50μm厚、0.5 mm寬的環形薄角膜基質(見圖4),以利于控制縫合深度,并且避免旋轉線結時線結劃破后彈力層(見圖5)。
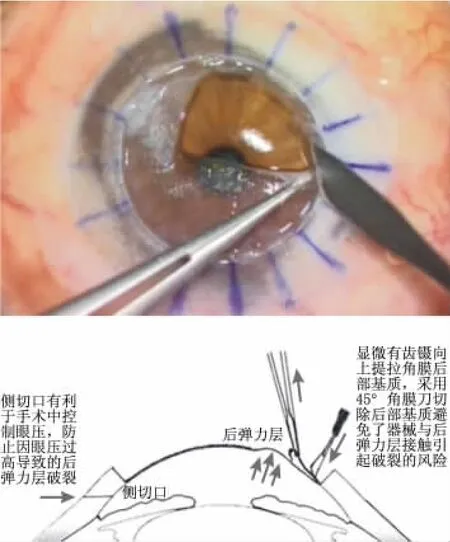
圖3 切開全部基質層之后,如眼壓過高引起后彈力層明顯前膨,可以于角膜緣做側切口并放出少許房水降低眼壓(下方為示意圖)
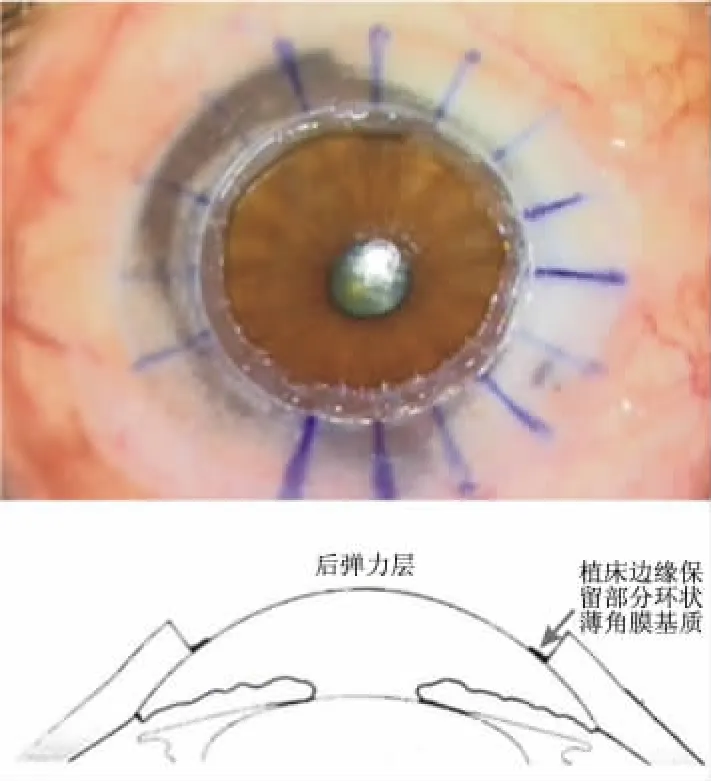
圖4 切除全部后部基質時于植床切口邊緣保留厚度約50μm的環狀薄角膜基質(下方為示意圖)
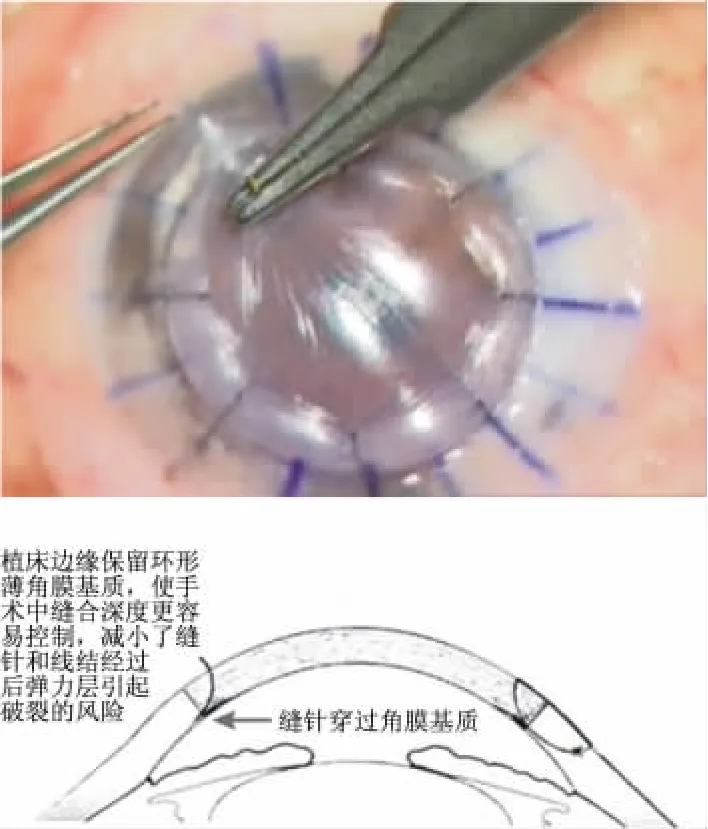
圖5 縫合過程中縫針可以在保留的薄基質上方進針,有利于縫合深度的控制,同時減小了手術過程中因縫針穿過角膜植床和旋轉線結時引發的角膜后彈力層破裂的風險(下方為示意圖)
(5)制作角膜側切口:如果在暴露后彈力層后發現眼壓偏高導致其前膨,此時為避免因眼壓過高引起后彈力層破裂,可選擇性進行前房穿刺。采用穿刺刀于11點位(右眼)或1點位(左眼)角膜緣做1 mm的側切口,放出房水約0.05 mL適當降低眼壓,也可從側切口注入約0.05 mL卡巴膽堿縮小瞳孔。如感染性角膜炎患者同時存在前房積膿,還可以通過此切口向前房內注入平衡鹽溶液將積膿沖洗干凈。
1.2.3 供體準備
采用角膜中期保存液或甘油冷凍保存的供者角膜充分復水。鉆切供者角膜環鉆直徑較鉆切植床環鉆直徑大0.25 mm,采用0.12 mm顯微平鑷將供者角膜后彈力層和內皮層完全剝離備用。
1.2.4 縫合角膜移植片
覆蓋供者角膜移植片后采用10-0尼龍線間斷(或連續)縫合。散光盤下觀察角膜映光環,并根據其形狀對縫線松緊進行調整,直至角膜映光環呈現相對比較規則的圓形后,采用0.12 mm顯微平鑷將線結旋轉入角膜植床側層間減少術后刺激癥狀。采用虹膜恢復器將角膜移植片壓入植床邊緣之下,使角膜移植片與植床緊密對合或略低于植床面以利于角膜上皮愈合。
1.3 術后觀察與并發癥處理
手術后對角膜移植片情況和短期視力恢復狀況進行觀察,同時對圍手術期并發癥的發生及處理進行記錄。手術并發癥處理方案:(1)后彈力層穿孔:手術過程中出現植床穿孔時,穿孔若小于1 mm,則往前房內注入無菌空氣氣密前房,繼續行DALK;若大于1 mm,無法氣密前房,則改行PK。(2)層間積液(雙前房):手術后出現角膜基質層與后彈力層之間積液,量較少則不做特殊處理進行觀察,待自行吸收;如積液量多引發后彈力層皺褶不易自行吸收,采用0.12 mm顯微平鑷輕柔地將角膜移植片與植床切口分開,層間液體在眼內壓的作用下自行溢出后,植床與角膜移植片緊密貼附。如因植床穿孔出現的雙前房經過上述處理層間積液仍然未吸收,則采用30號穿刺針穿刺進入前房,注入無菌空氣約0.2 mL將植床頂起并與角膜移植片緊密貼附。(3)原發病復發:如感染性角膜炎復發,首先根據術前診斷進行抗微生物藥物治療,如藥物治療不能控制,再行PK。
2 結果
共有37例患者(37只眼)成功行大泡技術輔助的暴露后彈力層的DALK(33例患者完全暴露后彈力層,3例微小穿孔和1例未穿孔的患者接近但未完全到達后彈力層)。1例斑塊狀角膜營養不良的患者1只眼(2.6%)發生植床大穿孔改行PK。
2.1 角膜移植片情況和移植后視力恢復狀況
角膜植床環鉆直徑7.5 ~9.5 mm,平均(7.91 ±0.47)mm;14例患者接受角膜中期保存液保存的供者角膜,23例患者接受甘油脫水-20℃冷凍保存的供者角膜。所有患者角膜移植片透明,與植床貼附良好,裂隙燈顯微鏡下難以見到層間界面(見圖6),眼前段OCT檢查顯示植床平均厚度(20.6±5.6)μm。
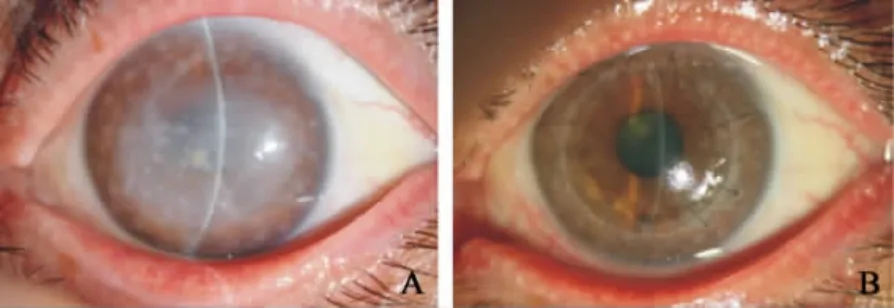
圖6 1例斑塊狀角膜營養不良患者手術前后眼部表現
最佳矯正視力(best spectacle corrected visual acuity,BSCVA)術前37例(38只眼)在手動/20 cm至0.05之間,成功接受DALK 37例患者(37只眼)術后恢復至0.1 ~1.0(P <0.01),術后平均隨訪時間(9.57±4.13)個月(1~16個月),其中 7例BSCVA≥0.8,12例 BSCVA 0.5 ~0.8(包含 1 例真菌再次感染行PK的患者),9例BSCVA 0.3~0.5,9例 BSCVA 0.1~0.3。患者 BSCVA 低于0.3的原因如下:1例自幼弱視,6例術后發現有老年性白內障,2例有并發性白內障。
2.2 圍手術期并發癥及其處理
術中并發癥:4例(10.5%,4/38)患者術中發生后彈力層穿孔。其中1例斑塊狀角膜營養不良患者分離后彈力層不充分,后彈力層與植床貼附緊密,術中發生植床穿孔超過1 mm,無法氣密前房,改行PK。3例感染性角膜炎患者(真菌性角膜炎1例、細菌性角膜炎2例),術中出現后彈力層微小穿孔(小于1 mm),向前房內注入無菌空氣后達到氣密狀態,繼續行DALK(保留了極薄的后部角膜基質,接近后彈力層)。術中未發生其他并發癥。
術后并發癥:(1)層間積液(雙前房)8例(21.6%,8/37)。2例為術中發生微小穿孔的患者,4例為采用甘油冷凍保存供者角膜的患者,另外2例為采用新鮮供者角膜的患者。4例自行吸收,3例層間放液后緩解,1例發生植床微小穿孔患者層間放液聯合前房注氣后緩解。(2)植床皺褶1例。該例為細菌性角膜炎患者術后出現瞳孔區植床較大皺褶,于術后第5天行角膜移植片重縫,調整縫線松緊后植床皺褶消失。(3)原發病復發1例。該例為尖孢鐮刀菌感染的患者,術前存在前房積膿和內皮斑,術后2~3 d出現再次感染征象,表現為植床浸潤并逐漸加重,角膜內皮斑和前房積膿重新出現。給予全身和局部抗真菌藥物治療5 d感染未能控制,再次手術切除感染的植床后行PK,感染控制。
3 討論
角膜組織自前而后分為5層:上皮層、前彈力層、基質層、后彈力層和內皮細胞層。成人角膜后彈力層厚度僅約10μm,光滑且韌性強[6]。由于發育的原因角膜后彈力層和基質層之間粘附并不緊密,有通過手術技術將其分離的可能。光滑的后彈力層界面使大泡技術輔助的DALK避免了層間界面粗糙引發的光學效果差的問題,但是由于后彈力層太薄,術中易發生穿孔,即使手術經驗豐富的醫生在操作過程中也會倍感壓力。
3.1 大泡技術輔助的暴露后彈力層DALK的原理
大泡技術輔助的暴露后彈力層DALK利用空氣在角膜基質彌散的力量將角膜后彈力層與角膜基質層分離。此手術方法國外主要用于圓錐角膜的治療。在圓錐角膜患者中的成功應用,使得這種技術應用于感染性角膜炎患者成為可能。大泡技術采用無菌空氣將后彈力層與基質層鈍性分離,大大降低了手術過程中后彈力層穿孔的風險。同時空氣在角膜基質內彌散后使得角膜基質增厚,更利于進一步向深層組織切削。
在向角膜后部基質注入無菌空氣的過程中,部分患者可能會有少許小氣泡進入前房。本組患者有12例前房出現小氣泡,原因可能是氣體在基質層和后彈力層之間彌散不均勻,部分氣體沿后彈力層向周邊彌散,通過房角處小梁網進入前房所致。
3.2 手術主要改良分析
角膜中央全厚約550μm,人的角膜后彈力層出生時只有約3μm,之后隨著內皮細胞不斷分泌而逐漸增厚,大約每10年生長3μm,因此成年人角膜后彈力層也僅有10~20μm[6]。暴露后彈力層DALK成功的關鍵是手術過程中如何避免后彈力層破裂。文獻報道在操作過程中發生后彈力層破裂的比例為9% ~23%[5,7]。有學者報道采用低滲水腫鈍性分離法和基質纖維鉤取聯合黏彈劑注入分離法分離后彈力層也達到了比較理想的效果,但是這兩種方法都會增加手術器械與后彈力層接觸的機會,初學者操作有難度,同時也可能增加器械接觸致后彈力層破裂的風險[8-9]。手術器械(尤其是邊緣銳利的器械)與后彈力層接觸是發生后彈力層破裂的高危因素,為了避免常規手術器械邊緣銳利可能導致的后彈力層破裂,Parthasarathy等[10]對角膜剪邊緣進行了改良,使其與后彈力層接觸的一側刀刃更鈍圓光滑,但是即便如此,手術剪刀仍然會不斷與后彈力層接觸,增加了后彈力層破裂的風險。我們對此進行了改良,結果只有約10%患者發生了后彈力層破裂;即使發生微小穿孔,通過前房內注入無菌空氣仍然可以順利完成DALK。
首先,我們將用角鞏膜剪剪除后部角膜基質方法改為一手提拉角膜基質,一手自上而下切除殘留基質的操作,最大限度地避免了器械與后彈力層接觸的機會。以往DALK多采用虹膜恢復器輔助下角膜刀將角膜后部基質十字形切開至環鉆邊緣,然后采用角鞏膜剪將周邊連接處的角膜基質剪除的方法[11]。此方法有2個步驟會導致手術器械直接與后彈力層接觸:(1)虹膜恢復器探到角膜基質與后彈力層之間,而且虹膜恢復器越向角膜周邊鈍性分離,與后彈力層接觸越緊密;(2)角鞏膜剪在剪除殘留角膜基質過程中會與后彈力層接觸(邊緣往往氣泡分離不充分,器械接觸最容易發生穿孔)。這都大大增加了手術過程中發生后彈力層破裂的風險。本文方法是左手輔助提拉殘留的后部角膜基質,使后部角膜基質與后彈力層分離,然后采用一次性角膜刀與角膜基質輕輕接觸并自上而下輕輕加壓,殘留的少量極薄的后部角膜基質很容易切開,在此過程中沒有任何手術器械與后彈力層接觸。
其次,我們利用側切口隨時根據術中情況控制眼壓,減小了因眼壓過高導致后彈力層破裂的風險。手術過程中眼壓的控制對順利完成手術也非常重要,眼壓過低不利于手術中切除殘留的后部角膜基質,而眼壓過高則可能因壓力過大發生后彈力層鈍性破裂。本文方法為暴露部分后彈力層后根據眼壓情況,選擇性采用穿刺刀制作角膜側切口,在后彈力層前膨明顯時,放出少許房水降低眼壓,避免術中局部后彈力層承受過大壓力而發生破裂。
最后,以往手術一般完全切除環鉆標記范圍內的角膜基質,周邊也完全暴露后彈力層。完全切除角膜基質不利于控制縫合深度,增加了縫合角膜移植片過程中因為縫針穿過植床造成后彈力層破裂的風險,同時也可能因縫線線結旋轉到角膜層間而劃破后彈力層。本文方法為在角膜環鉆標記的最外緣保留了約50μm厚、0.5 mm寬環形薄角膜基質,縫合過程中縫針在保留的薄基質上方進針,既利于縫合深度的控制,又能夠防止手術過程中因縫針穿過角膜植床和旋轉線結時引發的后彈力層破裂。
McKee等[12]體外采用人工前房對大泡技術輔助的DALK暴露的后彈力層進行了病理學觀察,結果顯示有透明邊緣的大泡完整暴露了后彈力層,而白色邊緣的大泡一般殘留平均7μm的角膜基質。利用本研究辦法容易分離并到達后彈力層(如視頻1所示,如果沒有見到毛糙的角膜基質我們就認為已經達到了后彈力層),但我們并沒有辦法對植床進行病理學檢查,術后測量植床平均厚度約20μm,基本符合本組患者后彈力層與內皮層的厚度總和。此外體外實驗和臨床手術操作可能有差異,不同手術者手術技巧對是否能充分暴露后彈力層影響也很大。這可能也是國內外目前還沒有大規模開展此手術的一個原因。隨著手術技術的進步,相信越來越多的醫生會逐漸開展此手術,后彈力層和內皮層沒有病變的角膜盲患者將從中受益。
從以上三方面改良的大泡技術輔助的暴露后彈力層DALK更容易操作,盡可能降低了操作過程中后彈力層發生破裂的風險,提高了DALK的臨床安全性,值得在臨床上推廣應用。
志謝 感謝山東省眼科醫院王利英護士為本文視頻配音
1 Xie L,Qi F,Gao H,et al.Major shifts in corneal transplantation procedures in north China:5316 eyes over 12 years[J].Br J Ophthalmol,2009,93(10):1291-1295.
2 Abdelkader A,Elewah El-SM,Kaufman HE.Confocal microscopy of corneal wound healing after deep lamellar keratoplasty in rabbits[J].Arch Ophthalmol,2010,128(1):75-80.
3 Anwar M,Teichmann KD.Big-bubble technique to bare Descemet's membrane in anterior lamellar keratoplasty[J].J Cataract Refract Surg,2002,28(3):398-403.
4 Kubaloglu A,Sari ES,Unal M,et al.Long-term results of deep anterior lamellar keratoplasty for the treatment of keratoconus[J].Am J Ophthalmol,2011,151(5):760-767.
5 Leccisotti A.Descemet's membrane perforation during deep anterior lamellar keratoplasty:prognosis[J].J Cataract Refract Surg,2007,33(5):825-829.
6 Bourne WM.Biology of the corneal endothelium in health and disease[J].Eye(Lond),2003,17(8):912-918.
7 Jhanji V,Sharma N,Vajpayee RB.Intraoperative perforation of Descemet's membrane during“big bubble”deep anterior lamellar keratoplasty[J].Int Ophthalmol,2010,30(3):291-295.
8 馬慧香,陳蔚,鄧姿峰,等.低滲水腫鈍性分離法在深板層角膜移植中的應用(附視頻)[J/CD].中華移植雜志:電子版,2011,5(1):37-41.
9 姚玉峰.全植床深板層角膜移植:基質纖維鉤取聯合黏彈劑注入分離的全植床后彈力膜暴露技術(附視頻)[J/CD].中華移植雜志:電子版,2011,5(1):55-57.
10 Parthasarathy A,Por YM,Tan DT.Use of a“small-bubble technique”to increase the success of Anwar's“big-bubble technique”for deep lamellar keratoplasty with complete baring of Descemet's membrane[J].Br J Ophthalmol,2007,91(10):1369-1373.
11 Ang M, Mehta JS, Mantoo S, et al. Deep anterior lamellar keratoplasty to treat microsporidial stromal keratitis[J].Cornea,2009,28(7):832-835.
12 McKee HD,Irion LC,Carley FM,et al.Residual corneal stroma in big-bubble deep anterior lamellar keratoplasty:a histological study in eye-bank corneas[J].Br J Ophthalmol,2011,95(10):1463-1465.

