超氧化物歧化酶活性的測定
史競艷,羅辛茹,2,鮑江鴻,趙子德,黃丹,向乾坤
(1.武漢生物工程學院化學與環境工程系,湖北 武漢 430415;2.湖北大學化學化工學院,湖北 武漢 430062)
超氧化物歧化酶(SOD)是一種以超氧陰離子O2·-為底物的金屬酶,能催化超氧自由基發生歧化反應,是機體內O2·-的天然消除劑,對機體細胞起保護作用,在防御O2·-的毒性、抗衰老[1]以及預防腫瘤和抗炎[2-3]等方面起著重要的生理作用.自1969年McCord和Fridovich[4]首次從牛紅細胞中分離出超氧化物歧化酶以來,陸續在各種不同的生物組織都分離純化出SOD,并對SOD的物理、化學、藥理、臨床和作用機理等方面進行了廣泛研究,建立了多種活力測定方法[5].其中采用較多的是鄰苯三酚法,這種方法具有操作簡單、快速、試劑便宜且用量小、重復性好等優點,但文獻報道的鄰苯三酚法測定超氧化物歧化酶活性的測定條件各不相同,而且研究的影響因素不夠全面,這就造成了測定結果的混亂和缺乏可比性,為此我們對鄰苯三酚自氧化法測定SOD活性的實驗條件進行詳細研究,探討測活體系中緩沖溶液的pH值、溫度、所含EDTA的濃度、鄰苯三酚的濃度以及SOD酶濃度等因素對測定結果的影響,找出鄰苯三酚測定超氧化物歧化酶活性的最優條件,其結果可對實際工作起到一定的指導作用,也可為進一步的酶促反應動力學研究提供實驗和理論依據.
1 實驗部分
1.1試劑與儀器試劑:牛血SOD(98%,活力為3 000 U),三羥甲基氨基甲烷(Tris,99.9%),鹽酸(開封東大化工有限公司),乙二胺四乙酸二鈉(EDTA-Na2,99.0%,天津市風船化學試劑科技有限公司),鄰苯三酚(貴州遵義佳宏化工有限責任公司),均為國產分析純試劑,水為二次蒸餾水.
儀器:SP-1920UV系列雙光束紫外-可見分光光度計,pHS-3E型數字酸度計,電子天平(BSA124S),恒溫水槽(SYP-Ⅱ).
溶液的配制如下.(1)0.1 mol·L-1Tris-HCl(pH=8.20含2.0 mmol·L-1EDTA)溶液:準確稱取12.114 g三羥甲基氨基甲烷和0.744 5 g乙二胺四乙酸二鈉,溶于水中,用稀鹽酸調pH值至8.20,定容至1 000 mL;(2) 0.01 mol·L-1HCl:準確移取10 mL 1 mol·L-1的HCl溶液稀釋至1 000 mL;(3)6 mmol·L-1鄰苯三酚溶液:準確稱取0.189 2 g鄰苯三酚,用0.01 mol·L-1HCl溶解,并定容于250 mL棕色容量瓶中,于4 ℃冰箱中保存,使用時可稀釋;(4) 4 μg·mL-1SOD溶液:用微量進樣器準確移取100 μL,1 mg·mL-1SOD原液于25 mL容量瓶中定容.所有溶液的配制均采用二次蒸餾水.
1.2實驗原理超氧化物歧化酶是一種能催化超氧陰離子(O2·-)發生歧化反應生成H2O2和O2的金屬酶,反應如下:2O2·-+ 2H+→O2+ H2O2.
在堿性條件下,鄰苯三酚可在羥基H+發生離解時與溶液中的溶解氧發生反應生成半醌自由基,并產生O2-;然后半醌自由基可進一步被O2·-氧化成具有強吸收的醌,如下式所示:
如果溶液中含有SOD,則O2·-一經產生即被SOD歧化生成H2O2和O2,半醌自由基不能形成具有強吸收的醌,檢測到的吸收強度將比無SOD時減弱,且減弱的程度與SOD的濃度或活性有關,依據此原理可對SOD的活性進行測定.
1.3實驗方法鄰苯三酚自氧化速率的測定:按照表1所示的加樣量加入試管中,于25 ℃恒溫水浴槽中恒溫20 min后,準確移取0.30 mL 的2.5 mmol·L-1鄰苯三酚(對照管用0.01 mol·L-1HCl代替),立即混勻,迅速倒入比色池中,在波長為320 nm下采用紫外-可見分光計對鄰苯三酚自氧化中間產物進行時間掃描,掃描間隔為1 s,掃描5 min,記錄該掃描曲線斜率即為鄰苯三酚的自氧化速率ΔA0,每次測定重復2~3次,確保實驗結果的準確性和重現性.
SOD活性的測定:SOD活性測定法按上述操作,加入鄰苯三酚前,先加入一定量SOD,并減少同體積二次蒸餾水,其他操作均與上述相同,每次實驗重復2~3次,記錄該曲線的斜率即為ΔASOD.鄰苯三酚自氧化的抑制率定義為:抑制率=(ΔA0-ΔASOD)/ΔA0×100%.

表1 鄰苯三酚自氧化速率測定加樣表
2 結果與討論
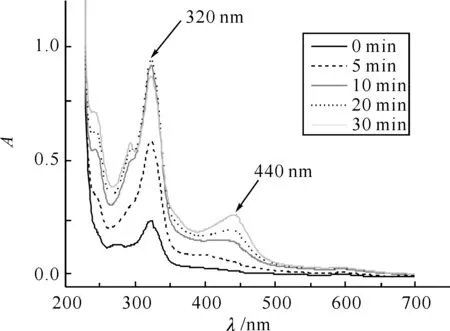
圖1 鄰苯三酚自氧化產物在不同時間掃描的吸收光譜
2.1鄰苯三酚自氧化中最大吸收波長的選擇鄰苯三酚自氧化產物在特定波長處有靈敏吸收峰,但在具體應用中,測定波長的選擇存在較大差異,主要有420 nm[6]和325 nm[7].為了準確測定其最大吸收峰位置,對鄰苯三酚自氧化過程在不同時間進行光譜掃描,掃描波長范圍為200 ~700 nm,其結果見圖1.由圖可看出,在反應一開始時即在320 nm處出現了最大吸收峰,420 nm處基本無吸收峰出現.隨自氧化反應的不斷進行,反應中間產物不斷積累,320 nm處峰的吸收強度不斷增加,在30 min時峰強度有所降低,主要是由于自氧化進程在30 min時反應已基本完成.而420 nm處直到10 min時才觀測到有峰出現,并且最大吸收峰的位置更準確地說應為440 nm處.文獻報道的最大吸收峰為420 nm和325 nm并不準確.考慮到峰的靈敏性和準確性問題,本實驗均選擇在波長為320 nm處進行測定.
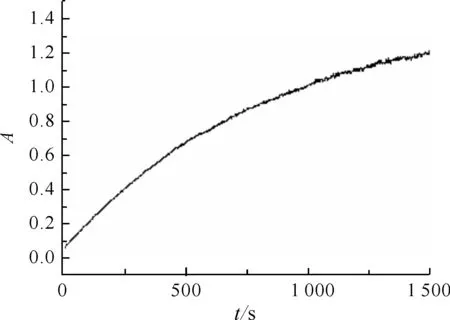
圖2 鄰苯三酚自氧化進程吸光度隨時間變化關系
2.2鄰苯三酚自氧化速率進程按照表1的加入量,在波長為320 nm下,對鄰苯三酚自氧化過程進行時間掃描,結果如圖2所示,在反應初期,吸光度隨時間變化呈線性,且線性關系維持至約5 min,此后斜率漸變平緩,期間反應液由無色轉變為棕黃色.為了準確表示反應初期鄰苯三酚的自氧化速率,我們每次實驗均選取了從30~210 s即3 min時間段內直線斜率來表示鄰苯三酚的自氧化速率ΔA0.
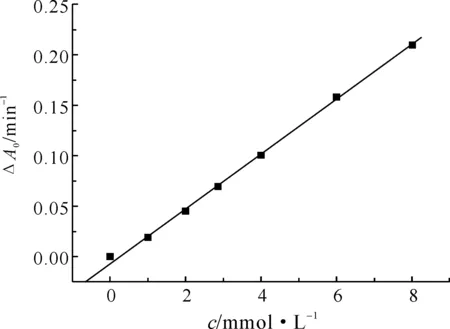
圖3 鄰苯三酚濃度對其自氧化速率的影響
2.3鄰苯三酚自氧化最佳濃度的確定鄰苯三酚濃度可對其自氧化產物的濃度產生影響,從而影響吸收信號的強度,因此,固定其他條件不變,僅改變鄰苯三酚的濃度,測定其對自氧化速率的影響,結果如圖3所示.實驗結果表明,隨著鄰苯三酚濃度的增大,自氧化速率也隨著增大,兩者呈線性關系,線性方程為ΔA/min-1=0.006 13+0.027 19c/mmol·L-1(R=0.999 09).結果說明鄰苯三酚自氧化具有一級反應特征.由圖可知,在鄰苯三酚濃度為2.5 mmol·L-1時,鄰苯三酚自氧化的曲線斜率約為0.06~0.07,基本滿足文獻[8]要求,因此在后面實驗中均選用鄰苯三酚的濃度為2.5 mmol·L-1.
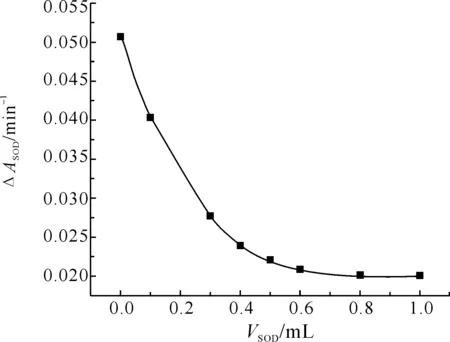
圖4 SOD的不同加入量對鄰苯三酚自氧化速率的影響
2.4超氧化物歧化酶的最佳加入量的選擇為了解SOD對鄰苯三酚自氧化速率的影響,固定鄰苯三酚的濃度為2.5 mmol·L-1不變,改變SOD的加入量,測定SOD的加入量對鄰苯三酚自氧化速率的影響,實驗結果如圖4所示,由圖可知,鄰苯三酚自氧化速率與酶的加入量成反比,這與鄰苯三酚法測定超氧化物歧化酶的機理[9]是一致的.在堿性條件下,鄰苯三酚可在羥基H+發生離解時與溶液中的溶解氧發生反應生成半醌自由基,并產生O2·-;然后半醌自由基可進一步被O2·-氧化成具有強吸收的醌,該醌在320 nm處有強吸收,但如果溶液中含有SOD,則O2·-一經產生即被SOD歧化生成H2O2和O2,半醌自由基不能形成具有強吸收的醌,因此檢測到的吸收強度將比無SOD時減弱,且減弱的程度與SOD的濃度或活性有關,SOD酶活就是通過對鄰苯三酚的抑制程度來測定的.因此,酶加入的越多,對鄰苯三酚的抑制就越強,自氧化速率就越小.但文獻[10]報道,最優的加酶量應為能抑制鄰苯三酚的自氧化下降約50%為宜,此時測定的準確度和靈敏度都會比較高,據此本實驗最終確定酶的加入量0.30 mL.
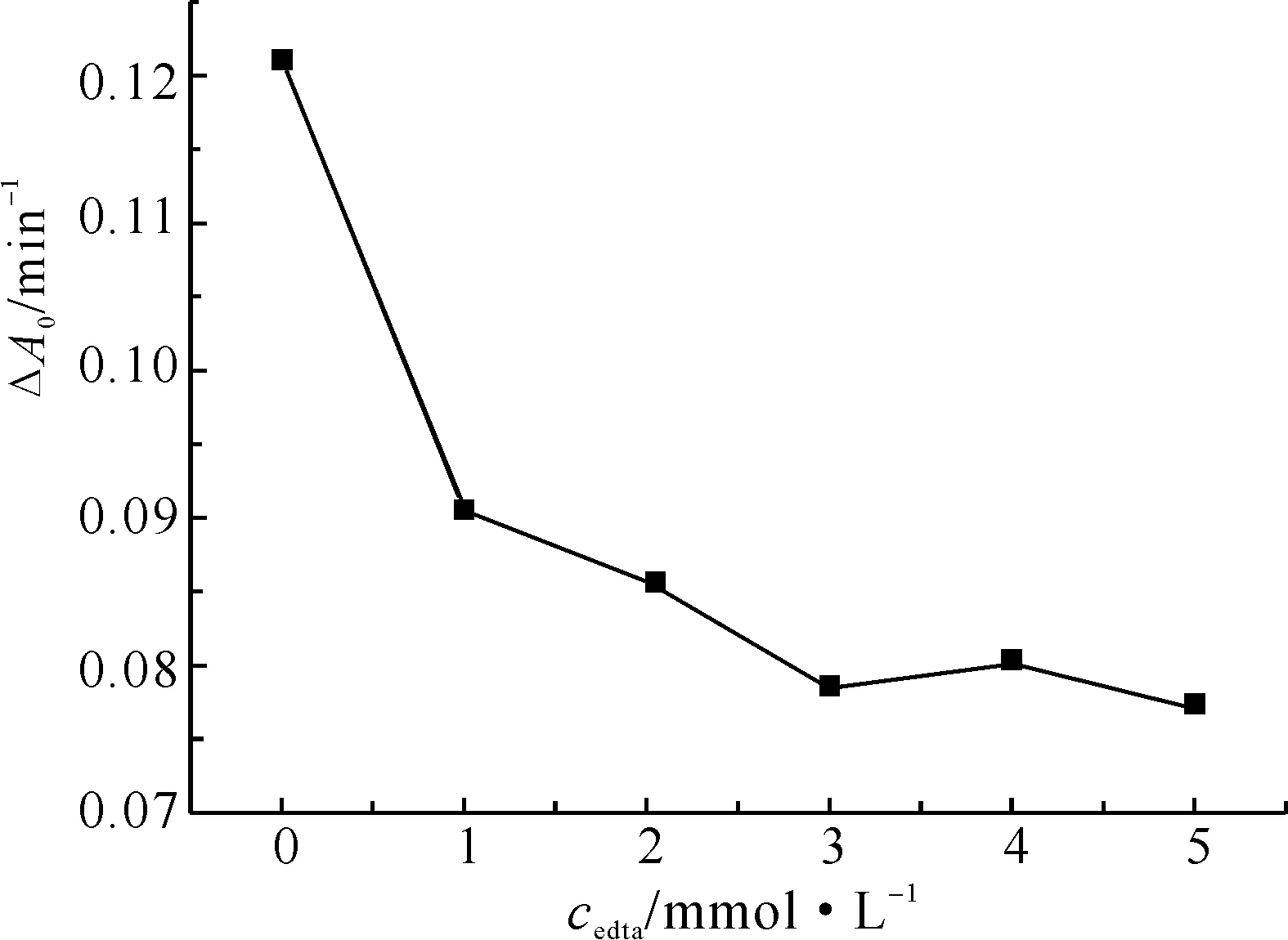
圖5 EDTA對鄰苯三酚自氧化速率的影響
2.5EDTA含量對鄰苯三酚自氧化速率的影響在鄰苯三酚經典自氧化方法中文獻報道的緩沖溶液介質組成較混亂,有的在緩沖液中加入EDTA,但也有不加的.為了考察EDTA在鄰苯三酚自氧化過程中的作用,我們配制了一系列EDTA濃度分別為0.0、1.0、2.0、3.0、4.0、5.0 mmol·L-1的Tris-HCl緩沖溶液,研究其對鄰苯三酚自氧化的影響,結果如圖5所示.由圖5可知,EDTA加入后對鄰苯三酚的自氧化進程有明顯的影響,并隨著EDTA加入量的增加,鄰苯三酚的自氧化速率不斷降低,在EDTA的濃度小于3 mmol·L-1時,EDTA對鄰苯三酚的影響比較明顯,而當EDTA的濃度大于3 mmol·L-1以后,對鄰苯三酚的自氧化速率影響較小.據文獻[9]報道,大多數金屬離子對鄰苯三酚自氧化速率有促進作用,盡管實驗中所用水為二次去離子水,但水中仍然不可避免還會有少量的金屬離子存在,當EDTA加入后,由于EDTA較強的配位能力,導致溶液中的金屬離子由于被絡合而失去對鄰苯三酚自氧化的促進作用,加入的EDTA越多,被絡合的金屬離子越多,自氧化速率就越慢,而當溶液中所有的的金屬離子都被絡合后,再增加EDTA,因為沒有了游離金屬離子的存在,因此自氧化的速率便維持恒定不變.考慮到SOD酶為Cu,Zn-SOD,本身就含有金屬離子,如果加入EDTA太多,有可能也會和SOD的金屬離子絡合,從而導致酶的失活,而加入EDTA太少,會使鄰苯三酚自氧化速率過高,導致自氧化反應速率不穩定.綜上分析,最終確定EDTA的加入濃度為2 mmol·L-1.

圖6 不同pH值對鄰苯三酚自氧化速率和SOD抑制率的影響(-自氧化速率,-抑制率)
2.6pH值對鄰苯三酚自氧化速率及SOD抑制率的影響鄰苯三酚在堿性條件下可發生自氧化反應,由此可知溶液的pH值在鄰苯三酚自氧化中起著重要作用,控制測定體系其他條件不變,僅改變緩沖溶液的pH值進行實驗.pH對鄰苯三酚自氧化速率和SOD抑制率的影響如圖6所示,結果表明,鄰苯三酚自氧化速率隨pH的升高而增大,這可能與pH值增大時鄰苯三酚的酚羥基中H+更易離解,形成的帶電基團能量較高、不穩定,而易被氧化有關[11].從圖中也可看出,SOD抑制率隨pH增加總體呈下降趨勢,其中在pH值為8.00~8.40時,SOD抑制率受pH值變化的影響不明顯,即在此范圍內pH值的微小變化并不會引起抑制率的明顯改變.在選擇最適宜pH時,要考慮兩方面的因素:一是要有較高的自氧化速率;二是要有明顯的抑制率,文獻[8]報道多采用加酶后抑制率為50%作為最適條件.因此,綜合考慮諸因素的影響,本文中選擇pH 8.20作為緩沖溶液適宜的pH值.
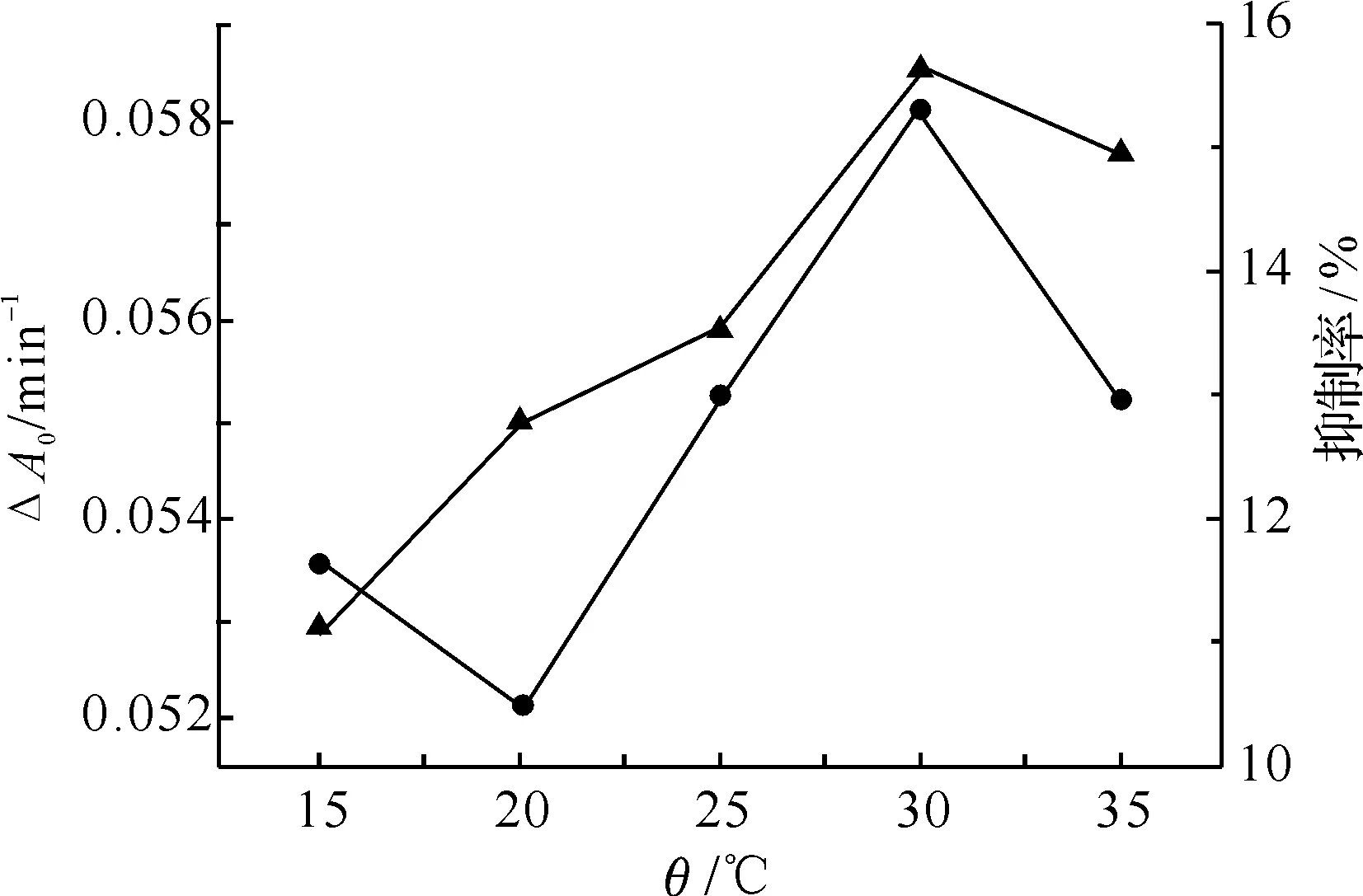
圖7 不同溫度對鄰苯三酚自氧化速率和SOD抑制率的影響(-自氧化速率,-抑制率)
2.7溫度對鄰苯三酚自氧化速率及SOD抑制率的影響為了考察溫度對鄰苯三酚自氧化速率及SOD抑制率的影響,固定其他條件不變,分別在15、20、25、30、35 ℃的反應溫度下測定溫度對鄰苯三酚自氧化速率和SOD抑制率的影響,結果如圖7所示.
由圖7可看出,溫度對鄰苯三酚自氧化速率和SOD抑制率總體來說影響較小,在溫度從15~35 ℃范圍內,自氧化速率變化范圍0.052~0.058,而抑制率的變化范圍11%~16%.從圖7也可以看出,隨溫度升高,抑制率總體呈上升趨勢,但考慮到在較高溫度下,自由基不穩定,衰減速率加快,使測定的靈敏度和穩定性大大降低,因此本研究均采用在室溫(25 ℃)下進行.
3 結論
本文中采用鄰苯三酚自氧化法測定超氧化物歧化酶的活性,該法具有操作簡便、快速、試劑便宜且用量小,重復性好等優點;通過對鄰苯三酚自氧化法測定SOD活性的實驗條件進行詳細研究,獲得了測定SOD活性的最優條件為:實驗溫度為25 ℃,0.1 mol·L-1Tris-HCl緩沖溶液(pH值為8.20且含2.0 mmol·L-1EDTA),鄰苯三酚濃度為2.5 mmol·L-1,控制酶的加入量為0.30 mL.
[1] Huang J Z, Lemire B D.Mutations in the C1 elegans succinate dehydrogenase ironsulfur subunit promote superoxide generation and prematureaging[J].Mol Biol,2009,387:559-569.
[2] Monari M,Trinchero A.Calabrese C1 superoxide dismutase in gastric adenocarcinoma:is it a clinical biomarker in the development of cancer[J].Biomarkers,2006,11(6):574-584.
[3] Weydert C J, Waugh T A, Ritchie J M.Overexpression of manganese or copperzinc superoxide dismutase inhibits breast cancer growth[J].Free Radic Biol Med, 2006, 41(2):226-237.
[4] McCord J M, Fridovich I.Superoxide dismutase anenzymic function forerythrocup rein[J].J Biol Chem, 1969,244:6049-6055.
[5] 鄒國林.對SOD研究中若干問題的看法[J].中國生化藥物雜志,1995,16 (4):186-189.
[6] 張龍翔,張庭芳,李令媛.生化實驗方法和技術[M].北京:高等教育出版社,1997:217.
[7] 鄧碧玉,袁勤生,李文杰.改良的鄰苯三酚自氧化測定超氧化物歧化酶活性的方法[J].生物化學與生物物理學進展,1991,18(2):163.
[8] 張宏,譚竹鈞.四種鄰苯三酚自氧化法測定超氧化物歧化酶活性方法的比較[J].內蒙古大學學報:自然科學版, 2002,33(6):677-681.
[9] 楊磊,陳冠華,崔建超,等.熒光動力學法測定超氧化物歧化酶的活性[J].分析化學研究報告,2008,36(4):489-493.
[10] 許申鴻,杭瑚,李遠平.超氧化物歧化酶鄰苯三酚測活法的研究及改進[J].化學通報,2001(8):516-519.
[11] 袁倬斌,高若梅.鄰苯三酚自氧化反應的動力學研究[J].高等學校化學學報,1997, 18(9):1438-1441.

