遠端胃癌病人不同胃腸吻合術對2型糖尿病的效果
楊方武,張炳遠,孫傳東,盧云,曲林林,張憲祥
(青島大學醫學院附屬醫院普外二科,山東 青島 266003)
隨著生活水平的提高,糖尿病成為嚴重危害人類健康的慢性疾病之一,其中90%者為2型糖尿病(T2DM),并且發病率逐年增加,嚴重威脅病人的健康和生命。糖尿病傳統的治療方法不能保證病人血糖恢復至正常水平,不能避免各種糖尿病并發癥的出現和進一步加重。近年來發現胃旁路術(GBP)和膽胰轉流術(BPD)等胃腸道重建類減肥手術不僅可明顯控制體質量,而且對并發的T2DM也有很好的治療效果[1-2]。但是不同胃腸吻合術對遠端胃癌并發T2DM病人治療效果的研究,臨床上報道甚少。2006年6月—2010年6月,我院外科手術治療遠端胃癌并發T2DM病人48例,本研究回顧性分析了其臨床資料,探討病人不同手術前后血糖控制情況。現將結果報告如下。
1 資料與方法
1.1 一般資料
我院行根治性遠端胃癌切除術的病人57例,病人均并發T2DM,48例有手術前后的完整資料并得到隨訪。48例病人中,男27例,女21例;年齡38~75歲,平均58.56歲;均經胃鏡病理檢查確診為胃癌,其中胃體癌11例,胃竇癌26例,幽門管癌11例;入院前確診者40例,采取飲食控制或接受降糖藥物治療;另8例病人入院后因常規檢查發現空腹或餐后高血糖或行葡萄糖耐量實驗(OGTT)后被確診為T2DM。納入標準;空腹血糖(FPG)>7.0 mmol/L;或者病人餐后2 h血糖(PG2h)≥11.1 mmol/L;或OGTT≥11.1 mmol/L。所有研究對象均無腺垂體(垂體前葉)、甲狀腺、腎上腺皮質功能紊亂等證據。
1.2 手術方法
根據胃癌手術治療原則進行遠端胃癌根治性手術,按胃腸吻合術后食物經過方式不同分為BILLROT HⅠ式胃腸吻合術(A組)與BILLROT HⅡ式胃腸吻合術(B組)。兩組間年齡、性別比較無明顯差異。均無絕對手術禁忌證。
1.3 檢查指標及結果判定
除常規檢查外,術前及術后1周、1個月、6個月分別檢測兩組病人的FPG及PG2h水平。術后第6個月的FPG、PG2h水平與術前比較,FPG<5.6 mmol/L、PG2h<7.8 mmol/L者為治愈;FPG、PG2h較術前下降≥2.0 mmol/L者為好轉;FPG、PG2h較術前無明顯下降者為無效。治愈+好轉為有效。
1.4 統計方法
應用SPSS 11.5和PPMS 1.5[3]統計學軟件進行數據處理。計量資料以±s表示,兩組間比較采用t檢驗,等級資料比較采用秩和檢驗。
2 結 果
兩組病人手術前FPG及PG2h水平比較差異無顯著性(P>0.05)。B組術后1周、1個月、6個月的FPG及PG2h水平明顯低于A組(t=3.56~8.04,P<0.01)。見表1。B組術后15例血糖恢復至正常,其中8例停藥,1例胰島素減量可維持正常FPG水平;術后6月FPG、PG2h水平較術前下降≥2.0 mmol/L者5例,無明顯下降者1例,治愈率為71.8%,有效率為95.2%。A組術后2例血糖恢復至正常,其中1例停藥可維持正常FPG水平;術后6月FPG、PG2h水平較術前下降≥2.0 mmol/L者1例,無明顯下降者24例,治愈率僅為7.4%,有效率僅為11.1%。兩組治療T2DM的有效率比較差異有極顯著意義(Uc=5.54,P<0.01)。
表1 兩組病人手術前后FPG及PG2h水平變化(c/mmol·L-1,±s)
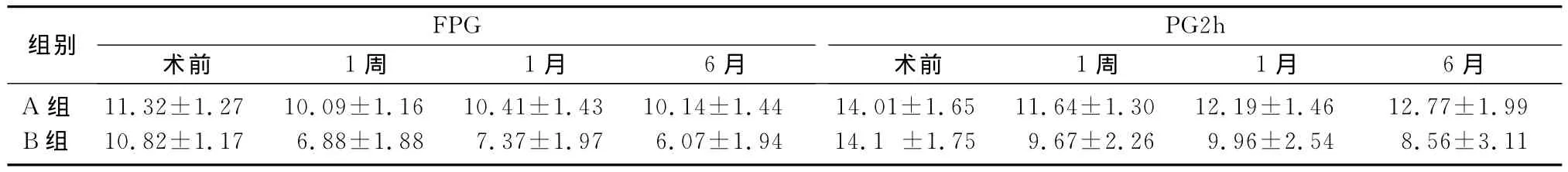
表1 兩組病人手術前后FPG及PG2h水平變化(c/mmol·L-1,±s)
組別FPG術前 1周 1月 6月PG2h術前 1周 1月 6月A組 11.32±1.27 10.09±1.16 10.41±1.43 10.14±1.44 14.01±1.65 11.64±1.30 12.19±1.46 12.77±1.99 B組 10.82±1.17 6.88±1.88 7.37±1.97 6.07±1.94 14.1 ±1.75 9.67±2.26 9.96±2.54 8.56±3.11
3 討 論
10多年前PORIES 等學者在總結手術治療肥胖病人的經驗時,無意中發現GBP及BPD手術可以使病人的體質量得到控制,同時其并發的糖尿病及其他并發癥亦得到緩解或治愈。目前GBP術控制T2DM在臨床上已取得了良好療效,而不同胃腸吻合術對遠端胃癌并發T2DM治療效果的研究,臨床報道甚少。本研究結果表明,采用BILLROT HⅡ式胃腸吻合術后,病人的FPG、PG2h水平能快速恢復至正常或接近正常的水平。而采用BILLROT HⅠ式胃腸吻合術的病人,其FPG、PG2h水平則沒有顯著變化。本文結果與其他學者的研究結果[4]大致相符,但也有一些不同之處,如少數BILLROT HⅠ式術后病人血糖恢復正常。我們推測可能與以下兩方面因素有關:①幽門被切除,食物同樣能較快進入空腸,對某些病人也產生了類似旁路手術的效應。②胃遠端尤其胃竇及十二指腸上段可能也參與腸-胰島軸中某些激素分泌的調節或產生。對BILLROTHⅡ式胃腸吻合術改善T2DM的機制尚不清楚,可能與以下機制有關:①胃旁路術后改變甜味功能。最近ANDRAS等[5]研究顯示,不管是動物模型還是人體胃腸吻合術術后都會影響胃腸肽類激素釋放,引起大腦中的甜味覺神經元變化,甜味覺神經元的電活動轉變為類似行為反應,減少對甜味物質偏好。病人手術后對甜味物質偏好降低和體質量減少有助于增加胰島素敏感性,降低血糖,從而緩解T2DM。②腸-胰島軸的改變。RUBINO等[6]推測,在腸道中可能同時存在產生腸促胰島素與抗-腸促胰島素的部位,后者主要分布在十二指腸與空腸,其能對抗胰島素活性導致胰島素抵抗,兩者均為食物刺激分泌并相互拮抗。BILLROTHⅡ式胃腸吻合術后由于抗-腸促胰島素分泌減少,從而解除了對胰島素的抵抗,緩解T2DM。
總之,本研究結果顯示,BILLROT HⅠ式胃腸吻合術病人術后FPG和PG2h水平與術前比較沒有明顯變化,相反BILLROT HⅡ式胃腸吻合術病人術后FPG和PG2h水平明顯降低。并發T2DM的遠端胃癌病人行BILLROT HⅡ式胃腸吻合術對其血糖控制具有一定的治療作用。但是由于觀察的例數尚少,還有待大樣本進一步的深入觀察和研究。
[1]LEE W J,WANG W,LEE Y C,et al.Effect of lapar oscopic mini-gastric bypass for type 2 diabetes mellitus:comparison of BMI>35and<35 kg/m2[J].J Gastrointest Surg,2008,12(5):945-952.
[2]PORIES W J,SWANSON M S,MCDONALD K G,et al.Who would have thought it?An operation proves to be the most effective therapy for adult-onset diabetes mellitus[J].Ann Surg,1995,222:339-350.
[3]周曉彬.醫用統計學軟件PPMS 1.5在醫學科學研究中的應用價值[J].青島大學醫學院學報,2011,47(6):504-506.
[4]李川,戚峰,劉彤.不同胃腸吻合術方式對胃癌合并2型糖尿病病人血糖的影響[J].天津醫藥,2010,38(6):489-491.
[5]ANDRAS H,PETER K,TAMER A,et al.Gastric bypass surgery alters behavioral and neural taste f unctions for sweet taste in obese rats[J].Am J Physiol Gastrointest Liver Physiol,2010,299:G967-G979.
[6]RUBINO F,FORGIONE A,CUMMINGS D,et al.The mechanism of diabetes control after gastrointestinal bypass surgery reveals a role of the proximal small intestine in the pathophysiology of type 2 diabetes[J].Ann Surg,2006,244(5):741-749.

