不同血液凈化方式對高脂血癥性胰腺炎的作用
常為民,楊進軍
(重慶市第九人民醫院ICU 400700)
近年來隨著人們生活水平的提高及飲食結構的改變,高脂血癥引起的急性胰腺炎逐漸增多,與其他原因所致的胰腺炎比較,高脂血癥性胰腺炎(hyperlipidemic pancreatitis,HLP)在發病機制、治療及預后等方面有其特殊之處,且更容易出現多器官功能不全[1]。目前,血液凈化技術已廣泛應用于HLP的治療,本研究旨在探討不同血液凈化方式對HLP的治療作用。
1 資料與方法
1.1 一般資料 本組26例患者中,男19例,女7例;年齡23~62歲(平均38.2歲)。按中華醫學會外科學會胰腺學組擬訂的急性胰腺炎診斷標準,排除膽道疾病、飲酒、暴飲暴食等致病因素,且血清三酰甘油大于或等于11.3mmol/L,分為HP+CVVH組(16例)及CVVH組(10例)。兩組性別、年齡及入院時血清三酰甘油水平、APACHEⅡ評分差異無統計學意義(P>0.05),具有可比性。
1.2 方法 兩組一般治療包括禁食、液體復蘇、胃腸減壓、胰酶抑制劑、皮下注射低分子量肝素、胰島素持續靜脈泵入、大黃灌腸及芒硝外敷等方法[2]。所有患者行股靜脈或頸內靜脈置管建立血管通路,HP+CVVH組患者先采用珠海麗珠公司大孔徑HA-330型血液灌流器行HP治療,血流量為200~250 mL/min,治療時間120min;HP后予DiapactCRRT機行CVVH,采用前置換,置換液流速30~50mL/min,超濾量根據患者容量指標調整,治療時間24h,血液凈化治療結束后12h復查血清三酰甘油,若大于或等于11.3mmol/L,行第二次HP+CVVH;若小于11.3mmol/L,只行CVVH 治療;CVVH組只行CVVH治療24h,兩組均行CVVH治療3次。血液凈化停止指標:腹部癥狀和體征消失或心率下降至90次/分鐘、呼吸頻率下降至20次/分鐘或三酰甘油低于5.65mmol/L[3]。
1.3 測定指標 密切觀察患者腹部情況,檢測生命體征,評估APACHEⅡ評分;測定兩組患者血液凈化前、血液凈化后12、36、72h的血清三酰甘油、腫瘤壞死因子α(tumor necrosis factor-α,TNF-α)的變化。
1.4 統計學方法 采用SPSS12.0軟件包進行統計學處理,數據比較采用t檢驗。以P<0.05為統計學意義。
2 結 果
入院時兩組患者血清三酰甘油、TNF-α、APACHEⅡ評分差異無統計學意義;血液凈化后12、36h兩組患者三酰甘油、TNF-α、APACHEⅡ評分與治療前比較均有所下降(P<0.05),CVVH+HP組下降幅度大于CVVH組(P<0.05),且CVVH+HP組在第2次血液凈化治療后三酰甘油水平已基本正常,腹痛、腹脹等癥狀明顯緩解,第3次只行CVVH治療;72hCVVH組三酰甘油水平達到安全范圍,腹痛、腹脹等癥狀明顯緩解;最終兩組各有兩名患者死亡,HP+CVVH組存活率(87.5%)高于CVVH 組(80%),見表1~3。

表1 兩組治療前、后血清三酰甘油的變化(mmol/L)
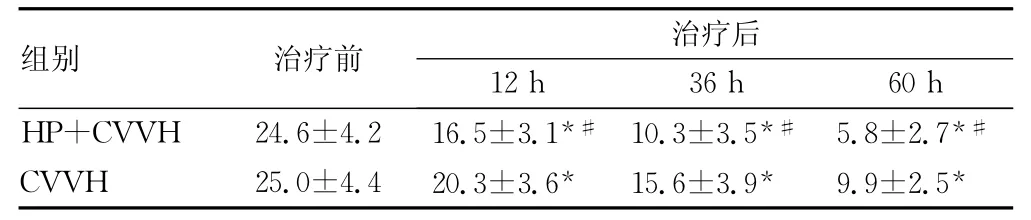
表2 兩組治療前、后APACHEⅡ評分的變化

表3 兩組治療前、后TNF-α的變化(ng/L)
3 討 論
高三酰甘油是急性胰腺炎的病因之一,隨著人們生活水平及飲食結構的改變,HLP發病率有上升的趨勢。目前認為其發生機制可能有以下幾點:(1)高脂血癥可導致血漿黏稠度升高,血漿處于高凝狀態,有利于血栓形成,導致胰腺微循環障礙;(2)血清脂質顆粒積聚,阻塞胰腺血管;(3)高血脂激活血小板,釋放具有強烈縮血管作用的血栓素A2(TXA2),同時損傷胰腺血管內皮細胞,使有擴血管作用的前列腺素(PGI2)分泌減少,導致TXA2/PGI2失衡,加重胰腺微循環障礙;(4)胰腺中的胰酶使三酰甘油分解為游離脂肪酸,直接對胰腺細胞產生毒性損傷,導致胰腺缺血壞死[4]。
HLP的臨床過程不同于其他原因引起的胰腺炎,早期臟器功能衰竭及后期胰腺膿腫、假性囊腫等并發癥發生率較高,其治療關鍵在于迅速降低三酰甘油和阻斷全身炎癥反應。通過禁食、皮下注射低分子肝素、持續靜脈滴注肝素和胰島素等內科處理,可使HLP患者的血脂水平下降,但重度高脂血癥患者對上述治療反應差,且不能阻斷已發展的炎癥反應。已有大量的臨床事實證明,血液凈化可以迅速降低三酰甘油水平,同時阻斷全身炎癥反應。Kyriakidis等[5]報道5例HLP行血液凈化可明顯減輕腹痛癥狀,無并發癥,無一人死亡。Yeh和Chen[6]對17例HLP患者實施血漿置換,患者血清三酰甘油、淀粉酶、脂肪酶顯著下降,13例完全康復。由于血漿置換需要大量的血漿和特殊儀器,且不能持續清除炎癥介質,故尚難廣泛應用于臨床。
持續血液濾過可通過對流的方式清除中、小分子物質,同時通過濾膜吸附部分大分子物質,阻斷全身炎癥反應,已廣泛應用于胰腺炎的治療[7]。對于 HLP,有學者提出可以利用CVVH時濾過膜的吸附作用降低血脂水平,但由于CVVH濾器膜面積非常有限,限制其對血脂的清除效果,同時三酰甘油會阻塞濾器中空纖維導致炎癥分子、介質的清除效率下降。因此,將CVVH與其他血液凈化方式聯合使用成為必要的治療手段。作者采用HP+CVVH聯合治療HLP,首先通過血液灌流器的吸附作用,使血清三酰甘油水平迅速下降,利于CV-VH的進行,然后利用CVVH持續清除炎癥分子及炎癥介質,阻斷全身炎癥的持續發展。本研究發現,HP+CVVH組在行2次血液凈化后,血脂水平已達到安全范圍,而CVVH組需行3次血液凈化治療后患者血脂水平才能達標,同時HP+CVVH組患者的腹痛、腹脹緩解時間也早于CVVH組,在相同時間點HP+CVVH組患者血清 TNF-α、APACHEⅡ均低于CVVH組,最終生存率也是HP+CVVH組較高。推測原因可能有以下幾點:(1)HP較CVVH能迅速降低血液中三酰甘油濃度,減輕高脂血癥對胰腺及機體的進一步損害;(2)血脂水平的下降可提高CVVH清除炎癥分子、介質的效率;(3)TNF-α生物活性形式為3聚體,相對分子質量為52 000,CVVH對其清除有限[8],而HP+CVVH能增加其清除率。本研究表明HP+CVVH比單用CVVH能迅速清除三酰甘油,減輕全身炎癥反應,改善預后。
[1] 賈林.高脂血癥性胰腺炎的臨床特征及其診治[J].現代消化及介入診療,2007,12(3):199-201.
[2] 毛恩強,湯耀卿,張圣道.高脂血癥性重癥急性胰腺炎規范化治療方案的探討[J].中國實用外科雜志,2003,23(9):542-545.
[3] Yadav D,Pitchumoni CS.Issunes in hyperlipidemic pancreatitis[J].J Clin Gastroenterol,2003,36(1):54-62.
[4] Hofbauer B,Friess H,Weber A,et al.Hyperlipaemia intensifies the course of acute oedematous and acute necrotizing pancreatitis in the rat[J].Gut,1996,38(5):753-758.
[5] Kyriakidis AV,Karydakis P,Neofytou N,et al.Plasmapheresis in the management of acute severe hyperlipidemic pancreatitis:report of 5cases[J].Pancreatology,2005,5:201-204.
[6] Yeh JH,Chen HC.Plasmapheresis for hyperlipidemic pancreatitis[J].J Clin Apher,2003,18:181-185.
[7] Jiang HL,Xue WJ,Li DQ,et al.influence of continuous veno-venous hemofiltration on the course of acute pancreatitis[J].World J Gastroenterol,2005,11:4815-4821.
[8] 蘇軍凱,李兆申.血液凈化治療高脂血癥性胰腺炎研究進展[J].胰腺病學,2006,6(5):310-312.

