鼻咽纖維血管瘤MRI表現及其影像學分期價值
閆鐘鈺,梁熙虹,李 靜,王振常
鼻咽纖維血管瘤雖為良性腫瘤,但其表現出侵襲性、易沿顱底孔道和裂隙蔓延生長,且由于組織學上瘤體內血管內皮細胞缺少肌層覆蓋,腫瘤極易出血,術前不恰當的手術方式包括穿刺活檢都可引起難以控制的出血,因此術前明確診斷,確定腫瘤起源部位、侵犯范圍及供血類型甚為關鍵,對指導臨床手術入路、減少創面及完整暴露手術野十分必要[1-2]。MRI以其良好軟組織分辨率和多斷面成像,可以準確確定腫瘤部位、范圍,區分腫瘤與周圍黏膜水腫以及顱內侵犯,明確診斷和指導腫瘤術前分期。筆者對74例鼻咽纖維血管瘤MRI表現進行回顧性分析,總結其MRI影像特征,并與手術分期對照,分析MRI分期在術前分期中的臨床價值。
1 材料與方法
1.1 一般資料
搜集1999年2月至2009年10月期間在我院耳鼻喉頭頸外科有完整手術記錄和病理結果的鼻咽纖維血管瘤患者94例,其中74例行MRI檢查,包括原發病例50例,有院外鼻部手術治療史24例,年齡范圍7~58歲,中位年齡18歲,74例均為男性。
鼻堵、鼻塞、鼻出血為常見癥狀,出血常為反復性,部分病例伴有鼻竇炎、頭痛、視力障礙及面頰部腫脹等。體檢:單側或雙側鼻咽部和或鼻腔內見紫色或粉紅色軟組織腫塊,表面光滑,有血管紋分布,觸之易出血。所有病例均行手術治療,手術方式有單純鼻內窺鏡下手術48例,鼻內鏡聯合顱面部開放腫瘤切除術18例,經面中部掀翻、鼻側切開或聯合開顱手術8例。
1.2 MRI檢查方法
MRI掃描采用GE Signa Twinspeed 1.5 T MR掃描儀(Waukesha, WI, USA),相控陣頭線圈,患者仰臥位,頭部固定。鼻竇MRI平掃包括FSE序列T1WI和T2WI,掃描參數:T1WI TR 400 ms,TE 12 ms,層厚5.0 mm,層間距 1.0 mm,FOV 20 cm×20 cm,矩陣 224×320, 激勵次數為1,帶寬20.8 Hz。橫斷面基線平行于聽眶下線,冠狀面垂直于硬腭,矢狀面平行于正中線。增強后行橫、冠、矢狀面掃描,掃描參數同平掃T1WI;其中橫斷面加頻率飽和法脂肪抑制序列。對比劑Gd-DTPA (469 mg I/ml,德國拜耳公司)劑量為0.1 mmol/kg,高壓注射器肘靜脈注入,流率2.5 ml/s。掃描方法、基線及方位參照中華放射學雜志2007年公布的由中華放射學雜志編委會制定的頭頸部MRI掃描規范指南(修改稿)[3]。由于該掃描規范是在我院臨床應用掃描規范基礎上制定,所以本組資料中2007前掃描方法、基線及方位均與上述指南一致。
術前MRI影像資料由2名有多年影像學診斷經驗的醫師共同閱片,分析MRI影像所見,對征象判斷不一致之處,由2名醫師共同協商解決。
1.3 MRI影像學表現
包括腫瘤發生部位、輪廓、邊緣、MR T1WI信號強度、T2WI信號強度、T2WI信號均勻度、MRI流空信號、強化程度。
1.4 分期方法及分期標準
分析患者MRI上累及范圍,記錄累及解剖結構及部位,確定74例MRI病變術前影像學分期,并與手術分期結果對照。對解剖部位分別進行標記,具體標記如下:(1)鼻咽鼻腔;(2)篩竇或上頜竇;(3)翼腭窩;(4)眶下裂;(5)眶尖;(6)眶上裂;(7)顳下窩;(8)顳窩;(9)舟狀窩;(10)圓孔和卵圓孔;(11)海綿竇;(12)咽旁間隙;(13)蝶竇;(14)翼突基底部和斜坡;(15)破裂孔;(16)視神經管;(17)前顱窩;(18)腭骨垂直板。
MRI影像分期參照Radkowski等[4]的臨床分期標準:Ⅰa期,局限于鼻腔和( 或) 鼻咽穹窿部;Ⅰb期,擴展入1個或多個鼻竇;Ⅱa期,少部分侵入翼腭窩;Ⅱb期,整個翼腭窩受侵犯,上頜竇后壁前移,眶骨侵蝕,上頜動脈移位;Ⅱc期,顳下窩和(或) 頰部受侵犯,或侵入翼板后方;Ⅲa期,顱底受侵(中顱窩、翼突根部),小部分顱內擴展;Ⅲb期,顱底受侵,廣泛顱內擴展伴有或不伴有海綿竇受侵。
1.5 統計學方法
鼻咽纖維血管瘤MRI征象頻數分布采用單因素方差分析進行比較,應用卡方檢驗、fisher和Monte Carlo精確檢驗,P值<0.05為差異具有統計學意義。采用Kappa一致性檢驗方法計算MRI分期模式與手術分期的一致性,Kappa值越高,MRI分期與手術分期越接近。數據分析采用SPSS 17.0統計學軟件。
2 結果
74例原發組和手術后復發組在T1WI信號強度、T2WI信號強度、T2WI信號均勻度、MRI強化方式、流空信號等方面都無統計學差異。但T1WI等信號、T2WI信號均勻度、流空信號以及增強后明顯不均勻強化等對鼻咽纖維血管瘤有特征性(表1,2)。
2.1 影像學表現
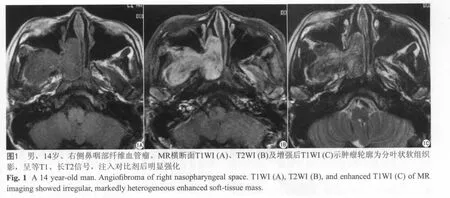
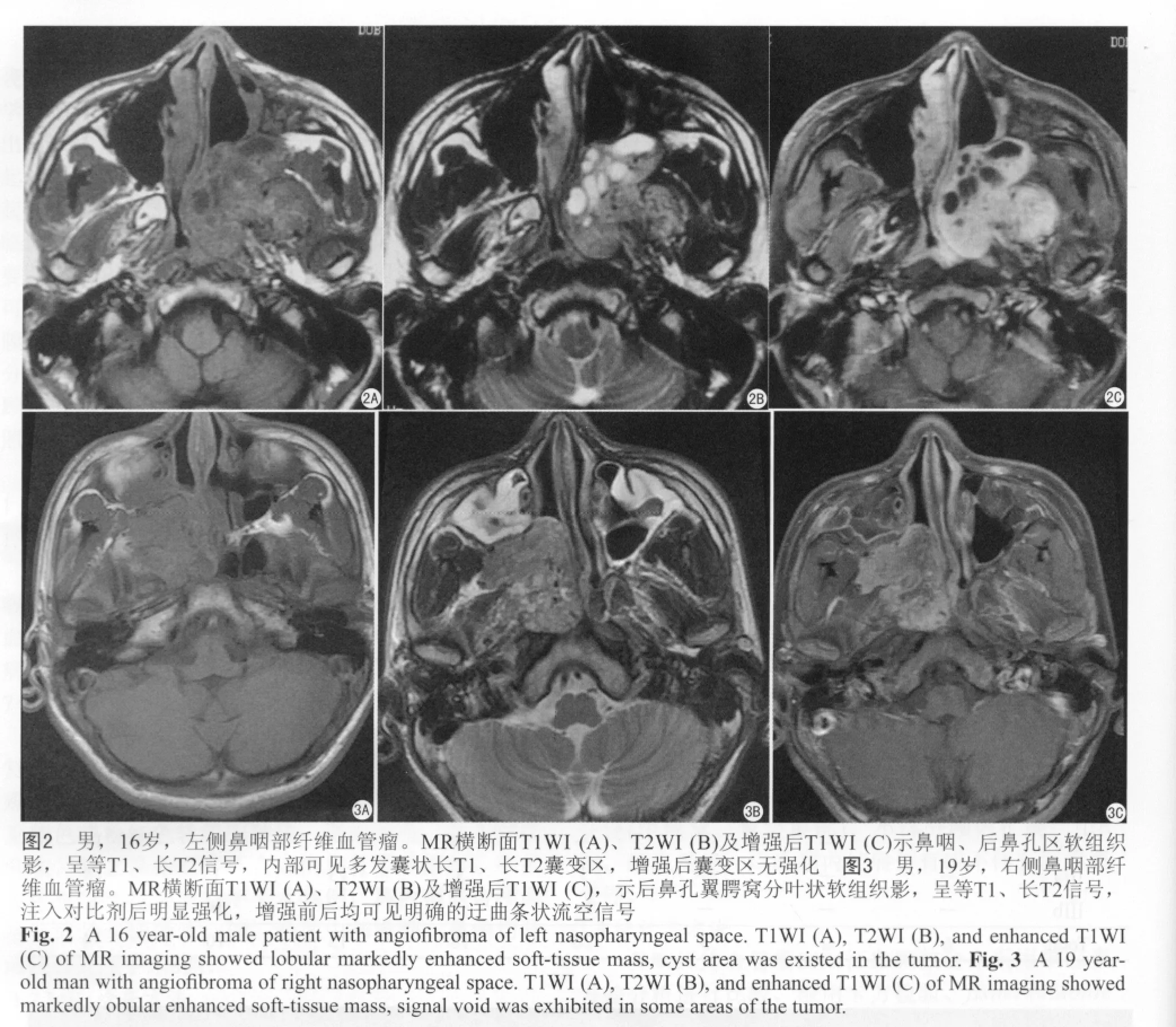
(1)原發部位:74例均位于鼻咽后鼻蝶腭孔區,以腫瘤中心為參照,偏左側37例,偏右側28 例,腫瘤巨大無法分清側別9例。(2)輪廓邊緣:74例中,輪廓光滑18例(24.3%),分葉狀56例(75.7%) (圖1);其中24例手術后復發病變中,21例輪廓呈分葉狀或不規則形,邊界清晰,3例有多次手術復發病史,邊界模糊。(3)形態特點:74例中不規則形42例(56.8%),圓形或橢圓形32例(43.2%)。(4)信號強度:與腦灰質相比,74例MRI檢查病例中,T1WI等信號69例(93.2%),稍低信號5例(6.8%),信號均勻,未見有高信號出現;T2WI高信號為主66例(89.1%),等信號為主8例(10.9%);T2WI信號不均勻66例(89.1%),信號均勻8例(10.9%),其中2例病變內見片狀更高信號區(圖2)。(5)流空信號:61例(82.4%)見明確流空信號(圖3),13例(17.6%)流空信號不明顯;其中原發組9例,手術后復發組4例。(6)增強程度:與平掃相比,注入對比劑后,74例中49例(66.2%)不均勻明顯強化,25例(33.8%)均勻強化。2例中心區呈囊變未強化區,周圍為強化的軟組織影(圖2)。
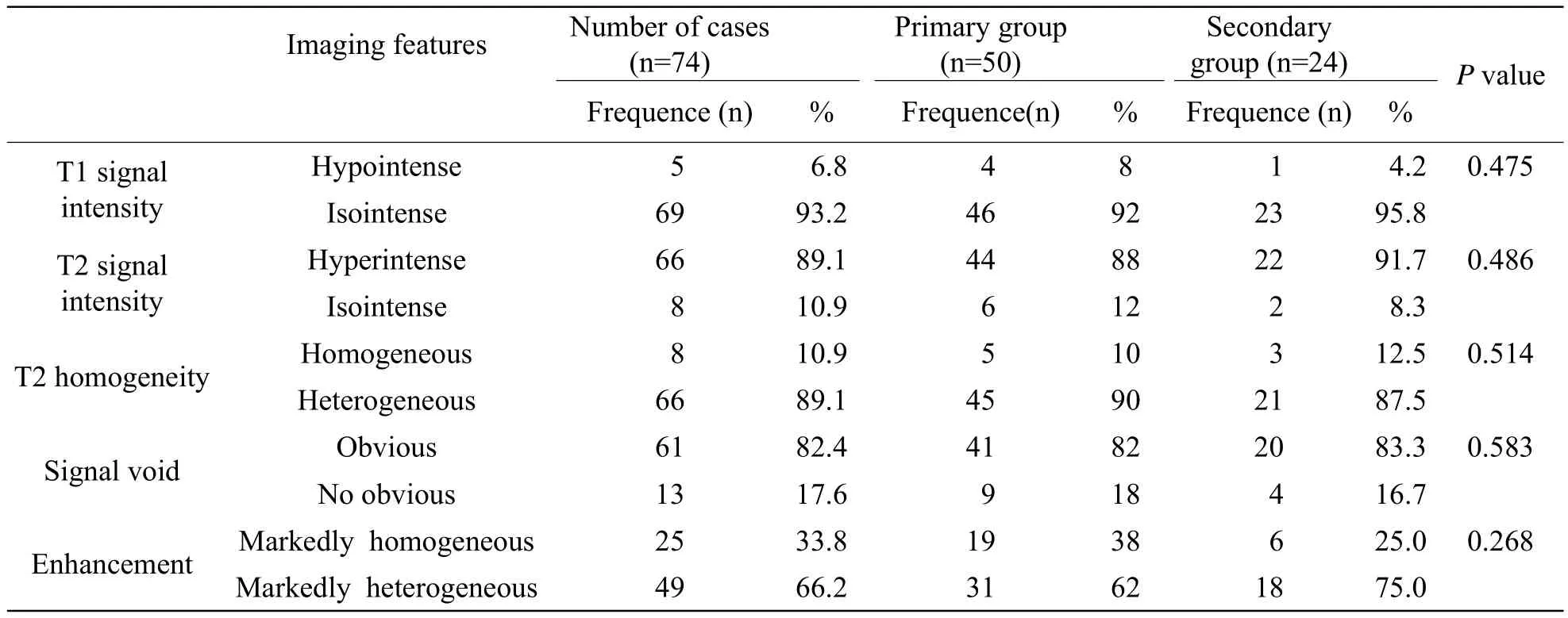
表1 74例鼻咽纖維血管瘤MRI特征頻數Tab.1 Frequency distribution of MR imaging features of 74 cases of nasopharyngeal angiofi broma
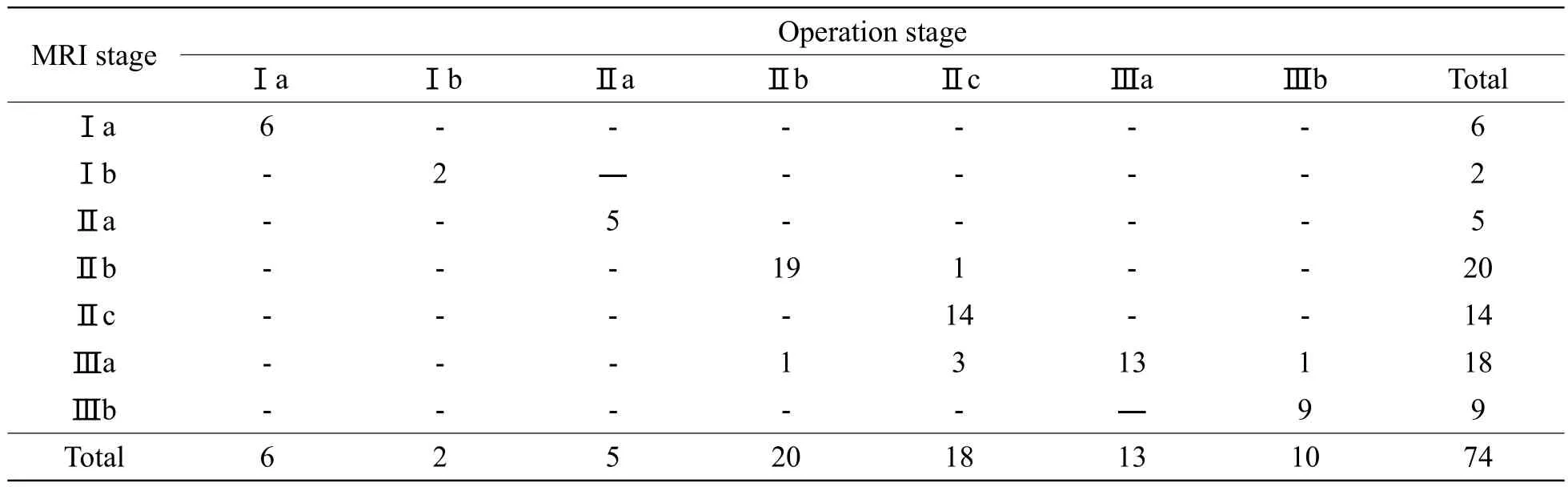
表2 74例MRI分期與手術分期對照結果(例)Tab. 2 Comparable results of MR stage and operation stage of 74 cases (n)
2.2 MRI分期與手術分期對照
74例MRI分期與手術分期對照結果見表2,Kappa值為0.92。MRI分期與手術分期不一致之處主要在Ⅲa期的判斷上,本組MRI分期有1例Ⅱb期變為Ⅲa期,3例Ⅱc期變為Ⅲa期。MRI由于中顱窩底及海綿竇硬腦膜反應性增厚而誤認為有顱內腦膜及海綿竇增厚累及,分期發生變化。
3 討論
正確診斷和術前認識鼻咽纖維血管瘤起源部位和累及范圍很重要,可以幫助確定腫瘤分期,有助于術式選擇、術前備血及術中瘤體完整性切除的估計。鼻咽纖維血管瘤是發生于青少年較少見的良性富血供腫瘤,好發于10~25歲青春期男性。病理上腫瘤通常由錯綜復雜血管網和纖維基質以不同比例構成,根據血管成分和纖維成分在腫瘤組織中所占比例,可分別稱其為血管纖維瘤或纖維血管瘤。鏡下血管內膜一般為單層內皮細胞,基底為不完整的平滑肌層,纖維樣基質可從致密的纖維區到水腫或黏液樣結締組織,其內細胞呈梭形或星形,但核的多形性和有絲分裂不明顯。
腫瘤起源于后鼻孔邊緣的周圍區域,包括硬腭后緣、梨骨后緣、鼻咽頂部、顳下窩、枕骨結節、蝶骨翼突及蝶骨翼突內側板的骨膜部,此處為腭骨蝶突、梨骨水平翼、蝶骨翼突根部匯合點,是口凹外胚層與前腸內胚層的分界線,胚胎期頰咽黏膜附著處,瘤體常沿此通路通過黏膜下以侵襲性生長方式擴展進入鼻、鼻咽、鼻竇、顳窩、顳下窩及顱內等鄰近結構。
3.1 MRI表現及術前診斷
鼻咽纖維血管瘤由血管和纖維組織以不同比例構成,腫瘤由富含膠原和纖維原細胞的纖維基質、不同口徑的血管排列形成,排列的血管缺乏肌層、彈性纖維和自主神經支配,因此腫瘤血供異常豐富而又容易出血[5]。腫瘤組織從周圍到中心區域有一逐漸成熟的梯度,而且腫瘤的成熟程度與腫瘤的蔓延有很好的相關性[6]。基于組織學及相關影響因素,鼻咽纖維血管瘤MRI信號有一定特點。本組中,T1WI以等信號為主占93.2%,低信號占6.8%,T2WI高信號占89.1%,等信號為主占10.9%,也說明不同病例信號變化較為復雜。T2WI信號不均勻性及應用MRI動態增強掃描技術可以反映腫瘤內部的這種組織學特性和構成。本組病例中T2WI信號不均勻占89.1%也說明了病變內部成分的多樣性。總之,鼻咽部分葉狀或不規則軟組織影,邊界清晰,MR T1WI等信號、T2WI不均勻高信號、點狀、條狀豐富流空信號以及增強后明顯強化特點幾乎可以肯定診斷。
鼻咽纖維血管瘤應與后鼻孔息肉、鼻咽癌、淋巴瘤等好發于鼻咽部腫瘤相鑒別。(1)影像上鼻咽癌主要表現為咽隱窩變淺消失,兩側咽腔結構不對稱,咽肌浸潤,咽旁間隙受壓外移,鄰近結構多數不清,頸部淋巴結如咽后組淋巴結轉移也常見。增強后軟組織強化不明顯,MRI無明確流空信號等均有助于鑒別。中老年患者多見,國內有一定的高發區。(2)后鼻孔血管瘤性息肉,也表現為鼻腔鼻竇后鼻孔軟組織腫塊,范圍局限,可見到腫瘤的蒂,竇腔內充滿軟組織影,伴或不伴竇壁骨質吸收破壞,結合患者年齡多能明確診斷;邊界清晰,MRI信號及增強后表現也有助于鑒別。
3.2 MRI在鼻咽纖維血管瘤術前分期應用及比較
MRI斷層影像對于鄰近鼻咽解剖深在、結構復雜顱底等結構顯示比較全面。MRI多方位多參數成像、軟組織分辨率高,可以顯示海綿竇、顱內垂體、視交叉、硬腦膜、翼管神經、圓孔內結構有無累及,與鄰近鼻腔鼻竇的慢性炎癥及息肉有區別。已有的研究認為,鼻咽纖維血管瘤的生長特性大多為推移式蔓延,因此侵入顱內的病變一般只累及硬腦膜,而且術中容易和硬腦膜剝離分開[7]。本組病例中大多只侵及海綿竇硬腦膜,只有2例伴有一側顳葉腦組織的水腫,無明確強化,無一例累及垂體及視交叉。MRI 還可以明確腫瘤與鼻腔鼻竇阻塞性炎癥之間的邊界,對腫瘤累及范圍描述更加準確。
本研究結果顯示,MRI分期模式與手術分期比較,一致性較好(Kappa=0.92)。 MRI軟組織分辨率高,增強后影像在一定程度上減少了假陽性病例,分期準確性有一定程度提高。同樣對于原發組與手術后復發組分期判斷,兩組中影像分期與手術分期不一致病例主要在Radkowski Ⅲa期,原發組有3例影像分期高于臨床分期,手術后復發組分別有1例影像分期高于臨床分期,1例評估低于臨床分期。影像學對于顱底浸潤,包括中顱窩底、翼突基部、海綿竇的顱內浸潤的判斷存在誤差。從解剖上來說,翼突基部位于翼腭窩的后部,內有翼腭隱窩所在,而處于翼管口的翼腭隱窩被認為是鼻咽纖維血管瘤的起源部位,腫瘤向后累及到翼骨基部的骨松質內和蝶骨大翼部分,復發率高達60%[8]。
MRI分期與手術分期不一致之處主要在Ⅲa期的判斷上,本組有1例Ⅱb期、3例Ⅱc期由于中顱窩底及海綿竇硬腦膜反應性增厚而認為有顱內結構累及。 MRI對鄰近腦膜及海綿竇增厚的判斷多采取兩側對比的方法,掃描時由于兩側層面不對稱常常誤判為一側腦膜增厚。
鼻咽纖維血管瘤顱內侵犯的途徑主要有:(1)從顳下窩侵蝕顱中窩底骨質;(2)從翼腭窩入眶上、下裂;(3)從蝶竇經上壁入海綿竇和(或)垂體窩;(4)從篩骨水平入顱中窩或沿破裂孔擴展入翼板。多數情況下鼻咽纖維血管瘤邊界清晰,是一種推進式生長方式,因此顱底骨質破壞可以很明顯,但顱內擴展及海綿竇受侵犯相對少見。MRI技術使得臨床醫師可更準確地為腫瘤分期及設計手術方案,并試圖使這一分期與患者預后建立關聯,評價這一分期的有用性,有利于術前計劃及治療結果的隨訪評估。
[1]Paris J, Guelfucci B, Moulin G, et al.Diagnosis and treatment of juvenile nasopharyngeal angilfibroma.Eur arch Otorhinolaryngol, 2001 258(3): 120-124.
[2]Szymanska A, Golabek W, Siwice H, et al.Juvenole angiofibroma:the value of CT and MRI for treatment planning and follow-up.Otolaryngol Pol, 2005, 59(1):85-90.
[3]The Editor Committee of Chin J Radiol.The CT and MR scanning guide in the head and neck.chin J Radiol, 2007,41(9): 996-999.中華放射學雜志編委會.頭頸部CT和MRI掃描規范指南(修改稿).中華放射學雜志, 2007, 41(9): 996-999.
[4]Radkowski D, McGill T, Healy GB.Angiofi broma changes in staging and treatment.Arch Otolaryngol Head Neck Surg, 1996, 122(2): 122-129.
[5]Beham A, Beham-Schmid C, Regauer S, et al.Nasopharyngeal angiolfi broma: true neoplasm or vascular malformation? Adv Anat Pathol, 2000, 7(1): 36-46.
[6]Liang J, Yi Z, Liang P.The nature of juvenile nasopharyngeal angiofibroma.Otolaryngol Head Neck Surg, 2000, 123(4): 475-481.
[7]Sennes LU, Butugan O, Sanchez TG, et al.Tissue maturation during the growth of juvenile nasopharyngeal angiofibroma.Ann Otol Rhinol Laryngol, 2004, 113(1):34-38.
[8]Danesi G, Panciera DT, Harvey RJ, et al.Juvenile nasopharyngeal angiofibroma: evaluation and surgical management of advanced disease.Otolaryngol Head Neck Surg, 2008, 138(5): 581-586.

