響應面法優化無溶劑體系磷脂酶A1催化酯化制備低聚甘油酯的研究
肖伊莎,汪 勇,張廣文
(暨南大學食品科學與工程系,廣東廣州510632)
響應面法優化無溶劑體系磷脂酶A1催化酯化制備低聚甘油酯的研究
肖伊莎,汪 勇,張廣文
(暨南大學食品科學與工程系,廣東廣州510632)
以工業油酸和低聚甘油為原料,經磷脂酶A1(Lecitase Ultra)催化酯化制備低聚脂肪酸甘油酯。利用響應面法優化實驗條件,研究反應時間、反應溫度、加酶量、加水量以及底物摩爾比值(工業油酸和低聚甘油摩爾比值)對其酯化率的影響。得出最佳反應條件為:反應溫度45℃,加酶量1.6wt%(占底物總質量),加水量4wt%(占底物總質量),反應時間12h,底物摩爾比值為1∶1。最佳條件下酯化反應平均酯化率可達到56.6%。采用HPLC-ESI質譜通過檢測相對分子質量驗證了部分低聚甘油酯產物的種類。
聚甘油酯,響應面法,磷脂酶A1,酯化
Abstract:Production of oligomerized polyglycerol fatty acid ester by esterification of industry grade oleic acid with oligomerized polyglycerol catalyzed by phospholipase A1(Lecitase Ultra) was investigated in this study.The reaction parameters including reaction time,reaction temperature,enzyme dosage,molar ratio of substrates(industry grade oleic acid to oligomerized polyglycerol) and water dosage were studied using response surface methodology(RSM).Optimum conditions obtained by RSM were as follows:reaction temperature 45℃,enzyme dosage 1.6wt%(of the substrates mass) molar ratio of oliomerized plyglycerol to fatty acid 1∶1,reaction time 12h and water dosage 4wt%.Under these conditions,esterification efficiency of the reaction mixture was 56.6%.Some oligomerized polyglycerol fatty acid ester molecular species were identified by HPLC-ESI-MS.
Key words:polyglycerol fatty acid ester;response surface methodology;phospholipase A1(Lecitase Ultra);esterification
聚甘油脂肪酸酯(polyglycerol fatty acid ester,PGFE)簡稱聚甘油酯,是由聚甘油與脂肪酸直接酯化或與甲酯、油脂進行酯交換而制得,是一類新型、高效、性能優良多羥基酯類非離子型表面活性劑,其具有乳化、保濕、抗菌等作用[1]。PGFE乳化性能比單甘脂優越,原因在于PGFE有更多的親水性羥基[2],且其親水性、親油性可以通過改變聚甘油聚合度、脂肪酸種類以及酯化度來實現,從親油性到親水性不同性能的一系列聚甘油產品,以適于各種特殊用途[3]。另外PGFE可很好地與其他乳化劑復配,具有良好的協同增效作用,因而至今PGFE的應用也已經逐步擴展到日化、石油、紡織、醫藥等領域[4-8]。我國PGFE的開發和應用起步較晚,與國外精致PGFE制品差距依然較大,且品種單一,目前我國PGFE產品的這種現狀已經不能滿足多層次、多行業、多領域的實際需求。現階段PGFE是聚甘油通過與脂肪酸酯化反應,或通過與動植物油脂進行酯交換反應得到。聚甘油和脂肪酸酯化主要方法有:脂肪酸酯化法、油脂酯交換法和酯酶合成法[9]。其中采用生物催化劑法制取PGFE,可以在較低溫度下反應,避免了使用傳統化學方法必須在高溫或者高壓下才能制取PGFE和提純產品缺陷,也有利于抑制副反應和提高產品質量,具有很好的發展前景。磷脂酶A1(Lecitase Ultra)是由一種基因改造的米曲霉微生物進行深層發酵制得的,我們前期研究發現其具有脂肪酶催化特性,可以催化脂肪酸和多元醇的酯化反應[10]。和脂肪酶相比,磷脂酶A1價格便宜,成本優勢明顯。本研究采用磷脂酶A1無溶劑體系催化酯化制備低聚甘油酯產品,詳細研究反應時間、反應溫度、加酶量和加水量以及底物摩爾比對酯化反應的影響,并通過響應面設計實驗獲得了最佳酯化條件(本研究中所指的低聚甘油原料為二聚和三聚甘油)。
1 材料與方法
1.1 材料與儀器
磷脂酶A1 丹麥諾維信公司,活力3000U/mL;工業油酸 濟南東潤精化科技有限公司采購;甘油、氫氧化鈉 市售化學純。
SZCL-2數顯職能控溫磁力攪拌器 鞏義予華儀器有限責任公司;HR-120電子天平、PL602-S精密天平 梅特勒-托利多中國地區有限公司;DT5-4低速離心機 北京時代北利離心機有限公司;GC-7820A氣相色譜 美國安捷倫公司;DHG-9123A電熱恒溫鼓風干燥箱 上海恒一科技有限公司;MD-80分子蒸餾設備 廣州漢維有限公司;LC-20AT液相色譜日本島津公司。
1.2 實驗方法
1.2.1 反應原料的合成與分析
1.2.1.1 低聚甘油的合成與分析 稱取60.0g甘油置于250mL三口燒瓶中,加入氫氧化鈉作為催化劑,在260℃的溫度和充滿氮氣保護的條件下反應4h,再通過二級分子蒸餾分別在110、170℃分離純化得到低聚甘油產品;由氣相色譜(GC)分析低聚甘油產品成分。
氣相色譜條件:色譜柱ATTM-Wax毛細管柱(15m×0.32mm×0.25μm),色譜條件為:進樣口:280℃,分流比:20∶1;檢測器:280℃;100℃保持0min,60℃/min升溫至165℃保持5min,60℃/min升溫至230℃保持3min,10℃/min升溫至240℃保持1min,10℃/min升溫至250℃保持1min,10℃/min升溫至260℃保持2min;載氣:高純氮氣,采用氫火焰檢測器(FID)。以各聚甘油物質出峰的峰面積為基數,采用歸一法計算個組分的相對含量[11]。低聚甘油組成為:甘油5.9%,二聚甘油60.0%,三聚甘油34.1%。
1.2.1.2 原料工業油酸的脂肪酸組成分析 GC分析脂肪酸組成,原料脂肪酸甲酯的制備參照GB/T 17376-2008。
氣相色譜條件:HP-5型毛細管柱(30m×0.32mm×0.25μm),進樣口:240℃,分流比:80∶1;檢測器:240℃;100℃保持0min,60℃/min升溫至170℃保持5min,60℃/min升溫至230℃保持3min。載氣:高純氮氣,采用氫火焰檢測器(FID)。以各脂肪酸出峰的峰面積為基數,采用歸一法計算個組分的相對含量[11]。
得到原料工業油酸的脂肪酸組成為亞油酸53.0%、亞麻酸5.5%、油酸17.2%和棕櫚酸24.3%。
1.2.2 單因素實驗 稱取工業油酸和一定摩爾比的低聚甘油置于50mL燒瓶中,依次加入一定量的磷脂酶A1和去離子水,通過數顯職能控溫磁力攪拌器控制溫度和攪拌轉速(300r/min),在真空(絕對壓力5kPa)下反應一定時間,分別考察反應溫度(30~70℃)、反應時間(2~14h)、磷脂酶A1添加量(0.4wt%~1.6wt%)、水的添加量(2wt%~12wt%)、反應底物摩爾比值(2∶1~1∶2)對酯化反應的影響。
每次酯化反應結束后,將反應液在3000r/min下離心10min分層,下層為極性相,即未反應完的低聚甘油,上層為油相,即低聚甘油酯和脂肪酸混合物,測定上層油相的酸值,并計算酯化率,酯化率按如下公式計算:
酯化率(%)=(AV0-AVr)/AV0×100
式中:AV0為工業油酸酸值;AVr為反應后油相酸值。
1.2.3 響應面實驗 根據單因素實驗結果以及因素影響分析,固定加水量為4wt%、反應溫度為45℃,進行響應面法優化實驗,對影響酯化反應的關鍵因素反應時間(A)、加酶量(B)、底物摩爾比值(低聚甘油和脂肪酸)(C)進行研究。以反應酯化率(Y)為響應值,得到酯化率和各個影響因素之間的關系回歸方程。確定酶催化酯化的最佳條件。用Design expert統計軟件設計響應面實驗,見表1。
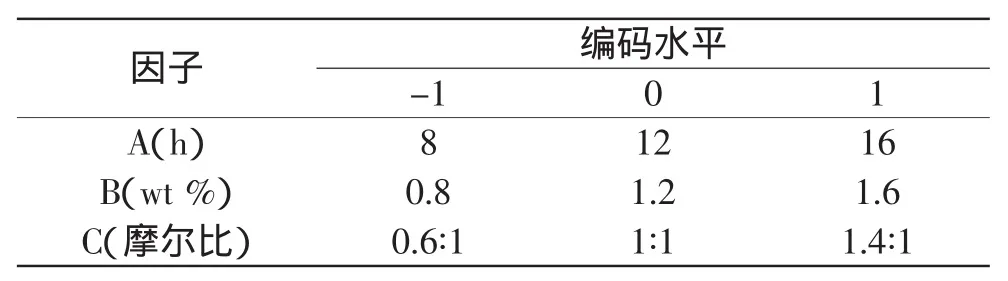
表1 Box-Behnken設計實驗因素水平及編碼Table 1 Box-Behnken design test factors and levels and coding table
1.3 分析方法
1.3.1 酸值測定 按GB/T 5530-2005滴定法測定。
1.3.2 酯化產物的HPLC和HPLC/ESI/MS分析 將響應面優化實驗的酯化產物配成10.0mg/mL的樣品。
HPLC條件為:流動相V(乙腈)∶V(異丙醇)∶V(甲酸)=55∶45∶0.05,流速0.5mL/min,柱溫40℃,紫外檢測波長210nm,色譜柱為Alltima silica C18,No.88171柱(250mm×4.6mm,5μm);質譜條件為:電噴霧(ESI)離子源,正離子模式,m/z:100~1500,離子掃描速率為5500amu/s。
2 結果與分析
2.1 單因素實驗
2.1.1 加水量對反應的影響 分別加入摩爾比值為1∶1的工業油酸和低聚甘油的底物和1.0wt%(底物重量)的磷脂酶A1,在溫度45℃、攪拌速度300r/min的條件下反應6h。考察加水量(wt%)對酶催化酯化反應的影響,結果見圖1。
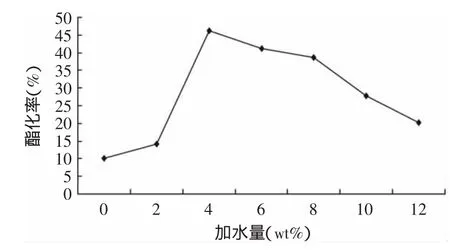
圖1 加水量對磷脂酶A1催化酯化反應的影響Fig.1 Effect of water loading on the FFA-glycerol esterification efficiency
從圖1可以看出,磷脂酶A1催化酯化反應加水量為4wt%的時候最合適,反應得到產物酸值最低。在酶催化酯化反應中,初始時加入適量的水可以活化酶并且提高酶的催化活性,因為水是保持酶構象并維持活力的因素之一[11]。但是理論上酯化反應是水解反應的逆反應,反應中產生過量的水會促使酯化反應逆向進行。所以我們在抽真空的環境下進行反應,使反應中生成的水被及時抽出,從而保證反應的熱力學平衡向需要的正方向進行[12]。
2.1.2 溫度對反應的影響 分別加入摩爾比值為1∶1的工業油酸和低聚甘油底物、1wt%磷脂酶A1和4wt%水,在攪拌速度300r/min的真空條件下反應6h,考察溫度對酶催化酯化反應的影響,結果見圖2。
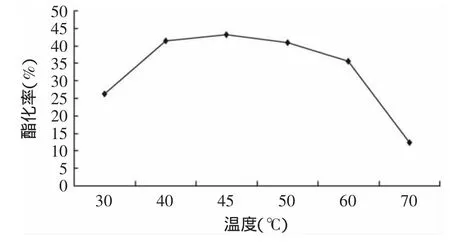
圖2 溫度對磷脂酶A1催化酯化反應的影響Fig.2 Effect of reaction temperature on the FFA-glycerol esterification efficiency
從圖2可以看出,磷脂酶A1催化酯化反應溫度為45℃的時候最合適,反應得到產物酸值最低為120.4mg KOH/g,即酯化率為最高43.2%,這與它催化部分酯化反應的最適溫度相同[13]。酶的活力與反應溫度的高低有直接的關系,溫度高,分子運動快,酶解速度快,但是當溫度過高時,它會影響酶蛋白的活力,使酶失去活性。
2.1.3 加酶量對反應的影響 分別加入摩爾比值為1∶1的工業油酸和低聚甘油的底物和4wt%水,在溫度45℃、攪拌速度300r/min的真空條件下反應6h。考察加酶量(wt%)對酶催化酯化反應的影響,結果見圖3。
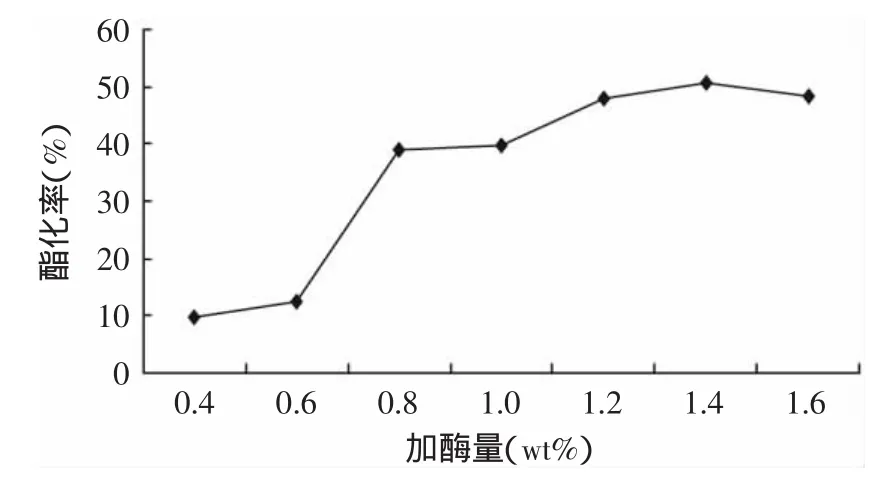
圖3 加酶量對磷脂酶A1催化酯化反應的影響Fig.3 Effect of catalyst loading on the FFA-glycerol esterification efficiency
酯化反應速度的快慢直接和酶的濃度相關。酶濃度高,參與反應的酶的分子就多,相應的酯化速度就快[14]。從圖3可以看出,隨著加酶量的增加,產物酸值不斷降低并且在加酶量為1.6wt%時達到最低值,此時酯化率為最高48%。但是當加酶量超過1.4wt%時,這種增長趨勢減緩,這是因為這時當酶與底物混合后的反應接觸面積趨于飽和,酶的增量對反應影響變小。
另外,酶是酯化反應中成本最高的原料,所以在保證酯化率的前提下較低的加酶量是反應工業化的前提條件。所以在實驗范圍內,當加酶量增加酸值不斷降低,但是從經濟角度講,加酶量1.4wt%為最佳反應條件,因為繼續提高加酶量并沒有明顯降低酸值。
2.1.4 底物的摩爾比值對反應的影響 分別加入不同摩爾比值的工業油酸和低聚甘油的底物、4wt%水和1.4wt%磷脂酶A1,在溫度45℃、攪拌速度300r/min的真空條件下反應6h。考察底物的摩爾比值對酶催化酯化反應的影響,結果見圖4。
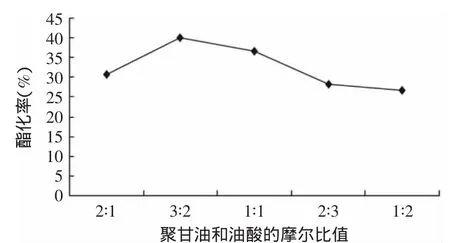
圖4 底物的摩爾比值對磷脂酶A1催化酯化反應的影響Fig.4 Effect of mole ratio of industrial oleic acid to polyglycerol on the esterification efficiency
低聚甘油和脂肪酸的底物摩爾比對酯化反應具有決定性的影響。從圖4可以看出,隨著低聚甘油和脂肪酸摩爾比增加,反應越徹底,并在低聚甘油與脂肪酸比值為1∶1時反應酯化率達到最高值為40.0%。然而,當底物摩爾比繼續提高,反應產物酸值反而升高,這是因為過多的低聚甘油增加了反應系統的粘度,同時增大了除去反應過程生成的水的難度,過量的水抑制反應物的移動和反應速率[15]。
2.1.5 時間對反應的影響 分別加入摩爾比值為1∶1的工業油酸和低聚甘油的底物,1.4wt%磷脂酶A1和4wt%水,在攪拌速度300r/min的真空條件下反應,考察溫度對酶催化酯化反應的影響,結果見圖5。
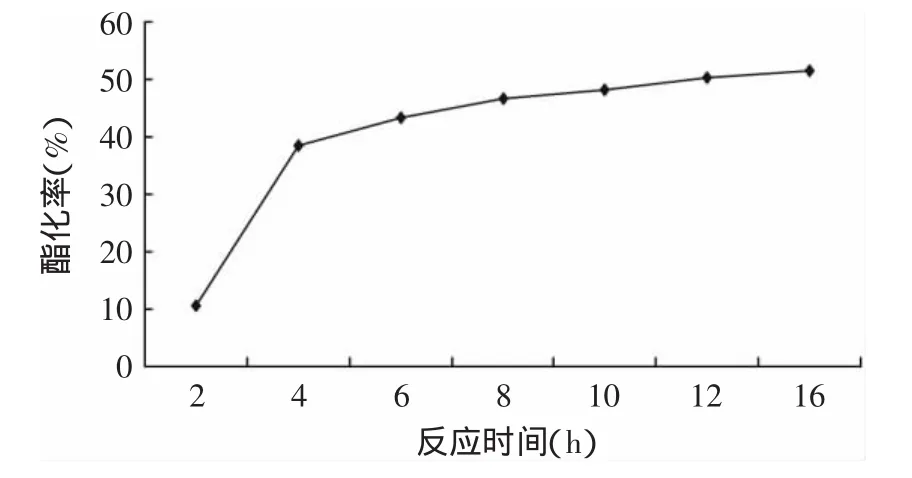
圖5 時間對磷脂酶A1催化酯化反應的影響Fig.5 Effect of reaction time on the esterification efficiency
從圖5可以看出,磷脂酶A1催化酯化反應隨著時間的延長,產物的酸值不斷降低。當反應12h后,產物酸值達到110左右,酯化率達到較高值47.6%。12h以后雖然反應時間延長,但產物酸值基本趨于穩定,反應整體達到了動態平衡。
2.2 響應面實驗
磷脂酶A1催化低聚甘油和油酸酯化響應面結果分別見表2。

表2 酯化反應的響應面設計及結果Table 2 Box-Behnken design test results
采用Design Expert軟件,對表2中反應酯化率實驗數據進行回歸擬合,得到反應酯化率對編碼自變量的二次多項回歸方程:
Y=49.22+2.79A+13.19B-6.3C-0.95AB-0.18AC+2.12BC-5.16A2-6.41B2-9.34C2
回歸模型方差分析見表3。由表3可知,回歸模型F值為21.89,p<0.01,表明回歸模型極顯著;失擬項p=0.0838>0.05,表明失擬項相對于絕對誤差是不顯著的,因此回歸模型無失擬因素存在;相關系數R2=0.9657,說明方程擬合情況較好,模型能解釋96.57%的反應產物酸值響應值的變化;由模型系數顯著性檢驗結果可知,加酶量和底物摩爾比值是極顯著因素,各因素對轉化率的影響順序為:B>C>A。
運用Design Expert軟件的回歸模型進行顯著因素水平的優化分析,求得最佳反應條件為:加酶量1.59wt%,底物摩爾比值0.91∶1,反應時間11.36h。預測酯化率最高為56.7%。考慮到實際操作的便利,確定酯化反應最佳條件為:加酶量1.6wt%,底物摩爾比值1∶1,反應時間12h。在上述條件下進行2次平行驗證實驗,得到酯化率分別為56.1%、57.0%,平均值為56.6%。實驗值與模擬計算值有較好的擬合性。酯化率沒有超過60%的原因是反應體系為無溶劑體非均相系,聚甘油粘度很大,反應體系傳質較困難,需要采用其他新型反應體系加強傳質。
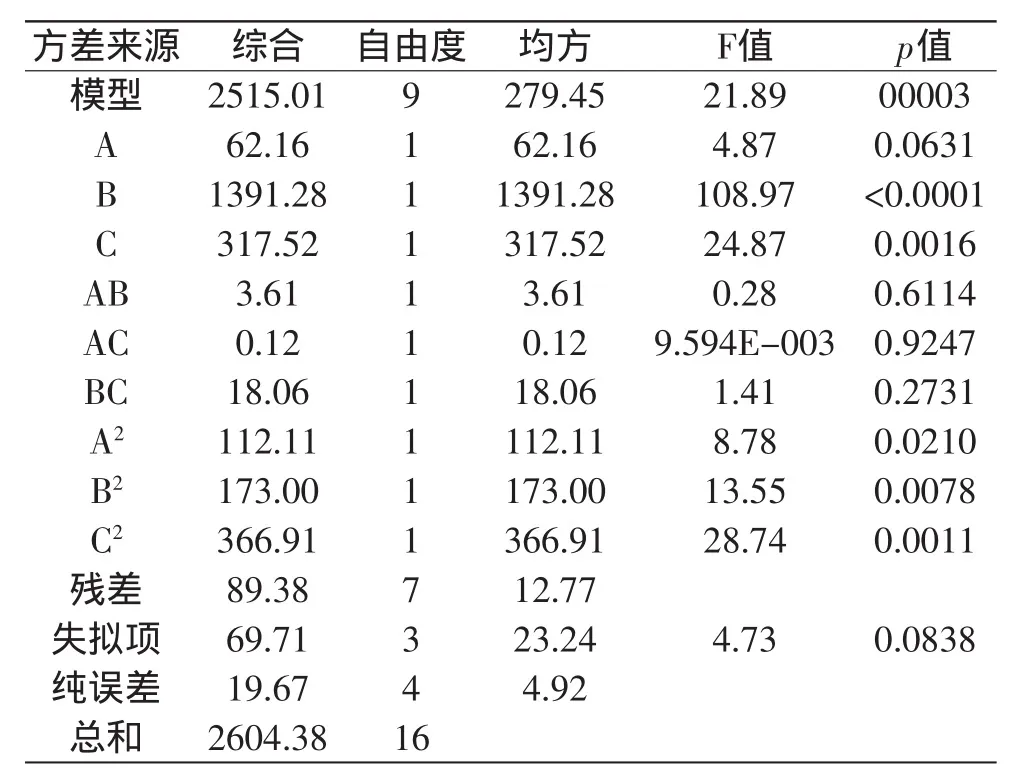
表3 回歸模型方差分析Table 3 ANOVA for the fitted quadratic polynomial model
2.3 酯化產物的HPLC和HPLC/ESI/MS分析鑒別
反相液相色譜法(HPLC-RP)分析中甘油酯的保留時間會隨著等效碳數(equivalent carbon number ECN)的增加而增加,ECN是由總碳數(CN)減去兩倍雙鍵(DB)所得,即ECN=CN-2DB,所以具有相同ECN的不同種類PGEF會被同時洗脫出來;采用HPLC分析時,樣品可以不需要進行衍生化處理,能直接將聚甘油酯組分按照類型分離,Brnmo Marcato等[16]采用HPLC分析聚甘油酯,獲得了較好的分離效果。
將按照最佳反應條件得到的酯化反應產物分別進行HPLC分離和HPLC/ESI/MS分析,得到低聚甘油酯的質譜圖譜見圖6。
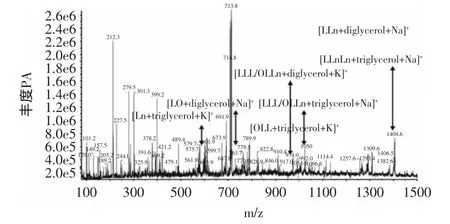
圖6 低聚甘油酯產物的HPLC-ESI-MS的正離子峰圖譜Fig.6 electropositive ionic peak HPLC-ESI-MS of the lowly polyglycero production
用HPLC/ESI/MS可以進一步分析鑒別產品中各種低聚甘油酯的成分。電噴霧離子化(ESI)技術只用于多電荷狀態下也穩定存在的大分子物質,加上幾乎沒有反常峰,非常適合測定物質分子量[16],其中物質的正離子峰通常會由Na或者K結合正離子得到,如圖6所示。由圖6可知,低聚甘油酯產物的HPLCESI-MS的正離子峰圖譜,圖譜中的低聚甘油酯產品中不同的二聚甘油酯和三聚甘油酯產物分別和鈉或鉀結合為分子離子,由圖6可看出部分產物的種類,如亞麻酸的三聚甘油單酯、油酸亞油酸的二聚甘油二酯以及亞油酸二聚甘油三酯等。由此可知,酶法催化低聚甘油酯化,由于空間阻力,低聚甘油的羥基并沒有完全酯化,而是部分酯化。
3 結論
3.1 磷脂酶A1可以催化酯化工業油酸和低聚甘油,優化方法后的產物,分別通過HPLC分離和HPLC/ESI/MS方法,分析確定了其中含的低聚甘油酯,其中催化酯化反應中酯化率受加酶量影響最大。
3.2 以酯化反應產物酸值為指標,采用三因素三水平的中心組合設計,對工業油酸和低聚甘油為原料制備低聚甘油酯的實驗條件進行優化,通過Design Expert軟件對實驗結果進行分析,確定最佳反應條件為:反應溫度45℃,加酶量1.6wt%,底物摩爾比值1∶1,反應時間12h,加水量為4wt%。最佳條件下酯化反應平均酯化率為為56.6%。
3.3 采用HPLC-ESI質譜通過檢測相對分子質量驗證了部分低聚甘油酯產物的種類,磷脂酶A1催化得到的聚甘油酯并未完全酯化,為部分酯化聚甘油酯。
[1]Carlos Ma rquez-Alvarez,Enrique Sastre,and Joaqu1 Perez-Pariente.Solid catalysts for the synthesis of fatty esters of glycerol,polyglycerols and sorbitol from renewable resources[J].Topics in Catalysis,2004,27(14):105-118.
[2]周燕霞,崔正剛,陳莉.聚甘油脂肪酸酯合成及應用[J].糧食與脂,2008(7):6-10.
[3]肖凱軍,郭丹丹,劉曉紅.聚甘油酯合成及特性研究[J].現代食品科技,2008,24(10):966-968.
[4]梁治齊,李金華.功能乳化劑與乳狀液[M].北京:中國輕工業出版社,2000,20-40.
[5]聶凌鴻.聚甘油脂肪酸酯合成與應用[J].糧食與油脂,2003(1):46.
[6]Kaiuhito C,Takase Y.Development of a novel polyglycerol monolaurate as a dete-rgent[J].Fragrance Journal,1996,24(1):64-67.
[7]胡國華,陳明.亞麻籽膠的特性及其在冰淇淋中的應用[J].冷飲與速凍食品工業,2003,9(4):23-25.
[8]周立國,張劍文,譚琛.各種聚甘油酯在保濕護膚化妝品中的應用研究[J].山東輕工業學院學報,2009,23(4):67-69.
[9]Charlemagne D,Legoy MD.Enzymatic synthesis of polyglycerol-fatty acid eater-s in a solvent-free system[J].JAOCS,1995,72(1):61-65.
[10]Wang LL,Wang Y,Hu CY,et al.Preparation of Diacylglycerol-Enriched Oil from Free Fatty Acid Using Lecitase Ultra-Catalyzed Esterificati-on[J].J Am Oil Chem Soc,2011,88(10):1557-1565.
[11]Watanabe T,Shimizu M,Sugiura M,et al.Optimization of reaction conditions for the production of DAG using immobili zeed 1,3-regiospecific lipase lipozyme RM IM[J].Journal of the American Oil Chemis ts Society,2003,80:1201-1207.
[12]楊繼國,楊博,寧正祥,等.全酶法制備甘油二酯的研究Ⅱ—脂肪酸酶法酯化反應的工藝優化[J].中國油脂,2009,34(3):15-19.
[13]Wang Y,Zhao M M,Ou S Y,et al.Preparation of a diacylglycerol-enriched soybean oilby phosphalipase A1 catalyzed hydrolysis[J].JournalofMolecularCatalysisB:Enzymatic,2009,56:165-172.
[14]Lo S K,Baharin B S,Tan C.P,et al.Lipase-catalysed production and chemi calll composition of diacylglycerols from soybean oil deodoriser distillate[J].European Journal of Lipid Science and Technology,2003,106:218-224.
[15]王杰,趙嵐峰,王樹力.實用高效液相色譜分析方法建立[M].第二版.北京:華文出版社,2001:81-100.
[16]Marcato B.Analysis of mixtures containing free fatty acids and MG,DAG and TG by HPLC with evaporative light-scattering detection[J].Journal of Chromatography A,1996,730:83-90.
Optimization of preparation of polyglycerol fatty acid ester catalyzed by Phospholipase A1 in a solvent free system using response surface methodology
XIAO Yi-sha,WANG Yong,ZHANG Guang-wen
(Department of Food Science and Engineering,Jinan University,Guangzhou 510632,China)
Q559
A
1002-0306(2012)20-0191-05
2012-04-05
肖伊莎(1988-),女,在讀碩士研究生,研究方向:食品科學。
粵港關鍵領域重點突破項目(2009A020700003)。

