磁性納米粒在抗腫瘤藥物中的應用
魏亞超 ,劉皈陽,張洪峰,顏青華,王樂,陳晨,李倩
1.河北省邯鄲市中心醫院藥劑科,河北 邯鄲 056001; 2.解放軍總醫院第一附屬醫院藥劑藥理科, 北京 100048
1 引言
目前,癌癥已經成為嚴重威脅人們生命的主要疾病之一,其引起的死亡人數超過了艾滋病、肺結核和瘧疾的總和。據統計,2007年全球新增癌癥病例1200多萬,死亡760萬,相當于每天有20,000余人死于癌癥[1]。由于人口增長和老齡化的問題,2050年全球新增癌癥病例將超2700萬,死亡人數也將達到1750萬。目前,目前臨床上治療腫瘤的方法主要有外科切除、放射治療和化學藥物治療。這些方法可抑制腫瘤進一步惡化,起到積極治療效果,但腫瘤定位、轉移和過量藥物的不良反應極大限制了它們的應用。隨著磁性納米粒的研究深入為抗腫瘤藥物的靶向制導、緩控釋釋放提供了依據,也為以上為題提供新的、可行的解決方法。本文將簡要介紹磁性納米粒的性質,然后重點對近年來其在藥物靶向、緩控釋領域中的研究做一綜述。
2 磁性納米粒的性質
磁性納米顆粒是一種處于納米級(1~100nm)的磁性材料,目前使用以鐵及鐵系氧化物居多(γ-Fe2O3及Fe3O4)。因其是納米量級的,所以具備以下性質:(1) 呈現超順磁性,產熱機制主要是奈爾馳豫(neel relaxation)[2]。在同樣的交變磁場作用下,單位質量相同成分的納米級鐵磁粒子產熱效率比微米級粒子高出1000倍[3],并且產熱性能穩定,產熱與粒徑關系不大[4]。(2) 腫瘤細胞對磁性納米粒的親和力比較高,這樣就保證了藥物能夠進入到腫瘤細胞發揮作用,同時降低正常細胞中的藥物濃度減少了毒副作用。(3) 具有良好的生物相容性和降解性,毒性較低甚至無毒。現在的研究已經證實醫用納米級Fe3O4磁性納米粒生物相容性較好,急性毒性低[5],而表面經過修飾的Fe3O4磁性納米粒生物相容性更好,毒性也更低[6]。(4) 磁性納米粒在腫瘤細胞分離后,在子細胞中同樣具有高保留性,可殺滅腫瘤子細胞。
3 用于腫瘤的靶向藥物治療
目前,抗腫瘤藥物均使用全身給藥的方式(靜脈給藥或口服給藥)。盡管可供選擇的化療藥物有200多種,但這些藥物無一例外都存在著嚴重的毒副反應,給腫瘤患者的生活質量帶來了很大影響,部分患者(特別是老年患者)往往無法耐受整個療程。近年來,雖然陸續出現了曲妥珠單抗、利妥昔單抗、吉非替尼、埃羅替尼等毒副反應較輕的分子靶向性腫瘤治療藥物,但這些藥物僅對特定的腫瘤,甚至是特定基因型的腫瘤有效,并且價格昂貴,難以普遍應用[7,8]。因此在腫瘤放、化療中,國內外都在尋找一種選擇性殺傷腫瘤細胞而不損傷正常組織細胞的方法。而磁性納米粒因為具有較強的磁響應性,為腫瘤的靶向治療提供了新的選擇。
與傳統靶向制劑相比,磁靶向制劑具有以下優點:(1)具有被動靶向和物理靶向雙重靶向效果,能夠更好地實現靶向給藥的目的。(2)穿越傳統藥物難以通過的血腦屏障(blood - brain barrier, BBB),提高腦內藥物濃度,發揮腦靶向作用,為中樞神經系統及其他腦內用藥開辟了新的途徑[9]。(3)載藥量高,增加藥物的穩定性和生物利用度,延長藥物作用時間,減少藥物用量。(4)可與腫瘤熱療聯合,達到聯合治療的效果。
龔連生等[10]觀察了磁性阿霉素白蛋白納米粒在移植性肝癌模型中的磁靶向性,他們的研究發現在磁場的作用下,磁性阿霉素白蛋白納米粒在大鼠移植性肝腫瘤中的聚集明顯增加(磁區腫瘤組織的發射活性為非磁區正常肝組織放射活性的8.7倍);即使肝腫瘤區沒有外加磁場,由于腫瘤組織和正常肝組織血管密度的差異,磁性阿霉素白蛋白納米粒在腫瘤組織中的分布也明顯高于正常肝組織(無外加磁場情況下,腫瘤組織的放射活性為正常肝臟的2.8倍)。該研究很好的說明了磁性藥物納米粒具有被動靶向和物理靶向的雙重靶向作用。
4 用于抗腫瘤藥物的緩控釋載體
隨著醫學和智能材料發展,現在越來越多的將磁性納米粒和一些新的智能材料結合起來制備成新型的靶向藥物緩控釋劑型。在目前的研究中,將磁性納米粒和脂質體、溫敏水凝膠結合起來作為抗腫瘤藥物緩控釋載體的比較多。
4.1 用于抗腫瘤藥物的緩釋載體 華中科技大學的董強等[11]采用逆相蒸發法研制出磁性吉西他濱隱形納米脂質體(MGSL),同時考察MGSL的理化性質等各項因素。結果顯示:優化制備的MGSL除了提高所攜帶的吉西他濱的穩定性、減低其毒副反應、延長其作用時間、減少其給藥量及給藥頻率以外,還能在定向于腫瘤部位的外磁場作用下有效提高腫瘤組織內化療藥物濃度,顯著抑制腫瘤組織的生長,發揮抗腫瘤效應。并且,單次給予MGSL,其體內藥物代謝動力學符合二室模型,其分布半衰期、消除半衰期、藥-時曲線下面積、表觀分布容積和消除率較單純的吉西他濱有著顯著性差異,表現出較好的體內緩釋效應。
陽兵等[12]也制備了載有多西紫杉醇的磁性聚乳酸-羥基乙酸納米緩釋微球,高效液相分析載藥高分子緩釋微球具良好的緩釋性能,細胞熱化療實驗發現磁性納米粒聯合載藥緩釋微球具有良好的熱協同效應。.
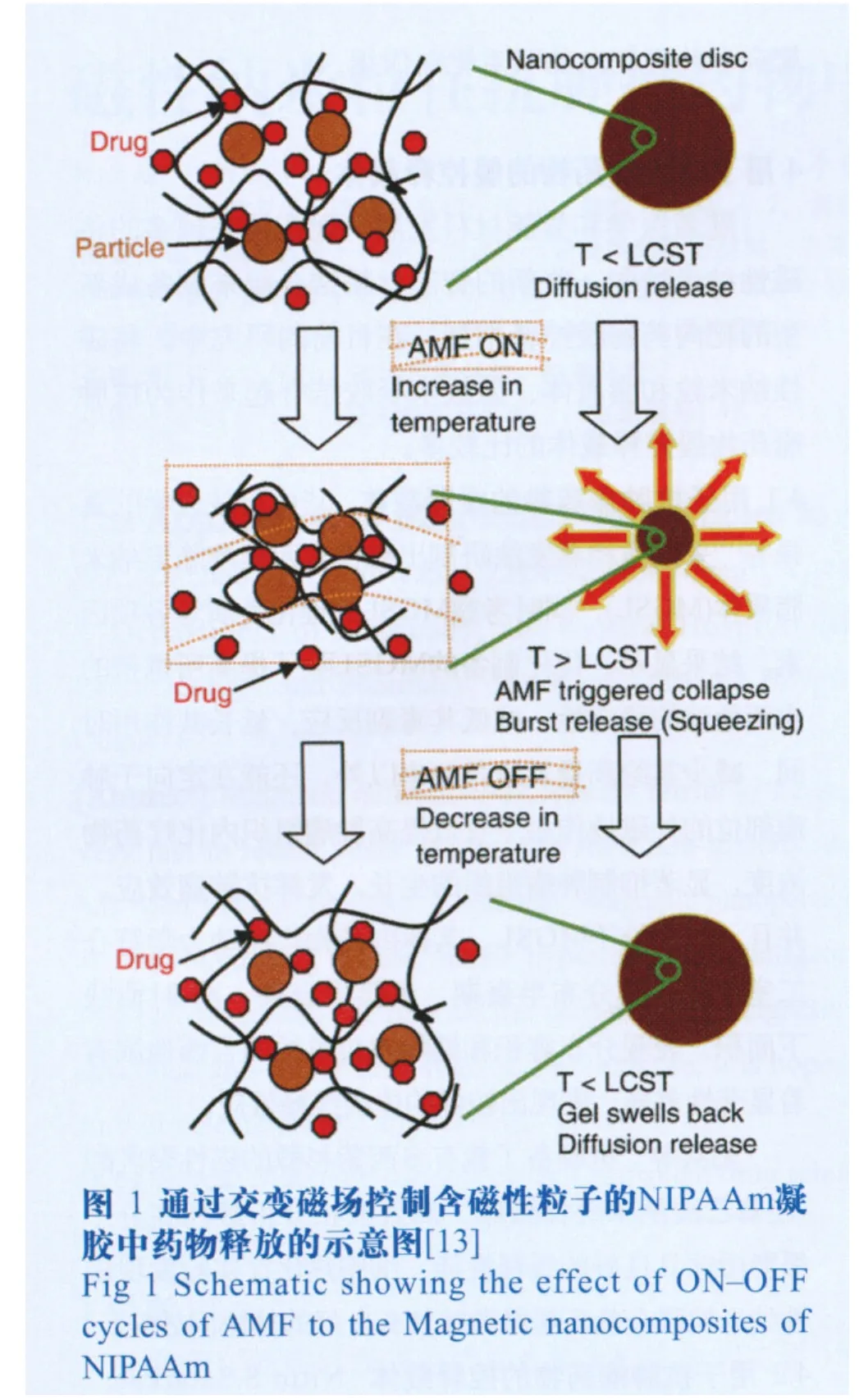
4.2 用于抗腫瘤藥物的控釋載體 Nitin S.Satarkar,J.Zach Hilt[13]將磁性納米粒和溫敏水凝膠結合,制備了載有藥物的磁性溫敏水凝膠。并通過交變磁場使磁性納米粒生熱進而控制溫敏水凝膠的溫度,而隨著溫度的變化溫敏水凝膠的體積會發生相應的變化,藥物的釋放速率也會發生變化。見圖1。
我們的研究[14]也表明,將磁性納米粒加入到PLGA-PEG-PLGA溫敏水凝膠中,通過體外交變磁場可以很好的控制水凝膠的溫度,進而通過控制水凝膠膠束的聚集于分散來控制藥物釋放速度。這樣就可以構建一個通過交變磁場來遠程控制藥物釋放的系統,使藥物按照患者的病情需要進行脈沖式釋放,大大提高了患者的順應性,減少了藥物的毒副作用。
中南大學譚亮等[15]制備了溫度敏感性脂質體磁性阿霉素納米粒(Ts-LMADM),并考察了制劑的控釋效果,研究結果表明Ts-LMADM在其相變溫度(42℃)附近41℃時,被包封的阿霉素的釋放量突然增至最大,為總包封量的(84.6士0.7)%,說明Ts-LMADM具有敏感的溫度控釋特性。
5 結語
磁性納米粒是近年來的研究熱點,除了在醫學方面的應用外,還被廣泛應用于各種苛刻條件的磁性流體密封、潤滑、減震、智能開關[16]、醫療器械、聲音調節、光顯示、發電、磁性納米粒選礦等多種領域。
雖然磁性納米粒因其獨特的優點使得其在很多領域有著良好的應用前景,但仍然有很多問題亟待解決。如:靶向給藥后的藥代動力學規律,與其結合應用新型智能材料(脂質體、溫敏水凝膠等)的穩定性和完整性,不同納米粒子的靶向性以及納米藥物磁性靶向所需磁場強度等方面仍需進一步研究。相信隨著科學的發展和醫學的進步,磁性納米粒的應用前景會越來越廣闊,也可以更好的服務于人類。
[1]陸建邦,孫喜斌.關于我國癌癥預防控制體系建設的思考[J].中國腫瘤, 2009,18(2): 98-100.
[2]王煦漫,古宏晨,楊正強,等.磁熱療用Fe3O4在交變磁場中的熱效應[J].上海交通大學學報, 2005,39(2): 275-278.
[3]Babincova M, Leszczynska D, Sourivong P, et al.Superparamagnetic gel a novel material for electromagnetically induced hyperthermia[J].J Magn Magn Mater, 2001, 225(1-2): 109-112.
[4]Ma M, Wu Y, Zhou J, et al.Size dependence of specific power absorp tion of Fe3O4 particles in AC magnetic field[J].J Magn Magn Mater, 2004, 268(1-2): 33-39.
[5]王國斌,夏澤鋒,陶凱雄,等.醫用納米級Fe3O4磁流體的急性毒理學實驗研究[J].華中科技大學學報(醫學版), 2004, 33(4): 452-458.
[6]鄒芬,潘一峰,張紅,等.聚乙二醇-聚乙烯亞胺/四氧化三鐵納米磁流體的毒性及其生物相容性[J].中國組織工程研究與臨床康復,2010, 14(3): 447-451.
[7]Ono M, Kuwano M.Molecular mechanisms of epidermal growth factor receptor (EGFR) activation and response to gefitinib and other EGFR-targeting drugs[J].Clin Cancer Res, 2006;12(24):7242-7251.
[8]Zangemeister-Wittke U.Antibodies for targeted cancer therapy technical aspects and clinical perspectives[J].Pathobiology, 2005,72(6): 279-286.
[9]劉嵐,唐萌,劉璐,等.Fe2O3-Glu納米顆粒在小鼠體內的代謝動力學研究[J].環境與職業醫學,2006,23:1.
[10]龔連生,張陽德,劉恕.磁性阿霉素白蛋白納米粒在移植性肝癌模型中的磁靶向性.中華肝膽外科雜志[J].2003,9(9):543-546.
[11]董強.磁性吉西他濱隱形納米脂質體的制備及其磁控靶向抑瘤作用的實驗研究[D].華中科技大學, 2007.
[12]陽兵, 趙凌云, 徐小雨, 等.磁流體聯合藥物緩釋載體介導的腫瘤磁感應熱化療[J].科技導報, 2010, 28(14):26-32.
[13]Nitin S.Satarkar,J.Zach Hilt.Magnetic hydrogel nanocomposites for remote controlled pulsatile drug release[J].Journal of Controlled Release.2008,130(3) : 246-251.
[14]魏亞超,劉皈陽,陳召紅.磁性溫敏水凝膠的制備及其在交變磁場中的熱效應研究[J].中國藥學雜志, 2012,47(9):57-59.
[15]譚亮.溫度敏感性脂質體包裹磁性阿霉素納米粒的制備及其物理性質的研究[D].中南大學,2009.
[16]Satarkar NS, Zhang W, Eitel RE, et al.Magnetic hydrogel nanocomposites as remote controlled microfluidic valves[J].Lab Chip.2009, 9(12):1773-1779.

