米非司酮配伍米索前列醇終止13~16周妊娠療效觀察
佟明香 張云蔚
自20世紀90年代以來,催經止孕藥物的發展日臻完善。其優點是方法簡便,不需宮內操作,故無創傷性,目前臨床最常用的藥物是米非司酮。米非司酮為孕激素受體水平拮抗藥物,具有終止早孕、抗著床、誘導月經及促進宮頸成熟等作用,已廣泛試用于孕49 d內的早孕婦女。隨著其臨床用途的不斷拓寬,其對于終止孕13~16周中期妊娠已獲得良好的效果。現就筆者所在醫院3年來80例患者臨床資料進行回顧分析。
1 資料與方法
1.1 一般資料 選取2009年3月-2012年2月來院就診要求終止妊娠的婦女,孕次1~5次,產次0~3次。納入標準:(1)妊娠13~16周且要求終止妊娠者;(2)經B超檢查宮內妊娠者;(3)胎兒雙頂徑(BPD)2.0~3.8 cm;(4)血常規、出凝血功能正常;(5)無產科和內科合并癥及米非司酮、米索前列醇使用禁忌證;(6)知情同意。將收治病例按孕周分組,其中孕13~14周53例(Ⅰ組),孕14周+1 d~15周14例(Ⅱ組),15周+1 d~16周13例(Ⅲ組)。年齡16~41歲,初次妊娠23例,2次妊娠31例,3次妊娠26例。
1.2 給藥方法 該80例患者相繼采用相同的服藥方法,即第1天晚飯后2 h,口服米非司酮100 mg(4片),第2天早飯后2 h同服,第2天晚飯后2 h同服,第3天晨空腹服用米索前列醇0.6 mg(3片)。若3 h后未臨產,可視宮縮情況加服米索前列醇0.6 mg(3片),3 h后可再加服0.6 mg(3片),共計1.8 mg。觀察妊娠物排出情況及陰道流血情況。
1.3 效果評價 記錄給藥時間、劑量,觀察宮縮、宮頸擴張、陰道流血以及不良反應,記錄妊娠物排出的時間,檢查胎兒、胎盤、胎膜排出是否完整,從而決定是否清宮。效果評定標準:(1)完全流產:服用第1次米索前列醇后9 h內妊娠物自然排出,超聲檢查無組織殘留,陰道流血少于月經量;(2)不完全流產:服用第1次米索前列醇后9 h內妊娠物部分排出,超聲檢查有組織殘留,陰道流血多于月經量;(3)失敗:1.8 mg米索前列醇服用后12 h,有宮縮,但無妊娠物排出。
2 結果
2.1 用藥次數 口服米索前列醇1次成功26例(32.5%),2次成功45例(56.3%),3次成功5例(6.3%)。
2.2 孕周與療效關系 妊娠物自然排出76例(95.0%),其中完全流產65例(81.3%),不完全流產11例(13.8%),失敗4例(5.0%)。見表1。完全流產者陰道流血量(80.5±20.5)ml,不完全流產者陰道流血量(130.5±20.5)ml。不完全流產者及失敗者給予清宮術,清宮術15例(18.8%),不完全流產者清宮術中出血不多,失敗4例鉗刮術中出血150 ml左右。清宮術后給予縮宮素20 U宮頸注射。無宮頸裂傷、子宮穿孔發生。其中1例失敗者,胎兒雙頂徑3.8 cm,分娩過程中胎位橫位。胎兒軀干、四肢、胎盤、胎膜鉗出后,只余胎頭于宮腔。卵圓鉗進入子宮腔,左手在恥骨聯合上方按壓固定宮底,鉗夾胎頭娩出。
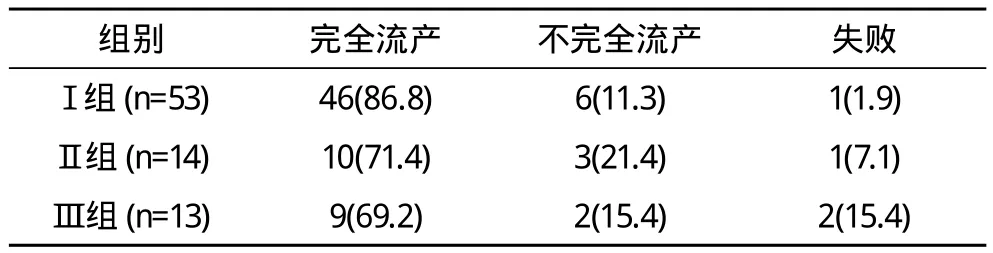
表1 孕周與療效觀察 例(%)
3 討論
米非司酮是一種合成類固醇,其結構類似炔諾酮,具有抗孕酮、糖皮質醇和輕度抗雄激素特性。米非司酮對子宮內膜孕激素受體的親和力比孕酮高5倍,因而能和孕酮競爭而與蛻膜的孕激素受體結合,從而阻斷孕酮活性而終止妊娠。同時由于妊娠蛻膜壞死,釋放內源性前列腺素,促進子宮收縮及宮頸軟化[1];通過改變激素分泌的平衡,導致絨毛滋養細胞變性、壞死,或通過抑制滋養細胞增殖,誘導和促進其凋亡[2]。米索前列醇是前列腺素E1的衍生物,對早孕及中孕者有良好的促宮頸成熟、擴張宮頸作用,對各期妊娠子宮均有收縮作用[3]。對于13~16周妊娠,一般引產方法效果不佳,且大多鉗刮術手術難度大,宮頸裂傷,子宮穿孔,術中出血,臟器損傷的發生率均較高,因此對術者的手術技能要求較高。而米非司酮聯合米索前列醇的使用,可促進妊娠物的排出,從而達到流產的目的。與此同時,米非司酮聯合米索前列醇的使用也替代了部分鉗刮術,避免了人為將細菌帶入宮腔的可能,從而減少了術后感染的機會及手術操作可能帶來的并發癥,增加了流產的安全性。患者不用住院,門診可進行,既減少了患者的經濟負擔,又避免了被迫延長孕周住院引產。對于不完全流產及失敗而需采取清宮術的患者,由于用藥后,宮頸已經軟化、擴張,宮口松弛,使手術易于操作,不易發生宮頸裂傷及子宮穿孔,在一定程度上也減輕了患者的痛苦。因此,米非司酮聯合米索前列醇終止13~16周妊娠,成功率高,陰道流血少,且二者均為口服,方法簡單,不良反應少,經濟、安全有效。
[1]樂杰.婦產科學[M].北京:人民衛生出版社,2008:266-267.
[2]楊雪峰,王淑芝.米非司酮抗早孕絨毛及蛻膜中雌孕激素受體的免疫組織化學研究[J].現代婦產科進展,2009,9(5):357-358.
[3]尚麗娟.米非司酮配伍米索前列醇終止帶器妊娠效果分析[J].中國婦幼保健,2009,24(1):116.

