木糖-甘氨酸美拉德反應(yīng)體系光譜特性和抗氧化性能的研究
于彭偉,劉登勇,周光宏
(南京農(nóng)業(yè)大學(xué)食品科技學(xué)院,肉品加工與質(zhì)量控制教育部重點(diǎn)實(shí)驗(yàn)室,江蘇 南京 210095)
木糖-甘氨酸美拉德反應(yīng)體系光譜特性和抗氧化性能的研究
于彭偉,劉登勇,周光宏*
(南京農(nóng)業(yè)大學(xué)食品科技學(xué)院,肉品加工與質(zhì)量控制教育部重點(diǎn)實(shí)驗(yàn)室,江蘇 南京 210095)
采用木糖和甘氨酸進(jìn)行模式美拉德反應(yīng),考察反應(yīng)進(jìn)程中產(chǎn)物pH值、吸光度及顏色參數(shù)的變化,并以1,1-二苯基-2-三硝基苯肼(DPPH)自由基清除能力、Fe2+螯合能力及油脂過氧化值(POV)為指標(biāo),研究美拉德反應(yīng)產(chǎn)物的抗氧化效果。結(jié)果表明:隨著反應(yīng)的進(jìn)行,產(chǎn)物由無色變?yōu)樗{(lán)色最后生成褐色;反應(yīng)pH值和L*值逐漸降低,a*值增大,b*值減小,但后期兩者變化不顯著。產(chǎn)物具有很好的Fe2+螯合能力,POV值較低,但清除DPPH自由基能力不強(qiáng)。總體而言,產(chǎn)物具有較強(qiáng)的抗氧化能力。
美拉德反應(yīng);光譜特性;抗氧化性
美拉德反應(yīng)(Maillard reaction)又稱羰氨反應(yīng)或非酶褐變反應(yīng),是指氨基化合物和羰基化合物之間發(fā)生的反應(yīng),是食品顏色及風(fēng)味產(chǎn)生的主要途徑之一[1-2]。研究表明美拉德反應(yīng)產(chǎn)物(主要是含類黑精,還原酮以及含N、S、O的雜環(huán)化合物)具有一定的抗氧化性。近年來,關(guān)于美拉德反應(yīng)產(chǎn)物(MRPs)的抗氧化性研究逐漸增加,而且成為當(dāng)今食品營(yíng)養(yǎng)學(xué)和食品化學(xué)領(lǐng)域的熱門課題,因?yàn)槟壳笆称饭I(yè)上廣泛應(yīng)用的抗氧化劑如BHA、BHT和TBHQ等是合成抗氧化劑,歐美國家己禁止使用[3]。MRPs是食品加工和儲(chǔ)藏過程中自身產(chǎn)生的一類物質(zhì),可認(rèn)為是天然的,有望成為下一代天然無毒的抗氧化劑,被期望用以代替現(xiàn)有食用抗氧化劑,正逐漸引起人們的關(guān)注[4-5]。
Hayase等[6]研究發(fā)現(xiàn)木糖-甘氨酸美拉德反應(yīng)體系生成一種藍(lán)色中間產(chǎn)物,并命名為Blue-M1。Murakami等[7]進(jìn)一步研究了木糖-甘氨酸產(chǎn)物與自由基清除能力之間的關(guān)系,證實(shí)其產(chǎn)物具有一定的自由基清除能力。因此,研究木糖-甘氨酸美拉德反應(yīng)產(chǎn)物可以為探索美拉德反應(yīng)終點(diǎn)及應(yīng)用新型食品色素和具有抗氧化性的功能性食品添加劑提供實(shí)驗(yàn)數(shù)據(jù)。本研究通過光譜掃描及顏色參數(shù)確定反應(yīng)進(jìn)程和反應(yīng)終點(diǎn),并通過相關(guān)指標(biāo)研究產(chǎn)物的抗氧化性。
1 材料與方法
1.1 材料、試劑與儀器
豬背最長(zhǎng)肌購自南京衛(wèi)崗集貿(mào)市場(chǎng)。
L-甘氨酸(生化純) 美國Amresco公司;菲洛嗪美國Sigma公司;1,1-二苯基-2-三硝基苯肼(1,1-diphenyl-2-picryl-hydrazyl,DPPH) 上海梯希愛化成工業(yè)發(fā)展有限公司;D-木糖(食品純) 北京嘉康源科技發(fā)展有限公司;碳酸氫鈉、氯化亞鐵、三氯甲烷、冰乙酸等其他化學(xué)試劑均為分析純。
pH計(jì) 瑞士梅特勒-托利多公司;CR-400型色差儀 日本柯尼卡公司;UV-2450型紫外分光光度計(jì) 日本島津公司;SpectraMax M2e型酶標(biāo)儀 美國分子儀器公司;ZKSY-600智能恒溫水浴鍋 南京科爾儀器設(shè)備有限公司。
1.2 方法
1.2.1 MRPs的制備
分別稱取D-木糖、L-甘氨酸和NaHCO3,加入二次蒸餾水配制成木糖1mol/L、甘氨酸0.2mol/L和NaHCO30.1mol/L的美拉德反應(yīng)體系,用10mol/L NaOH溶液調(diào)節(jié)pH值至9.0。將此配制的溶液等份分裝于10mL離心管中,放入水浴鍋(30℃),開始計(jì)時(shí),蓋上水箱蓋子予以避光。每隔24h取樣,樣品取出后立即在冰浴中冷卻5min,再放入4℃冷庫保存,作為樣品液待測(cè)。
1.2.2 對(duì)產(chǎn)物的光譜掃描
用UV-2450型紫外分光光度計(jì)對(duì)MRPs于波長(zhǎng)400~700nm范圍進(jìn)行光譜掃描,為保證讀數(shù)在適合范圍內(nèi),將反應(yīng)物稀釋一定倍數(shù)。
用SpectraMax M2e型酶標(biāo)儀對(duì)MRPs在所需波長(zhǎng)(預(yù)實(shí)驗(yàn)測(cè)定最佳激發(fā)波長(zhǎng)為3 47 nm,最佳發(fā)射波長(zhǎng)為460nm處測(cè)定吸光度。為保證讀數(shù)在適合范圍內(nèi),將反應(yīng)物稀釋一定倍數(shù)。
1.2.3 色差的測(cè)定
打開色差儀,校正調(diào)試后,將測(cè)試頭放在待測(cè)樣品上。準(zhǔn)確吸取MPRs 2.5mL,放在待測(cè)樣品槽中,測(cè)定其L*、a*、b*值。其中,L*值代表亮度;a*值代表紅度,正值越大樣品顏色越偏紅,負(fù)值越大樣品顏色越偏綠;b*值代表黃度,正值越大樣品顏色越偏黃,負(fù)值越大樣品顏色越偏藍(lán)。
1.2.4 鐵離子螯合能力的測(cè)定
按文獻(xiàn)[8]稍加修改,通過評(píng)價(jià)在562nm波長(zhǎng)處鐵離子-菲洛嗪混合物的吸光度來研究MRPs的鐵離子螯合能力。取稀釋4倍的MRPs 5mL,加入0.1mL 2mmol/L的氯化亞鐵溶液和0.2mL 5mmol/L的菲洛嗪溶液,混合均勻。同時(shí)取質(zhì)量濃度為0.4g/100mL茶多酚做同樣處理,混合液室溫靜置10min,于562nm波長(zhǎng)處測(cè)定吸光度。較高的鐵離子螯合能力導(dǎo)致在562nm波長(zhǎng)處較低的吸光度。用式(1)計(jì)算鐵離子螯合能力。
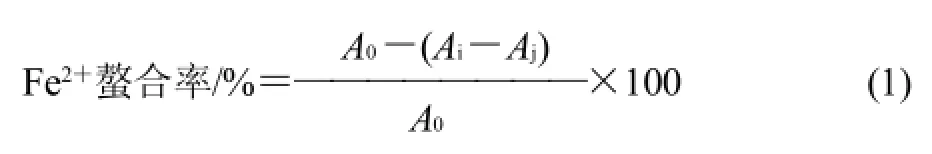
式中:A0為未加MRPs溶液所測(cè)得的吸光度;Ai為加MRPs后溶液所測(cè)得的吸光度;Aj為MRPs的吸光度。
1.2.5 過氧化值(POV)的測(cè)定
參照GB/T 5009.37—2003《食用植物油衛(wèi)生標(biāo)準(zhǔn)的分析方法》[9]測(cè)定POV值。油脂氧化過程中產(chǎn)生過氧化物,與KI作用,生成游離碘,以Na2S2O3溶液滴定,計(jì)算含量。稱取0.2g左右的MRPs,加入8g大豆油,置于20mL燒杯中,同時(shí)取0.4%茶多酚做同樣處理并加入一滴吐溫-60助溶,用薄膜密封瓶口放常溫(5~10℃) 50d,用式(2)計(jì)算POV值。

式中: X為試樣的過氧化值(meq/kg);V1為試樣消耗硫代硫酸鈉標(biāo)準(zhǔn)滴定溶液體積/mL;V2為試劑空白消耗硫代硫酸鈉標(biāo)準(zhǔn)滴定溶液體積/mL;c為硫代硫酸鈉標(biāo)準(zhǔn)滴定溶液的濃度/(mol/L);m為試樣質(zhì)量/g。
1.2.6 DPPH自由基清除能力的測(cè)定
對(duì)文獻(xiàn)[10]方法做適當(dāng)修改。取稀釋5倍的MRPs 2mL及0.1mmol/L的DPPH乙醇溶液2mL加入同一具塞試管中搖勻,同時(shí)取0.4g/100mL茶多酚做同樣處理,于室溫密閉靜置30min,未加樣品液為空白,無MRPs處理為對(duì)照,于517nm波長(zhǎng)處測(cè)定吸光度。用式(3)計(jì)算DPPH自由基清除率,清除率越大抗氧化能力越強(qiáng)。
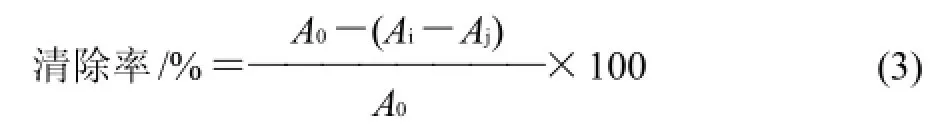
式中:A0為未加MRPs 時(shí)DPPH 溶液的吸光度;Ai為加MRPs后DPPH溶液的吸光度;Aj為MRPs的吸光度。
1.3 數(shù)據(jù)處理
用Microsoft Excel統(tǒng)計(jì)處理,用SAS 8.2進(jìn)行線性分析和鄧肯多重比較(Duncan’s multiple-range test)。每個(gè)處理重復(fù)3次。
2 結(jié)果與分析
2.1 美拉德反應(yīng)進(jìn)程的變化
2.1.1 反應(yīng)體系pH值的變化
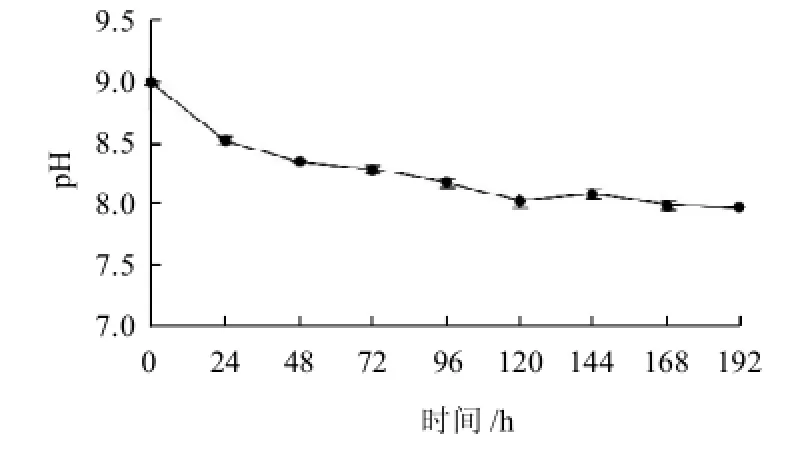
圖1 L-甘氨酸與D-木糖反應(yīng)的美拉德產(chǎn)物pH值Fig.1 pH values of MRPs of L-glycine and D-xylose
在反應(yīng)初始的24h內(nèi),pH值有明顯的下降,反應(yīng)速率較快,而反應(yīng)至192h,pH值為7.97,因此前24h的pH值下降水平占總下降水平的46.6%,較其他時(shí)間點(diǎn)有顯著下降(P<0.05)。反應(yīng)體系pH值的下降主要是由于羰基在加熱過程中不斷地與堿基基團(tuán)-氨基進(jìn)行縮合,使得游離的氨基被封閉,致使體系的pH值不斷下降,在體系反應(yīng)接近終點(diǎn)時(shí),沒有足夠的羰基與氨基進(jìn)行縮合,導(dǎo)致p H值趨于平穩(wěn)。
2.1.2 MRPs的光譜掃描
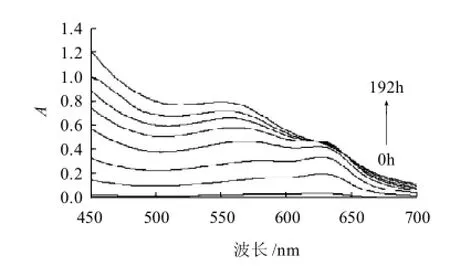
圖2 L-甘氨酸與D-木糖反應(yīng)的美拉德產(chǎn)物的可見吸收光譜Fig.2 Visible absorption spectra of MRPs of L-glycine and D-xylose
由圖2可知,MRPs在570nm和627nm波長(zhǎng)處有兩個(gè)吸收峰。加熱24h后,在627nm波長(zhǎng)處出現(xiàn)吸收峰,溶液呈現(xiàn)藍(lán)綠色,該物質(zhì)是類黑精的前體物,與Murakami等[7]的研究一致。隨反應(yīng)的進(jìn)行,在96h于570nm波長(zhǎng)處出現(xiàn)另一吸收峰,Shirahashi等[11]最新研究表明該吸收峰處的物質(zhì)和藍(lán)色物質(zhì)一樣是MRPs的前體物質(zhì),該物質(zhì)的生成表明反應(yīng)體系已進(jìn)入高級(jí)階段,此后570nm波長(zhǎng)處吸收峰逐漸增大,且吸收峰發(fā)生藍(lán)移,可能是物質(zhì)結(jié)構(gòu)發(fā)生變化,不斷生成新物質(zhì)導(dǎo)致吸收光譜的吸收峰向短波方向的移動(dòng)。在120h時(shí),藍(lán)色產(chǎn)物(627nm波長(zhǎng)處吸收峰)峰值達(dá)到最大,此后逐漸減小,表明產(chǎn)物聚合消除速率大于生成速率,說明在120h藍(lán)色產(chǎn)物即作為前體物參與最終反應(yīng)階段。
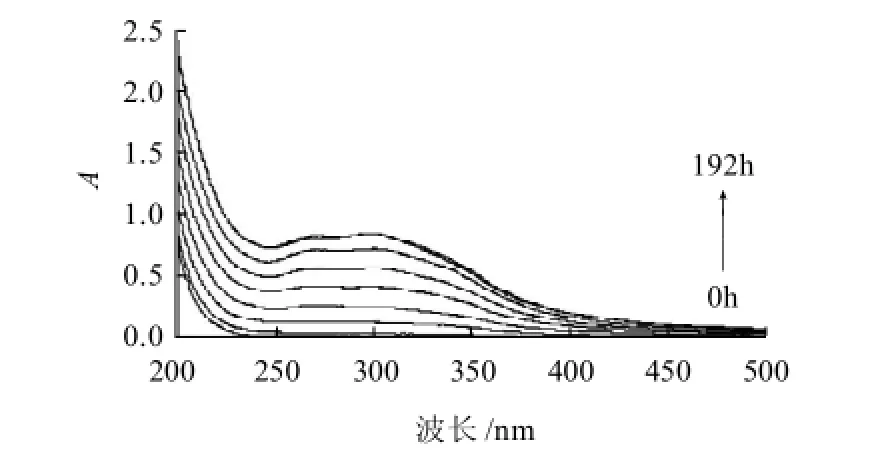
圖3 L-甘氨酸與D-木糖反應(yīng)的美拉德產(chǎn)物的紫外吸收光譜Fig.3 UV absorption spectra of MRPs of L-glycine and D-xylose
由圖3可知,反應(yīng)進(jìn)行到72h美拉德反應(yīng)產(chǎn)物在272nm和298nm波長(zhǎng)處產(chǎn)生吸收峰,這兩處的吸收峰主要是美拉德反應(yīng)中高級(jí)階段的無色小分子中間體[12]。隨著反應(yīng)的進(jìn)行兩吸收峰逐漸增大,在168h達(dá)到最大值,之后趨于平穩(wěn)。表明高級(jí)階段中小分子參與最終反應(yīng)階段,經(jīng)過環(huán)化、降解、縮合等,形成褐色產(chǎn)物[13]。
2.1.3 MRPs的熒光強(qiáng)度(FI)變化

圖4 L-甘氨酸與D-木糖反應(yīng)的美拉德產(chǎn)物的熒光強(qiáng)度Fig.4 Fluorescence intensity of MRPs of of L-glycine and D-xylose
首先對(duì)MRPs進(jìn)行適當(dāng)稀釋,確定最佳激發(fā)與發(fā)射波長(zhǎng)分別為347nm和460nm,以測(cè)定各時(shí)間點(diǎn)反應(yīng)產(chǎn)物的熒光強(qiáng)度。由圖4可知,F(xiàn)I隨時(shí)間延長(zhǎng)線性增加,線性相關(guān)系數(shù)(R2)達(dá)到0.9606(P<0.0001)。FI在168h出現(xiàn)最大值,然后降低。FI表征了高級(jí)階段熒光小分子的產(chǎn)生狀態(tài),反應(yīng)在前168h持續(xù)增加,然后降低,高級(jí)階段小分子物質(zhì)相互聚合成褐色類黑精,導(dǎo)致聚合消除速率大于生成速率,表明美拉德反應(yīng)進(jìn)入終極階段。這與Benjakul等[14]研究認(rèn)為熒光化合物是棕色物質(zhì)的前體,熒光強(qiáng)度達(dá)最大之后隨著加熱時(shí)間的延長(zhǎng),熒光化合物逐漸分解為棕色物質(zhì)而呈現(xiàn)下降趨勢(shì)相一致。
2.1.4 MRPs的色澤變化
模式美拉德反應(yīng)比較復(fù)雜,產(chǎn)物較多,色澤變化明顯。本實(shí)驗(yàn)?zāi)J襟w系顏色首先由無色變?yōu)闇\藍(lán)色,顏色繼續(xù)加深變?yōu)樯钏{(lán)色,最終生成褐色產(chǎn)物。圖5描述了色差(L*、a*、b*值)隨時(shí)間的變化趨勢(shì)。
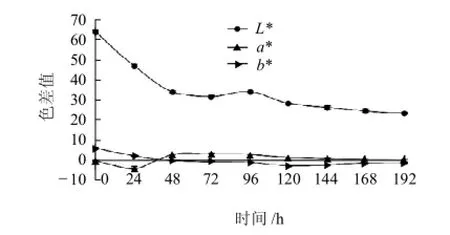
圖5 L-甘氨酸與D-木糖反應(yīng)的美拉德產(chǎn)物的色差值Fig.5 Color parameters of MRPs of L-glycine and D-xylose
由圖5可知,在初始48h內(nèi),b*值和L*值隨時(shí)間延長(zhǎng)線性下降(P<0.0001),之后下降緩慢,趨于平穩(wěn)。而在初始48h內(nèi),a*值顯著下降后上升,在48h達(dá)最大,之后緩慢降低。初始24h色差值的變化表明反應(yīng)體系速率較快,溶液先由無色變?yōu)闇\藍(lán)色,隨著反應(yīng)進(jìn)行,溶液又由淺藍(lán)色變?yōu)樯钏{(lán)色,最終生成褐色產(chǎn)物。
2.1.5 美拉德反應(yīng)終點(diǎn)的確定

表1 MRPs光譜特性與色差值參數(shù)相關(guān)系數(shù)Table1 Correlation coefficients between spectroscopic characteristics and color parameters of MRPs
由表1可知,A627nm和b*值、L*值相關(guān)系數(shù)分別為-0.89846和-0.90558,均為顯著負(fù)相關(guān)(P<0.01),表明隨藍(lán)色產(chǎn)物的生成,美拉德反應(yīng)產(chǎn)物顏色變藍(lán)且顏色逐漸加深。FI和A627nm呈極顯著正相關(guān)(P<0.01),藍(lán)色產(chǎn)物和具熒光的小分子物質(zhì)隨反應(yīng)的進(jìn)行幾乎呈線性增加,但熒光小分子物質(zhì)在168h達(dá)最大量后開始減小,而藍(lán)色物質(zhì)在120h達(dá)最大量后減少,說明藍(lán)色物質(zhì)較熒光分子物質(zhì)先進(jìn)入最終反應(yīng)階段。由以上可以判斷反應(yīng)在進(jìn)行到120h時(shí),以藍(lán)色產(chǎn)物為主的前體物進(jìn)入最終反應(yīng)階段,所以判定反應(yīng)到120h為反應(yīng)進(jìn)入終級(jí)階段。
2.2 MRPs抗氧化性的研究
MRPs的抗氧化性主要從DPPH自由基清除、金屬離子螯合力和抗油脂氧化三方面著手進(jìn)行分析,同時(shí)取0.4g/100mL茶多酚作對(duì)比,以判斷MRPs的抗氧化能力。
2.2.1 MRPs的Fe2+螯合能力
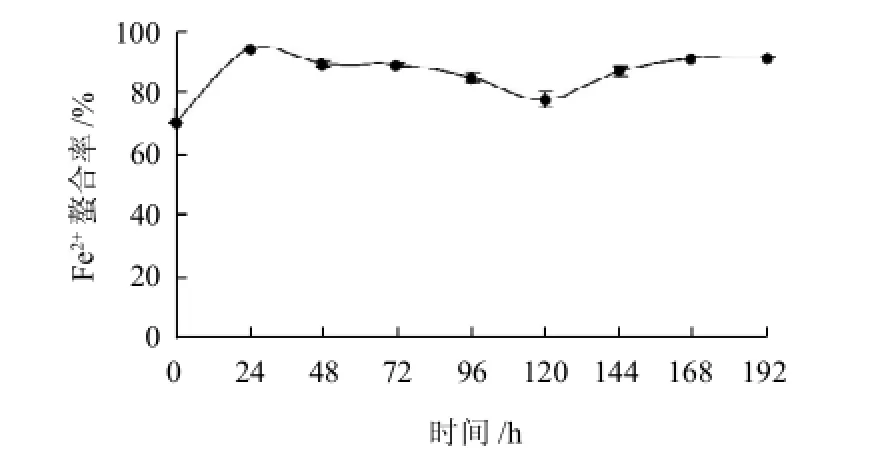
圖6 L-甘氨酸與D-木糖反應(yīng)的美拉德產(chǎn)物Fe2+螯合能力Fig.6 Ferrous ion-chelating activity of MRPs of L-glycine and D-xylose
實(shí)驗(yàn)發(fā)現(xiàn)不加熱體系產(chǎn)物(0h產(chǎn)物)的Fe2+的螯合率已高達(dá)69.6%,可能是由于甘氨酸本身具有金屬離子螯合能力的緣故。由圖6可知,在24h內(nèi)產(chǎn)物Fe2+螯合能力顯著增強(qiáng)(P<0.05),達(dá)到最大值為94.3%,隨后Fe2+螯合能力有所降低,在120h產(chǎn)物Fe2+螯合能力最弱,為77.4%。120h后產(chǎn)物Fe2+螯合能力增強(qiáng),維持在90%左右,可能是由于反應(yīng)前期具有Fe2+螯合能力的產(chǎn)物分解,螯合能力降低,120h之后,隨著最終產(chǎn)物-類黑晶的生成,F(xiàn)e2+螯合能力又重新增強(qiáng),并保持穩(wěn)定。0.4g/100mL茶多酚對(duì)Fe2+螯合率僅為10.4%,產(chǎn)物Fe2+螯合能力明顯優(yōu)于0.4g/100mL茶多酚。
2.2.2 MRPs的POV值
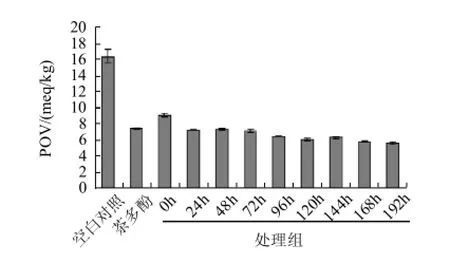
圖7 L-甘氨酸與D-木糖反應(yīng)的美拉德產(chǎn)物的POV值Fig.7 POV of MRPs of L-glycine and D-xylose
由圖7可知,CK組(空白組)POV值最高(16.37meq/kg),和其他各組差異極顯著(P<0.05),表明油脂氧化嚴(yán)重。處理組中0h的POV值最高(9.06meq/kg),但顯著低于CK組,可能是由于室溫條件下,美拉德反應(yīng)又開始進(jìn)行,生成抗氧化性物質(zhì),或者是由于甘氨酸具有一定的抗氧化性,從而抑制油脂的氧化。0h組POV值顯著高于其他各MRPs處理組(P<0.05),其他各組POV值均低于0.4g/100mL茶多酚處理組,說明MRPs抗油脂氧化能力優(yōu)于0.4g/100mL茶多酚。其中192h處理組最低(5.60meq/kg),表明192h處理組的抗油脂氧化能力最強(qiáng)。
2.2.3 MRPs對(duì)DPPH自由基的清除能力
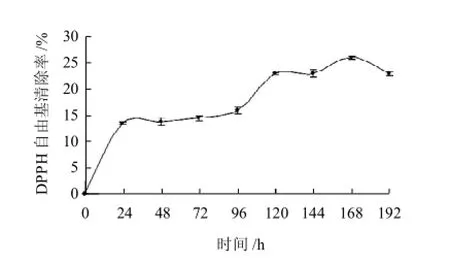
圖8 L-甘氨酸與D-木糖反應(yīng)的美拉德產(chǎn)物對(duì)DPPH自由基清除能力Fig.8 DPPH free radical scavenging activity of MRPs of L-glycine and D-xylose
由圖8可知,反應(yīng)體系產(chǎn)物對(duì)DPPH自由基的清除能力較差,最高清除率僅為25.8%,出現(xiàn)在168h,而0.4g/100mL茶多酚對(duì)DPPH自由基清除率達(dá)到91.6%,可見體系產(chǎn)物對(duì)DPPH自由基清除能力要比茶多酚差一些。實(shí)驗(yàn)結(jié)果與Cammerer等[15]認(rèn)為美拉德反應(yīng)在堿性環(huán)境中產(chǎn)物清除自由基能力強(qiáng)正好相反,產(chǎn)物對(duì)DPPH自由基清除率較低可能是由于MRPs沒有產(chǎn)生足夠的H原子或自由基中間體與DPPH形成穩(wěn)定的分子結(jié)構(gòu)。在初始24h內(nèi),產(chǎn)物DPPH自由基清除率隨反應(yīng)時(shí)間延長(zhǎng)呈線性增加。在168h達(dá)到最大值后下降,可能是抗氧化性物質(zhì)分解或生成其他物質(zhì),導(dǎo)致對(duì)DPPH自由基清除能力下降。

表2 DPPH自由基清除能力和FI、色差值參數(shù)相關(guān)系數(shù)Table2 Correlation coefficients among fluorescence intensity, color parameters and DPPH free radical scavenging activity of MRPs
由表2可知,DPPH自由基清除能力和FI、L*值、b*值存在顯著相關(guān)性。DPPH自由基清除能力和FI相關(guān)系數(shù)達(dá)到0.89070,為顯著正相關(guān)(P<0.01)。此結(jié)論與Morales等[16]研究在美拉德反應(yīng)中,其產(chǎn)物與熒光物質(zhì)有著很好的線性關(guān)系的結(jié)論一致。DPPH自由基清除能力與L*值、b*值也具有顯著負(fù)相關(guān)(P<0.01),表明隨反應(yīng)顏色的加深,自由基清除能力加強(qiáng),因此在一定程度上可以用美拉德反應(yīng)顏色的變化表征自由基的清除能力。
3 結(jié) 論
本實(shí)驗(yàn)通過甘氨酸-木糖反應(yīng)研究體系產(chǎn)物光譜特性和色差參數(shù)確定反應(yīng)終點(diǎn),為食品行業(yè)中確定美拉德反應(yīng)進(jìn)程提供一定的理論依據(jù),反應(yīng)產(chǎn)物具有很好的Fe2+螯合能力和抗油脂氧化能力,但對(duì)DPPH自由基清除能力較弱,這還需要進(jìn)一步的研究。該體系產(chǎn)物具有較好的抗氧化功能,又因?yàn)榉磻?yīng)產(chǎn)生的特征亮色色素,使得產(chǎn)物被用作食品色素及具有抗氧化能力的功能性食品添加劑成為可能。下一步工作的重點(diǎn)將主要就美拉德反應(yīng)可能產(chǎn)生的有害物質(zhì)進(jìn)行分析和檢驗(yàn),為應(yīng)用于食品行業(yè)提供一定的安全理論依據(jù)。
[1]WALLER G R, FEATHER M S. The Maillard reaction in foods and nutrition[M]. Washington D C, USA: ACS, 1983.
[2]FUJIMAKI M, NAMIKI M, KATO H. Amino-carbonyl reactions in food and biological systems[C]//Proceedings of the 3rd International Symposium on the Maillared Reaction. Amsterdam: Elsevier, 1986: 363-371.
[3]WANG Huiying, SUN Tao. Progress in research of antioxidative activity of Maillard reaction products[J]. Food Science and Technology, 2007, 8: 12-15.
[4]OSADA Y, SHIBAMOTO T. Antioxidative activity of volatile extracts from Maillard model systems[J]. Food Chemistry, 2006, 98(3): 522-528.
[5]EISSA H A, FADEL H H M, IBRAHIM G E, et al. Thiol containing compounds as controlling agents of enzymatic browning in some apple products[J]. Food Research International, 2006, 39(8): 855-863.
[6]HAYASE F, TAKAHASHI Y, TOMINAGA S, et al. Identification of blue pigment formed in a D-xylose-glycine reaction system[J]. Bioscience, Biotechnology, and Biochemistry, 1999, 63(8): 1512-1514.
[7]MURAKAMI M, SHIGEEDA A, DANJO K, et al. Radical-scavenging activity and brightly colored pigments in the early stage of the Maillard reaction[J]. Journal of Food Science, 2002, 67(1): 93-96.
[8]CHAN E W C, LIM Y Y, CHEW Y L. Antioxidant activity of Camellia sinensis leaves and tea from a lowland plantation in Malaysia[J]. Food Chemistry, 2007, 102(4): 1214-1222.
[9]中華人民共和國衛(wèi)生部. GB/T 5009.37—2003 食用植物油衛(wèi)生標(biāo)準(zhǔn)的分析方法[S]. 北京: 中國標(biāo)準(zhǔn)出版社, 2004.
[10]JING H, KITTS D D. Antioxidant activity of sugar-lysine Maillard reaction products in cell free and cell culture systems[J]. Archives of Biochemistry and Biophysics, 2004, 429(2): 154-163.
[11]SHIRAHASHI Y, WATANABE H, HAYASE F. Identification of red pigments formed in a D-xylose-glycine reaction system[J]. Biosci Biotechnol Biochem, 2009, 73(10): 2287-2292.
[12]AJANDOUZ E H, TCHIAKPE L S, ORE F D, et al. Effects of pH on caramelization and Maillard reaction kinetics in fructose-lysine model systems[J]. Journal of Food Science, 2001, 66: 926-931.
[13]SARA I F S, WIM M F, MARTINUS A J S, et al. A review of Maillard reaction in food and implications to kinetic modeling[J]. Food Science and Technology, 2000, 11(9): 364-373.
[14]BENJAKUL S, LERTITTIKUL W, BAUER F. Antioxidant activity of Maillard reaction products form a porcine plasma protein-sugar model system[J]. Food Chemistry, 2005, 93: 189-196.
[16]MORALES F J, JIMENEZ-PEREZ S. Free radical scavenging capacity of Maillard reaction products as related to colour and fluorescence[J]. Food Chemistry, 2001, 72(1): 119-125.
Spectroscopic Characteristics and Antioxidant Properties of Xyl-Gly Maillard Reaction System
YU Peng-wei,LIU Deng-yong,ZHOU Guang-hong*
(Key Laboratory of Meat Processing and Quality Control, Ministry of Education, College of Food Science and Technology, Nanjing Agricultural University, Nanjing 210095, China)
Maillard reaction products (MRPs) were prepared using xylose and glycine by model Maillard reaction. The pH value, absorbance and color parameters of the MRPs were determined. Meanwhile, the antioxidant effect was evaluated in terms of DPPH free radical scavenging activity, ferrous ion-chelating activity and lipid peroxidation inhibitory activity. The results showed that the colorless reaction system became blue and finally showed brown color as the reaction proceeded. Moreover, the pH and L* value gradually decreased. The a* value increased, while the b* value revealed an opposite change. However, the two color parameters changed little during the later part of the reaction. The MRPs exhibited good ferrous ion-chelating activity, and resulted in a lower peroxide value, but possessed weak DPPH free radical scavenging activity. In general, the products had strong antioxidant properties.
Maillard reaction;spectroscopic characteristics;antioxidant properties
TS201.2
A
1002-6630(2012)01-0054-05
2011-01-19
國際科技合作項(xiàng)目(2009DFA31770)
于彭偉(1985—),男,碩士研究生,研究方向?yàn)槿馄钒踩c質(zhì)量控制。E-mail:pengwei1985101@sina.com
*通信作者:周光宏(1960—),男,教授,博士,研究方向?yàn)槿馄房茖W(xué)與食品安全。E-mail:ghzhou@njau.edu.cn

