小劑量氫氯噻嗪腸溶片的制備及體外釋放度測定
江蘇省南通大學附屬東臺醫院(224200) 蔡偉 李健 姜曜 張美和 紀冬霞
小劑量氫氯噻嗪腸溶片的制備及體外釋放度測定
江蘇省南通大學附屬東臺醫院(224200) 蔡偉 李健 姜曜 張美和 紀冬霞
目的 制備小劑量氫氯噻嗪腸溶片,并對其體外釋放度進行測定。方法 選用適宜的輔料制備氫氯噻嗪片芯,用Ⅱ號丙烯酸樹脂為腸溶包衣材料制備腸溶片,采用紫外分光光度法測定氫氯噻嗪腸溶片的含量和釋放度。結果 在包衣增重6%,包衣轉速20~30r/min,熱處理時間為2小時時,制備的腸溶衣在鹽酸溶液中2小時不裂片不崩解,在磷酸鈉緩沖液中釋放度符合2005版中國藥典要求。結論 采用該工藝制備氫氯噻嗪腸溶片,方法可行,重現性好,制備的腸溶片在鹽酸溶液中和磷酸緩沖液中的釋放度符合2005版中國藥典標準。
氫氯噻嗪 腸溶片 釋放度
氫氯噻嗪為中效排鈉利尿劑,用于治療原發性高血壓已有40余年的歷史[1],具有作用溫和、無耐藥性、毒副反應小及加強其它降壓藥物降壓效果等優點[2]。主要不良反應包括:低鉀血癥,干擾腎小管尿酸排泄,糖耐量降低、血糖、尿糖升高,脂代謝紊亂等,而這些不良反應大多數與劑量有關[3]。有研究表明,小劑量與大劑量氫氯噻嗪相比,有同樣的降壓效果,都能降低總的心腦血管事件和總病死率,但只有小劑量氫氯噻嗪能降低冠脈事件的發生[4-6]。因此,國內外高血壓防治指南多推薦使用小劑量噻嗪類利尿劑[7]。為滿足患者的需求,國內已有制成25mg的氫氯噻嗪緩釋片、氫氯噻嗪-β-環糊精包合物、氫氯噻嗪分散片等報道。本研究結合臨床診療指南,考慮到氫氯噻嗪片水溶性差、味微苦、對胃腸道有刺激作用以及穩定性差等問題,研制規格為每片12.5mg的氫氯噻嗪腸溶片。
1 儀器與試藥
1.1 儀器 ZPS8型旋轉式壓片機(上海天祥健臺制藥機械有限公司),DBL-3多功能制粒包衣機(重慶廣廈干燥設備工程公司),RCZ-6B型溶出度儀(上海黃海藥檢儀器廠),UV-2401型紫外分光光度計(日本島津)。
1.2 試藥 氫氯噻嗪對照品(中國藥品生物制品檢定所,批號:100309-200910),氫氯噻嗪(常州制藥廠有限公司,批號:091009,純度:99.98%),交聯聚維酮(PVPP)、低取代羥丙纖維素(LHPC)、交聯羧甲基纖維素鈉(CCNa)、微晶纖維素(湖洲展望藥業有限公司),丙烯酸II號樹脂(上海運宏化工制劑輔料技術有限公司),硬脂酸鎂(上海元越化工有限公司),羥丙甲基纖維素(上海試劑分裝站),聚維酮(PVP)、滑石粉(廣西龍勝華美滑石粉開發有限公司)。
2 氫氯噻嗪腸溶片的制備
2.1 片芯的制備
2.1.1 崩解劑的選擇 根據崩解劑吸水后的溶脹性能指標(即膨潤度)進行選擇,選取PVPP、CCNa、LHPC3種常用崩解劑,通過測定其膨潤度來考察吸水后的溶脹性能。稱取適量崩解劑,置量筒中,振搖平整,讀取體積,然后加適量水于量筒中,攪勻,常溫下擺放24小時后,讀取膨脹后的水合體積。水合體積與干燥的崩解劑體積之比即為膨潤度。試驗結果見表1。

表1 不同崩解劑的膨潤度
由實驗結果得知,PVPR的膨潤度最大,說明其膨脹能力在3種崩解劑中最強,因此選擇其為片芯的崩解劑。
2.1.2 崩解劑用量的確定 制備含崩解劑PVPR分別為1%、2%、3%、5%的片芯,再包腸溶衣,測定腸溶片的釋放度,結果見圖1。由圖1可見,崩解劑為1%、2%時,主藥釋放慢,45分鐘時藥物的釋放度不符合藥典標準,崩解劑在3%以上時,釋放度均大于標示量的70%。故崩解劑的用量為3%。

圖1 崩解劑劑量對藥物釋放的影響
2.1.3 填充劑的選擇 各種填充劑對片芯崩解時間的影響是:微晶纖維素崩解時間為139.6秒,硫酸鈣平均崩解時間為196.4秒,糊精平均崩解時間為223.5秒。提示微晶纖維素在稀堿中溶解并溶脹,具有良好的流動性和可壓性,崩解時間較短,藥物易于分散,故選擇微晶纖維素作為填充劑。
2.1.4 粘合劑的選擇 分別以羥丙甲纖維素(HPMC)、PVP為粘合劑制備片芯,考察兩者的崩解時間,結果平均崩解時間為115.6秒,PVP平均崩解時間為135.7秒。再分別考察腸溶片的釋放度。結果顯示,以HPMC為粘合劑的片芯崩解快,腸溶片釋放度比以PVP為粘合劑的腸溶片釋放度高。所以確定以HPMC為粘合劑。
2.1.5 片芯的制備 根據最終處方,片芯的規格為100mg,將處方量氫氯噻嗪、PVPP、微晶纖維素、HPMC過100目篩3次,攪拌均勻,PVP為粘合劑,用濕法制顆粒,再過16目篩制粒,于55℃處干燥,過18目篩整粒,加適量硬脂酸鎂混勻,選用沖頭直徑6mm,硬度70N,壓制成片芯。
2.2 腸溶片的制備
2.2.1 選擇與配制包衣材料 片芯包腸溶衣,包衣材料選用Ⅱ號丙烯酸樹脂,PEG-6000為增塑劑,滑石粉為抗粘劑。將Ⅱ號丙烯酸樹脂用85%乙醇溶解制成5%樹脂溶液,將滑石粉和苯二甲酸二乙脂、聚山梨醇等混勻、研磨加入Ⅱ號丙烯酸樹脂溶液中,加入色素混勻后,慢速攪拌20分鐘,用120目篩濾過除去顆粒,得到包衣液。
2.2.2 包衣增重 根據輔料性能和腸溶片劑型的要求,在片芯表面上應覆蓋一定厚度的腸溶包衣,才能抵御較長時間胃酸(0.1mol/L)的侵蝕。制備包衣增重分別為2%、4%、6%、8%時,考察制劑的釋放度,其結果見圖2。
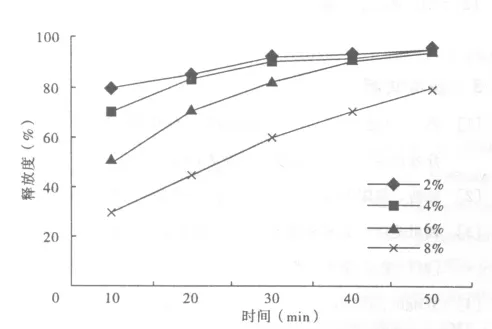
圖2 不同包衣增重對藥物釋放的影響
實驗結果分析表明,包衣增重為2%、4%時,有部分片劑在人工胃液中產生裂片,不能達到腸溶片的要求。包衣增重為8%時,片劑在人工胃液中崩解時間過長,釋放度減小。最后本實驗選取包衣增重為6%。
2.2.3 包衣鍋轉速 考察包衣鍋轉速分別為10r/min、20r/min、30r/min、40r/min時制成的藥物的釋放度。當包衣鍋轉數為10r/min時,片芯無法正常滾動,影響包衣效果。當轉速為20~30r/min時,腸溶片的釋放度符合藥典要求。
2.2.4 片劑烘干時間 將同一批次的片劑包腸溶衣后,分別放入烘箱中2小時、4小時、6小時,讓包衣材料形成致密的衣膜。考察在不同烘干時間下腸溶片的釋放度。結果提示,烘干處理2小時已能形成致密的薄膜衣,達到腸溶的要求,所以最后的烘干時間為2小時。
2.2.5 包衣程序 將片芯放置于包衣鍋內旋轉,包衣過程中持續吹入熱空氣,片芯預熱,包衣液進入噴槍,均勻噴曬向包衣鍋內。噴霧速率1mL/min;霧化壓力0.2MPa;包衣鍋轉數20-30r/min;包衣溫度35℃左右;包衣增重6%;包衣結束后放置于35℃左右的烘箱中烘干2小時即得。
2.2.6 批間重現性 以最終工藝和處方連續制備3批樣品,進行體外釋放度測定,考察批間重現性。結果:制備的腸溶片在人工胃液中2小時無裂片或崩解,檢測出氫氯噻嗪含量均<標示量的10%;在磷酸鹽緩沖液中(人工腸液)釋放度均>70%,符合2005版藥典要求,批間重現性好。
3 含量測定與體外釋放度測定
3.1 含量測定
3.1.1 測定波長的選擇 分別將氫氯噻嗪、氫氯噻嗪腸溶片和輔料制作成溶液,濾過。在200~400nm波長范圍內進行紫外線掃描,主藥在波長273m處有最大吸收,而輔料在此波長基本無吸收,故選擇273nm為測定波長。
3.1.2 標準曲線的繪制 精密稱取氫氯噻嗪12.5mg溶于100mL的容量瓶中,加稀鹽酸定容。分別量取1.0mL、2.0mL、4.0mL、6.0mL、8.0mL、10.0mL置于10mL容量瓶中,用稀鹽酸稀釋至刻度,在波長273nm處測定吸收度。以吸收度(A)對藥物濃度(C)進行回歸分析,得到方程A=0.0630C+0.0047。氫氯噻嗪檢測線性范圍為100~400μg/mL(r=0.999,n=6)。
3.1.3 精密度試驗 按線性范圍內分別配制高、中、低3種濃度的氫氯噻嗪溶液,按上述方法測定吸收度,計算實際濃度。同日內測定日間精密度(RSD),再連續3日分別測定RSD。結果日內RSD=0.41%(n=3),日間RSD=0.65(n=3)。
3.1.4 加樣回收率試驗 分別配制高、中、低3種濃度氫氯噻嗪溶液,加入適量的輔料,測定吸收度,求加樣回收率。結果平均回收率為100.18%,RSD=0.62%(n=3)。
3.1.5 氫氯噻嗪腸溶片含量測定 取20片本品,除去包衣層,研細。精密稱取適量(約相當于氫氯噻嗪12.5mg)置100mL量瓶中,加鹽酸溶液(24→1000)適量,使溶解、濾過,精密量取濾液5mL,置另一100mL量瓶中,用鹽酸溶液稀釋至刻度,搖勻,在273nm波長處進行紫外線掃描,測定吸光度。計算含量。
3.2 釋放度測定
3.2.1 鹽酸中釋放量 量取0.1mol/L 鹽酸溶液750mL,注入每個溶出杯,加溫使溶液溫度保持在(37±5)℃,調整轉速為100r/min并保持穩定,取6片12.5mg氫氯噻嗪腸溶片投入轉籃中,開動儀器運轉2小時,立即在取樣點吸取適量溶液,并在30秒內經0.8um的微孔濾膜濾過,濾液按含量測定的方法進行測定,計算每片在鹽酸中的釋放量。
3.2.2 緩沖液中釋放量 在溶出杯中加入0.2mol/L磷酸鈉溶液250mL(必要時用2mol/L鹽酸溶液或氫氧化鈉溶液調節pH值至6.8±0.05),轉速溫度不變,依法操作,分別于10分鐘、20分鐘、30分鐘、45分鐘、60分鐘時,取液濾過,并補加相同體積的緩沖液。濾液按含量測定的方法進行測定,計算每片在緩沖液中的累積釋放量。
4 結論與討論
經多次實驗驗證,12.5mg的氫氯噻嗪腸溶片在0.1mol/L鹽酸溶液中2小時不崩解,在0.2mol/L磷酸鈉溶液中每片的釋放量均大于標示量的70%。
采用紫外分光光度法測定氫氯噻嗪的釋放度和含量,操作簡便,結果準確,可用于氫氯噻嗪腸溶片的質量控制。
目前臨床上常用的氫氯噻嗪都是普通片劑,且規格是10mg、25mg、50mg[8],在治療原發性高血壓時,指南均推薦小劑量12.5mg。氫氯噻嗪與血管緊張素轉換酶抑制劑(ACEI)、ARBEH、β受體阻滯劑、鈣通道阻滯劑(CCB)聯合用藥時,也推薦小劑量[9]。患者服用10mg的氫氯噻嗪,劑量偏小,不符合治療指南的要求,而服用12.5mg時需要將25mg的片劑掰開,易導致服用劑量不準確和服用依從性不高。小劑量腸溶片具有良好的療效和性價比,為滿足患者的需求,應盡快研制出規格為每片12.5mg的氫氯噻嗪腸溶片。
[1]蔡偉,李健,姜曜,等 .不同劑量氫氯噻嗪治療原發性高血壓的療效觀察[J].中國醫院藥學雜志,2011,2:57
[2]徐浩 .臨床用藥須知[M].天津:天津電子出版社,2005:950
[3]四川美康醫藥軟件研究開發有限公司 .藥物臨床信息參考[M].重慶:重慶出版社,2008,1035
[4]Wright JM.Choosing a first-line drug in the management of elevated blood preasure:what is the evidence?1:Thiazide[M].CMAJ,2000,163:57
[5]Wright JM,Lee CH,Chambers GK.Systematic review of antihypertensive therapics:does the evidence assist in choosing a first-line drug[J].CMAJ,1999,161:25
[6]Weir MR,Flack JM,applegate WB.Tolerablility,safety,and quality of life and hypertensive therapy:the case for low-dose diuretics[J].Am Jmed.1996,101:83
[7]王文 .中國高血壓防治指南(2009 年 基 層 版).http://www.365heart.com
[8]中國藥典 .二部[S].2005,407
[9]中華醫學會心血管病學分會高血壓學組 .利尿劑治療高血壓的中國專家共識[J].中華高血壓雜志,2011,03:217
The preparation and the release in vitro determination of small dosage of hydrochlorothiazide entericcoated tablets
Cai Wei,Li Jian,Jiang Yao,et al.The Dongtai Hospital of Nantong University,Dongtai,224200,China.
Objective Manufacturing small dosage of hydrochlorothiazide enteric-coated tablets and determining its release in vitro.Method Choosing condign accessories to manufacture hydrochlorothiazide tablets,and selecting the model No.II acrylic acid polymers as enteric-coating material to produce enteric-coated tablets,and then,mensurating the contains and the release rate of hydrochlorothiazide enteric-coated tablets with the uv-speetrophotometric method.Result The manufactured enteric-coated tablets,when its coating gains 6%weight and has the rotational speed between 20and 30r/min,and the heat-treatment time reaches 2h,don't split and collapse in the hydrochloric acid solution,furthermore,its release rate in the sodium diphosphate solution meets the standard of the chinese pharmacopoeia 2005edition.Conclusion This technics,introduced to produce the hydrochlorothiazide enteric-coated tablets,is practical and has great reproducibility,moreover,when the produced enteric-coated tablets are put in the hydrochloric acid solution or sodium diphosphate solution,its release rate is up to the standard of the chinese pharmacopoeia 2005edition.
hydrochlorothiazide enteric-coated tablet release rate
(本文編輯 劉社民)
2010年鹽城市醫學科技科研課題項目:編號YK2010042

