新型水溶性大環席夫堿錳(Ⅱ)配合物的合成及其模擬超氧化物歧化酶的活性研究*
袁澤利,吳 慶,楊興變,胡慶紅,鐘永科,周旭美,張銘欽
(遵義醫學院 藥學院,貴州 遵義 563003)
錳的配位化學由于其生物功能,而愈來愈引起人們的廣泛興趣。在某些生物酶中,錳的配位環境多為咪唑的氮和羧基及水分子的氧原子配位[1,2]。在模型配合物的研究方面,由于席夫堿配體具有與生物體系有關的N,O給體,且配位環境可調,與生物體環境比較接近,這激發了人們對該類化合物在生物生理功能作用機制及其模型配合物研究的興趣。
超氧化物歧化酶(SOD)是一類氧化還原酶,在防止有氧生物免受氧化性損傷中具有重要的作用[3]。市售的SOD系從動物血液中提取,存在操作煩瑣、價格昂貴、在體內壽命短及分子量較大不能透過細胞膜等缺點,限制了其在臨床中的應用。為此,研究者們致力于用化學方法合成模擬SOD。然而,已有模擬配合物的SOD活性不甚理想。可能是由于人工合成的模擬SOD的水溶性差使其在生理條件下的活性受到影響,妨礙了在醫藥方面的應用。因此寄希望于合成出水溶性的模擬SOD以開發實際應用價值。目前,有關開鏈水溶性席夫堿錳配合物的研究取得了一些進展[4,5],而有關水溶性大環席夫堿配體及其錳配合物卻鮮見文獻報道。
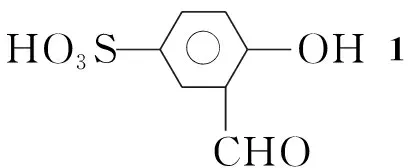
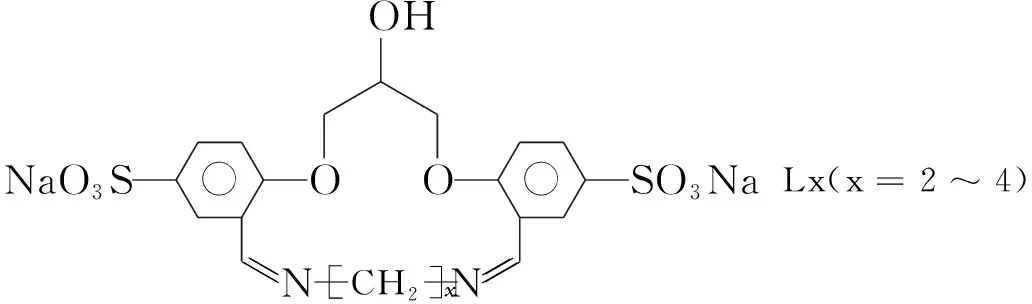
Scheme1
1 實驗部分
1.1 儀器與試劑
WRS-2A型數字熔點儀(溫度未校正);TU-1901型雙光束紫外可見分光光度計;BrukerAV-500型核磁共振儀(D2O為溶劑,TMS為內標);Varian 1000 FT-IR型紅外光譜儀(KBr壓片);MS HP-1100型質譜儀;Vario ELⅢ型元素分析儀;SG 7200 HPT型超聲振蕩儀。
1按文獻[10]方法制備;乙二胺,1,3-丙二胺,1,4-丁二胺,水楊醛,化學純;其余所用試劑和溶劑均為分析純;實驗用水為二次蒸餾水。
1.2 合成
(1)2的合成
在三口瓶中依次加入Na2CO323.32 g,1 4.02 g(20 mmol)的50%乙醇(100 mL)溶液,于50 ℃超聲振蕩使其完全溶解;于30 min內緩慢滴加1,3-二氯-2-丙醇1.28 g(10 mmol)的50%乙醇(20 mL)溶液,滴畢,超聲振蕩60 min。冷卻至室溫,抽濾,濾餅依次用水、稀鹽酸洗滌數次,用50%無水乙醇重結晶,真空干燥得白色長方型晶體2 4.26 g,收率84.6 %, m.p.98 ℃~101 ℃;1H NMRδ: 10.18(s, 2H, CHO), 8.07(s, 1H, OH), 7.91~6.95(m, 6H, ArH), 4.62(m, 1H, CHOH), 4.37(s, 4H, CH2); IRν: 3 452, 2 758, 1 675, 1 248, 1 010, 1 245, 1 045 cm-1; Anal.calcd for C17H16O11S2: C 44.35, H 3.50; found C 44.42, H 3.63。
(2) Lx的合成(以L2的合成為例)
將2 0.94 g(2 mmol)溶于75%乙醇(100 mL)中,攪拌下加熱至回流;于1 h內緩慢滴加乙二胺0.12 g(2 mmol)的乙醇(20 mL)溶液,滴畢,回流反應5 h。旋蒸至溶液體積約20 mL,冷卻后置冰箱中過夜,抽濾,濾餅真空干燥得微黃色固體粉末L2。
分別以1,3-丙二胺和1,4-丁二胺代替乙二胺,用類似方法合成微黃色固體L3和黃色固體L4。
L2: 產率41.31%,m.p.138 ℃~140 ℃; UV-Visλmax: 310, 245 nm;1H NMRδ: 9.58(s, 2H, CH=N), 8.41(s, 1H, OH), 7.60~6.44(m, 6H, ArH), 4.78(m, 1H, CHOH), 4.50(s, 4H, OCH2), 4.02(s, 4H, NCH2); IRν: 3 438, 1 637, 1 498, 1 400, 1 238, 1 112 cm-1; MSm/z: 480(M+-4); Anal.calcd for C19H20O9S2: C 47.10, H 4.16, N 5.78; found C 47.28, H 4.03, N 5.88。
L3: 產率38.51%,m.p.115 ℃~118 ℃; UV-Visλmax: 309, 250 nm;1H NMRδ: 9.45(s, 2H, CH=N), 8.39(s, 1H, OH), 7.75~6.62(m, 6H, ArH), 4.75(m, 1H, CHOH), 4.65(s, 4H, OCH2), 4.02(s, 4H, NCH2), 2.11(m, 2H, CH2); IRν: 3 495, 1 641, 1 510, 1 400, 1 240, 1 005, 1 120 cm-1; MSm/z: 497(M++1); Anal.calcd for C20H22O9S2: C 48.18, H 4.45, N 5.62; found C 48.29, H 4.39, N 5.48。
L4: 產率27.06%,m.p.109 ℃~111 ℃; UV-Visλmax: 310, 252 nm;1H NMRδ: 9.40(s, 2H, CH=N), 8.28(s, 1H, OH), 7.78~6.45(m, 6H, ArH), 4.81(m, 1H, CHOH), 4.72(s, 4H, OCH2), 4.28(s, 4H, NCH2), 2.05~1.98(m, 4H, CH2); IRν: 3 505, 1 640, 1 448, 1 402, 1 246, 1 110 cm-1; MSm/z: 511(M+-1); Anal.calcd for C21H24O9S2: C 49.21, H 4.72, N 5.47; found C 49.46, H 4.28, N 5.37。
(3) MnLx的合成(以MnL2的合成為例)
將NaOH 0.16 g(4 mmol)和L2 0.97 g(2 mmol)溶于50%乙醇(25 mL)中,攪拌下緩慢滴加醋酸錳0.49 g(2 mmol)的乙醇(25 mL)溶液,滴畢,回流反應2 h。冷卻后置冰箱中過夜,過濾,濾餅依次用少量冰無水乙醇、冰水洗滌,真空干燥得棕色粉末MnL2。
用類似方法合成棕色粉末MnL3和MnL4。
MnL2: 產率66.48%,m.p.>300 ℃; UV-Visλmax: 325, 251 nm; IRν: 3 550, 3 406, 1 620, 1 458, 1 384, 1 245, 1 115, 496, 424 cm-1; MSm/z: 642(M++1-H2O-OAc-); Anal.calcd for C23H24O13S2Na2Mn·H2O: C 38.39, H 3.64, N 3.89, Na 6.39; found C 38.28, H 3.53, N 3.88, Na 6.51。
MnL3: 產率68.12%,m.p.>300 ℃; UV-Visλmax: 330, 248 nm; IRν: 3 560, 3 416, 1 615, 1 452, 1 383, 1 252, 1 120 , 478, 430 cm-1; MSm/z: 714(M+-1-2H2O); Anal.calcd for C24H26O13S2Na2Mn·2H2O: C 38.36, H 4.02, N 3.73, Na 6.12; found C 38.16, H 3.97, N 3.78, Na 6.07。
MnL4: 產率52.76%,m.p.>300 ℃; UV-Visλmax: 328, 250 nm; IRν: 3 557, 3 420, 1 610, 1 452, 1 388, 1 260, 1 130, 498, 427 cm-1.MSm/z: 671(M++1-2H2O-OAc-); Anal.calcd for C25H28O13S2Na2Mn·2H2O: C 39.22, H 4.21, N 3.66, Na 6.01; found C 38.28, H 4.33, N 3.61, Na 6.13。
2 結果與討論
2.1 配體及配合物的表征
實驗結果表明,合成的配體及其錳配合物均具有良好的水溶性。配合物中鈉的含量用醋酸鈾酰鋅測得,其實驗值與計算值吻合較好。
1H NMR分析表明,9.40~9.58處的吸收峰分別對應于配體CH=N質子特征峰;6.44~7.78附近為芳香質子吸收峰;8.28~8.41處對應于柔性鏈中OH質子吸收峰;與該羥基相聯的CH在4.75~5.23;而4.50~4.72為NCH2質子吸收峰;4.02~4.18為OCH2質子吸收峰;在1.98~2.11為L3,L4烷基二胺的CH2質子吸收峰。
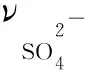
配體及配合物在雙蒸餾水中的UV-Vis數據測定表明,它們的光譜圖相似,都有兩個相似的吸收帶,即在250 nm附近吸收峰屬于苯環的π-π*躍遷吸收,而在配體中的310 nm吸收峰屬于分子中C=N雙鍵的π-π*躍遷吸,在形成配合物該吸收峰均發生了一定程度的紅移,進一步證明配體與金屬離子存在了配位作用[6]。
MS分析表明,配體均觀察到相應的分子離子峰,而在形成配合物后觀察到其失去結晶水和一定的配位OAc-碎片峰;元素分析的實測值與理論值基本相符。這些數據進一步證明了合成得到的化合物為預期目標分子結構。
2.2 配合物對的清除作用
席夫堿型模擬SOD的活性測定多以DMF,DMSO等為溶劑[13,14]。本文合成的以磺酸修飾的SOD模型配合物可溶于水,且在水中具有良好的溶解度,故采用雙蒸水為溶劑測定其活性。
采用鄰苯三酚自氧化法[13]測定了MnLx的歧化超氧陰離子活性,以探索用人工合成的化合物代替SOD用于臨床治療的可能性,并與文獻[14]中SOD作對照。
以抑制率[η=(1-νt/ν0)×l00%]對濃度(c)作圖得標準曲線。在標準曲線上即可找到IC50值(表1)。
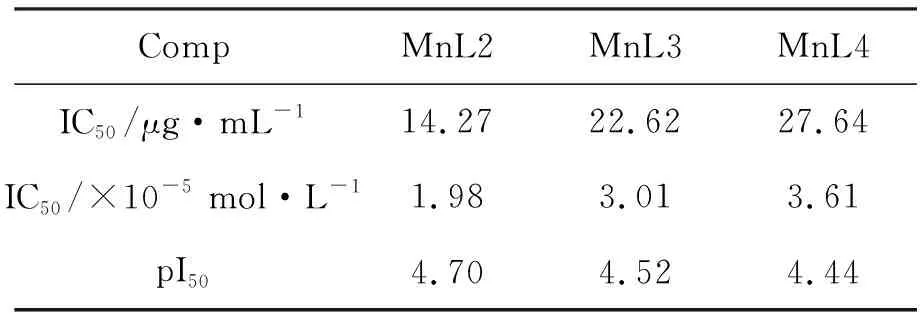
表1配合物的IC50值和pI50值*
*pI50=-lgIC50
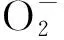
[1] Najafpour M M.A possible evolutionary origin for the Mn4 clusterin photosystem Ⅱ:From manganese superoxide dismutase to oxygen evolving complex[J].Origins Life Evol Biosphere,2009,39(2):151-163.
[2] Gohdes J W, Armstrong W H.Synthesis,structure,and properties of [Mn(salpn)(EtOH)2](ClO4) and its aerobic oxidation product [Mn(salpn)O]2[J].Inorg Chem,1992,31(3):368-373.
[3] 王建華,雷文,王遠亮.SOD酶模型配合物的合成及催化歧化作用——1,3,4-噻二唑類希夫堿配合物的合成、表征及對超氧離子的抑制作用[J].合成化學,2002,10(4):314-317.
[4] 石先瑩,魏俊發術,高中強,等.水溶性席夫堿型錳配合物的合成、表征及其模擬超氧化物歧化酶活性研究[J].有機化學,2007,27(8):1027-1030.
[5] 朱必學,阮文娟,高峰,等.水溶性手性Salen Mn(Ⅲ)的光譜性質及其對氨基酸客體的分子識別研究[J].化學學報,2004,62(1):58-65.
[6] Ze-Li Yuan, Qi-Long Zhang, Bi-Xue Zhu.A new series of dinucleating macrocyclic ligands and their complexes of zinc(Ⅱ)[J].Polyhedron,2008,27(1):344-348.
[7] 袁澤利,胡慶紅,吳慶,等.新型大環席夫堿化合物的合成及其抗菌活性研究[J].有機化學,2009,29(2):279-282.
[8] 袁澤利,吳慶,楊興變,等.含雙酰腙類新型席夫堿大環化合物的合成與表征[J].化學世界,2010,51(5):289-291.
[9] 吳慶,袁澤利,徐遠飛,等.新型含硫雜環席夫堿型大環化合物的合成及其殺菌活性[J].合成化學,2010,18(5):608-610.
[10] 吳雪梅,董健媛等.磺化水楊醛縮苯胺含Cu配合物的合成表征及催化性質研究[J].化學世界,2007,48(8):456-459.
[11] 張生萬,張有賢,曹曉峰,等.新試劑1-羥基-2-(6-溴-2-苯并噻唑偶氮)-8-氨基-3,6-萘二磺酸的合成及性能的研究[J].化學試劑,1993,15(4):205-210.
[12] Wang R M,Feng H X,He Y E,etal.Preparation and catalysis of NaY-encapsulated Mn(Ⅲ) schiff-base complex in presence of molecular oxygen[J].J Mol Catal A,2000,151(1):253-259.
[13] 吳慶,江艷,袁澤利,等.新型雙核Cu(Ⅱ)席夫堿化合物的合成及其模擬超氧化物歧化酶活性研究[J].數理醫藥學雜志,2009,22(5):578-580.
[14] 吳輝祿,高憶慈.超氧化物歧化酶模型化合物的合成、表征及其SOD活性研究[J].化學通報,2002,66(11):770-774.

