高砷難處理金精礦細菌氧化-氰化提金
楊 瑋, 覃文慶, 劉瑞強, 任允超
(1. 中南大學 資源加工與生物工程學院,長沙 410083;2. 山東黃金礦業(萊州)有限公司精煉廠,萊州 261441;3. 山東黃金集團煙臺設計研究工程有限公司,煙臺 264006)
高砷難處理金精礦細菌氧化-氰化提金
楊 瑋1, 覃文慶1, 劉瑞強2, 任允超3
(1. 中南大學 資源加工與生物工程學院,長沙 410083;2. 山東黃金礦業(萊州)有限公司精煉廠,萊州 261441;3. 山東黃金集團煙臺設計研究工程有限公司,煙臺 264006)
通過在高砷金精礦中配入不同比例的低砷碳酸鹽型金精礦,使其所含硫、砷及鐵等主要礦物成分含量發生變化,研究給礦中鐵砷摩爾比對難處理高砷金精礦細菌氧化-氰化浸出效果的影響。結果表明:含砷金精礦中鐵砷摩爾比直接影響細菌預氧化的效果,同時也影響細菌的活性和溶液中鐵砷摩爾比的變化,給礦中鐵砷摩爾比越高,溶液中的鐵砷摩爾比也越高,且隨著給礦中鐵砷摩爾比的增加,溶液中鐵砷摩爾比的變化幅度加大,給礦中鐵砷摩爾比介于4.6~5.2之間,有利于細菌預氧化和氰化浸出,鐵、砷氧化率分別由6.14%和7.38%提高到89.90%和93.60%,金、銀浸出率分別由64.18%和35.93%提高到97.78%和88.83%,較好地改善細菌氧化效果,穩定和優化細菌預氧化過程。
高砷難處理金精礦;細菌氧化;氰化提金
隨著易處理黃金資源的日漸枯竭,難處理含金礦石成重要的可用資源,其處理技術也成為我國黃金生產發展的瓶頸。大多數礦石之所以難處理是因為金呈細粒或微細粒被包裹在硫化物中,在氰化過程中不能與氰化物接觸[1]。高砷金礦是公認的難處理礦石,其中金絕大部分包裹在黃鐵礦和毒砂中,難以與氰化物直接接觸[2], 直接氰化的回收率低。 在我國,難選冶含砷金礦占相當大的比例,砷為氰化浸金的主要干擾元素之一,金礦石中砷的原生礦物是毒砂,而大多數難浸金精礦中的主要砷礦物也是毒砂[3]。這類金精礦采用機械磨礦等普通方法很難使金顆粒解離,因此,在浸金前必須進行預處理,目前預處理的方法主要有培燒、加壓氧化和細菌氧化3大技術。細菌氧化預處理技術因具有成本低、能耗小、污染少且設備簡單易于操作等特點而更具有競爭力[4-7],越來越受到人們的關注。
生物提金工藝利用氧化亞鐵硫桿菌,氧化黃鐵礦和毒砂等金屬礦物,使被礦物包裹的金顆粒裸露,能充分與浸金溶劑接觸而有利于浸出,可使金的回收率大幅提高,但影響生物提金的因素很多,歸結起來主要有 3類:生物因素、礦物因素和工藝因素[8]。在礦物因素中,礦物含砷量的大小直接影響細菌氧化的效果(目前金精礦含砷的高低并沒有統一劃分標準,本文作者結合國內外主要金精礦的細菌氧化處理廠生產實際,界定含砷量在8%以上的為高砷金精礦),對于含砷量高的原料,細菌氧化也有其局限性,因此,有關學者針對高砷金精礦的細菌氧化-氰化提金開展大量的研究工作,包括浸礦機理、菌種篩選馴化、核心反應器及工藝條件等方面。如金世斌等[9]對金精礦生物氧化過程中砷的氧化行為研究后指出,生物氧化過程中毒砂中砷主要被 Fe3+氧化,是間接作用的生物氧化過程,氧化液中As3+含量與試樣的砷含量有關;楊洪英等[10-11]研究氧化亞鐵硫桿菌 SH-2T氧化毒砂的機理,并采用HQ20211嗜熱菌對含砷11.78%金精礦的氧化預處理, 金的回收率大大提高;羅志雄等[12]對中度嗜熱嗜酸鐵氧化菌 MLY和嗜酸氧化亞鐵硫桿菌(Acidthiobacillus ferrooxidans,At.f ) 氧化處理含砷金精礦的機理及浸礦效果進行了研究;戴紅光[13]研究用中溫菌預氧化-氰化浸出湖北某難浸高砷高硫金精礦;柳建設等[14]設計了實驗室規模的氣升式生物反應器,用于高砷難處理金精礦的細菌氧化預處理;崔日成等[15]研究了pH 值對浸礦細菌的活化以及金精礦脫砷的影響;佟琳琳等[16]通過不同礦漿濃度的細菌氧化預處理實驗, 發現含砷金精礦細菌氧化渣的金浸出率隨著礦漿濃度的增大而降低;李萬全等[17]和李育林等[18]研究了含砷難處理金精礦在不同磨礦細度、細菌接種量、氧化時間、氧化溫度及通氣量工藝條件下的預氧化效果,但目前尚未見通過改變給料中各種礦物成分的配比來提高難處理高砷金精礦細菌氧化-氰化浸出效果的系統研究。本文作者根據原料中硫、砷及鐵等主要成分和黃鐵礦及毒砂等主要礦物的不同,考察給礦及溶液中的砷鐵摩爾比對河北某高砷金精礦的細菌預氧化及氰化浸出過程的影響,為指導生產實踐提供操作依據。
1 實驗
1.1 礦樣
試驗用礦樣取自河北某高砷礦,該礦石中金屬礦物主要為黃鐵礦、毒砂、方鉛礦、磁黃鐵礦及少量的黃銅礦、閃鋅礦、黑鎢礦、輝銻礦等。脈石礦物主要為石英,其次為綠泥石、斜長石、云母、方解石和磷灰石等。主要載金礦物為黃鐵礦、毒砂和石英,金粒的嵌存狀態主要為賦存于黃鐵礦及石英中的包裹金和賦存于黃鐵礦、毒礦及石英的晶隙間的晶隙金,且多與毒砂連生。礦樣的主要元素化學成分分析結果如表1所列。從化學分析可以看出,該礦砷、鐵、硫的含量比較高,占87.31%,其中硫化物含量近30%,屬于典型的高砷高硫金精礦。

表1 高砷金精礦化學成分分析Table 1 Chemical composition in high arsenic gold concentrate (mass fraction, %)
1.2 菌種
試驗用菌種TCJ采自山東某黃金冶煉企業,該組合菌種開始最高耐砷濃度為12 g/L,在生產中要求進料礦漿濃度為 20%,含砷最好不超過 6%,經過企業幾年來的運行及馴化,該菌種的耐砷能力可以達到15 g/L。
1.3 試驗方法
細菌氧化試驗在5 L攪拌氧化槽中進行,采用萊寧A1000攪拌槳,通過DRZ-5型實驗室細菌氧化反應罐夾套加熱溫度控制器進行溫度控制,通過ZW-0.6/7立式空氣壓縮機、2 M氣瓶、自力式壓力調節閥和 LZB-10型玻璃轉子流量計進行充其量的控制。
細菌氧化試驗基本條件如下:磨礦細度小于 38 μm占86%,礦漿濃度為10% ,溫度為40 ℃,充氣量為0.4 m3/h,攪拌速度為900 r/min,用濃硫酸調礦漿pH值為2.0,當pH值穩定后加入營養物和接種物,接種物取自現場氧化槽溢流礦漿靜置后的固體沉淀物,加入量為50 g,營養物加入量為硫酸銨2 g、磷酸氫二鉀1 g、硫酸鎂1 g。
試驗中用上海精科雷磁儀器廠生產的 pHB-4型便攜式酸度計測量浸出體系的pH 值,用甘汞參比電極和金屬鉑電極測定浸出體系的氧化還原電位,浸出液中總鐵的濃度用原子吸收光譜測定,Fe2+濃度用重鉻酸鉀滴定法測定,采用次亞磷酸鹽滴定法測定液砷濃度。
氰化浸出試驗在XTD-5L型攪拌浸出槽中進行,試驗基本條件如下:浸出礦漿濃度為40%,氰化鈉濃度為0.7%,浸出pH值在11.5以上,浸出時間為48 h。
2 實驗結果
2.1 高砷礦直接氰化與細菌氧化試驗
2.1.1 高砷礦直接氰化試驗
為了考察該高砷金精礦的浸出性能,對其在磨礦細度為粒度小于 38 μm 的占 86%時進行直接氰化試驗,試驗結果如表2所列。
由表2可以看出,粒度小于39 μm的金有一半被氰化鈉直接浸出來,而且氰化鈉和石灰的消耗量較小,但是直接氰化浸出48 h,金浸出率僅為58.96%,銀的浸出率為35.63%,屬于典型的高硫高砷難浸礦石。

表2 高砷礦直接氰化浸出結果Table 2 Results of ore with high arsenic content by direct cyanide leaching
2.2 高砷礦細菌氧化-氰化浸出試驗
對此高砷礦直接氰化回收率太低,因此,對其進行預氧化,氧化渣再進行氰化浸出,判斷是否可以提高金銀浸出率。礦樣細菌氧化過程中氧化還原電位、pH值、液體中鐵、砷濃度及鐵、砷氧化率隨時間變化的曲線如圖1和2所示。
由圖1可知,此高砷礦的細菌氧化過程中,經過312 h氧化,礦漿氧化還原電位由290 mV上升到368 mV,上升得非常緩慢,而且pH值幾乎也沒變化。圖2所示為高砷礦液體中鐵砷濃度及氧化率變化曲線。由圖2可知,礦漿中液體鐵由最初的558 mg/L上升為2 158 mg/L,鐵的氧化率僅為6.14%;液體砷由最初的188.41 mg/L上升為1 627 mg/L,砷的氧化率為7.38%,說明在這段時間內礦樣幾乎沒有被氧化,因此,對該高砷礦直接進行細菌氧化效果不佳。對該氧化渣進行氰化浸出試驗,試驗結果如下:金浸出率64.18%,銀浸出率35.93%,氰化鈉消耗10 kg/t,浸出率也只是略有提高,浸出效果較差。

圖1 高砷礦電位及pH值隨時間的變化曲線Fig.1 Variation curves of potential and pH value with time of ore with high arsenic content

圖2 高砷礦液體中鐵砷濃度及氧化率變化曲線Fig.2 Variation curves of iron-arsenic concentration and oxidation ratio in ore liquid with high arsenic content
2.2 混礦降砷細菌氧化試驗
由以上試驗可以看出,當金精礦中砷的含量過高時,很難進行細菌氧化,因此,需要降低試樣中砷的含量,這可以通過配礦來實現。
2.2.1 配礦的選擇
配礦種類的選擇有基于兩個原則:1) 含砷較低;2) 容易被細菌氧化,以實現在和高砷礦按照一定比例配入后降低原料中砷的同時,可以較快啟動細菌氧化反應。根據該原則選擇了另一含砷金精礦,為便于區分,以下稱之為配礦,其主要元素含量、直接氰化及細菌氧化氰化浸出情況分別如表3、表4和圖3所列。
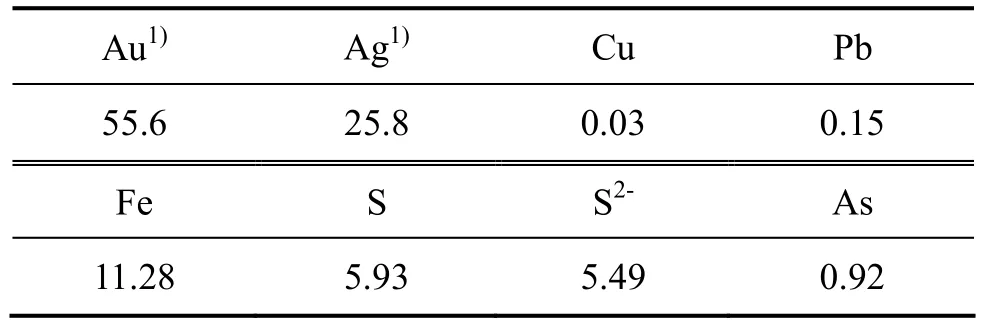
表3 配礦的化學成分分析Table 3 Chemical composition of core blending (mass fraction, %)

表4 配礦直接氰化浸出和細菌氧化后的浸出結果Table 4 Results of direct cyanide leaching and leaching after bacterial oxidation for blending ore

圖3 配礦電位及鐵砷氧化率隨時間的變化曲線Fig.3 Variation curves of potential and iron-arsenic oxidation ratio with time for blending ore
由表3、表4及圖3可知,該金精礦中含硫化物較低,不到 6%,配礦的直接氰化回收率都比較低,金和銀的浸出率分別只有 32.74%和 74.90%;在其細菌氧化過程中,礦漿氧化還原電位及鐵、砷的濃度都一直處于上升狀態,鐵、砷氧化率也不斷提高;對細菌氧化后的氧化渣進行氰化,金、銀浸出率分別提高到 96.34%和 80.20%,充分說明配礦的細菌預氧化效果較好,配礦很適合進行細菌氧化處理。
由表4可知,配礦經細菌預氧化后,其中金的浸出率提高很多,達到96.34%,但是由于該配礦含有大量的碳酸鹽,在預氧化過程中消耗大量的硫酸,耗酸量達 320 kg/t,因此,盡管其浸出率較高,從經濟角度考慮,還是無法單一采用此礦進行生產。
生產實際中,在保證細菌氧化及金氰化浸出效果的前提下,盡可能減少配礦的比例,因此,按照高砷礦與混礦銨質量比為1:2、1:3、1:5和1:8的比例進行試驗。
2.2.2 混礦細菌氧化試驗
將高砷礦與配礦分別按照質量比為1:2、1:3、1:5和1:8進行混合后化驗分析,為便于區分,簡稱為不同比例混礦,其主要元素的含量如表5所列。不同比例混礦細菌氧化過程中氧化還原電位及鐵、砷氧化率隨時間變化的曲線如圖4~6所示。

表5 不同比例混礦中主要元素含量Table 5 Main elements contents in mix ore with different blending ratios (mass fraction, %)
由圖4~6可知,高砷礦經配礦后,無論是礦漿電位還是鐵和砷的氧化率均大幅改善,細菌氧化效果大幅度提高,其中質量比1:5混礦的效果最佳,其氧化還原電位、鐵和砷的氧化率都高于其他比例混礦的,所用的氧化時間最短,氧化速率最快(曲線斜率最大),其次是質量比為1:8、1:3和1:2的混礦礦樣。
由以上試驗可以看出,高砷礦、配礦及不同比例混礦時鐵與砷的氧化時間是不同的,結果如表6所列。

圖4 不同比例混礦電位變化曲線Fig.4 Variation curves of potential for mix ore with different blending mass ratios

圖5 不同比例混礦中鐵氧化率的變化曲線Fig.5 Variation curves of iron oxidation rate in mix ore with different blending mass ratio

圖6 不同比例混礦中砷氧化率的變化曲線Fig.6 Variation curves of arsenic oxidation ratio for mix ore with different mass ratios

表6 各種礦樣中鐵、砷的氧化時間Table 6 Oxidating time of iron and arsenic in various ore samples
盡管延遲期和對數期沒有嚴格的劃分依據,但還是能看出一些規律,由表6可以看出,質量比1:5混礦對細菌活性的影響也相對最小,主要表現在這種比例混礦細菌氧化鐵的延遲期最短為144 h,對數期最長為206 h;氧化砷的延遲期最短為148 h,對數期相對較長,為127 h;同時由表中可以看出,TCJ菌氧化砷時對數期比氧化鐵時的對數期要短。
2.2.3 混礦細菌氧化后氰化浸出試驗
對上述比例混礦氧化渣進行氰化浸出試驗,試驗結果如表7所列。
由表7可以看出,不同質量比的混礦在經過細菌氧化之后進行氰化浸出,相對單獨的高砷礦或者配礦來說,浸出率提高很多,說明氧化預處理效果明顯,但是不同質量比混礦中金、銀的浸出率相差不大,因此,細菌氧化速率的快慢和氧化時間的長短就顯得尤為重要,另外,氰化鈉作為氰化浸出的主要成本構成,其單耗相差還是比較大,綜合來講,質量比1:5混礦的浸出率和氰化鈉單耗都較為合適。

表7 不同比例混礦氧化渣氰化浸出結果Table 7 Cyanide leaching of oxidizing tailings in mix ore with different blending mass ratios
3 分析與討論
在生物氧化過程中作為主要載金礦物的黃鐵礦和毒砂可能會發生以下主要氧化還原反應[19-22]:

由以上反應可知:1) 在細菌氧化還原黃鐵礦及毒砂的過程中,黃鐵礦的氧化是一個產酸反應,毒砂的氧化是一個耗酸反應,并且生成As3+。在一定條件下,Fe3+可以將 As3+氧化成 As5+,在這些反應過程中,關鍵控制因素是細菌的活性、體系的氧化還原電位和pH,直接影響反應的持續性和砷的價態及轉化;2) Fe3+與被氧化的礦物進行化學反應。氧化產生的Fe2+由細菌氧化為Fe3+后,再進入反應中循環,維持著生物氧化過程;3) 砷先以As3+的狀態進入溶液中,含砷高的精礦As3+在整個氧化過程中占主導作用,而含砷低的精礦中只是在氧化的初始階段占主導作用,當初始階段黃鐵礦存在量較大時,As3+迅速被氧化為 As5+;4)黃鐵礦是決定生物氧化過程中砷的氧化狀態的主要因素,盡管Fe3+是強氧化劑,但不能直接將As3+氧化成As5+,而需與黃鐵礦共同作用才能氧化成As3+;5) As3+對細菌的抑制能力遠大于 As5+對細菌的抑制能力[9-11]。
高砷礦中由于含砷高,在整個氧化過程中,As3+在溶液中占主導作用,對細菌產生較強的抑制作用,使其失去活性,接種物中的Fe3+氧化礦物生成的Fe2+無法被細菌氧化為Fe3+,因此,高砷礦的生物氧化過程無法持續循環進行,主要表現為氧化過程電位上升得非常緩慢,以及pH值變化很小,說明溶液中的Fe3+和Fe2+的摩爾比基本沒有變化,氧化過程中沒有發生S被氧化為硫酸或者Fe2+被氧化為 Fe3+的情況,從而造成溶液 pH值降低,即高砷礦的細菌氧化沒有辦法啟動。
低砷礦中含砷低,As3+只是在氧化的初始階段占主導作用,并且由于黃鐵礦的存在As3+迅速被氧化為As5+,因此,細菌沒有受到強烈抑制而活性好,Fe3+氧化礦物生成的Fe2+被細菌氧化為Fe3+,所以氧化反應持續進行,在氧化開始電位上升較慢但仍處于上升階段。
由于Fe3+需與黃鐵礦共同作用才能氧化As3+,而配礦的硫化物含量較低不到 6%,因此,隨著氧化的進行,As3+的濃度有一個積累的過程,當達到一定值時,細菌盡管在低砷環境中,但活性仍受到As3+的影響,由于TCJ菌的耐砷能力較強,在適應一段時間后又恢復活性,因此在配礦的氧化開始反應階段,砷的氧化率先上升后下降又上升出現反復。總體來說,盡管低砷礦的細菌氧化反應能夠啟動和進行,但是由于其硫化物含量較少,碳酸鹽含量較多,因此,鐵和砷的氧化率并不是很高,鐵的氧化率65.63%,砷的氧化率55.96%,盡管鐵砷氧化率不高,但由于配礦碳酸鹽含量大,在pH值為2的條件下,預氧化后還是讓金暴露,因此,金的浸出率并不低。
將高砷礦和配礦按照一定比例混合后,盡管只是一個簡單的物理混合過程,但可以較好地解決兩種單獨原料預氧化中存在的問題:一是含砷量降低,有利于細菌的生存和活性恢復,細菌可以選擇性地先吸附在低砷的配礦礦物表面,Fe3+將礦物氧化后產生的Fe2+被細菌氧化為Fe3+,并為細菌提供能量,這樣氧化反應能夠啟動;二是高砷礦中硫化物含量高,其中的黃鐵礦可以彌補低砷配礦中黃鐵礦含量不高的缺陷,在有黃鐵礦存在的條件下,As3+被氧化成 As5+,從而減少對細菌的抑制,更有利于細菌氧化,因此,混礦后的鐵和砷的氧化率都普遍高于單一的高砷礦或者配礦。
由試驗可知,含砷金精礦中各種礦物的比例直接影響著細菌預氧化的效果,根據原料中硫、砷及鐵等主要成分和黃鐵礦及毒砂等主要礦物的不同,按一定比例進行混合配料會改善原料的細菌預氧化效果。通過混礦試驗可以看出,高砷礦和配礦的質量比為 1:5時,各項指標最好。綜合整個試驗中高砷礦、配礦及各種混礦的鐵砷摩爾比與鐵砷硫氧化率、金銀浸出率及氰化鈉單耗的關系曲線如圖7所示。
由圖 7可知,給礦中鐵砷摩爾比在 4.6~5.2之間時,鐵砷氧化率及金銀浸出率都比較好,因此,在配料時要注意高砷礦與配礦的質量比,使給礦中的鐵砷摩爾比介于此范圍,亦有利于細菌預氧化和氰化浸出。
為了考察試驗中溶液中的鐵砷摩爾比變化情況,繪制高砷礦、配礦以及各種混礦的溶液中鐵砷摩爾比對時間變化曲線如圖8所示。
由圖8可知,給礦中鐵砷摩爾比高,溶液中的鐵砷摩爾比也高,同時隨著給礦中鐵砷摩爾比的增加,溶液中鐵砷摩爾比變化的幅度加大,變化頻率加快。因此,給料中鐵與砷的摩爾比不僅影響As3+的氧化,同時也會影響溶液中鐵砷摩爾比的變化,從而影響溶液中砷酸鐵的穩定性。

圖7 不同給礦鐵砷摩爾比與氧化率Fe/As摩爾比、浸出率及氰化鈉單耗的關系曲線Fig.7 Variation curves of oxidation rate of As, Fe, S and leaching rate of Au, and consumption of NaCN with mole ratio of Fe to As in feeding
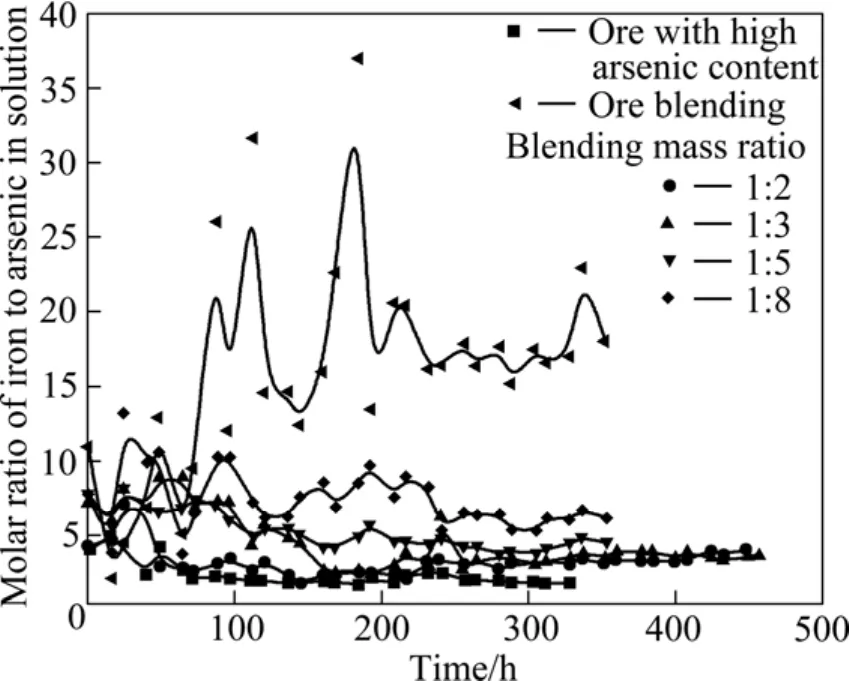
圖8 不同給礦溶液中鐵砷摩爾比變化曲線Fig.8 Variation curves of iron-arsenic molar ratio in different ore feeding liquids
4 結論
1) 通過配入合適的原料處理高砷礦,可以改善細菌氧化效果,并且獲得較好的技術經濟指標,但是配料時需要考慮不同原料中硫、砷及鐵等主要成分和黃鐵礦、毒砂等主要礦物的組成,按照一定的比例混合,以保證給料中各種主要礦物的比例在合適的水平上,試驗高砷礦配礦的適宜質量比為1:5。
2) 含砷金精礦給礦中的鐵砷摩爾比不同會影響細菌的活性和溶液中的鐵砷摩爾比,選擇合適的給礦鐵砷摩爾比有利于細菌預氧化過程的穩定和優化,試驗高砷礦配礦鐵砷摩爾比在4.6~5.2之間較為合適。
REFERENCES
[1] FRASER K S, WALTON H, WELLS J A. Processing of refractory gold ore[J]. Minerals Engineering, 1991(4):1029-1041.
[2] 楊洪英, 范 金, 崔日成, 鞏恩普. 難處理高砷金礦的細菌氧化-提金研究[J]. 貴金屬, 2009, 30(3): 1-3.YANG Hong-ying, FAN Jin, CUI Ri-cheng, GONG En-pu.Study on bacterial oxidation-extraction gold of refractory gold ore[J]. Precious Metals, 2009, 30(3): 1-3.
[3] EHRLICH H L. Past, present and future of biohydrometalhrgy[J].Hydrometallurgy, 2001, 59(2/3): 127-134.
[4] AKCIL A. Potential bioleaching developments towards commercial reality: Turkish metal mining’s future[J]. Minerals Engineering, 2004, 17(3): 477-480.
[5] CABRAL T, IGNATIADIS I. Mechanistic study of the pyrite-solution interface during the oxidative bacterial dissolution of pyrite (FeS2) by using electrochemical techniques[J]. International Journal of Mineral Processing, 2001,62(1/4): 41-64.
[6] TIPRE D R, DAVE S R. Bioleaching process for Cu-Pb-Zn bulk concentrate at high pulp density[J]. Hydrometallurgy, 2004, 75:37-43.
[7] WATLING H R. The bioleaching of sulphide minerals with emphasis on copper sulphides—A review[J]. Hydrometallurgy,2006, 84(1/2): 81-108.
[8] 楊麗麗, 楊洪英, 范有靜,王大文, 朱長亮, 孫會蘭. 難處理金礦石細菌氧化的影響因素研究[J]. 貴金屬, 2007, 28(1): 58-62.YANG Li-li, YANG Hong-ying, FAN You-jing, WANG Da-wen,ZHU Chang-liang, SUN Hui-lan. Study on influencing factors of bacterial oxidation of refractory gold ores[J]. Precious Metals,2007, 28(1): 58-61.
[9] 金世斌, 馬金瑞, 郝福來. 金精礦生物氧化過程中砷的氧化行為初探[J]. 黃金, 2009, 30(8): 41-43.JIN Shi-bin, MA Jin-rui, HAO Fu-lai. Preliminary discussion on the arsenic oxidization behavior in gold concentrate biologic oxidization process[J]. Gold, 2009, 30(8): 41-43.
[10] 楊洪英, 楊 立, 魏緒鈞. 氧化亞鐵硫桿菌(SH-T)氧化毒砂的機理[J]. 中國有色金屬學報, 2001, 11(2): 323-327.YANG Hong-ying, YANG Li, WEI Xu-jun. Mechanism on biooxidation of arsenopyrite with Thiobacillus ferrooxidans strain SH-T[J]. The Chinese Journal of Nonferrous Metals, 2001,21(2): 323-327.
[11] 楊洪英, 鞏恩普, 訾建威, 楊 立. 嗜熱菌對高砷金精礦氧化-氰化提金試驗研究[J]. 東北大學學報: 自然科學版, 2006,27(4): 426-429.YANG Hong-ying, GONG En-pu, ZI Jian-wei, YANG Li.Experimental investigation on gold recovery from high-As concentration through bio-oxidation/cyanidation with thermophilic bacteria[J]. Journal of Northeastern University:Natural Science, 2006, 27(4): 426-429.
[12] 羅志雄, 張廣積, 方兆珩. 采用中溫菌和常溫菌浸出含砷金精礦[J]. 中國有色金屬學報, 2007, 17(8): 1342-1347.LUO Zhi-xiong, ZHANG Guang-ji, FANG Zhao-heng.Bioleaching arsenic-containing gold concentrates with MLY and At.f[J]. The Chinese Journal of Nonferrous Metals, 2007, 17(8):1342-1347.
[13] 戴紅光. 湖北某難處理金精礦中溫菌預氧化-氰化浸出試驗研究[J]. 濕法冶金, 2009, 28(2): 81-83.DAI Hong-guang. Experiment research on pre-oxidation by moderate bacteria and leaching by cyanide for a refractory gold concentrate[J]. Hydrometallurgy of China, 2009, 28(2): 81-83.
[14] 柳建設, 王鏵泰, 閆 穎, 王秀美, 賀治國, 邱冠周. 氣升式反應器中細菌氧化預處理難浸金精礦的浸出參數優化[J]. 礦冶工程, 2008, 28(5): 35-39.LIU Jian-she, WANG Hua-tai, YAN Ying, WANG Xiu-mei, HE Zhi-guo, QIU Guan-zhou. Optimum parameters for bacterial pre-oxidation of refractory gold concentrate in an airlift reactor[J]. Mining and Metallurgical Engineering, 2008, 28(5):35-39.
[15] 崔日成, 楊洪英, 張谷平, 范 金. pH值對浸礦細菌的活化以及金精礦脫砷的影響[J]. 東北大學學報: 自然科學版, 2008,29(11): 1597-1600.CUI Ri-cheng, YANG Hong-ying, ZHANG Gu-ping, FAN Jin.Effect of pH value on activation of bioleaching bacteria and dearsenification of gold ore concentrates[J]. Journal of Northeastern University: Natural Science, 2008, 29(11):1597-1600.
[16] 佟琳琳, 姜茂發, 楊洪英, 殷書巖. 湖南某高砷難處理金精礦的細菌氧化-氰化提金實驗研究[J]. 貴金屬, 2008, 29(1):15-18.TONG Lin-lin, JIANG Mao-fa, YANG Hong-ying, YIN Shu-yan.Experimental investigation on gold extraction from high-as concentrate in Hunan province through bio-oxidation/cyanidation[J]. Precious Metals, 2008, 29(1): 15-18.
[17] 李萬全, 張永奎, 陳 寧, 梁 穎, 黃亞潔. 某高硫砷難浸金精礦的細菌氧化預處理[J]. 金屬礦山, 2007(2): 42-44.LI Wan-quan, ZHANG Yong-kui, CHEN Ning, LIANG Ying,HUANG Ya-jie. Bio-oxidation pretreatment of high arsenic high sulfur refractory gold concentrate [J]. Metal Mine, 2007(2):42-44.
[18] 李育林, 伍贈玲, 吳在玖, 張永奎. 高硫高砷金精礦細菌氧化-氰化浸金試驗研究[J]. 濕法冶金, 2005, 24(2): 73-76.LI Yu-lin, WU Zeng-ling, WU Zai-jiu, ZHANG Yong-kui.Bacterial oxidation and cyanide leaching process of gold concentrate containing arsenic and sulphur[J]. Hydrometallurgy of China, 2005, 24(2): 73-76.
[19] BALLESTER A, AMILS R. Biohydronetallurgy and the environment toward the mining of 21st century[M]. Netherlands:Elsevier Scicence B V, 1999: 431-441.
[20] LANGHANS D, LORD A, LAMPSHIRE D. Biooxidation of an arsenic-bearing refractory gold ore[J]. Minerals Engineering,1995, 8(2): 147-158.
[21] 崔日成, 楊洪英, 張谷平, 馬玉蕊, 范 金, 李科峰. 毒砂型高砷金精礦的細菌氧化[J]. 化工學報, 2008, 59(12): 3090-3094.CUI Ri-cheng, YANG Hong-ying, ZHANG Gu-ping, MA Yu-rui,FAN Jin, LI Ke-feng. Biooxidation of high arsenic gold concentrate with arsenopyrite type[J]. Journal of Chemical Industry and Engineering, 2008, 59(12): 3090-3094.
[22] 楊松榮, 邱冠周, 胡岳華, 謝紀元. 含砷難處理金礦石生物氧化工藝及其應用[M]. 北京: 冶金工業出版社, 2006: 93.YANG Song-rong, QIU Guan-zhou, HU Yue-hua, XIE Ji-yuan.The biological oxidation technology and application of refractory gold ores containing arsenic[M]. Beijing:Metallurgical Industry Press, 2006: 93.
Extraction of Au from high arsenic refractory gold concentrate by bacterial oxidation-cyanidation
YANG Wei1, QIN Wen-qing1, LIU Rui-qiang2, REN Yun-chao3
(1. School of Resources Processing and Bioengineering, Central South University, Changsha 410083, China;2. The Refinery of Shandong Gold Mining Co., Ltd., Laizhou 261441, China;3. Engineering Design & Research Co. Ltd., Shandong Gold Group, Yantai 264006, China)
Through blending low arsenic carbonate gold concentrate with different ratios into high arsenic-containing gold concentrate and changing the content of major ores, such as sulfur, arsenic and iron, the effect of iron-arsenic molar ratio on the bacteria oxidating-cyaniding extraction from high arsenic-containing refractory gold concentrate was investigated. The result shows that the iron-arsenic mole ratio of arsenic-containing gold concentrate has direct effect on the bacteria oxidation, bacteria activity and iron-arsenic molar ratio in solution. High iron-arsenic mole ratio in feeding results in high iron-arsenic ratio in solution. With iron-arsenic molar ratio increasing, the iron-arsenic ratio increases, and the frequency of change accelerates. The iron-arsenic ratio ranging from 4.6 to 5.2 is helpful to bacteria oxidizing-cyaniding extraction, the oxidation ratios of iron and arsenic increase to 89.90% and 93.60% from 6.14% and 7.38%, respectively. The extraction rate of gold and silver increase to 97.78% and 88.83% from 64.18% and 35.93%,respectively. Choosing appropriate iron-arsenic molar ratio can effectively improve the bacterial oxidation, stabilizes and optimize the process of bacterial pre-oxidation.
high arsenic refractory gold concentrate; bacterial oxidation; cyaniding gold extraction
TF80
A
1004-0609(2011)05-1151-08
國家重點基礎研究發展計劃資助項目(2010CB630905)
2010-08-25;
2010-11-22
楊瑋,高級工程師,博士;電話:13507710579;E-mail:ywmsco@126.com
(編輯 龍懷中)

