D001陽離子交換樹脂分離紅曲霉發酵液中γ-氨基丁酸的研究
嵇 豪 蔣冬花 周 琴 汪鵬榮 董夏夢 蔡琪敏
(浙江師范大學化學與生命科學學院,金華 321004)
D001陽離子交換樹脂分離紅曲霉發酵液中γ-氨基丁酸的研究
嵇 豪 蔣冬花 周 琴 汪鵬榮 董夏夢 蔡琪敏
(浙江師范大學化學與生命科學學院,金華 321004)
研究了紅曲霉發酵液中的γ-氨基丁酸(GABA)分離純化工藝。對3種脫色劑進行篩選,D101樹脂對紅曲發酵液具有最高的脫色率和GABA得率。分別以靜態和動態吸附-解析方法考察D001離子交換樹脂對GABA的最優分離條件,結果表明:脫色發酵液pH下上樣,上樣流速為1 BV/h,采用水和2 mol/L氨水兩步洗脫,洗脫液濃縮后結晶為透明針狀,GABA的總得率為45.4%。
γ-氨基丁酸 紅曲霉發酵液 D001陽離子樹脂 分離
γ-氨基丁酸(GABA)是一種廣泛存在于動植物中的一種非蛋白質氨基酸,由谷氨酸經谷氨酸脫羧酶催化轉化而來,是存在于哺乳動物脊髓、大腦中的重要的抑制性神經遞質,具有突觸后抑制作用,可通過突觸后膜超極化、減少離子內流,降低細胞代謝及氧消耗等機制,是突觸后神經元處于保護性抑制狀態,并可通過突出前抑制減少谷氨酸的釋放,從而減少灌注區神經元的死亡[1-2]。報道的GABA生理功能基本與抑制性神經遞質有關,主要包括降血壓功能,促生長功能,促進生殖,治療癲癇,抗衰老等[3]。
目前GABA的制備方法主要有化學合成法和生物合成法[4]。其中生物合成法生產主要是利用微生物技術,通過篩選優良高產的安全菌種,發酵生產GABA制劑,可以認為是天然食品添加劑,我國衛生部于2009年將食品級GABA確定為新資源食品用于食品生產加工。食品級GABA主要以谷氨酸鈉為原料經乳酸菌發酵,再分離純化得制品。紅曲是我國傳統具有藥食兩用的發酵產品,現代研究證明紅曲所具有的降壓作用主要是由紅曲霉的次級代謝產物GABA所引起的。紅曲霉的高度安全性為GABA的生產提供了另一條可靠的途徑[5]。本文試圖通過使用陽離子交換樹脂對紅曲霉發酵液中的GABA進行分離純化,為食品級GABA的商業生產提供一定的技術支持。
1 材料與方法
1.1 材料
活性炭:浙江省金華市醫藥公司;D001陽離子交換樹脂,D101,D301大孔吸附樹脂:西安藍曉科技有限公司;GABA標準品:SIGAMA公司;高產GABA紅曲霉發酵液(6 g/L)[6]:浙江師范大學微生物研究室。
1.2 主要儀器設備
RE-52B旋轉蒸發儀:上海亞榮生化儀器廠;SHZ-D循環水式多用真空泵:河南省予華儀器廠;BT600-2J蠕動泵:保定蘭格恒流泵有限公司;100GPDRO反滲透純水儀:上海和泰儀器有限公司;3.0 cm×50 cm玻璃層析柱:海門市盛邦實驗儀器廠。
1.3 試驗方法
1.3.1 紅曲霉發酵液預處理
取紅曲霉發酵液沸水浴10 min后12 000 r/min離心15 min[7],取上清液4℃冰箱保存備用。
1.3.2 GABA含量和色價的測定
采用改良紙層析法測定 GABA含量[8]。按0.004 g/mL加入顯色劑茚三酮到展開劑中,取5 μL發酵上清液點樣,GABA標準品做參比。采用新華一號層析紙展開后于90℃下顯色10 min。將待測樣和標準品斑點剪下,用0.1%硫酸銅∶75%乙醇=2∶38的洗脫液洗脫,于520 nm處比色測定。平行3次,取平均值。另配置不同濃度的GABA標準液,按上述方法洗脫比色,以GABA濃度對A520繪制標準曲線,GABA濃度可根據吸光度大小由標準曲線查得。
GABA損失率=(脫色前GABA含量-脫色后GABA含量)/脫色前GABA含量×100%
脫色率=(脫色前色價-脫色后色價)/脫色前色價×100%
取發酵液上清液,用去離子水適當稀釋后以去離子水為參比在505 nm下測吸光度。
發酵液色價=OD505×稀釋倍數
1.3.3 樹脂的預處理
以去離子水浸泡樹脂洗去大量泡沫,乙醇浸泡后漂至上清液澄清,再用去離子水洗至無醇味。2 mol/L NaOH浸泡6 h后水洗至中性,再用2 mol/L HCl浸泡6 h水洗至中性,最后將樹脂浸泡于去離子水中備用[9]。
1.3.4 靜態吸附試驗
將一定初始濃度的GABA加入250 mL的錐形瓶中,再各加入一定量的樹脂,用NaOH或HCl調節發酵上清液pH值,恒溫振蕩至平衡。吸附平衡后,液相濃度由改良紙層析法確定,吸附相濃度由下式計算[9]:
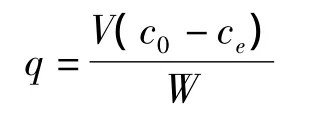
式中:q為平衡吸附量/mg/每克濕樹脂;V為溶液體積/L;c0為GABA初始質量濃度/g/L;ce為GABA平衡時的質量濃度/g/L;W為離子交換樹脂質量/g。
1.3.5 動態吸附與洗脫
將已經過預處理的發酵液,調至一定的pH值,用蠕動泵控制一定的流速上樣,同時用分部收集器對流出液分部收集,測定其中的GABA含量。以流出液體積為橫坐標,ce/c0為縱坐標,繪制穿透曲線。
配制一定濃度的洗脫劑,蠕動泵恒速上柱,分部收集器收集流出液,測定流出液GABA含量。以洗脫液體積為橫坐標,GABA濃度為縱坐標,繪制洗脫曲線。
2 結果與分析
2.1 紅曲發酵液的脫色
紅曲色素是紅曲霉的主要次級代謝產物之一,工業上利用紅曲霉液體深層發酵生產紅曲色素,常作為食品添加劑應用于食品工業[10]。本試驗所采用的高產GABA紅曲霉X27產紅曲色素能力良好,發酵液色價達到22.4 U/mL,因此從發酵液中分離純化GABA的首要任務是將色素脫除。分別以大孔樹脂D101、D301和活性炭顆粒作為脫色劑,從脫色結果上看,以D101大孔樹脂作為脫色劑,在添加量30%以上時脫色效果顯著,脫色率達到90%以上。活性炭作為常用的脫色劑,脫色效果較為顯著,但由于其不易再生、成本高,且脫色要求溫度高,GABA損失率大。綜合上述優缺點,選用30%的D101對發酵上清液進行脫色處理。
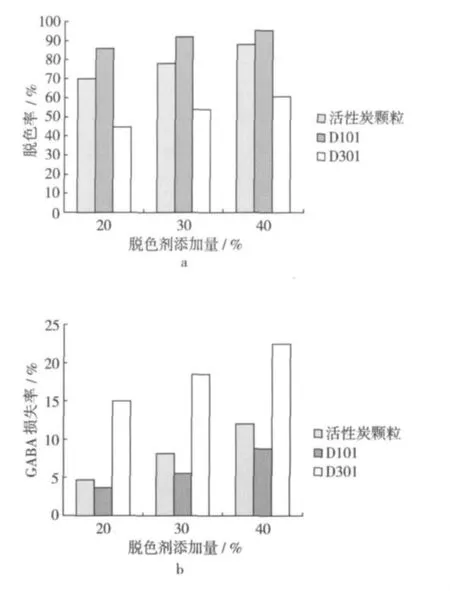
圖1 脫色劑對脫色率及GABA損失率的影響
2.2 pH對D001交換容量的影響
pH是影響離子交換平衡關系的重要因素。GABA是兩性電解質,其凈電荷取決于自身等電點及溶液的pH值。理論上選擇一個酸性環境,GABA主要呈陽離子狀態,有利于同陽離子樹脂的交換[11]。在靜態吸附試驗中,酸性條件下,樹脂保持一個較大的交換容量,pH在5~7之間,樹脂的交換容量達到最大值,之后隨著pH的升高交換容量快速下降。由于樹脂中的H+與GABA發生交換,導致交換體系的pH值下降;而經過脫色的發酵液主要成分為GABA(pI=7.5)及其前體物質谷氨酸(pI=3.22),當體系的pH下降,谷氨酸質子化易與GABA發生競爭吸附,導致交換容量降低。因此對GABA和谷氨酸的分離需要在動態吸附過程中進一步考察。紅曲霉為嗜酸腐生真菌,因此其發酵液一般保持在酸性環境,經脫色處理的發酵上清液pH為5.86,可以直接用來上柱。
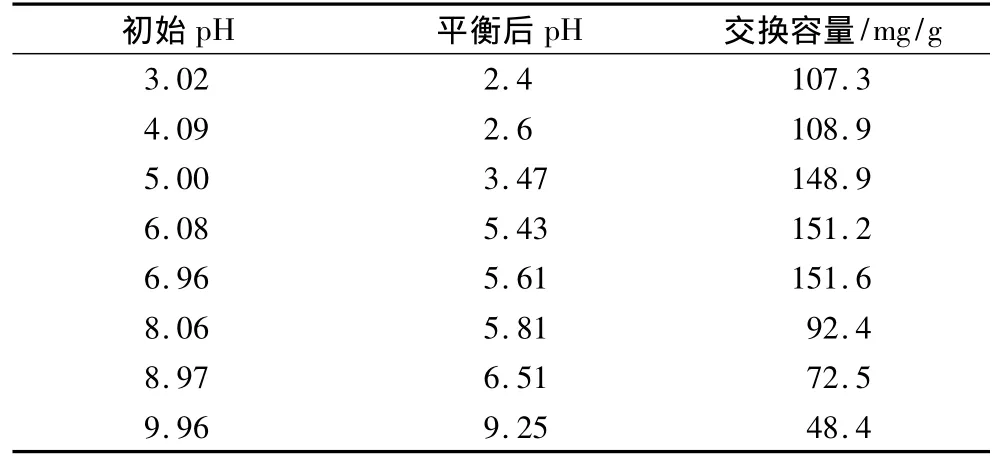
表1 pH對D001樹脂交換容量的影響
2.3 D001樹脂對GABA的吸附等溫線及吸附動力學曲線
吸附等溫線是指在一定溫度下溶質分子在兩相界面上進行的吸附過程達到平衡時它們在兩相中濃度之間的關系曲線。在室溫條件下,D001陽離子交換樹脂的吸附等溫線如圖2所示。隨著GABA的濃度升高,D001樹脂的交換容量增大,當質量濃度大于5 g/L后,繼續增加GABA濃度對樹脂的交換容量影響不大。
相對于凝膠型樹脂,大孔樹脂具有表面積大,交換速度快等特點,因此大孔樹脂的利用率更高。在靜態試驗中,分別測定各時間點的樹脂交換容量,圖2顯示D001樹脂很快對GABA進行吸附作用,并在60 min時離子交換量達到最大值,交換容量達160 mg/g。因此選擇大孔型強酸性陽離子交換樹脂D001作為GABA的分離介質是合適的。
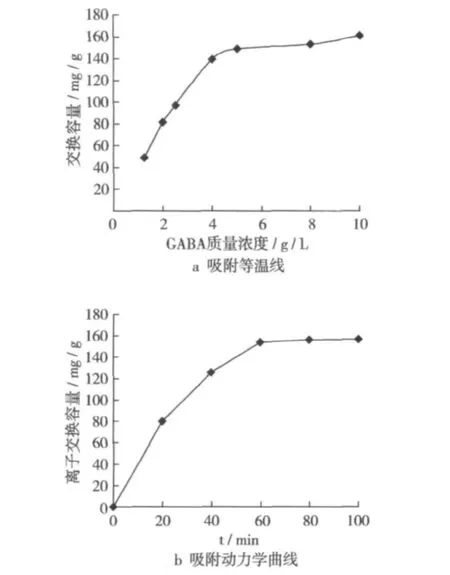
圖2 D001樹脂對GABA的吸附等溫線及吸附動力學曲線
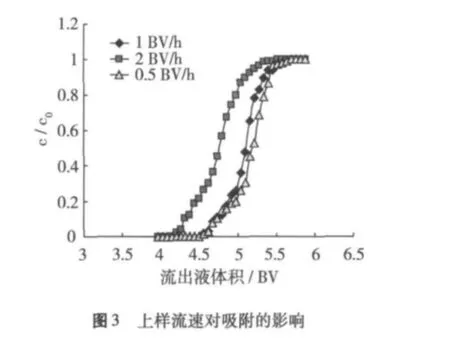
2.4 上樣流速對吸附的影響
上樣液選擇的流速是離子交換過程中的一個重要參數,為了使物質發生有效的交換,必須使固液兩相有充分的接觸時間。流速過快容易造成交換區拉長,提前發生滲漏。流速過慢則降低交換效率。如圖3所示,分別以0.5、1、2 BV/h的流速上樣。當流速為2 BV/h時,穿透點出現較早,樹脂提前發生滲漏,造成GABA流失。流速下降則穿透點延遲,樹脂利用率高。流速降為0.5 BV/h穿透點變化不大,且鑒于低流速導致上柱時間延長,適宜的上樣流速選擇為1 BV/h。
2.5 洗脫液濃度對解吸的影響
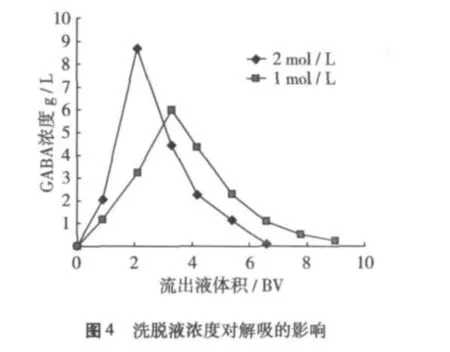
氨基酸離子交換的常用洗脫劑有氨水、銨鹽溶液和NaOH溶液等,由于氨水具有揮發性容易除去且不易帶入雜質,所以選擇氨水作為洗脫劑。上樣過程中,部分前體物質谷氨酸通過競爭作用被樹脂吸附,直接用氨水洗脫無法保證兩種物質的分離效果。由于谷氨酸是酸性氨基酸,因此可以在氨水洗脫前以大量去離子水對樹脂進行水洗處理,處于解離狀態的谷氨酸易被去離子水洗去。
分別以1、2 mol/L的氨水作為洗脫劑,1 BV/h的流速對飽和樹脂柱進行洗脫,測定各取樣點的GABA含量。以1 mol/L氨水為洗脫劑時,GABA峰形較寬,峰值不集中,洗脫劑使用量大;而使用濃度更高的氨水,由于離子強度大置換速度快,峰值較為集中,洗脫周期短,因此應選擇2 mol/L的氨水作為洗脫劑。
2.6 洗脫液收集、濃縮與結晶
一般的結晶方法有冷卻結晶、蒸發結晶及反應結晶3種工藝[12]。另外,氨基酸結晶工業中常向氨基酸水溶液中加入適量有機溶劑來降低其飽和濃度達到結晶的目的[13]。收集洗脫液后經旋轉蒸發儀于60℃下真空濃縮得GABA固形物,少量去離子水復溶后立即加入8倍體積無水乙醇,將溫度降至室溫后再于4℃冰箱靜置12 h后,過濾收集晶體。如圖5所示GABA結明晶為透針狀,GABA的總收率為45.4%。
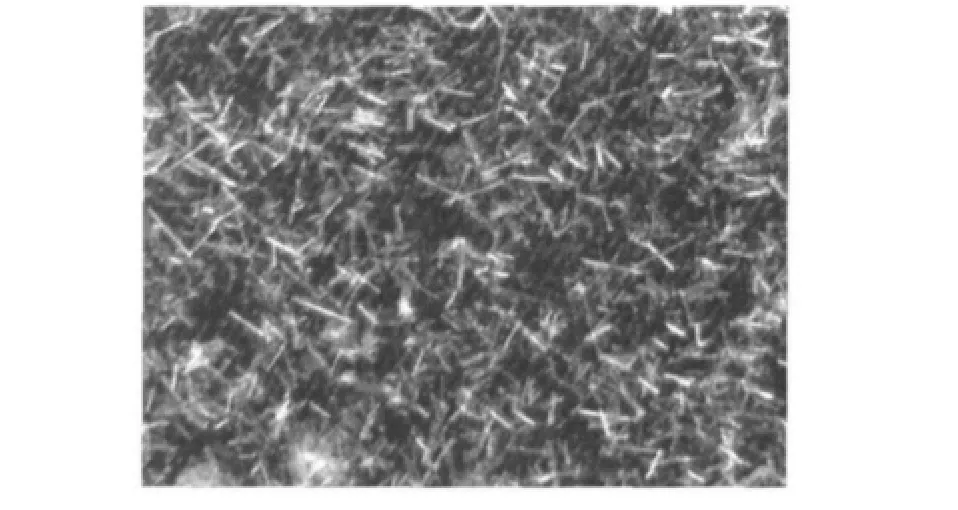
圖5 GABA的針狀結晶
3 結論
通過離子交換法分離純化紅曲霉發酵液中GABA,比較3種脫色劑的脫色效果及GABA損失率選擇D101大孔樹脂作為紅曲發酵液的脫色劑。30%的D101添加量脫色率達到90%以上,且GABA損失率僅5%左右。
在靜態試驗下,考察了上樣液的最佳上樣pH及D001對GABA的等溫吸附線及吸附動力學。結果顯示D001樹脂與GABA交換速度快,效率高,經過脫色的發酵液pH適宜直接上柱。
在動態條件下,選擇1 BV/h的上樣流速,氨水洗脫前用去離子水水洗除去谷氨酸,洗脫液氨水的濃度為2 mol/L,收集發酵液濃縮后結晶可得透明針狀結晶,GABA的總得率為45.4%。
[1]Nicolas B,Bouche B,Hillel F.GABA signaling:a conserved and ubiquitous mechanism[J].Trends in Cell Biology,2003,13(2):607-611
[2]Bassry S,Alan B,Michel M.Metabolism and function of gamma - amino butyric acid[J].Trend in Plant Science,1999,4(11):446-453
[3]許建軍,江波,許時嬰.γ-氨基丁酸(GABA)——種新型的功能食品因子[J].食品工業科技,2003,24(1):109-110
[4]白松,林向陽,阮榕生,等.γ-氨基丁酸的分布和制備[J].現代食品科技,2005,21(2):202 -205
[5]Kono I,Himeno K.Changes in γ - aminobutyric acid content during beni- koji making[J].Biosci Biotechnol Biochem,2000,64:617 -619
[6]Jiang DH,Ji H,Ye Y,et al.Studies on screening of higher c-aminobutyric acid-producing Monascus and optimization of fermentative parameters[J].European Food Research and Technology,2011,232(3):541 - 547
[7]蔣冬花,后加衡,李杰,等.紅腐乳中高產γ-氨基丁酸紅曲霉菌株的篩選[J].浙江師范大學學報:自然科學版,2007,30(4):447 -452
[8]夏江,梅樂和,黃俊,等.產γ-氨基丁酸的乳酸菌株篩選及誘變[J].核農學報,2006,2(5):379 -382
[9]付勇,吳國光,彭奇均.D001型陽離子交換樹脂吸附L-蘇氨酸[J].化工進展,2007,26(3):422 -425
[10]趙燕,溫輝梁,胡曉波.紅曲色素及其在食品工業中的應用[J].中國食品添加劑,2004,(4):90 -93
[11]劉崇鳳,付彩霞.氨基酸等電點與 pKa的關系[J].曲阜師范大學學報,1996,22(1):97 -99
[12]馮容保.氨基酸的結晶工藝[J].發酵科技通訊,2002,31(4):11-12
[13]馬強,張濤,江波,等.γ-氨基丁酸結晶熱力學的研究[J].食品工業科技,2010,31(2):77 -79.
Study on Separation of γ-Aminobutyric Acid from Monascus Fermentation Broth by D001 Ion-exchange Resins
Ji Hao Jiang Donghua Zhou Qin Wang Pengrong Dong Xiameng Cai Qimin
(College of Chemistry and Life Sciences,Zhejiang Normal University,Jinhua 321004)
The separation process of γ-Aminobutyric acid(GABA)from monascus fermentation broth was researched.Three types of decolorants were selected,and the D101 exhibited high decoloring ratio and high GABA yield.The static and dynamic adsorption-desorption performances were investigated to obtain optimized conditions of GABA separation by D001 ion - exchange resins.The result showed that the optimum parameters were as follows:original pH of decolor fermentation broth,sample flow - rate of 1 BV/h,elution method of two steps by using water and 2 mol/L aqueous ammonia.The transparence needle crystal of GABA was obtained after the effluent concentrated.The total recovery rate was 45.4%.
γ -Aminobutyric acid,monascus fermentation broth,D001 ion-exchange resins,separation
Q819
A
1003-0174(2011)08-0095-05
國家自然科學基金(31070008),浙江省自然科學基金(Y3090343)
2010-11-02
嵇豪,男,1986年出生,碩士,應用微生物學
蔣冬花,女,1964年出生,教授,微生物學和植物病理學

